Похожие презентации:
Биологические полимеры. Белки
1. Биологические полимеры. БЕЛКИ
Жизнь есть способ существования белковых тел,существенным моментом которого является постоянный
обмен веществ с окружающей их внешней природой,
причем с прекращением этого обмена веществ
прекращается и жизнь, что приводит к разложению белка»
Ф.Энгельс
2. Химический состав
Основные химические элементы, входящие всостав белков
С(углерод) – 50%
O(кислород) – 17-24%
H(водород) – 6,5-7,3%
N(азот) – 15-18%
S(сера) – 0,2-2,4%
Белки – это полимеры, мономерами которых
являются аминокислоты.
20.01.2006
Презентация
Стр. 2
3. Строение аминокислот
Общая формула:20.01.2006
- основная группа
- кислотная группа
- радикал
Презентация
Стр. 3
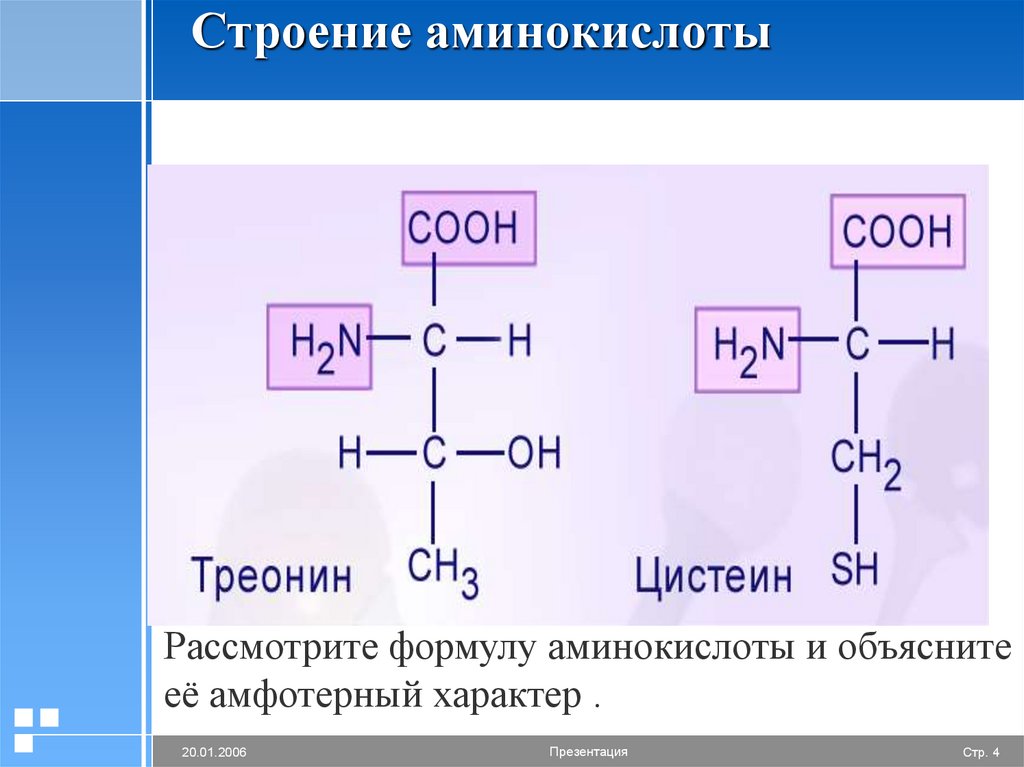
4.
Строение аминокислотыРассмотрите формулу аминокислоты и объясните
её амфотерный характер .
20.01.2006
Презентация
Стр. 4
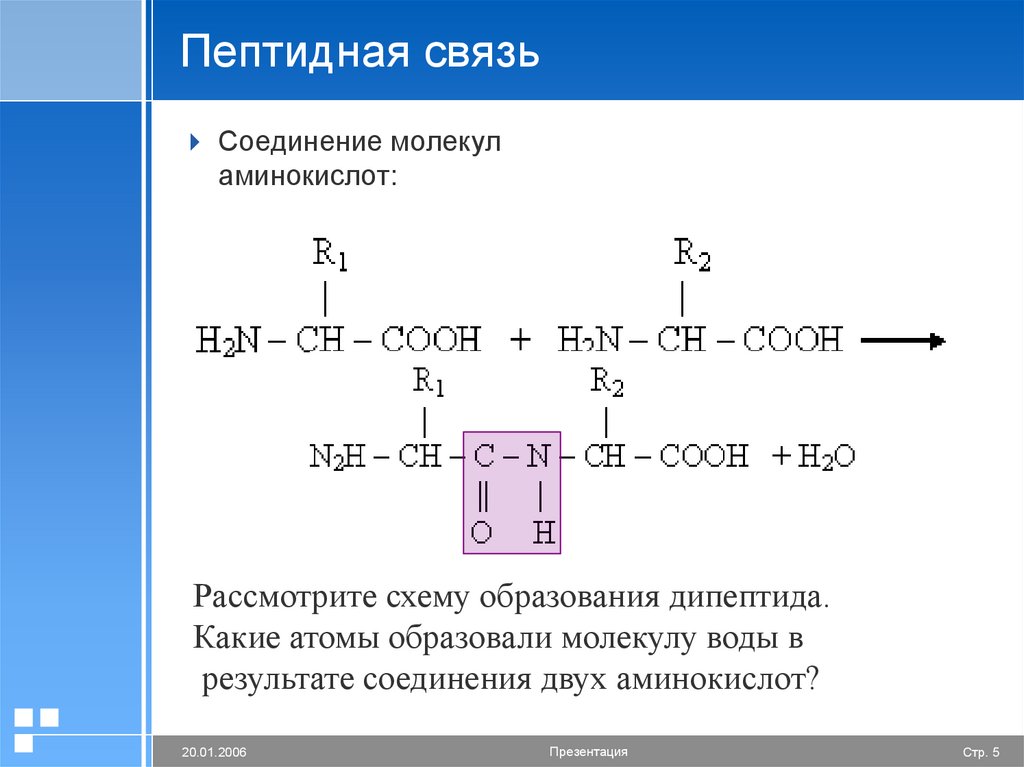
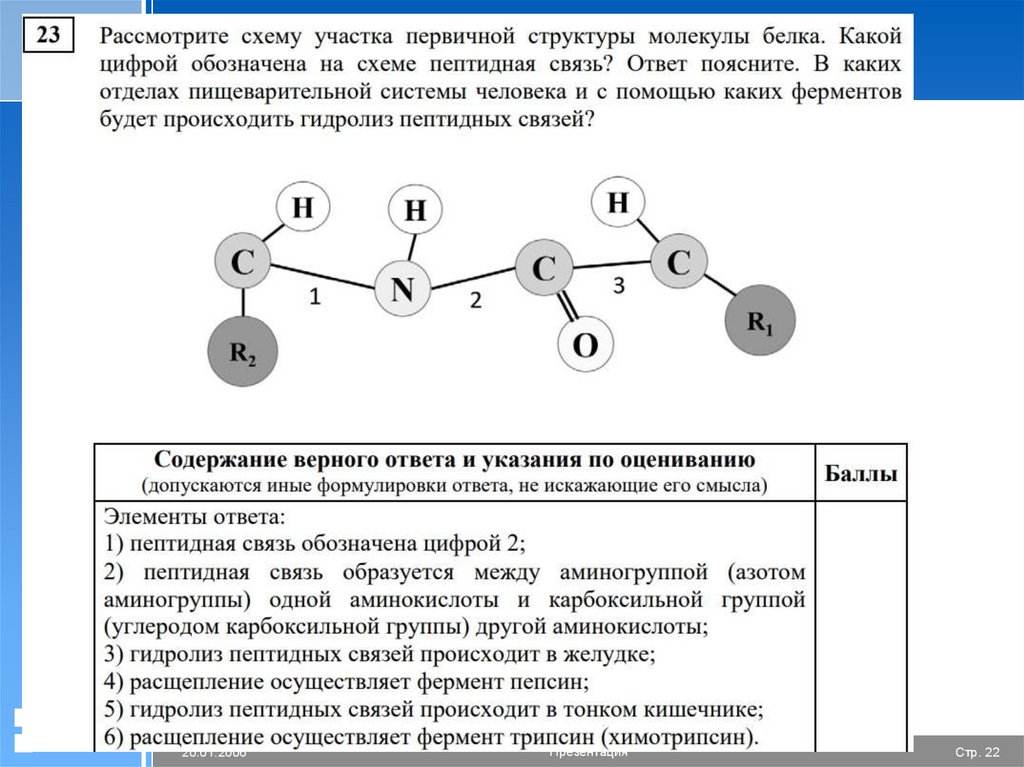
5. Пептидная связь
Соединение молекуламинокислот:
Рассмотрите схему образования дипептида.
Какие атомы образовали молекулу воды в
результате соединения двух аминокислот?
20.01.2006
Презентация
Стр. 5
6. Полимер, состоящий из аминокислот
20.01.2006Презентация
Стр. 6
7.
20.01.2006Презентация
Стр. 7
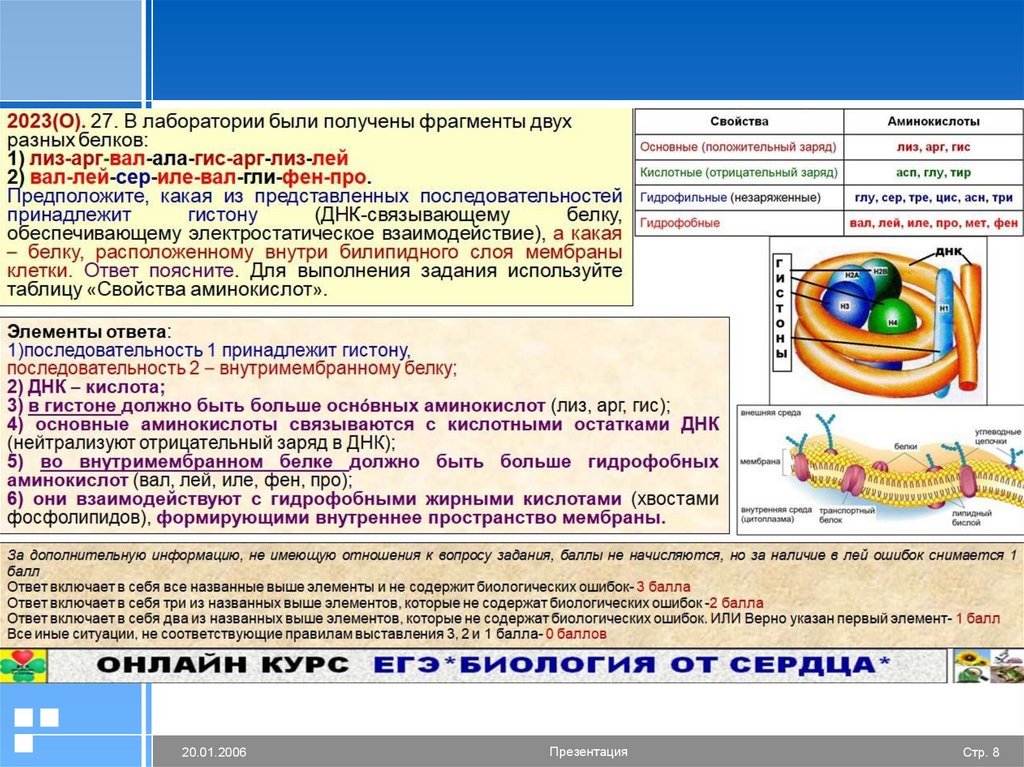
8.
20.01.2006Презентация
Стр. 8
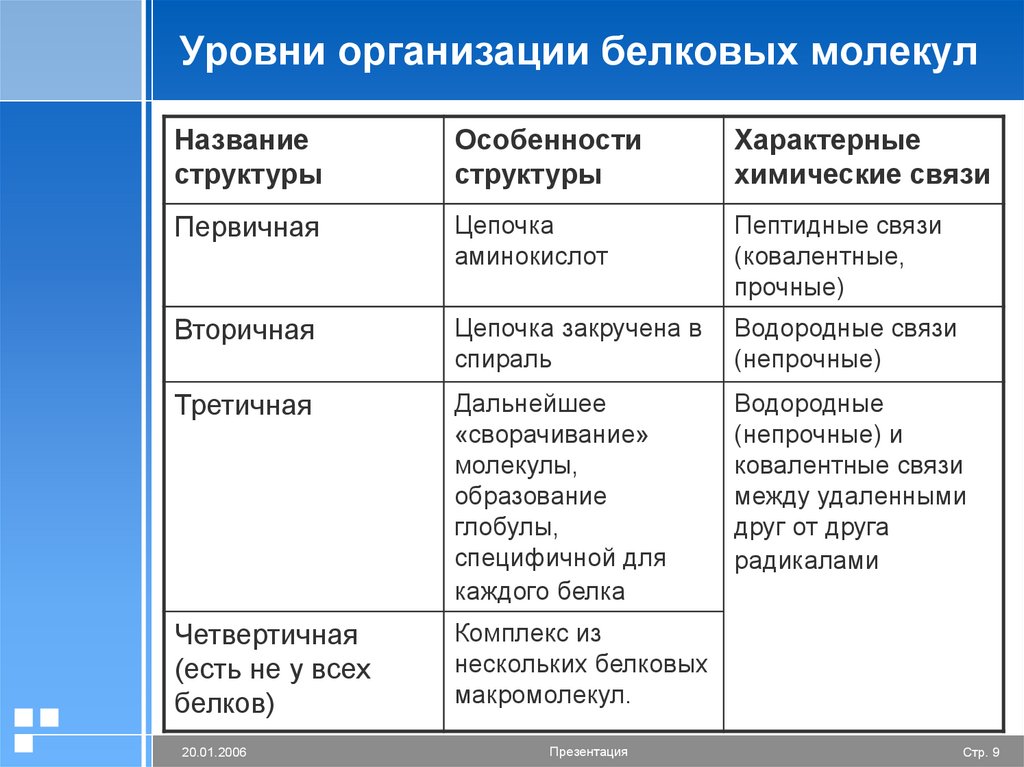
9. Уровни организации белковых молекул
Названиеструктуры
Особенности
структуры
Характерные
химические связи
Первичная
Цепочка
аминокислот
Пептидные связи
(ковалентные,
прочные)
Вторичная
Цепочка закручена в
спираль
Водородные связи
(непрочные)
Третичная
Дальнейшее
«сворачивание»
молекулы,
образование
глобулы,
специфичной для
каждого белка
Водородные
(непрочные) и
ковалентные связи
между удаленными
друг от друга
радикалами
Четвертичная
(есть не у всех
белков)
Комплекс из
нескольких белковых
макромолекул.
20.01.2006
Презентация
Стр. 9
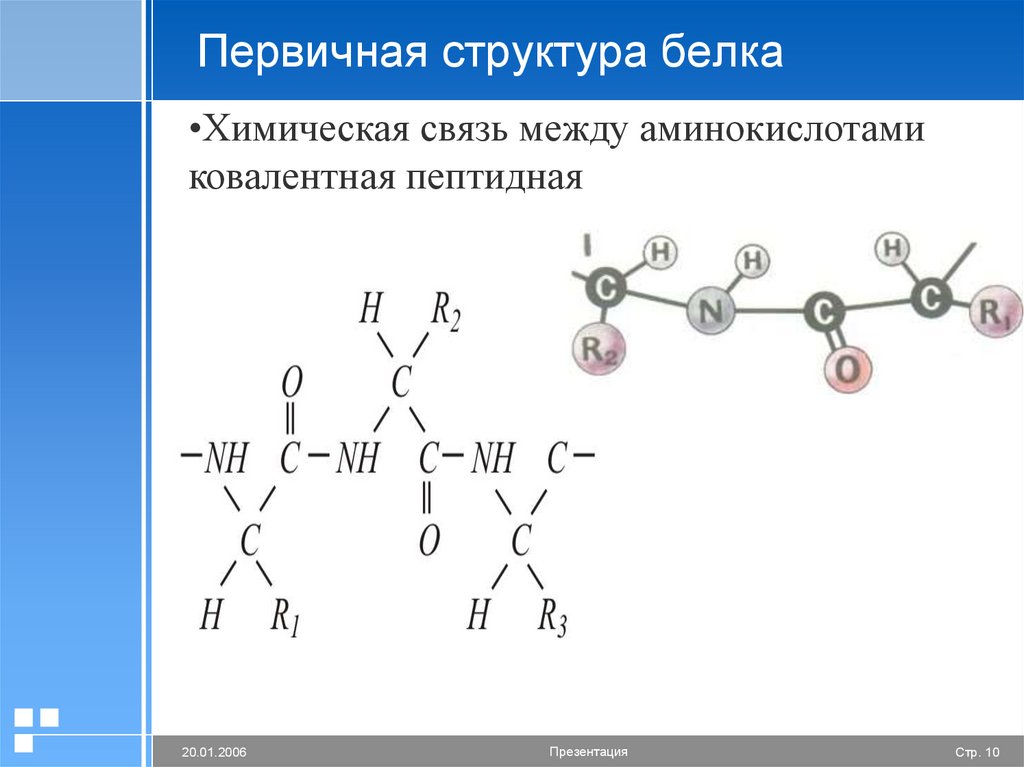
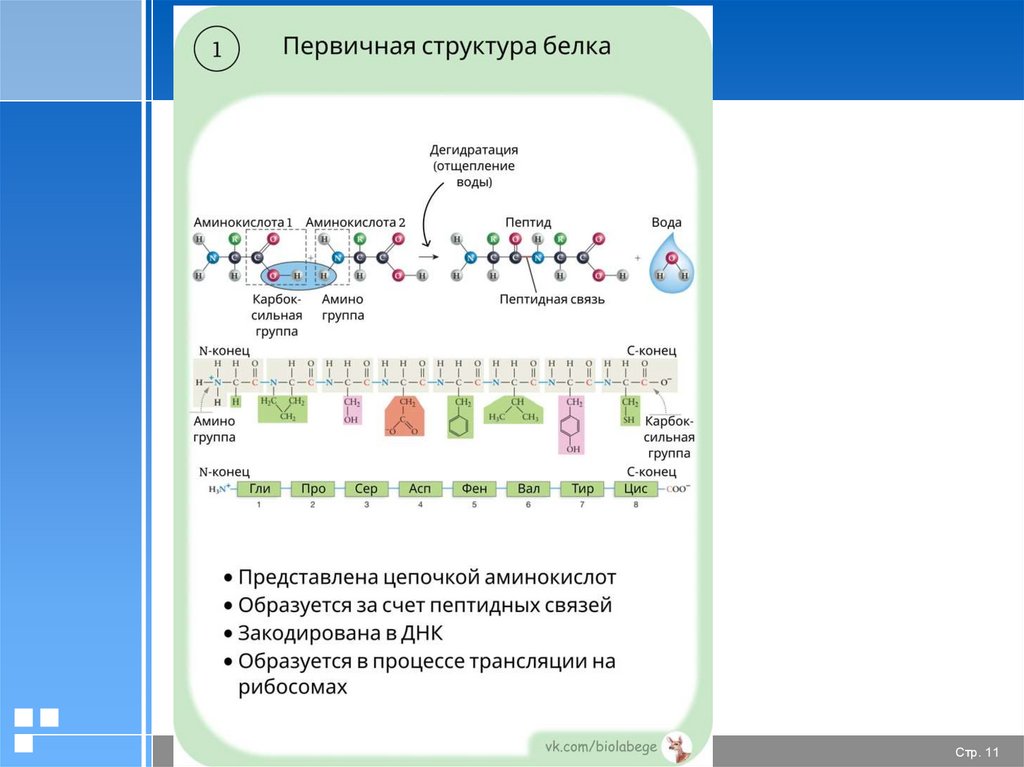
10. Первичная структура белка
•Химическая связь между аминокислотамиковалентная пептидная
20.01.2006
Презентация
Стр. 10
11.
20.01.2006Презентация
Стр. 11
12. Вторичная структура белка
Между аминокислотами возникаютдополнительные многочисленные водородные
связи
20.01.2006
Презентация
Стр. 12
13.
20.01.2006Презентация
Стр. 13
14.
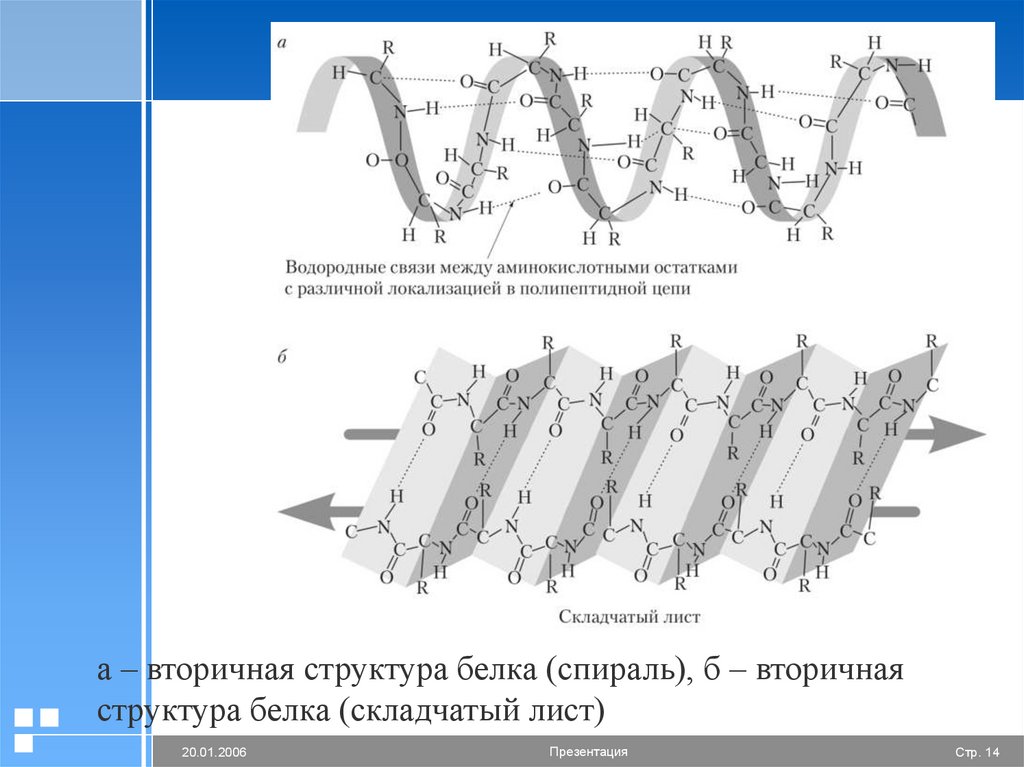
а – вторичная структура белка (спираль), б – вторичнаяструктура белка (складчатый лист)
20.01.2006
Презентация
Стр. 14
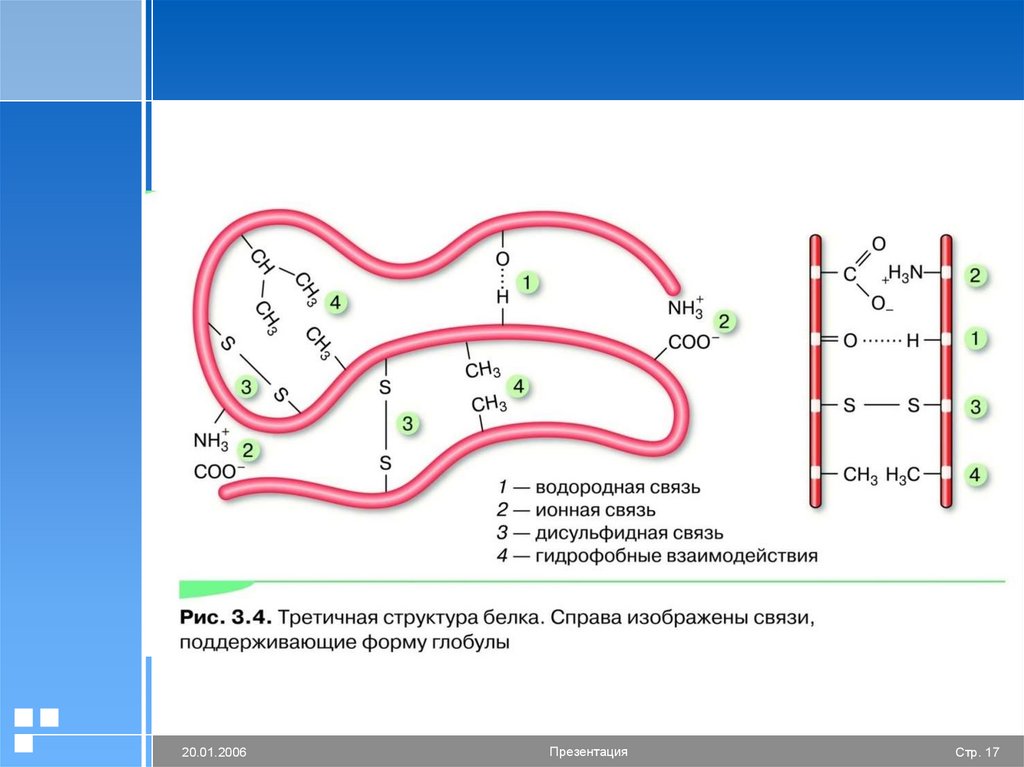
15. Третичная структура белка
Образована дисульфидными (S-S-),гидрофобными и ионными связями
20.01.2006
Презентация
Стр. 15
16.
20.01.2006Презентация
Стр. 16
17.
20.01.2006Презентация
Стр. 17
18. Четвертичная структура белка
Её образуют ионные, водородные,гидрофобные связи.
20.01.2006
Презентация
Стр. 18
19.
20.01.2006Презентация
Стр. 19
20.
20.01.2006Презентация
Стр. 20
21.
20.01.2006Презентация
Стр. 21
22.
20.01.2006Презентация
Стр. 22
23.
20.01.2006Презентация
Стр. 23
24. Денатурация белка
Денатурация белка - нарушение природнойвторичной и третичной структуры белка под
действием природных факторов (температуры,
радиации, химических веществ, и т.д.)
Виды денатурации:
Обратимая
Необратимая
20.01.2006
Презентация
Стр. 24
25. Схема денатурации белка
20.01.2006Презентация
Стр. 25
26.
20.01.2006Презентация
Стр. 26
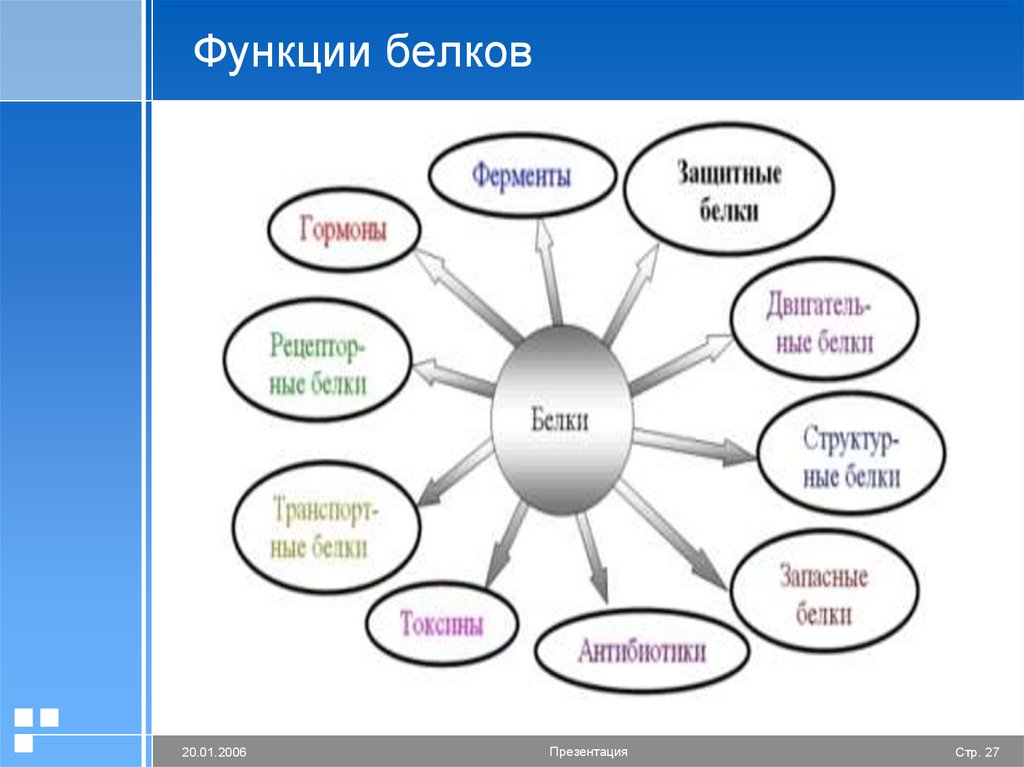
27. Функции белков
20.01.2006Презентация
Стр. 27
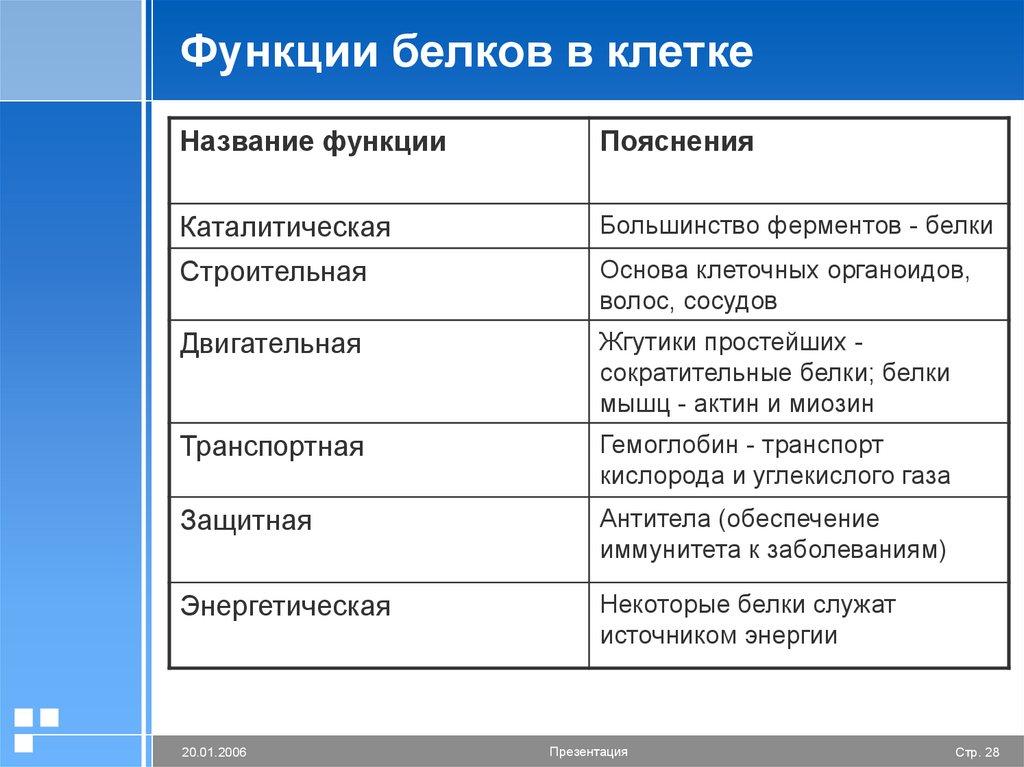
28. Функции белков в клетке
Название функцииПояснения
Каталитическая
Большинство ферментов - белки
Строительная
Основа клеточных органоидов,
волос, сосудов
Двигательная
Жгутики простейших сократительные белки; белки
мышц - актин и миозин
Транспортная
Гемоглобин - транспорт
кислорода и углекислого газа
Защитная
Антитела (обеспечение
иммунитета к заболеваниям)
Энергетическая
Некоторые белки служат
источником энергии
20.01.2006
Презентация
Стр. 28














 Биология
Биология








