Похожие презентации:
Изомерия, её виды
1.
Изомерия, её виды2.
Изомерия (от греческих слов «изос» – «равный» и «мерос» – «часть»,«доля») — явление существования химических соединений — изомеров, —
одинаковых по составу и молекулярной массе, но различающихся по
строению или расположению атомов в пространстве и по свойствам.
Й. Берцелиус
Ввёл в химию
термин
«изомерия».
Объяснение термина
«изомерия» получено на
основе теории химического
строения А. М. Бутлерова
и стереохимического учения
Я. Вант-Гоффа.
3.
Бутан С4Н10–
CH3
CH3 – CH2 – CH2 – CH3
CH3 – CH – CH3
н-бутан
изобутан
Жидкость;
реагирует с натрием;
C2H6O
кипит при +78,5 0С.
Газ;
не реагирует с натрием
кипит при -23 0С.
CH3 – CH2 – OH
CH3 – O – CH3
этиловый спирт
диметиловый эфир
4.
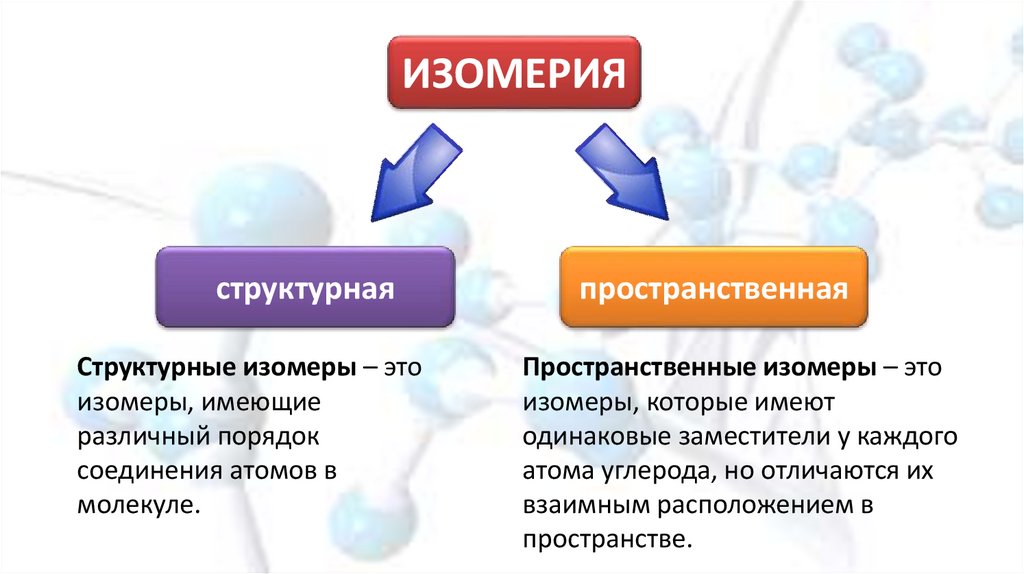
ИЗОМЕРИЯструктурная
Структурные изомеры – это
изомеры, имеющие
различный порядок
соединения атомов в
молекуле.
пространственная
Пространственные изомеры – это
изомеры, которые имеют
одинаковые заместители у каждого
атома углерода, но отличаются их
взаимным расположением в
пространстве.
5.
Структурная изомерияПоложения
функциональных
групп
Углеродного
скелета
Положения
кратных связей
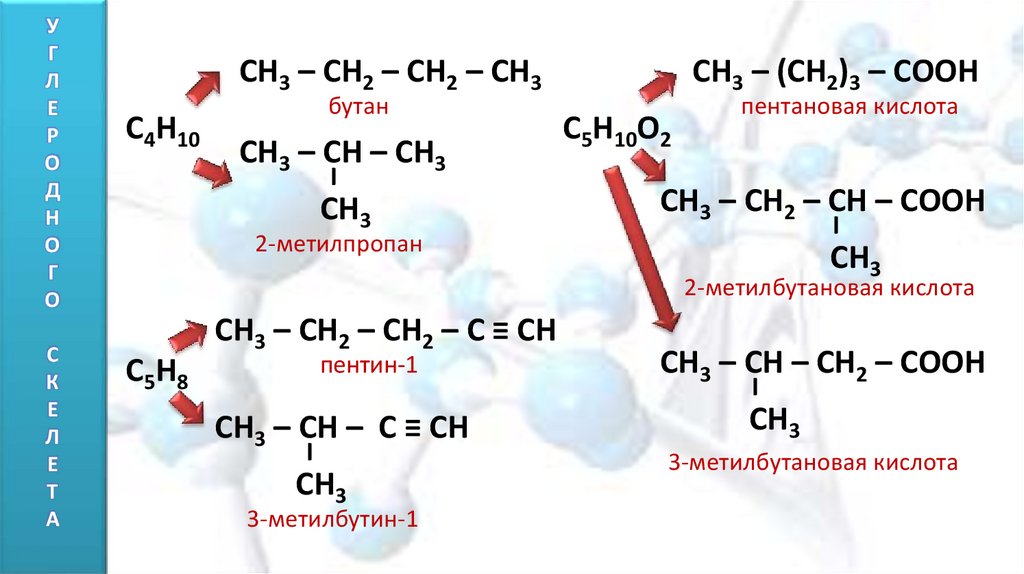
6.
С4Н10бутан
CH3 – CH – CH3
CH3 – (CH2)3 – COOH
С5Н10О2
пентановая кислота
CH3 – CH2 – CH – COOH
–
CH3
2-метилпропан
CH3
2-метилбутановая кислота
CH3 – CH2 – CH2 – C ≡ CH
пентин-1
CH3 – CH – C ≡ CH
CH3
3-метилбутин-1
CH3 – CH – CH2 – COOH
–
С5Н8
–
С
К
Е
Л
Е
Т
А
CH3 – CH2 – CH2 – CH3
–
У
Г
Л
Е
Р
О
Д
Н
О
Г
О
CH3
3-метилбутановая кислота
7.
С5Н12Опентанол-1
CH3 – CH2 – CH – CH2 – OH
CH3
2-метилбутанол-1
С4Н8О2
O
H–C
O – CH2 – CH2 – CH3
пропилметаноат
O CH3
H–C
O – CH – CH3
–
С
К
Е
Л
Е
Т
А
CH3 – (CH2)3 – CH2 – OH
–
У
Г
Л
Е
Р
О
Д
Н
О
Г
О
изопропилметаноат
8.
ПО
Л
О
Ж
Е
Н
И
Е
К
Р
А
Т
Н
Ы
Х
С
В
Я
З
Е
Й
Изомерия положения кратных связей характерна для
алкенов, алкинов и диенов.
Алкены
CH3 – CH2 – CH = CH2
Алкины
CH3 – CH2 – C ≡ CH
CH3 – CH = CH – CH3
CH3 – C ≡ C – CH3
бутен-2
бутин-2
бутен-1
бутин-1
Диены
CH2 = C = CH – CH3
бутадиен-1,2
CH2 = CH – CH = CH2
бутадиен-1,3
9.
ПО
Л
О
Ж
Е
Н
И
Е
Спирты
CH3 – CH2 – CH2 – OH
пропанол-1
бутанамин-1
CH3 – CH2 – CH – CH3
OH
NH2
пропанол-2
α-аминопропановая кислота
–
бутанамин-2
Аминокислоты
CH3 – CH – COOH
CH2 – CH2 – COOH
NH2
NH2
–
Г
Р
У
П
П
Амины
CH3 – CH2 – CH2 – CH2 – NH2
–
CH3 – CH – CH3
–
ф
У
Н
К
Ц
И
О
Н
А
Л
Ь
Н
Ы
Х
Изомерия положения функциональных групп характерна
для спиртов и аминов, аминокислот.
β-аминопропановая кислота
10.
Межклассовая изомерияСпирты и простые эфиры
CH3 – CH2 – OH
CH3 – O – CH3
этанол
диметиловый эфир
Алкины и диены
CH3 – CH2 – C ≡ CH
бутин-1
CH2 = CH – CH = CH2
бутадиен-1,3
Насыщенные одноосновные
карбоновые кислоты и сложные эфиры
CH3 – COOH
этановая кислота
HCOOCH3
метилметаноат
11.
Пространственная изомериягеометрическая
оптическая
12.
ГЕ
О
М
Е
Т
Р
И
Ч
Е
С
К
А
Я
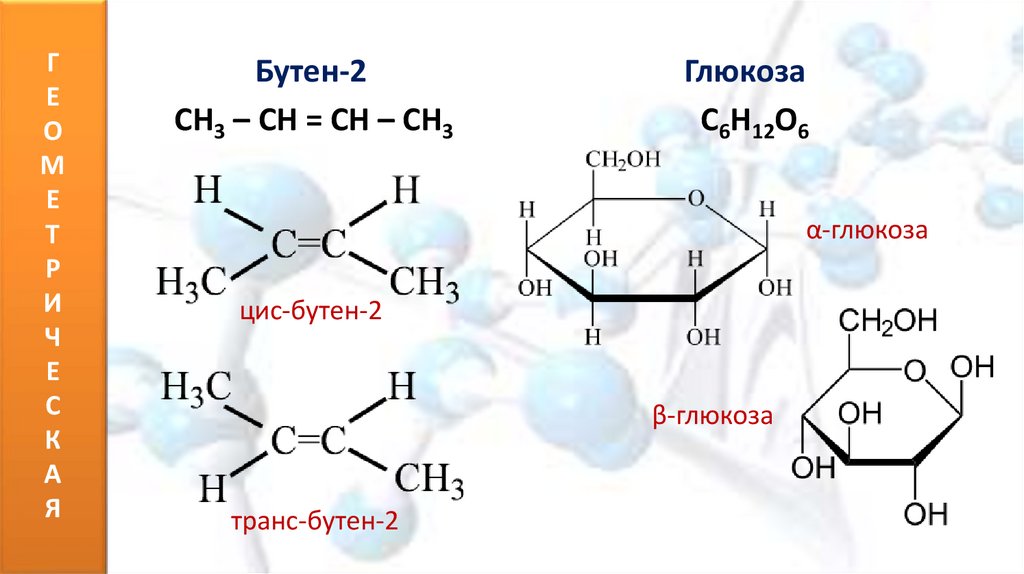
Бутен-2
CH3 – CH = CH – CH3
Глюкоза
C6H12O6
α-глюкоза
цис-бутен-2
β-глюкоза
транс-бутен-2
13.
ОП
Т
И
Ч
Е
С
К
А
Я
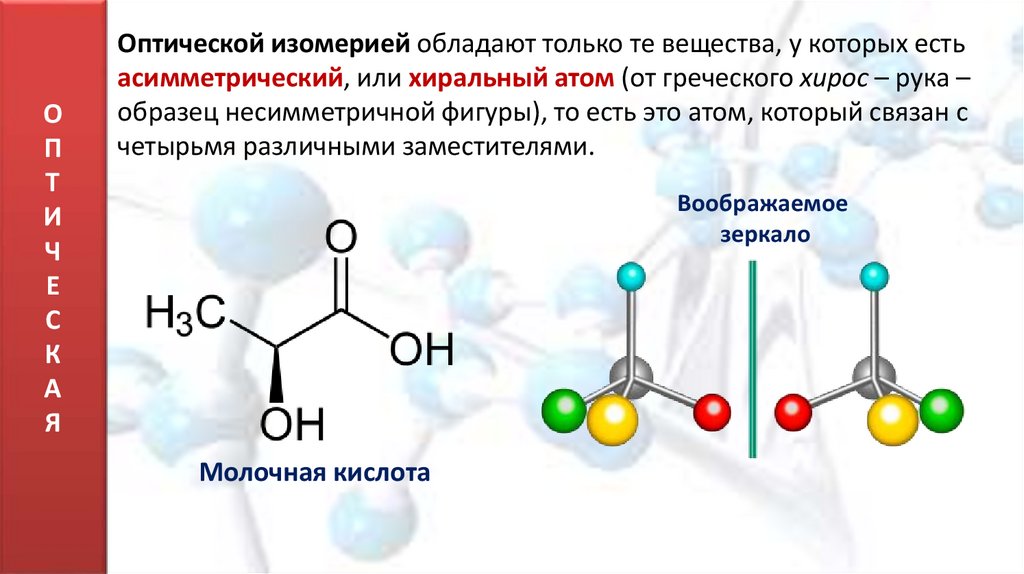
Оптической изомерией обладают только те вещества, у которых есть
асимметрический, или хиральный атом (от греческого хирос – рука –
образец несимметричной фигуры), то есть это атом, который связан с
четырьмя различными заместителями.
Воображаемое
зеркало
Молочная кислота
14.
ОП
Т
И
Ч
Е
С
К
А
Я
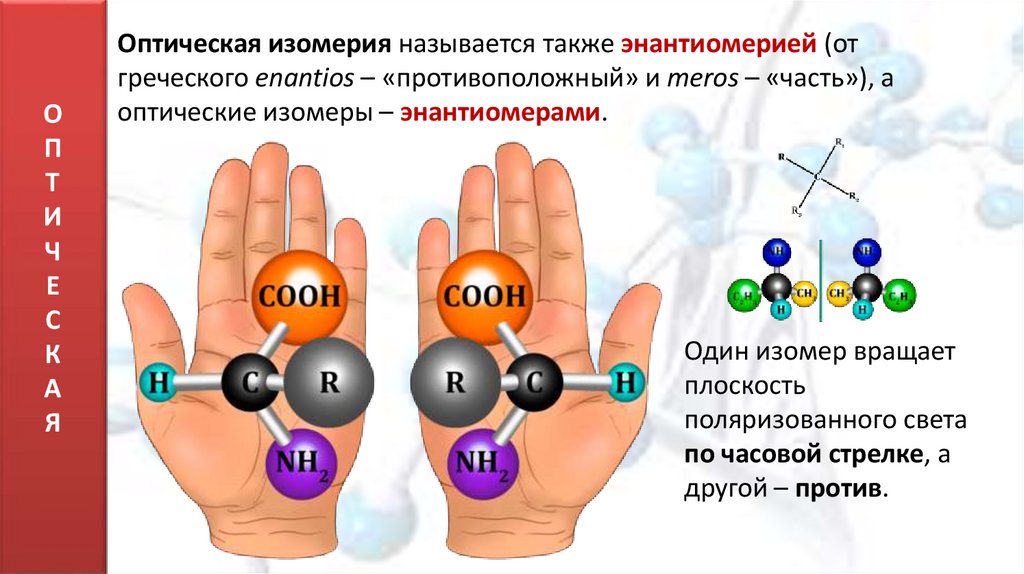
Оптическая изомерия называется также энантиомерией (от
греческого enantios – «противоположный» и meros – «часть»), а
оптические изомеры – энантиомерами.
Один изомер вращает
плоскость
поляризованного света
по часовой стрелке, а
другой – против.









 Химия
Химия








