Похожие презентации:
Витамины. Нормы потребления витаминов
1.
Лекция 8Витамины 1
2.
ОПРЕДЕЛЕНИЯВитамины (от “vita” и “амин”)
обладают следующими признаками:
- низкомолекулярные органические соединения (молек.масса В12 1355.38)
- не синтезируются организмом человека (должны поступать с пищей)
- не входят в структуру тканей
- не используются как источник энергии (не АТФ и др. …)
- необходимы в малых количествах для нормального протекания
биохимических и физиологических процессов
И НЕ ОБЯЗАТЕЛЬНО АМИНЫ!
3.
ОПРЕДЕЛЕНИЯВитаминоподобные вещества – вещества, соответствующие
признакам витаминов, но
- способны частично синтезироваться в организме
- могут входить в структуру тканей (липоевая кислота, эссенциальные
полиненасыщенные жирные кислоты и др.)
Провитамины – прямые предшественники витаминов
для вит.А – каротиноиды,
для вит. D – стерины.
4.
ОПРЕДЕЛЕНИЯАвитаминоз – комплекс симптомов, возникающих из-за достаточно
длительного и полного или почти полного отсутствия одного из витаминов.
Полиавитаминоз – недостаточность нескольких витаминов
Гиповитаминоз – частичная, но уже проявившаяся специфическим образом,
недостаточность витамина
- пищевой
- эндогенный
- дисвитаминоз (несовместимость витаминов)
Гипервитаминоз – комплекс симптомов, возникающих из-за длительного
избыточного введения витамина в организм.
Почти все случаи - для жирорастворимых витаминов.
5.
Обратить внимание:Нормы потребления витаминов разные при разной массе тела, на
разных стадиях развития и в разных физиологических состояниях
ДЛЯ ТИАМИНА (В1)
мг/день
Младенцы до 6 месяцев
– 0,2
Младенцы 7-12 месяцев
– 0,3
Дети 1-3 года
– 0,5
Дети 4-8 лет
– 0,6
Дети 9-13 лет
– 0,9
Мужчины от 14 лет и старше – 1,2
Девушки 14-18 лет
– 1,0
Женщины 19 лет и старше – 1,1
Для КР ориентироваться на цифры, указанные в презентации
6.
Вещества, препятствующие проявлению функций витаминов –антивитамины и антагонисты витаминов. Чем отличаются?
Примеры антивитаминного действия:
для тиамина (В1):
- рыба, морепродукты (фермент тиаминаза)
- кофе, чай (ухудшают всасывание)
для биотина (H):
- авидин (в белке куриного яйца)
Пример антагониста
для вит. К, стимулирующего свертывание крови – кумарин, резко замедляющий этот процесс
Но есть и синергисты
Аскорбиновая кислота (вит С) и биофлавоноиды (вит Р)
7.
История открытия витаминовС 17 века
Болезни обмена:
- Цинга (вит. С)
- Бери-бери (вит В1)
- Куриная слепота (вит А)
8.
История открытия витаминовНиколай Иванович Лунин
Экспериментально доказал необходимость
присутствия витаминов и минеральных
элементов в питании. 1880 год
Показал, что смесь состоящая только из белков,
углеводов, жиров и воды недостаточна для
питания
Гоуленд Хопкинс
Нобелевская премия по химии 1929 года
(совместно с Христаном Эйкманом). Формулировка
Нобелевского комитета:
«За открытие витаминов, стимулирующих процессы
роста».
Казимир Функ
Ввел термин
«витамины»
в 1911-1912 годах
Установил структуру
витаминов В1 и В3
9.
Классификация (с 1956г.)1) Водорастворимые
2) Жирорастворимые
3) Витаминоподобные вещества – обладающие многими, но не всеми
признаками витаминов. Частично синтезируются в организме и могут входить в структуру
тканей (оротовая кислота, пангамовая кислота, липоевая кислота, метилметионин, эссенциальные
полиненасыщенные жирные кислоты)
Условность классификации!
Витамины обозначаются буквами,
обычно в соответствии с порядком их открытия
10.
Водорастворимые витамины1) В1 (тиамин)
2) В2 (рибофлавин)
3) В3 (РР, никотинамид, никотиновая
кислота, ниацин)
4) В5 (пантотеновая кислота)
5) В6 (пиридоксин, пиридоксаль,
пиридоксамин)
6) фолиевая кислота (Вс, реже В9 )
7) В12 (кобаламин)
8) Инозит и его фосфорный эфир фитин
9) H (биотин)
10) С (аскорбиновая кислота)
11) P (полифенолы, биофлавоноиды)
Большинство водорастворимых
витаминов входят в структуру
коферментов и простетических групп
ферментов
11.
Витамин В1 (тиамин) - антиневритныйCl
-
В чистом виде впервые выделен
Б. Янсеном (1926)
Жвачные не нуждаются
пиримидиновое
кольцо
АТФ
АМФ
тиазоловое
кольцо
ТПФ-киназа
(в основном в печени и
головном мозге)
Биохимически активная форма
Тиаминпирофосфат (ТПФ или ТДФ)
12.
Биохимическая роль В1Кофермент (в виде ТПФ = ТДФ) в ряде ферментов, например:
- в пируватДГ-комплексе (цикл Кребса)
- в α-кетоглутаратДГ-комплексе (цикл Кребса)
- в транскетолазе (пентозомонофосфатный (ПМФ)-цикл)
- в ряде ферментов синтеза аминокислот с разветвленной боковой цепью (вал, лей, др.)
Схема реакции с участием В1
реакции синтеза или расщепления связей около карбонильной группы
13.
АвитаминозБери-бери (от сингальского beri – слабость, синоним: алиментарный
полиневрит) – сухая (поражение головного мозга), сердечная, острая формы
Нарушение метаболизма пировиноградной кислоты
и накопление ее в тканях.
Блокирование транскетолазных реакций в ПМФЦ –
снижение синтеза НАДФН и рибозы
Питание очищенным рисом и при алкоголизме
Паралич и судороги конечностей
Слева - голубь при развившемся
авитаминозе В1;
Справа – он же через 3 часа после
введения 4 мг фракции
из дрожжей, содержащей B1
14.
Суточная потребность В1 1 – 1,2 мгГиповитаминоз витамина В1 начинается если взрослый человек получает половину
нормального количества витамина в течение 5-6 дней
Основные источники витамина В1
- дрожжи
- рисовые и мучные отруби
- гречиха
- соя
- ржаная мука
- яичный желток
- печень, почки, мозг, свинина, говядина
В кислых растворах
гораздо устойчивее к нагреванию,
чем в щелочных
15.
В2 (рибофлавин)(от лат. flavus – желтый)
(флавин)
16.
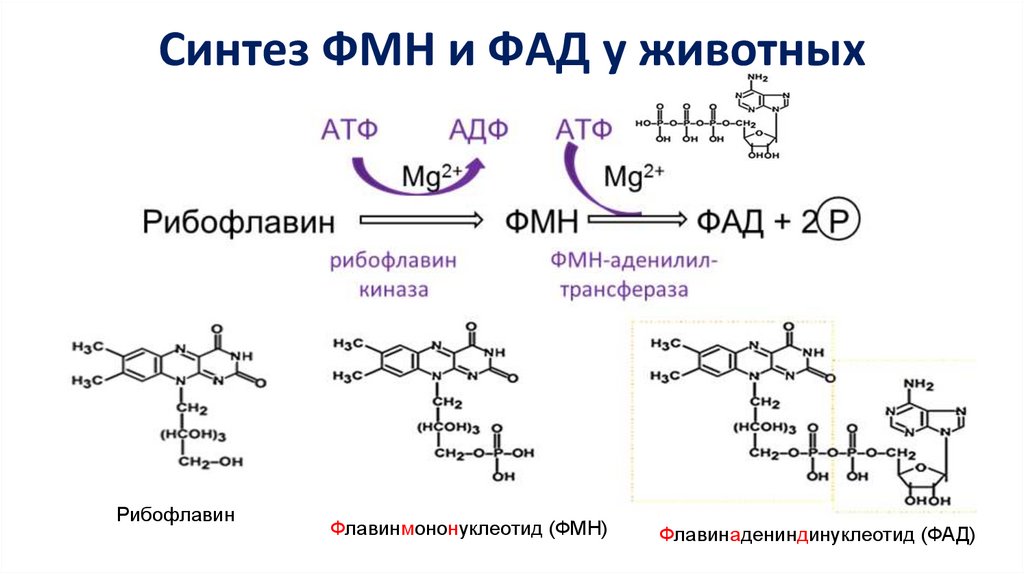
Синтез ФМН и ФАД у животныхРибофлавин
Флавинмононуклеотид (ФМН)
Флавинадениндинуклеотид (ФАД)
17.
Биохимическая роль В2:работает в простетических группах ФМН и ФАД
ФМН
ФАД
Окисленное
состояние
Восстановленное
состояние
ФМНН2
ФАДН2
18.
Биохимическая роль В2:работает в простетических группах ФМН и ФАД
ФМН
ФАД
Окисленное
состояние
Восстановленное
состояние
ФМНН2
ФАДН2
19.
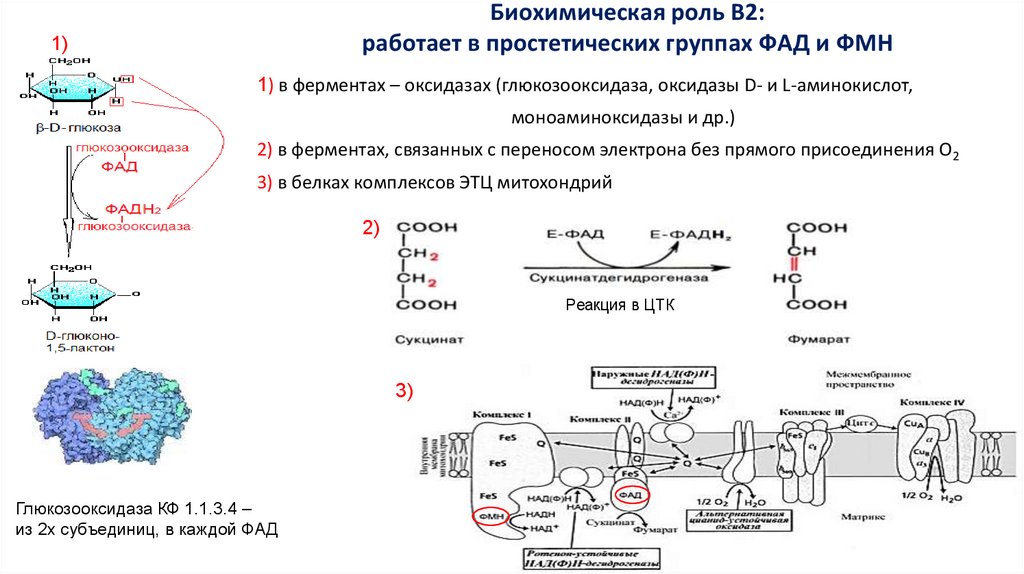
Биохимическая роль В2:работает в простетических группах ФАД и ФМН
1)
1) в ферментах – оксидазах (глюкозооксидаза, оксидазы D- и L-аминокислот,
моноаминоксидазы и др.)
2) в ферментах, связанных с переносом электрона без прямого присоединения О2
3) в белках комплексов ЭТЦ митохондрий
2)
Реакция в ЦТК
3)
Глюкозооксидаза КФ 1.1.3.4 –
из 2х субъединиц, в каждой ФАД
20.
Источники и недостаточность витамина В2СУТОЧНАЯ НОРМА:
Взрослые 2-4 мг
Дети 1-2 мг
ИСТОЧНИКИ:
Молоко, мясо, хлеб,
Меньше – растительная пища
КАРТИНА ГИПО- И АВИТАМИНОЗА:
- “заеды” на губах;
- специфическое воспаление языка глоссит;
- изменения в структуре глаза (кератиты, катаракта);
- заболевания кожи (себоррея, псориаз)
21.
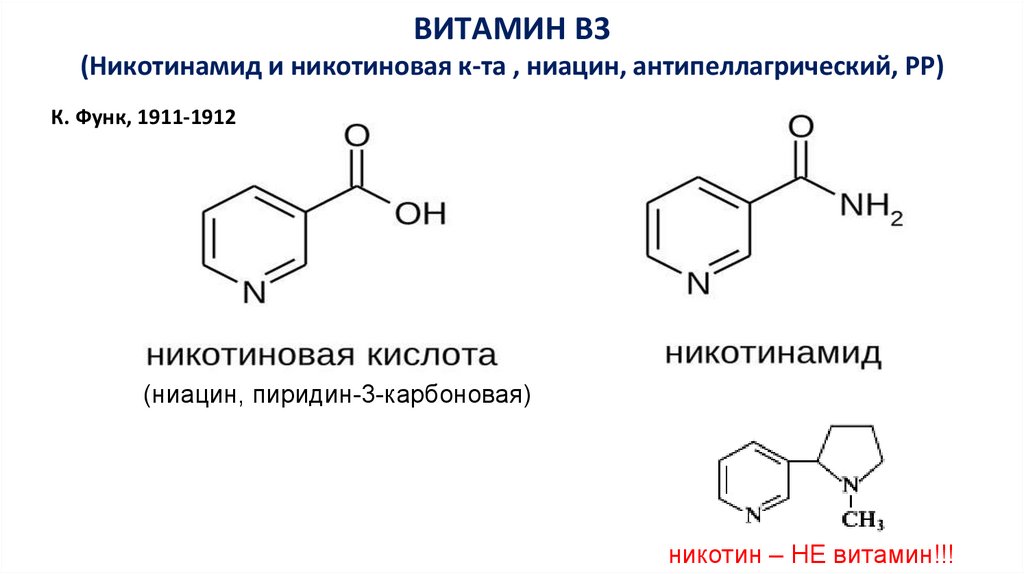
ВИТАМИН В3(Никотинамид и никотиновая к-та , ниацин, антипеллагрический, PP)
К. Функ, 1911-1912
(ниацин, пиридин-3-карбоновая)
никотин – НЕ витамин!!!
22.
Биохимическая роль В3 –работают в составе коферментов НАД и НАДФ
Никатинамидадениндинуклеотид (НАД+)
Никатинамидадениндинуклеотид- фосфат (НАДФ+)
23.
Биохимическая роль В3 –работают в составе коферментов НАД и НАДФ
окисленный
восстановленный
Никотинамидные дегидрогеназы нужны для более чем 150 реакций:
- Дегидрирования (окисления),
- N-алкилирования,
- изомеризации,
- для клеточного дыхания и энергетического обмена…
24.
1. Прямое восстановительное аминированиефермент – глутаматдегидрогеназа (глутаматДГ)
Активный центр
формируется при
взаимодействии двух
отдельных доменов
25.
Примеры реакций с НАДНАД – реакции окисления-восстановления (дыхание)
НАДФ – реакции синтеза (синтез жирных кислот, пентоз)
26.
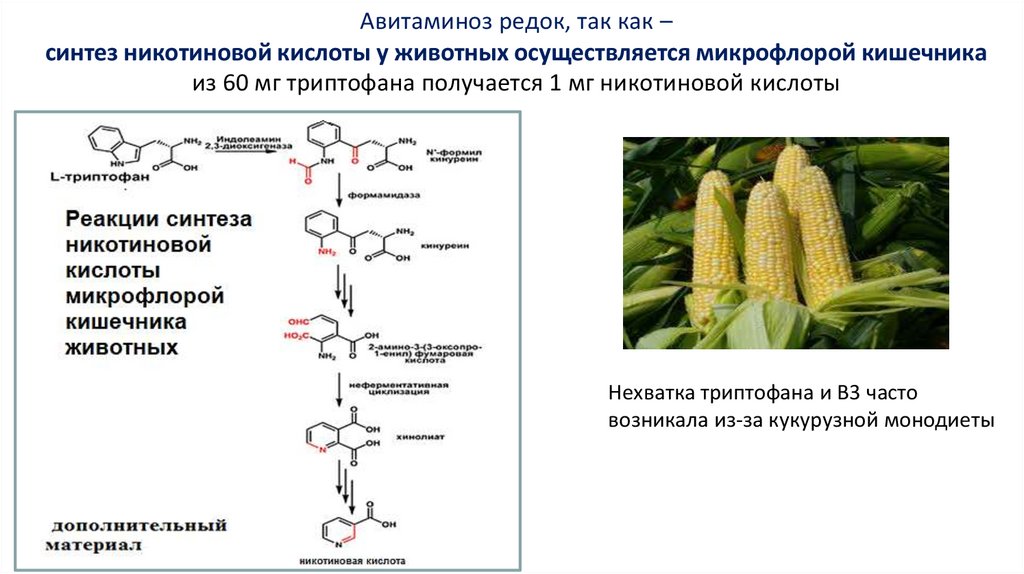
Авитаминоз редок, так как –синтез никотиновой кислоты у животных осуществляется микрофлорой кишечника
из 60 мг триптофана получается 1 мг никотиновой кислоты
Нехватка триптофана и В3 часто
возникала из-за кукурузной монодиеты
27.
Авитаминоз никотинамида. Пеллагра(итал. Pelle agra – шершавая кожа)
1) Симметричные дерматиты на открытых
солнцу участках
2) Специфические стоматиты, гингивиты,
“черный язык” со вздутиями и трещинами
3) Расстройства пищеварения (диарея)
4) Расстройства нервной системы (деменция)
28.
Источники и потребность в никотинамиде илиникотиновой кислоте
• Источники: сухие пивные и пекарские дрожжи, зерновые
продукты.
• Потребность 6,5 мг на 1000 ккал пищи
(в среднем 15-22 мг в сут)
29.
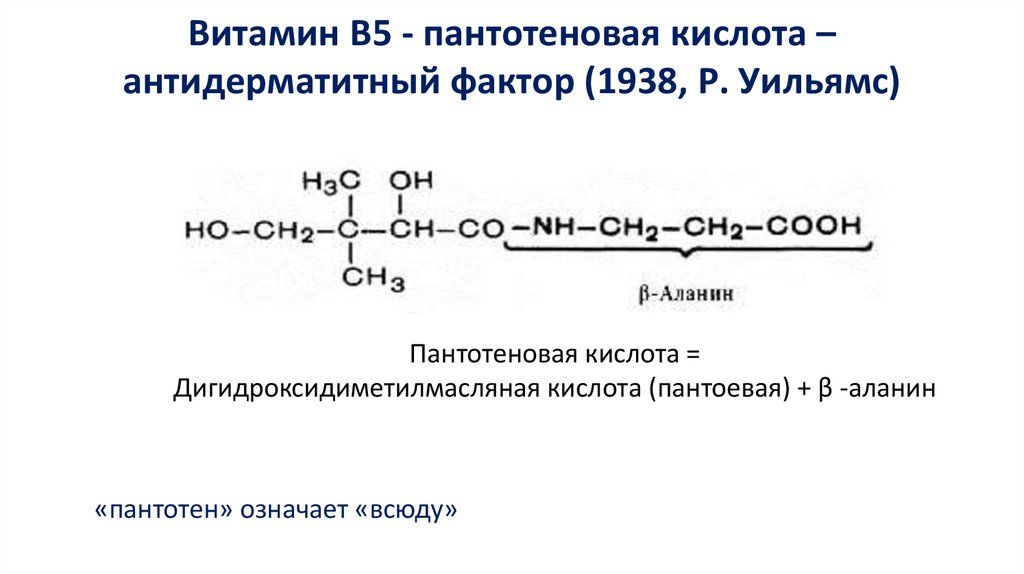
Витамин В5 - пантотеновая кислота –антидерматитный фактор (1938, Р. Уильямс)
Пантотеновая кислота =
Дигидроксидиметилмасляная кислота (пантоевая) + β -аланин
«пантотен» означает «всюду»
30.
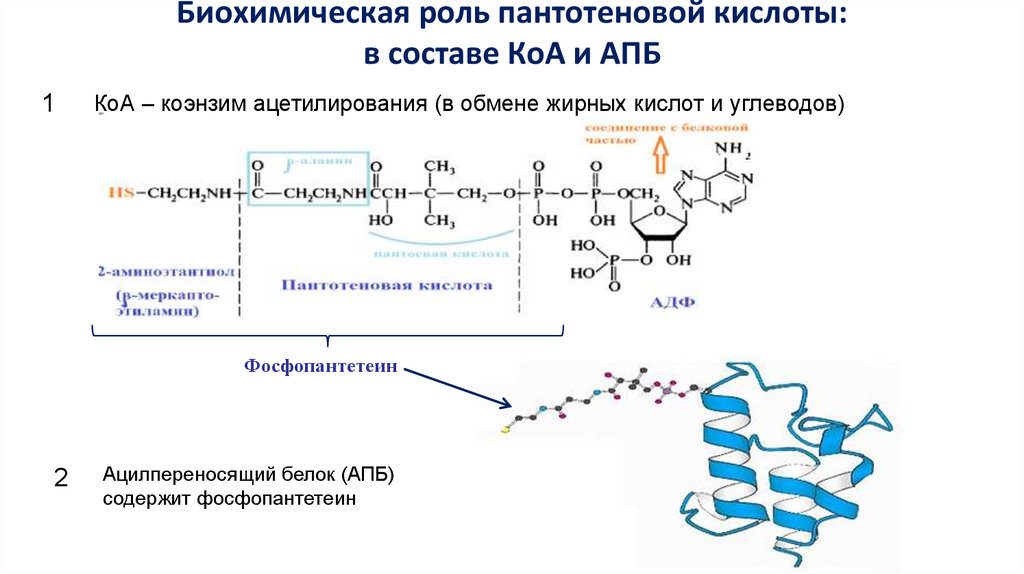
Биохимическая роль пантотеновой кислоты:в составе КоА и АПБ
1
КоА – коэнзим ацетилирования (в обмене жирных кислот и углеводов)
Фосфопантетеин
2
Ацилпереносящий белок (АПБ)
содержит фосфопантетеин
31.
Биохимическая роль пантотеновой кислоты:в составе КоА и АПБ
В составе КоА работает с ферментами ацетилирования:
- в ЦТК – в пируватдегидрогеназной системе и α-кетоглутаратдегидрогеназной системе
- в β-окислении жирных кислот
- в других реакциях ацетилирования – присоединения СН3СО-групп
В составе АПБ
- в синтезе жирных кислот
32.
Авитаминоз и источники В5ИСТОЧНИКИ: “вездесущая”, особенно много
- в пчелином маточном молочке
- в пивных дрожжах.
Частично, но недостаточно, синтезируется
микрофлорой кишечника человека
СУТОЧНАЯ ПОТРЕБНОСТЬ:
10 мг
Пантотеновая кислота
Пантенол
АВИТАМИНОЗ:
дерматиты,
выпадение волос,
дегенеративные изменения миелиновой оболочки спинного
мозга.
(Миелин – это комплекс, основная часть которого – липид
галактоцереброзид).
33.
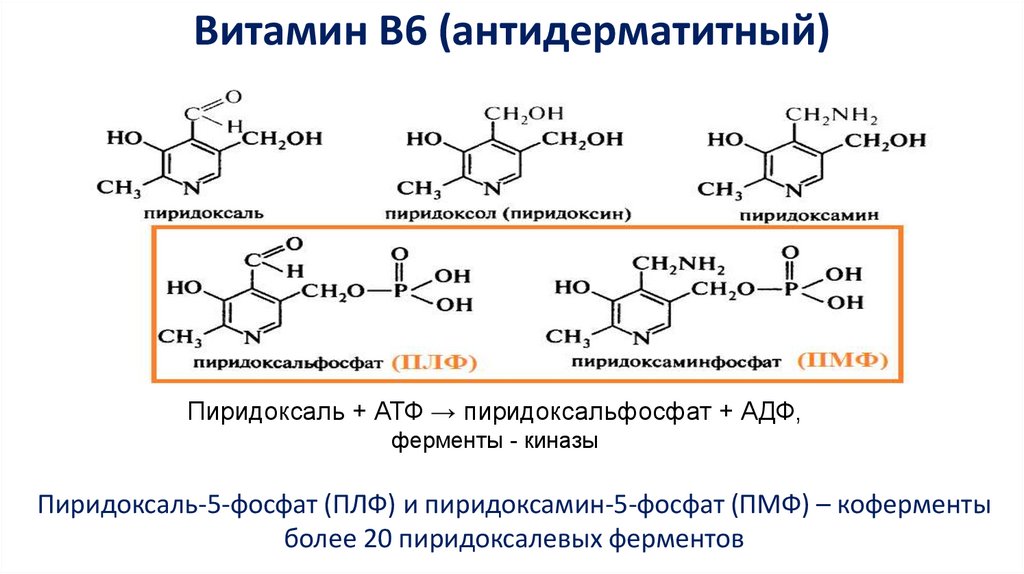
Витамин В6 (антидерматитный)Пиридоксаль + АТФ → пиридоксальфосфат + АДФ,
ферменты - киназы
Пиридоксаль-5-фосфат (ПЛФ) и пиридоксамин-5-фосфат (ПМФ) – коферменты
более 20 пиридоксалевых ферментов
34.
Биохимическая роль В6 –коферменты в фосфорилированных формах
Более 20 пиридоксалевых ферментов
- Аминотрансферазы (перенос аминогруппы при переаминировании)
и другие реакции в лекции 3
-
Декарбоксилазы аминокислот (необратимое отщепление СО2 от СООН-группы аминокислот с
образованием биогенных аминов)
Ферменты неокислительного дезаминирования серина и треонина, окисления триптофана,
Ферменты превращения серосодержащих аминокислот,
Взаимопревращение серина и глицина
Ферменты синтеза δ (дельта)-аминолевулиновой кислоты – предшественника синтеза гема
35.
Источники и суточная потребность витамина В6Источники: Бобовые, картофель, мясо, печень
Потребность: 2 мг, но точно не установлено,
т.к. частично синтезируются микрофлорой кишечника.
Авитаминоз:
Угнетение выработки эритроцитов, воспалительные процессы кожи,
замедление роста, нарушение обмена триптофана и др. аминокислот
36.
Итог:1) В1 (тиамин) – кофермент, реакции синтеза или расщепления связей
около карбонильной группы;
2) В2 (рибофлавин) – простетическая группа, окислительновосстановительные реакции, получение АТФ;
3) В3 (РР, никотинамид, никотиновая кислота, ниацин) –
кофермент, более 150 окислительно-восстановительных реакций;
4) В5 (пантотеновая кислота) – кофермент, обмен жирных кислот и ЦТК;
5) В6 (пиридоксаль, пиридоксамин) – кофермент, обмен аминокислот.





























 Биология
Биология








