Похожие презентации:
Амины
1.
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ«КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ ПРОФЕССОРА В.Ф. ВОЙНОЯСЕНЕЦКОГО»
МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
ТЕМА: «АМИНЫ»
Преподаватель химии: Агафонова Н.В.
2.
План лекции1. Состав и классификация аминов.
2. Номенклатура аминов.
3. Изомерия аминов.
4. Физические свойства.
5. Химические свойства.
6. Анилин.
7. Способы получения.
8. Применение аминов.
3.
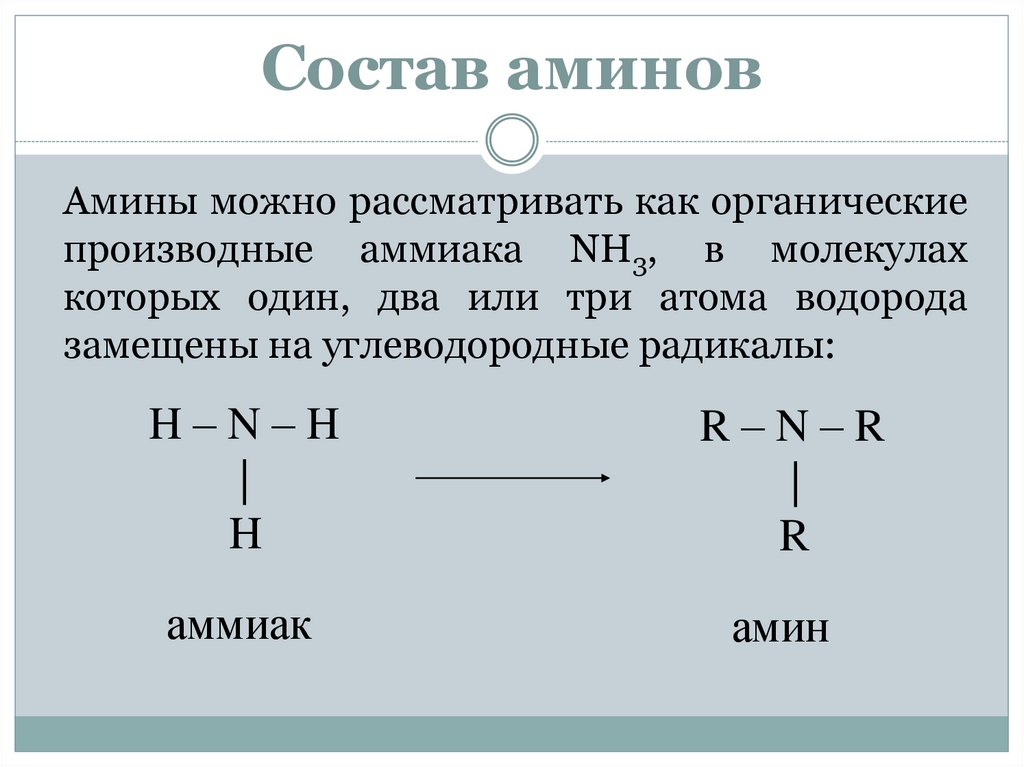
Состав аминовАмины можно рассматривать как органические
производные аммиака NH3, в молекулах
которых один, два или три атома водорода
замещены на углеводородные радикалы:
H–N–H
|
H
R–N–R
|
R
аммиак
амин
4.
RNH2R2NH
R3N
Функциональная группа
NH2 называется
аминогруппой.
5.
Классификация аминов1. От природы радикала.
2. От числа замещенных на радикалы
атомов водорода.
6.
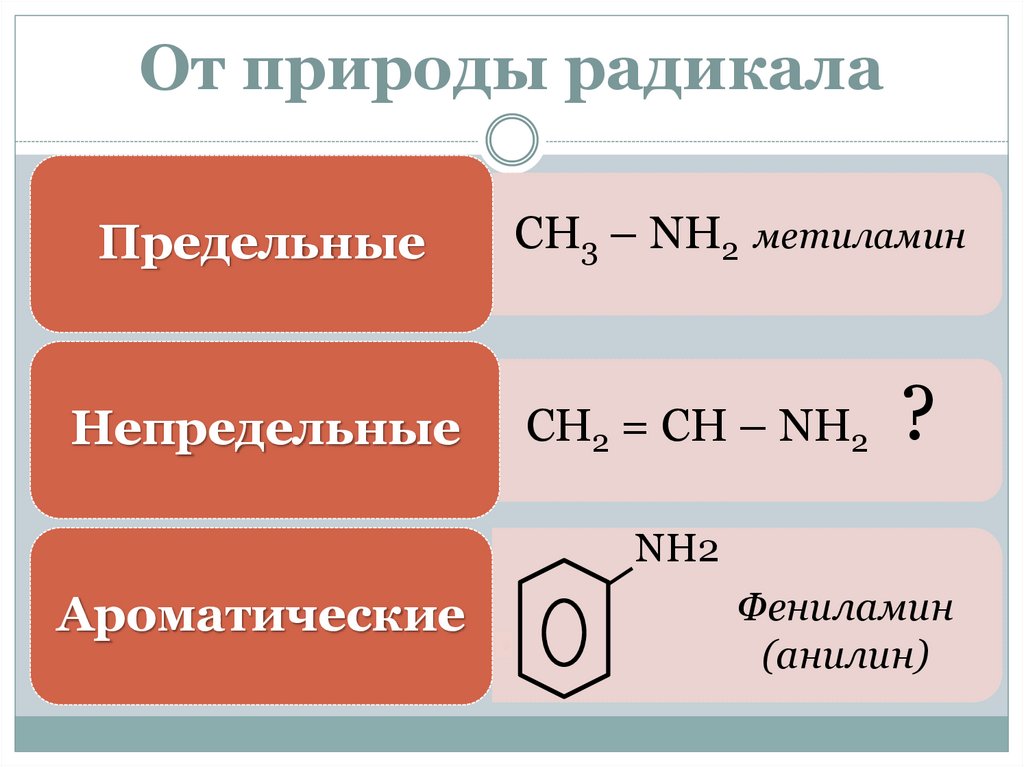
От природы радикалаПредельные
СН3 – NH2 метиламин
Непредельные
СН2 = СН – NH2
?
NH2
Ароматические
Фениламин
(анилин)
7.
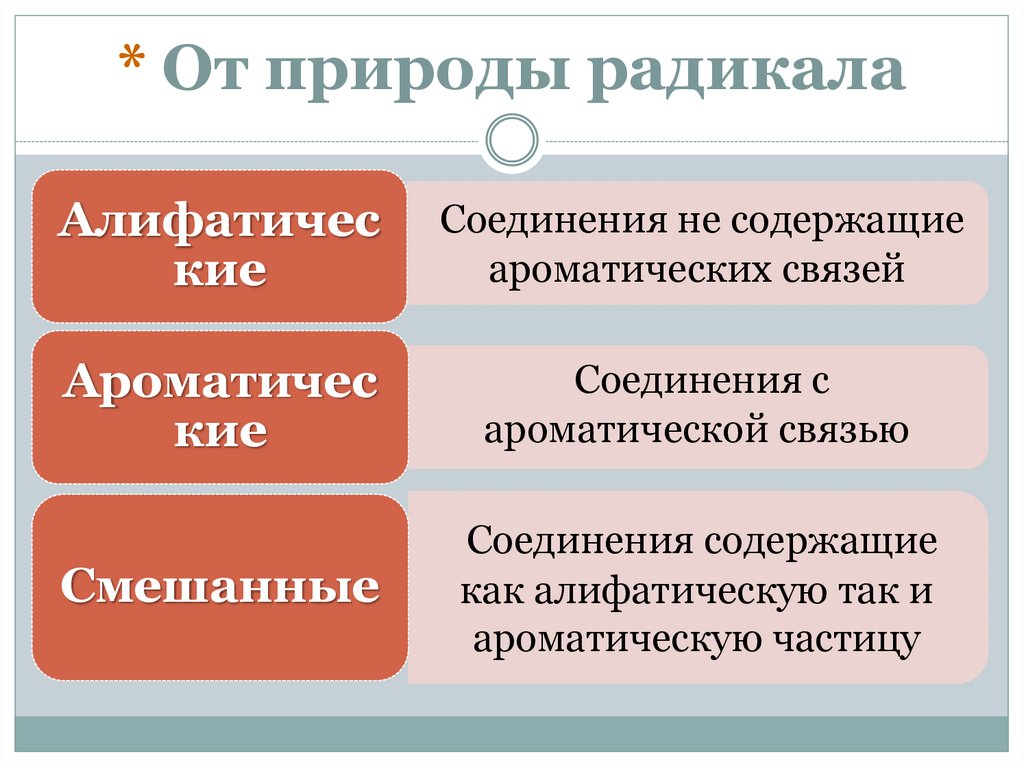
* От природы радикалаАлифатичес
кие
Соединения не содержащие
ароматических связей
Ароматичес
кие
Соединения с
ароматической связью
Смешанные
Соединения содержащие
как алифатическую так и
ароматическую частицу
8.
Смешанные аминыC6H5-NH-СН3 Метилфениламин
C6H5-N(СН3)2 Диметилфениламин
9.
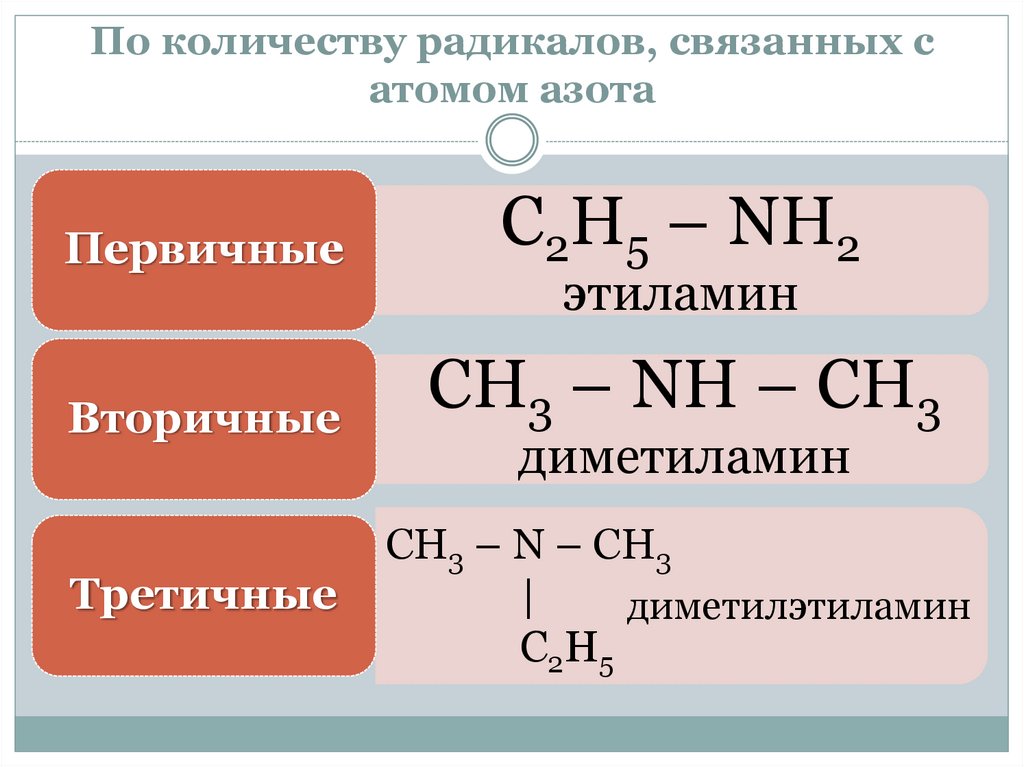
По количеству радикалов, связанных сатомом азота
Первичные
С2Н5 – NH2
Вторичные
СН3 – NH – СН3
Третичные
этиламин
диметиламин
СН3 – N – СН3
|
диметилэтиламин
С2Н5
10.
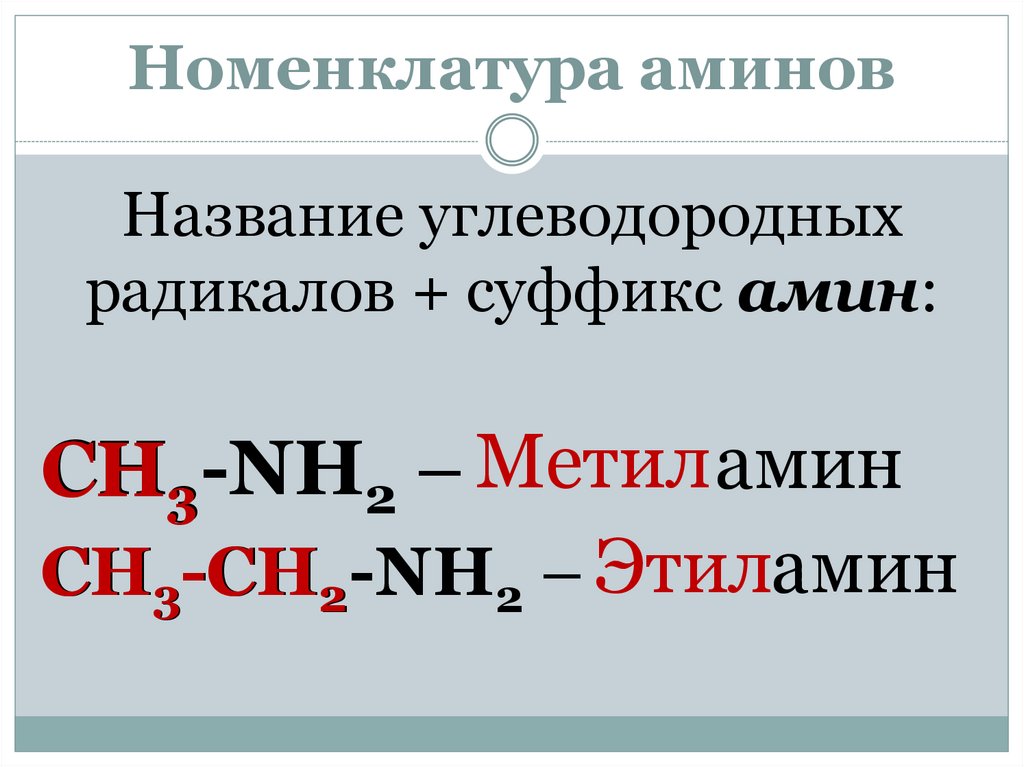
Номенклатура аминовНазвание углеводородных
радикалов + суффикс амин:
CH3-NH2 – Метиламин
CH3-CH2-NH2 – Этиламин
11.
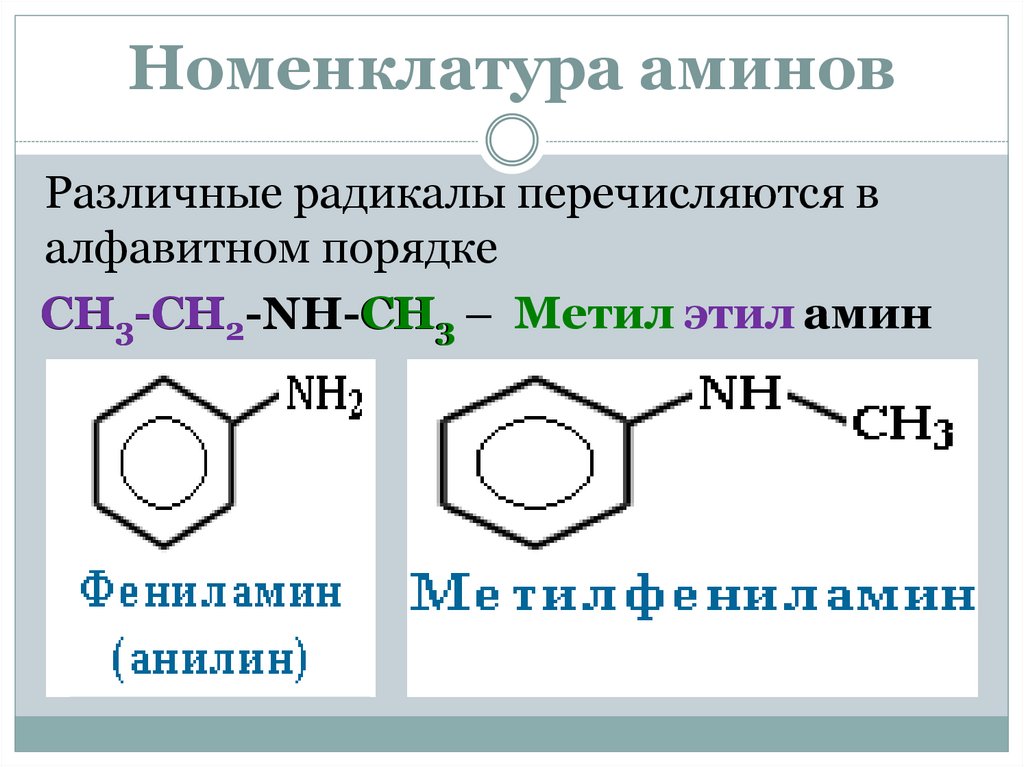
Номенклатура аминовРазличные радикалы перечисляются в
алфавитном порядке
CH3-CH2-NH-CH
CH3 – Метил этил амин
12.
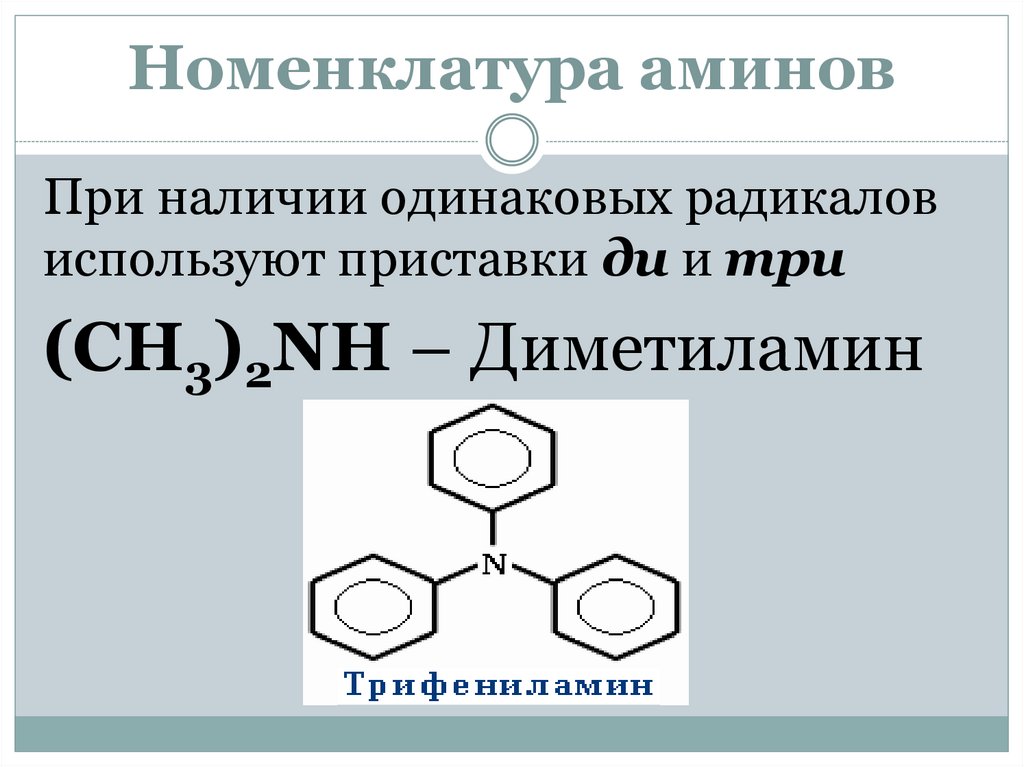
Номенклатура аминовПри наличии одинаковых радикалов
используют приставки ди и три
(CH3)2NH – Диметиламин
13.
Номенклатура аминовАмины часто называют как производные
углеводородов. В этом случае аминогруппа
указывается в названии суффиксами амин (одна
группа -NH2), диамин (две группы -NH2) и т.д. с
добавлением цифр, отражающих положение этих
групп в главной углеродной цепи:
3
1
2
CH3-CH2-CH2-NH2 – Пропан амин - 1
3
4
1
2
H2N-CH
CH2-CH2-CH(NH
-CH
-CH3
2)-CH
Бутан диамин - 1, 3
14.
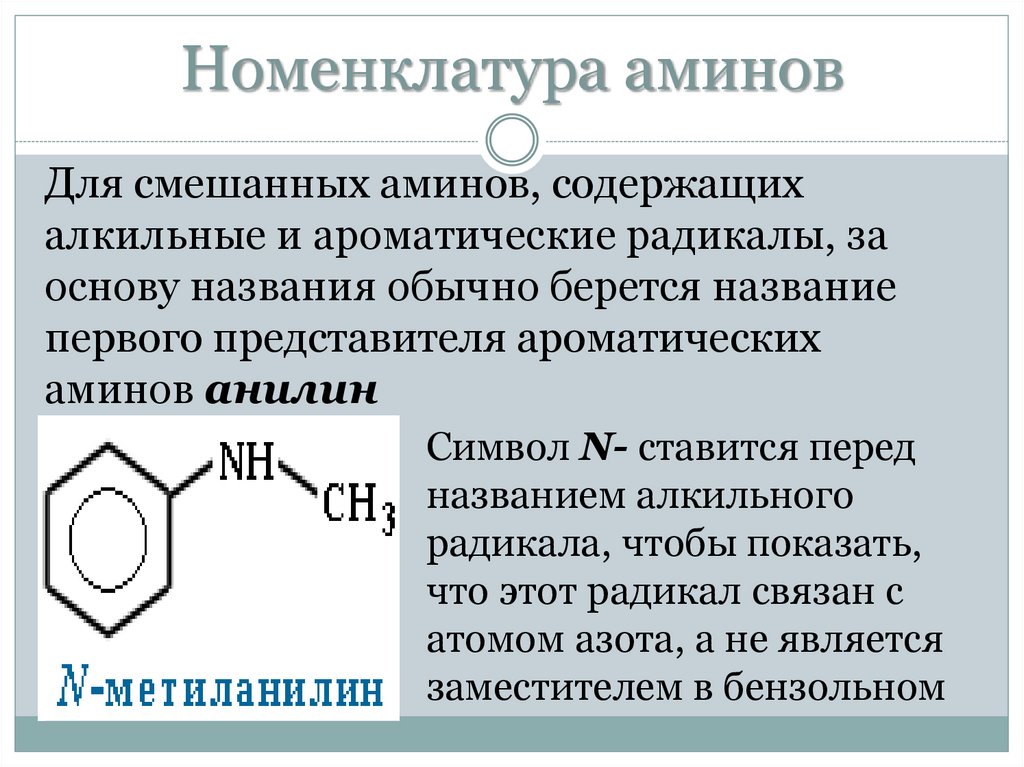
Номенклатура аминовДля смешанных аминов, содержащих
алкильные и ароматические радикалы, за
основу названия обычно берется название
первого представителя ароматических
аминов анилин
Символ N- ставится перед
названием алкильного
радикала, чтобы показать,
что этот радикал связан с
атомом азота, а не является
заместителем в бензольном
15.
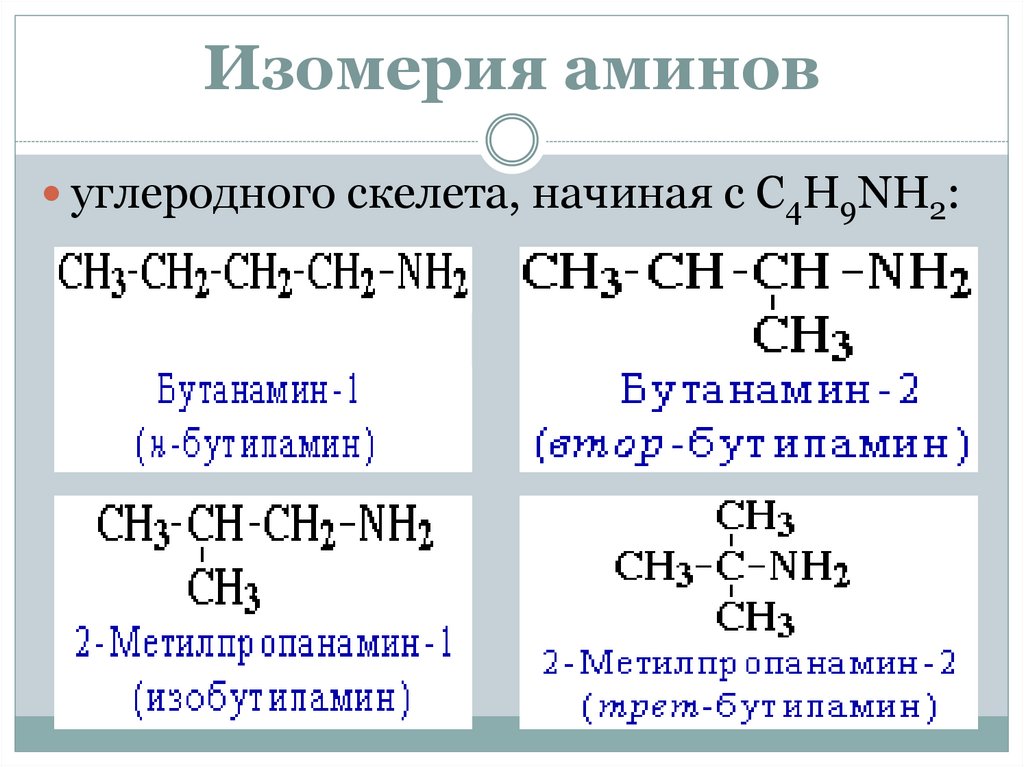
Изомерия аминовуглеродного скелета, начиная с С4H9NH2:
16.
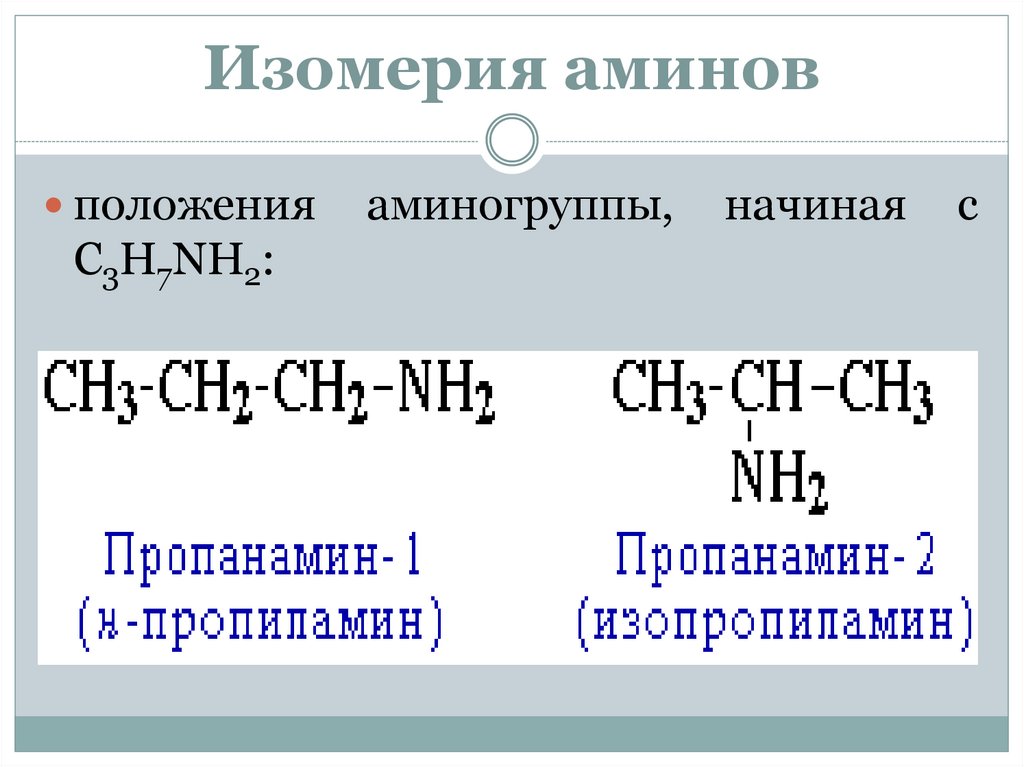
Изомерия аминовположения
С3H7NH2:
аминогруппы,
начиная
с
17.
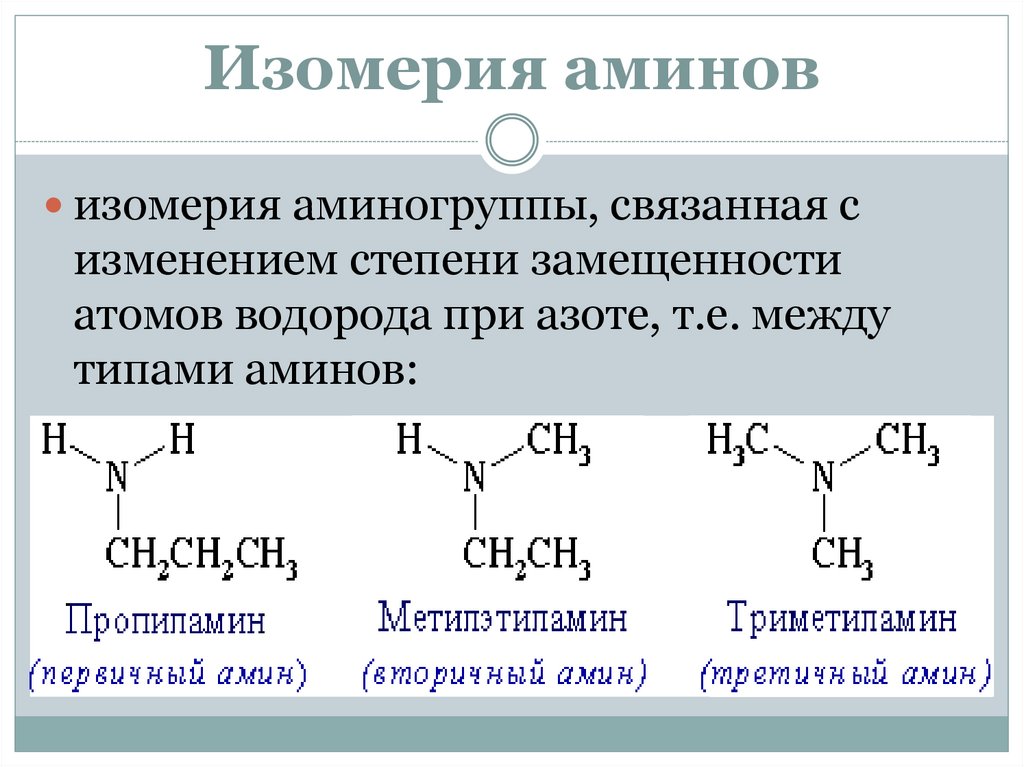
Изомерия аминовизомерия аминогруппы, связанная с
изменением степени замещенности
атомов водорода при азоте, т.е. между
типами аминов:
18.
Физические свойства аминовПри обычной температуре только низшие
алифатические амины CH3NH2, (CH3)2NH и
(CH3)3N – газы (с запахом аммиака);
Средние гомологи – жидкости (с резким рыбным
запахом);
Высшие амины – твердые вещества без запаха.
Ароматические – бесцветные высококипящие
жидкости или твердые вещества.
19.
Химические свойстваПо химическим свойствам
амины похожи на аммиак и
проявляют основные свойства.
Причина основных свойств
аммиака – наличие у атома азота
неподеленной электронной пары,
которая участвует в образовании
донорно-акцепторной связи с
ионом водорода.
20.
Для аминов характерны ярковыраженные основные свойства
(за что их часто называют
органическими основаниями)
21.
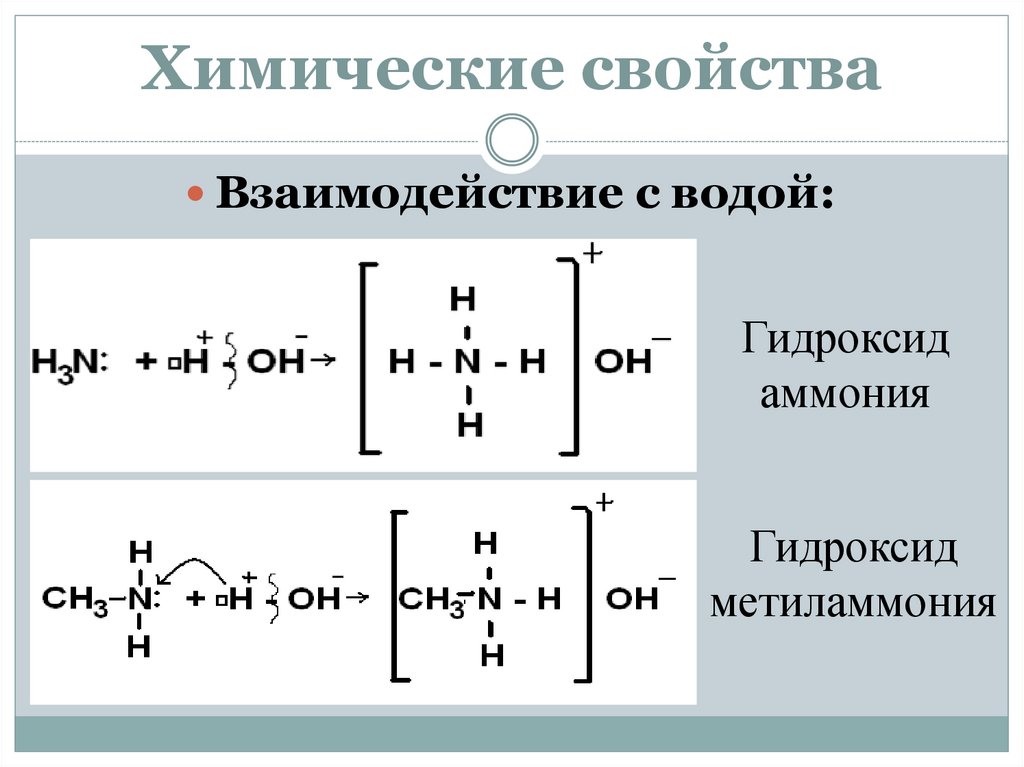
Химические свойстваВзаимодействие с водой:
Гидроксид
аммония
Гидроксид
метиламмония
22.
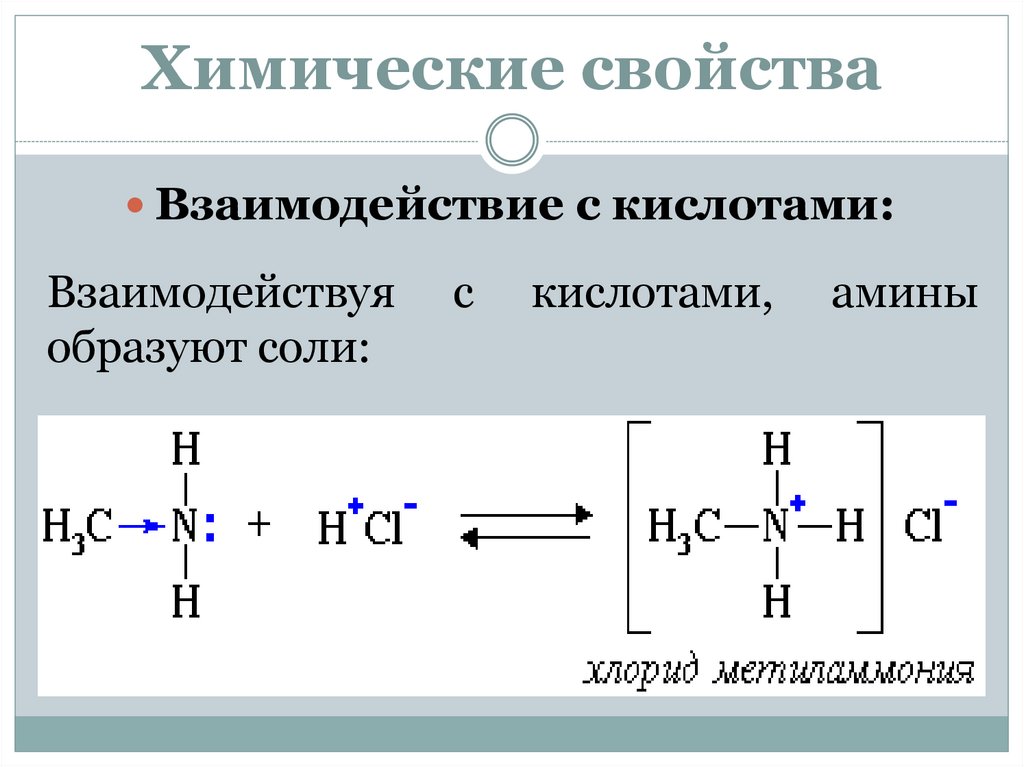
Химические свойстваВзаимодействие с кислотами:
Взаимодействуя
образуют соли:
с
кислотами,
амины
23.
Соли аминов – твердые вещества, хорошорастворимые в воде. Щелочи (более
сильные основания) легко вытесняют из
них амины:
24.
Химические свойстваРеакция горения:
Реакция горения (полного окисления)
аминов на примере метиламина:
4СH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2
25.
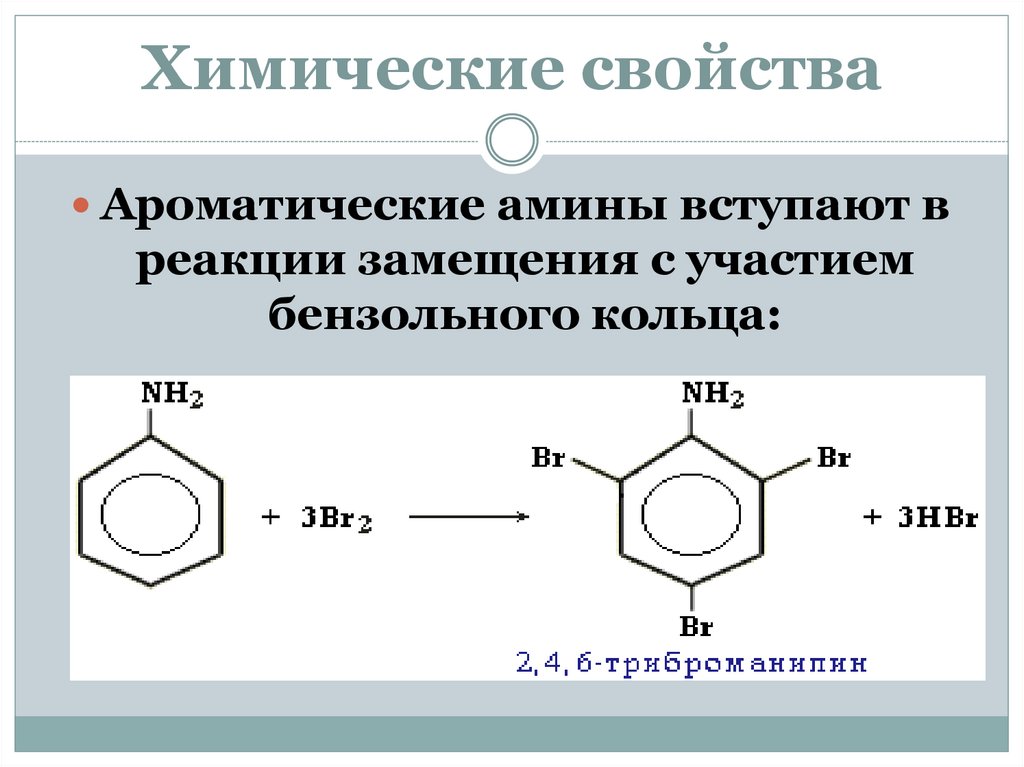
Химические свойстваАроматические амины вступают в
реакции замещения с участием
бензольного кольца:
26.
Анилин (фениламин С6H5NH2)Бесцветная маслянистая
жидкость, малорастворимая
в воде. На воздухе легко
окисляется, приобретая
вначале светло-коричневы, а
затем темный цвет.
Анилин – сильное ядовитое
вещество.
27.
Анилин оказывает негативное воздействие нацентральную нервную систему. Вызывает
кислородное голодание организма за счёт
изменений эритроцитов.
В организм анилин проникает при дыхании, в
виде паров, а также через кожу и слизистые
оболочки. Всасывание через кожу усиливается
при нагреве воздуха или приёме алкоголя.
28.
Получение аминовВосстановление нитросоединений:
Важнейший ароматический амин – анилин –
образуется при восстановлении нитробензола
Эта реакция носит имя русского
химика Н.Н. Зинина,
осуществившего ее впервые в
1842 г.
29.
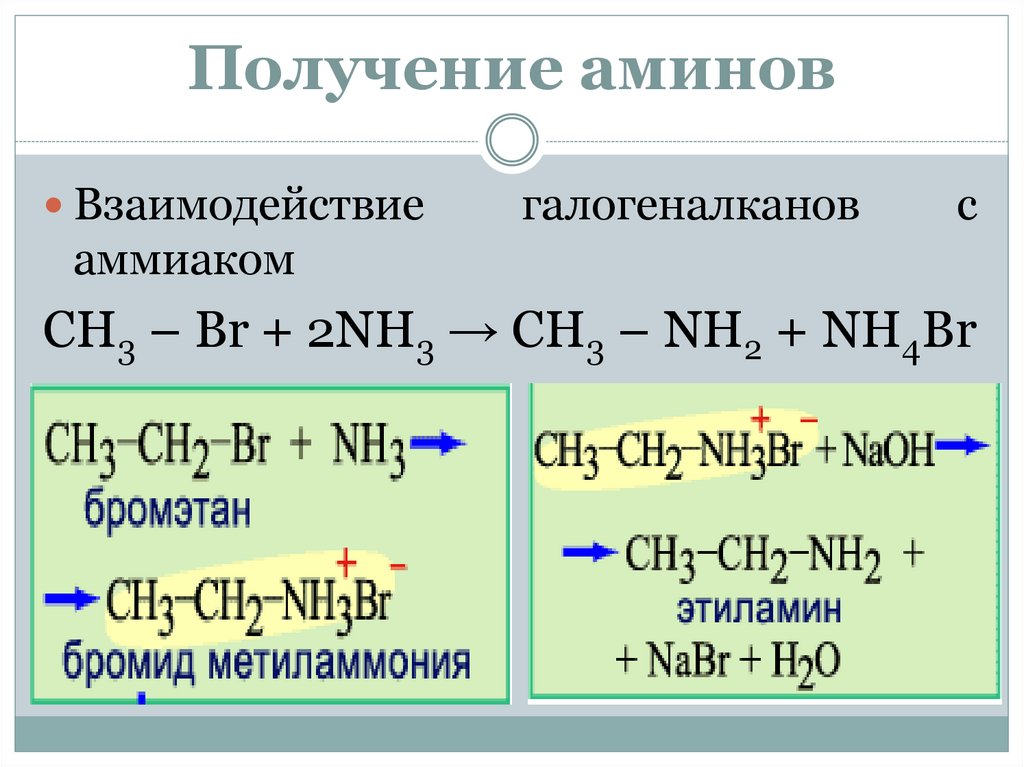
Получение аминовВзаимодействие
галогеналканов
с
аммиаком
СН3 – Br + 2NH3 → CH3 – NH2 + NH4Br
30.
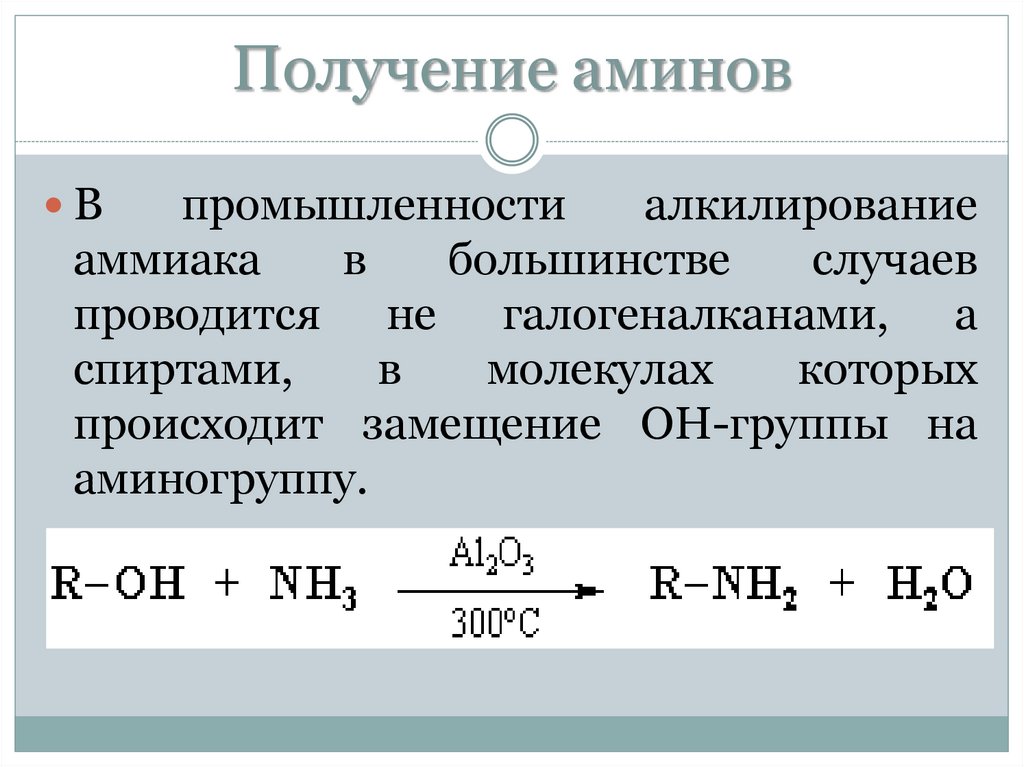
Получение аминовВ
промышленности
алкилирование
аммиака
в
большинстве
случаев
проводится не галогеналканами, а
спиртами,
в
молекулах
которых
происходит замещение ОН-группы на
аминогруппу.
31.
Применение32.
Контрольные вопросыКакие органические соединения называются
аминами?
Как даются названия аминам по международной
номенклатуре?
Напишите структурную формулу 2-метил-3,3диэтилоктанамин-1. Составьте изомеры данного
вещества.
Пропишите химические свойства аминов на
прмере 3-метилбутанамин-1
33.
ЛитератураОсновная литература:
1. Габриелян, О. С. Химия. 10 класс. Базовый уровень : учебник / О. С.
Габриелян. - 4-е изд., стер. - М. : Дрофа, 2016. - 192 с.
Дополнительная литература:
1. Грандберг, И. И. Органическая химия : учеб. для бакалавров / И. И.
Грандберг, Н. Л. Нам. - 8-е изд. - М. : Юрайт , 2013. - 608 с
Электронные ресурсы:
1. ЭБС КрасГМУ «Colibris»
2. ЭБС Консультант студента ВУЗ
3. ЭБС Консультант студента Колледж
4. ЭМБ Консультант врача
5. ЭБС Айбукс
6. ЭБС Букап
7. ЭБС Лань
8. ЭБС Юрайт
9. СПС КонсультантПлюс
10. НЭБ eLibrary
33
34.
34Спасибо за внимание


















 Химия
Химия








