Похожие презентации:
Комплексные соединения кобальта(II, III) с триэтилентетрамином в водных растворах
1.
ФГБОУ ВО «МАРИЙСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»ИНСТИТУТ ЕСТЕСТВЕННЫХ НАУК И ФАРМАЦИИ
КАФЕДРА ХИМИИ
Исса Айгуль Айдаровна
Комплексные соединения кобальта(II, III)
с триэтилентетрамином в водных растворах
Научный руководитель – к.х.н. Щеглова Н.В.
Йошкар-Ола
2025
1
2.
23.
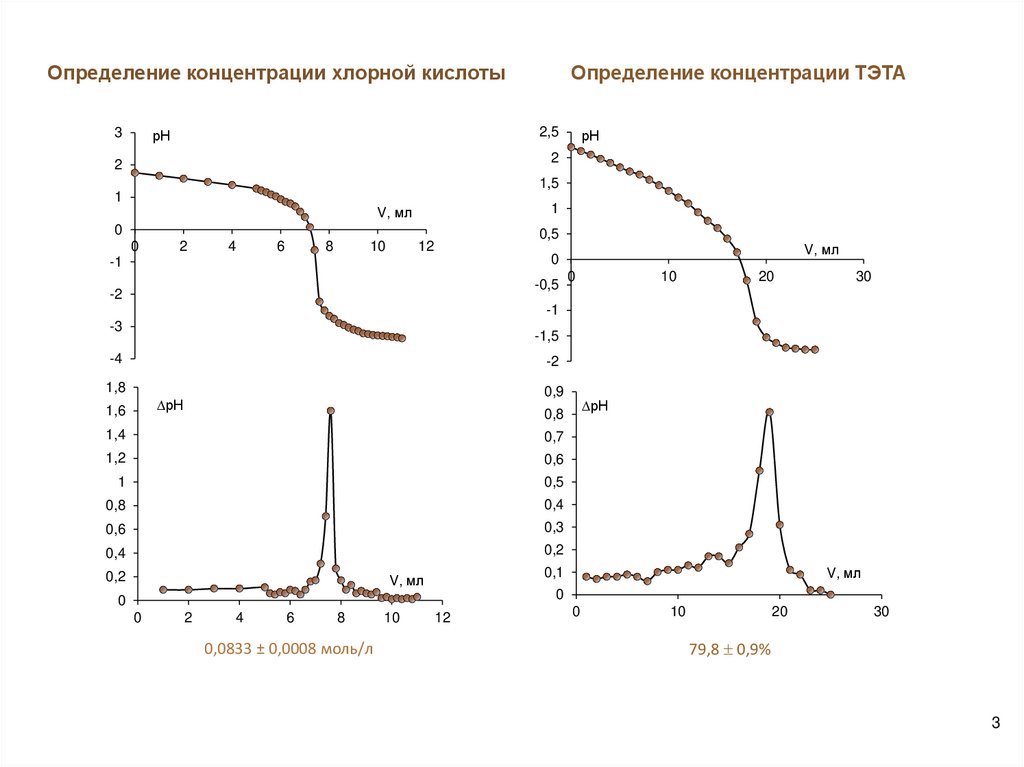
Определение концентрации хлорной кислоты3
Определение концентрации ТЭТА
2,5
рН
рН
2
2
1,5
1
1
V, мл
0
0
2
4
6
8
10
0,5
12
V, мл
0
-1
-0,5
-2
0
10
20
30
-1
-3
-1,5
-4
-2
1,8
0,9
рН
1,6
рН
0,8
1,4
0,7
1,2
0,6
1
0,5
0,8
0,4
0,6
0,3
0,4
0,2
0,2
V, мл
0,1
V, мл
0
0
0
2
4
6
8
0,0833 ± 0,0008 моль/л
10
12
0
10
20
30
79,8 0,9%
3
4.
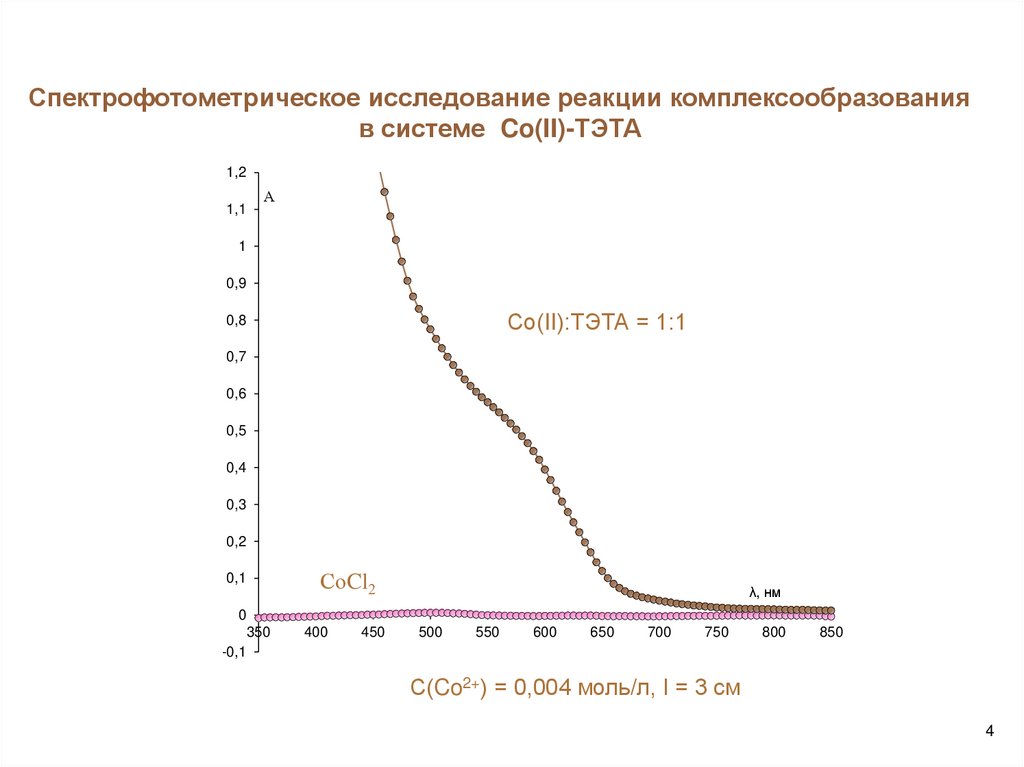
Спектрофотометрическое исследование реакции комплексообразованияв системе Co(II)-TЭТА
1,2
1,1
А
1
0,9
Со(II):ТЭТА = 1:1
0,8
0,7
0,6
0,5
0,4
0,3
0,2
СоCl2
0,1
λ, нм
0
350
400
450
500
550
600
650
700
750
800
850
-0,1
С(Co2+) = 0,004 моль/л, l = 3 см
4
5.
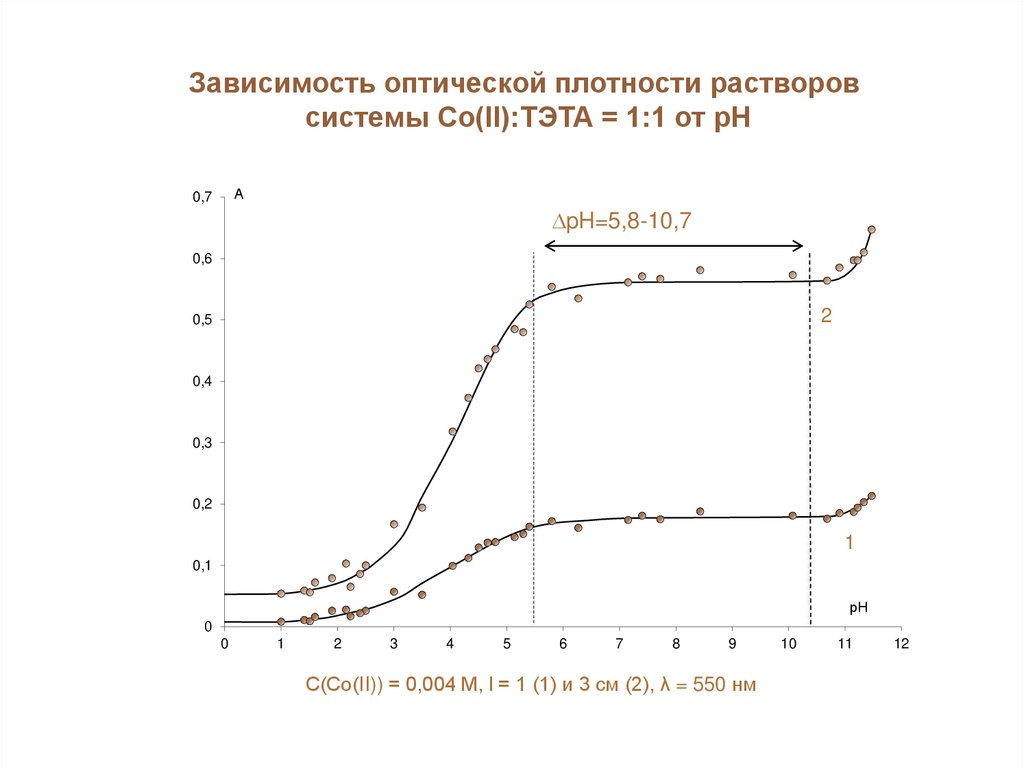
Зависимость оптической плотности растворовсистемы Со(II):ТЭТА = 1:1 от рН
А
0,7
pH=5,8-10,7
0,6
2
0,5
0,4
0,3
0,2
1
0,1
рН
0
0
1
2
3
4
5
6
7
8
9
C(Со(II)) = 0,004 M, l = 1 (1) и 3 см (2), λ = 550 нм
10
11
12
6.
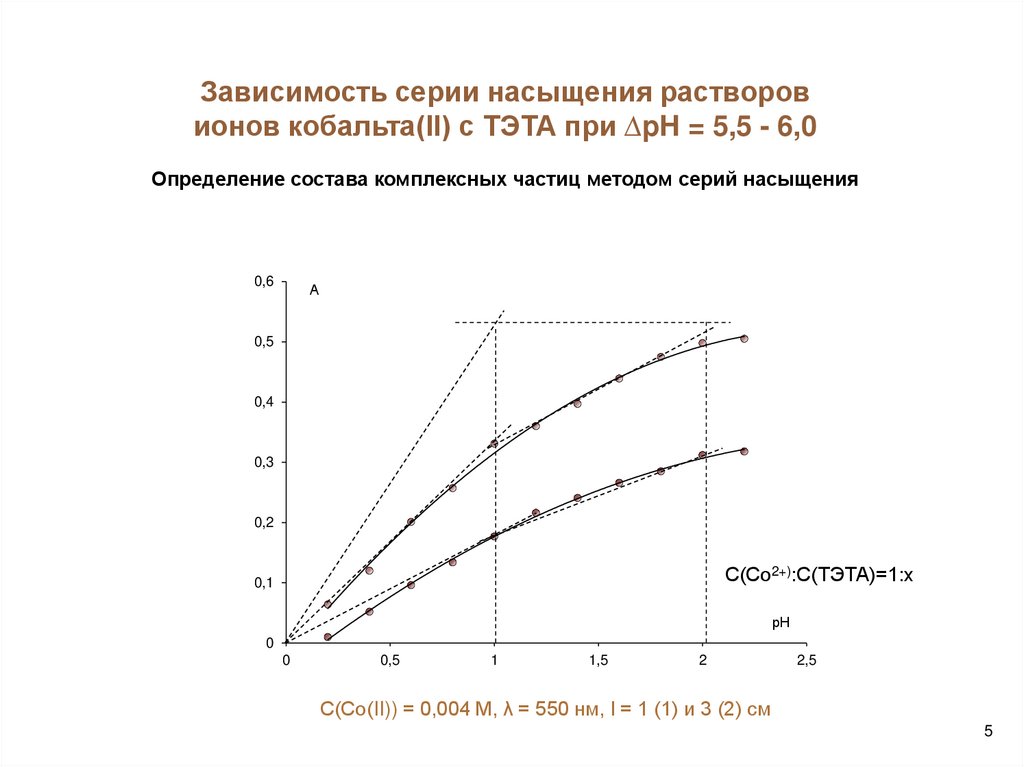
Зависимость серии насыщения растворовионов кобальта(II) с ТЭТА при ∆pH = 5,5 - 6,0
Определение состава комплексных частиц методом серий насыщения
0,6
А
0,5
0,4
0,3
0,2
С(Со2+):С(ТЭТА)=1:х
0,1
рН
0
0
0,5
1
1,5
2
2,5
C(Со(II)) = 0,004 M, λ = 550 нм, l = 1 (1) и 3 (2) см
5
7.
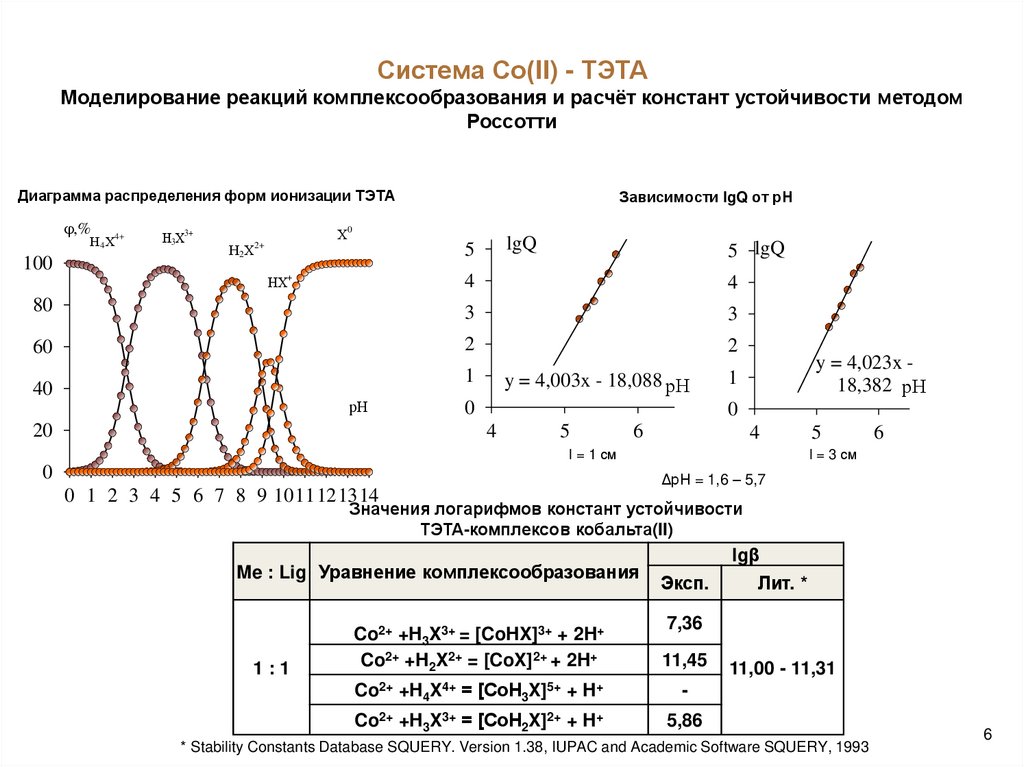
Система Со(II) - ТЭТАМоделирование реакций комплексообразования и расчёт констант устойчивости методом
Россотти
Диаграмма распределения форм ионизации ТЭТА
,%
Н4Х4+
100
Н3Х3+
Х0
2+
Н2Х
Зависимости lgQ от рН
lgQ
5
5 lgQ
4
4
80
3
3
60
2
2
1
1
НХ+
40
рН
20
y = 4,003x - 18,088 рН
0
y = 4,023x 18,382 рН
0
4
5
6
4
l = 1 см
0
5
6
l = 3 см
ΔрН = 1,6 – 5,7
0 1 2 3 4 5 6 7 8 9 1011121314
Значения логарифмов констант устойчивости
ТЭТА-комплексов кобальта(II)
Me : Lig Уравнение комплексообразования
1:1
lgβ
Эксп.
Лит. *
7,36
Co2+ +H3X3+ = [CoHX]3+ + 2H+
Co2+ +H2X2+ = [CoX]2+ + 2H+
11,45
Co2+ +H4X4+ = [CoН3X]5+ + H+
-
Co2+ +H3X3+ = [CoН2X]2+ + H+
5,86
11,00 - 11,31
* Stability Constants Database SQUERY. Version 1.38, IUPAC and Academic Software SQUERY, 1993
6
8.
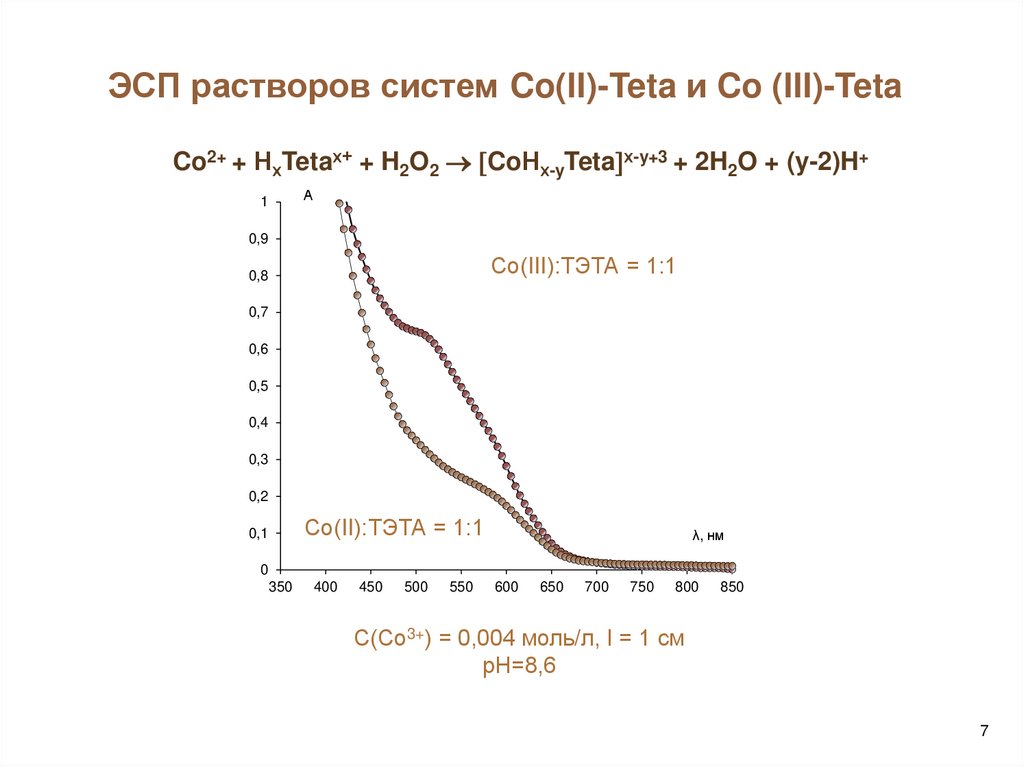
ЭСП растворов систем Co(II)-Teta и Co (III)-TetaCo2+ + НхTetaх+ + H2O2 CoНх-yTeta х-y+3 + 2H2O + (y-2)H+
А
1
0,9
Со(III):ТЭТА = 1:1
0,8
0,7
0,6
0,5
0,4
0,3
0,2
Со(II):ТЭТА = 1:1
0,1
λ, нм
0
350
400
450
500
550
600
650
700
750
800
850
C(Со3+) = 0,004 моль/л, l = 1 см
рН=8,6
7
9.
Система Со(III) - ТЭТА8
10.
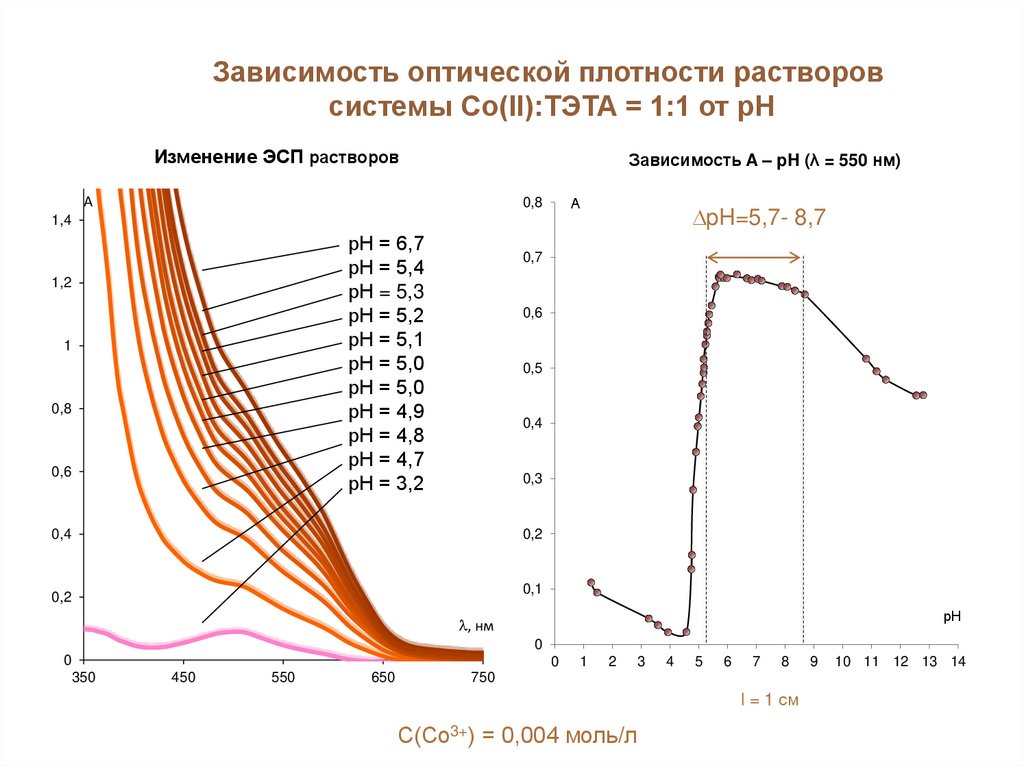
Зависимость оптической плотности растворовсистемы Со(II):ТЭТА = 1:1 от рН
Изменение ЭСП растворов
Зависимость A – pH (λ = 550 нм)
А
А
0,8
pH=5,7- 8,7
1,4
рН = 6,7
рН = 5,4
рН = 5,3
рН = 5,2
рН = 5,1
рН = 5,0
рН = 5,0
рН = 4,9
рН = 4,8
рН = 4,7
рН = 3,2
1,2
1
0,8
0,6
0,7
0,6
0,5
0,4
0,3
0,2
0,4
0,1
0,2
рН
, нм
0
0
0
350
450
550
650
1
2
3
4
5
6
7
8
750
l = 1 см
C(Со3+) = 0,004 моль/л
9
10 11 12 13 14
11.
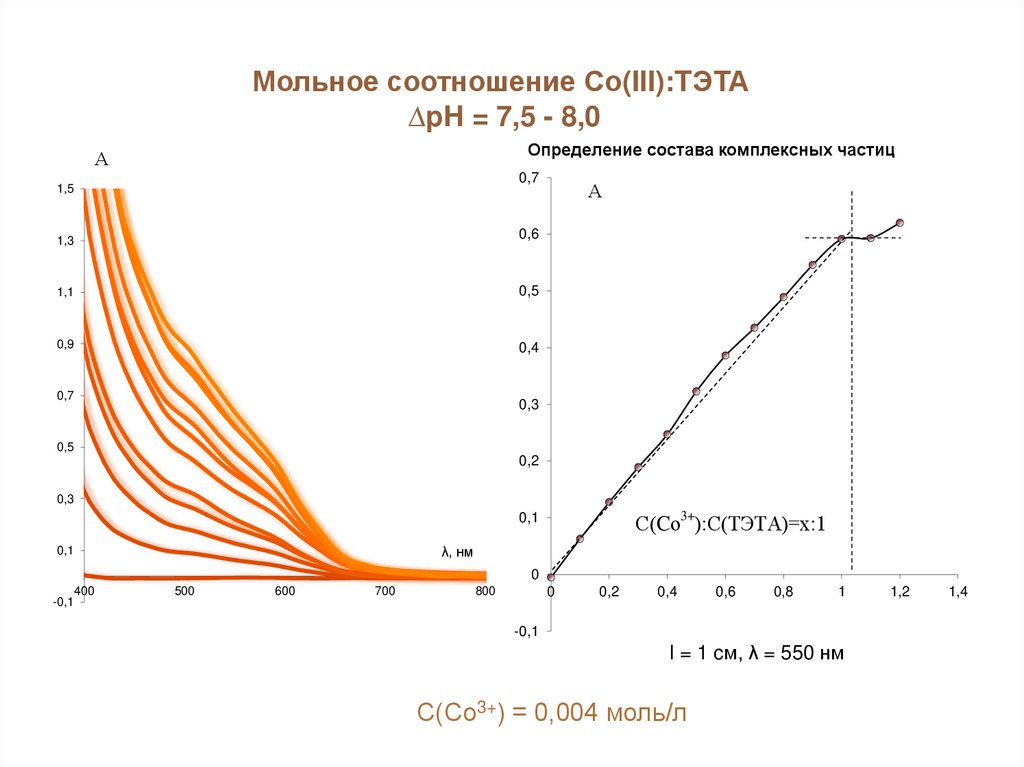
Мольное соотношение Со(III):TЭТА∆pH = 7,5 - 8,0
Определение состава комплексных частиц
А
0,7
1,5
1,3
0,6
1,1
0,5
0,9
0,4
0,7
А
0,3
0,5
0,2
0,3
С(Cо3+):С(ТЭТА)=х:1
0,1
λ, нм
0,1
0
400
500
600
700
0
800
-0,1
0,2
0,4
0,6
0,8
1
-0,1
l = 1 cм, λ = 550 нм
C(Со3+) = 0,004 моль/л
1,2
1,4
12.
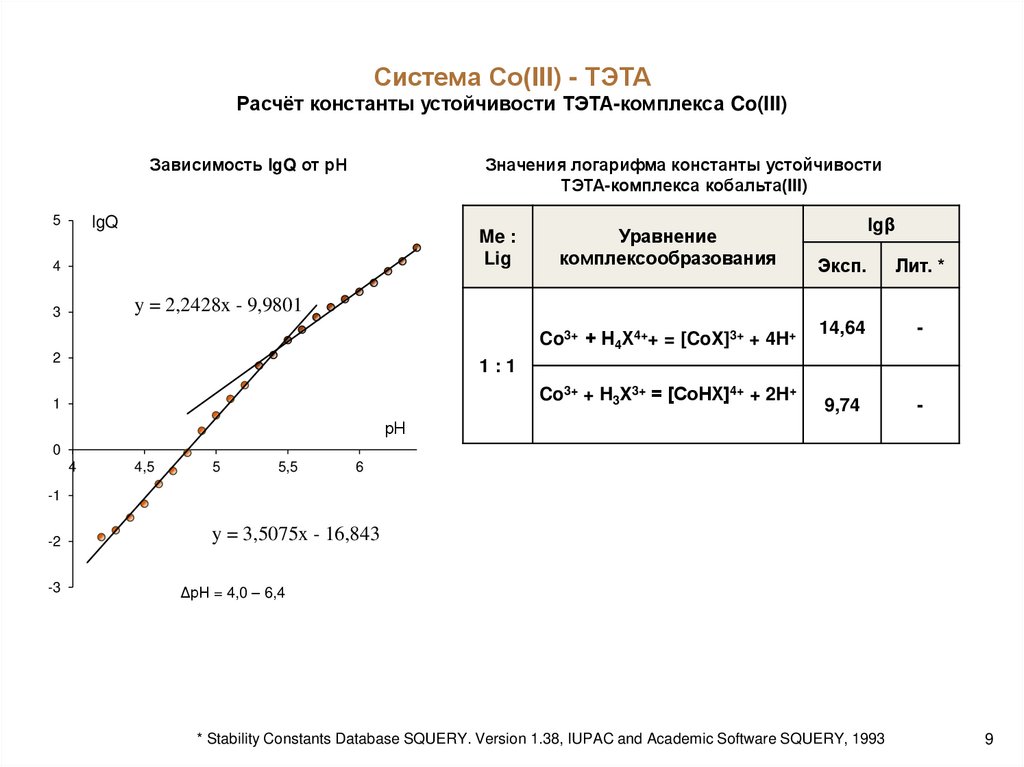
Система Со(III) - ТЭТАРасчёт константы устойчивости ТЭТА-комплекса Co(III)
Зависимость lgQ от рН
5
Значения логарифма константы устойчивости
ТЭТА-комплекса кобальта(III)
lgQ
Me :
Lig
4
Уравнение
комплексообразования
lgβ
Эксп.
Лит. *
14,64
-
9,74
-
y = 2,2428x - 9,9801
3
Co3+ + Н4Х4++ = [CoX]3+ + 4H+
2
1:1
Co3+ + H3X3+ = [CoНX]4+ + 2H+
1
рН
0
4
4,5
5
5,5
6
-1
-2
-3
y = 3,5075x - 16,843
ΔрН = 4,0 – 6,4
* Stability Constants Database SQUERY. Version 1.38, IUPAC and Academic Software SQUERY, 1993
9
13.
Выводы10




 Химия
Химия








