Похожие презентации:
Тема 4. Виды химической связи и типы кристаллическ
1. Виды химической связи и типы кристаллических решёток
2.
Химическая связь – это силы взаимодействия, которые соединяютотдельные атомы в молекулы, ионы, кристаллы.
Виды химических связе:
Ковалентная неполярная связь.
Химическая связь, которая возникает в результате образования общих
электронных пар, называется ковалентной.
Связь, возникающая между одинаковыми неметаллами, называется
ковалентной неполярной.
Например:
H2
H· + ·H → H •• H
3.
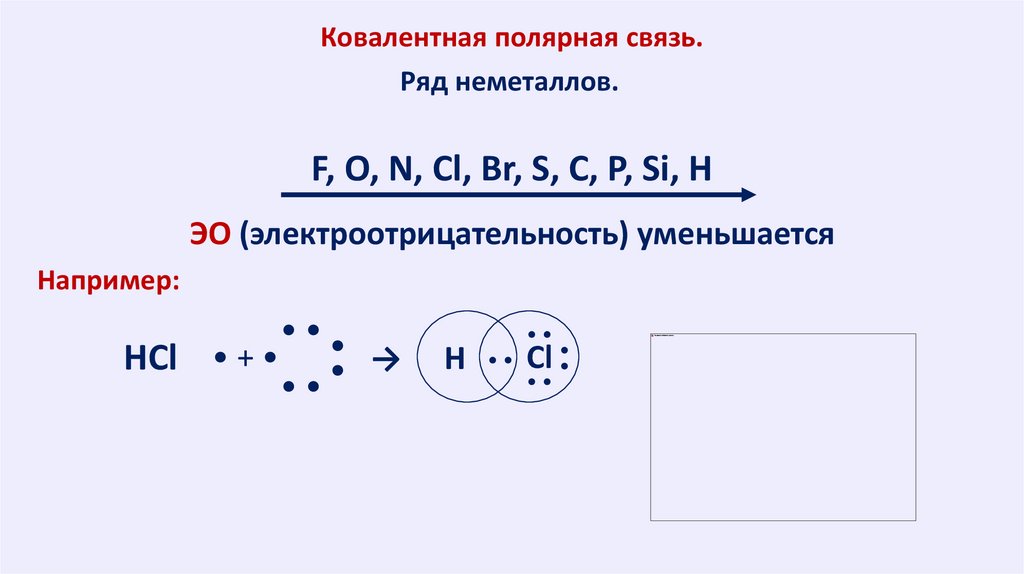
Ковалентная полярная связь.Ряд неметаллов.
F, O, N, Cl, Br, S, C, P, Si, H
ЭО (электроотрицательность) уменьшается
Например:
•
→
•
H • • Cl
•
•
HCl • +
•
•
4.
Ионная связь – это связь, которая образуется между ионами.Ион – это частица, образующаяся в результате отдачи или принятия
электрона.
Например:
NaCl – хлорид натрия (поваренная соль).
23
35,5 0
0
35,5 -1
23
+11
+1
0
+1
Na
)))
+
Cl
)))
→
[
Na
))]
[
Cl
)))]
+17
+11
+17
28 1
28 7
28
2 88
1e
0
-1
Na + Cl → NaCl
5.
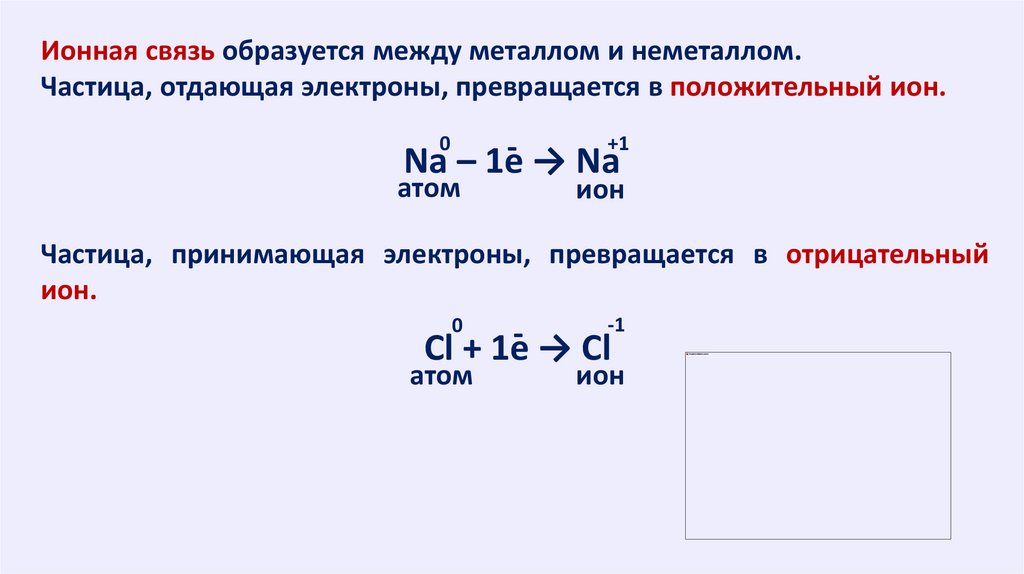
Ионная связь образуется между металлом и неметаллом.Частица, отдающая электроны, превращается в положительный ион.
+1
Na – 1e → Na
0
атом
ион
Частица, принимающая электроны, превращается в отрицательный
ион.
-1
Cl + 1e → Cl
0
атом
ион
6.
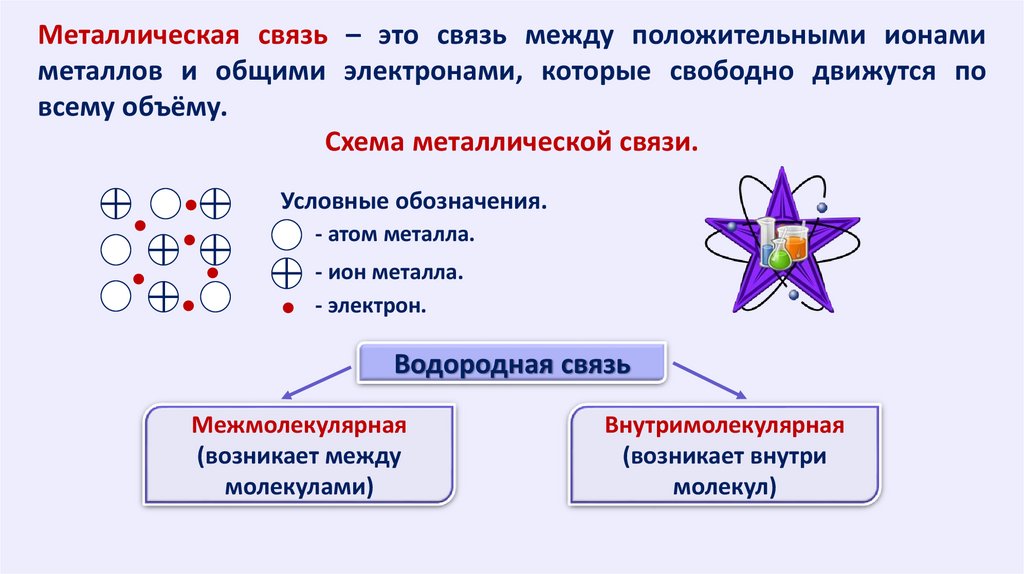
Металлическая связь – это связь между положительными ионамиметаллов и общими электронами, которые свободно движутся по
всему объёму.
Схема металлической связи.
•
Условные обозначения.
- атом металла.
- ион металла.
- электрон.
Водородная связь
Межмолекулярная
(возникает между
молекулами)
Внутримолекулярная
(возникает внутри
молекул)
7.
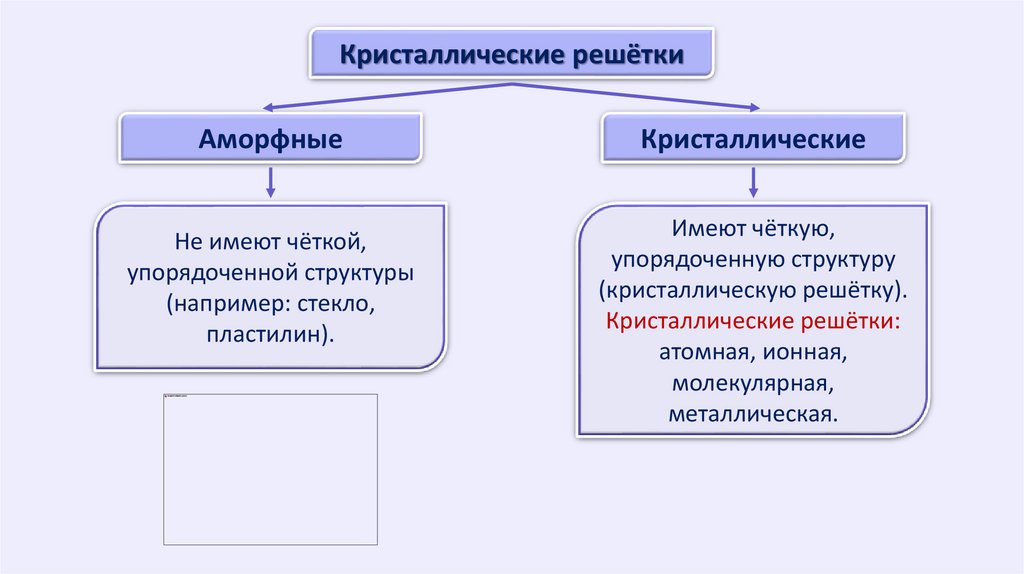
Кристаллические решёткиАморфные
Не имеют чёткой,
упорядоченной структуры
(например: стекло,
пластилин).
Кристаллические
Имеют чёткую,
упорядоченную структуру
(кристаллическую решётку).
Кристаллические решётки:
атомная, ионная,
молекулярная,
металлическая.
8.
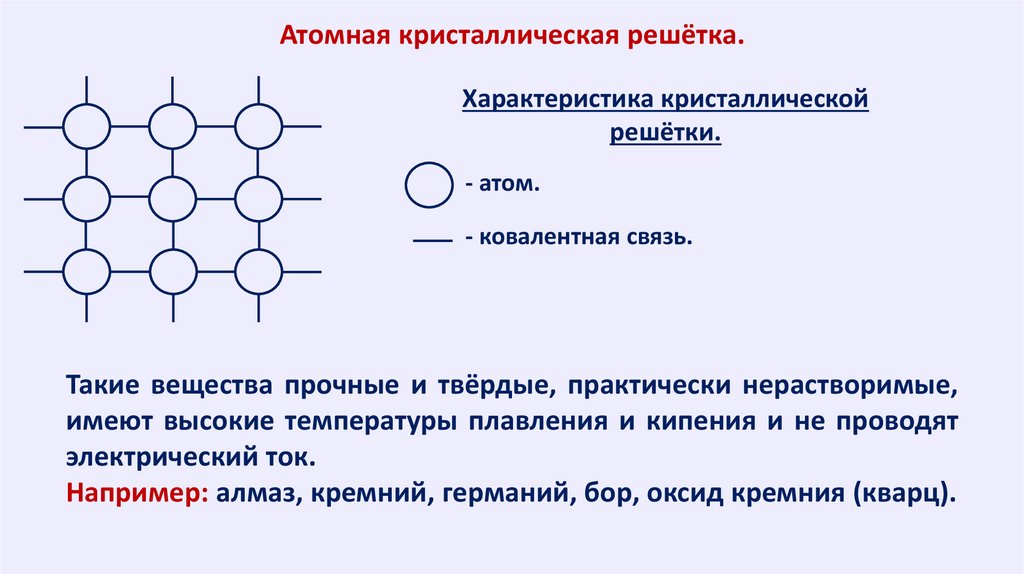
Атомная кристаллическая решётка.Характеристика кристаллической
решётки.
- атом.
- ковалентная связь.
Такие вещества прочные и твёрдые, практически нерастворимые,
имеют высокие температуры плавления и кипения и не проводят
электрический ток.
Например: алмаз, кремний, германий, бор, оксид кремния (кварц).
9.
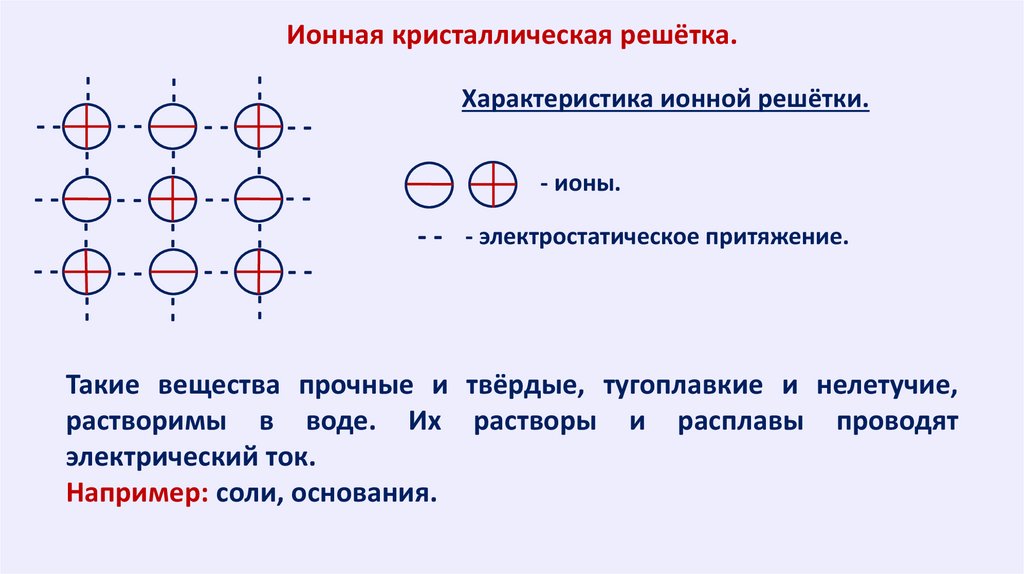
Ионная кристаллическая решётка.--
--
--
--
--
---
--
---
--
- электростатическое притяжение.
--
---
- ионы.
--
--
--
--
--
Характеристика ионной решётки.
---
--
---
--
Такие вещества прочные и твёрдые, тугоплавкие и нелетучие,
растворимы в воде. Их растворы и расплавы проводят
электрический ток.
Например: соли, основания.
10.
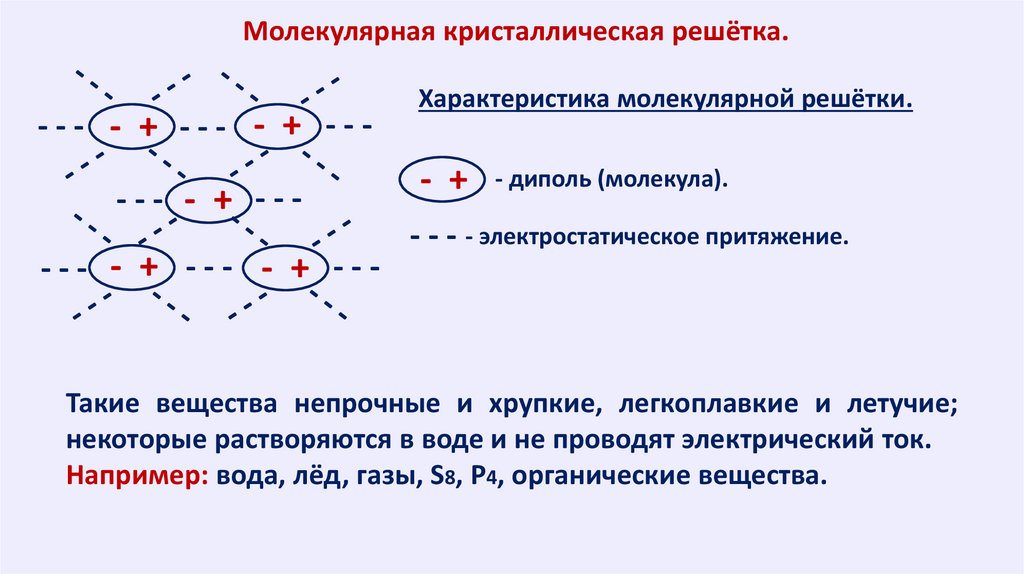
Молекулярная кристаллическая решётка.--- - + --- - + ----- - + ----- - + --- - + ---
Характеристика молекулярной решётки.
- + - диполь (молекула).
- - - - электростатическое притяжение.
Такие вещества непрочные и хрупкие, легкоплавкие и летучие;
некоторые растворяются в воде и не проводят электрический ток.
Например: вода, лёд, газы, S8, P4, органические вещества.
11.
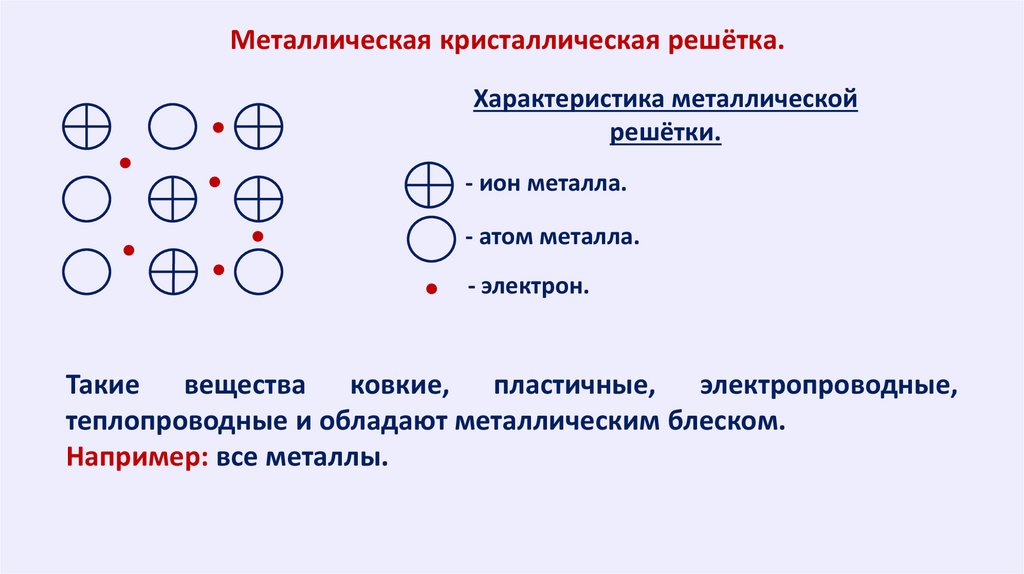
Металлическая кристаллическая решётка.Характеристика металлической
решётки.
- ион металла.
- атом металла.
- электрон.
Такие вещества ковкие, пластичные, электропроводные,
теплопроводные и обладают металлическим блеском.
Например: все металлы.



 Химия
Химия








