Похожие презентации:
https___school.mos.ru_ej_attachments_files_218_377_994_original_A0B588B5BDB8B5D0D0D0D0D12087B580B5B7D1D1D0D0D0D0D0
1. РАСЧЕТЫ по химическим уравнениям
2.
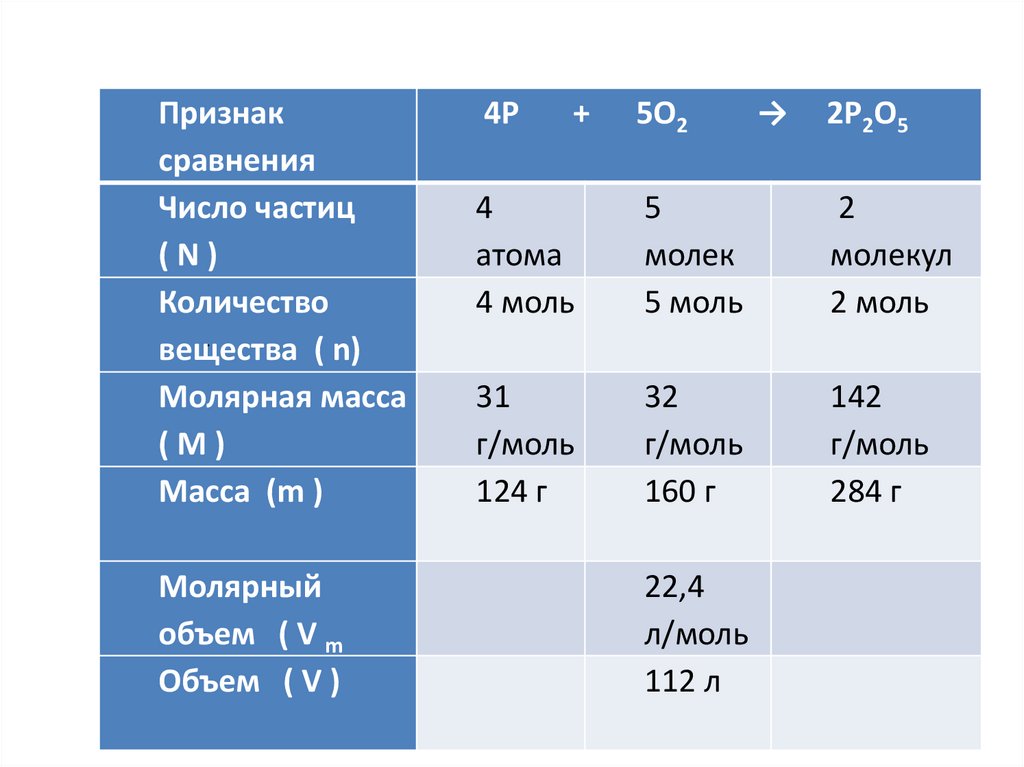
Признаксравнения
Число частиц
(N)
Количество
.
вещества
( n)
Молярная масса
(M)
Масса (m )
Молярный
объем ( V m
Объем ( V )
4Р
+
5О2
→
2Р2О5
4
атома
4 моль
5
молек
5 моль
2
молекул
2 моль
31
г/моль
124 г
32
г/моль
160 г
142
г/моль
284 г
22,4
л/моль
112 л
3.
Условие. При взаимодействии кислорода с фосфором,образовалось 4 моль оксида фосфора (V). Вычислите
массу кислорода.
Решение:
Дано:
n(P2О5) =4 моль
m (О2) = ?
x моль 4 моль
4P + 5 О2 = 2 P2О5
5 моль 2 моль
Пропорция:
x
4 моль
5 моль
=
2 моль
x·2 = 5·4
x = 10 моль О2
m(O2) = n · M = 10 моль · 32 г/моль =
320 г.
Ответ: m (О2) = 320 г.
4.
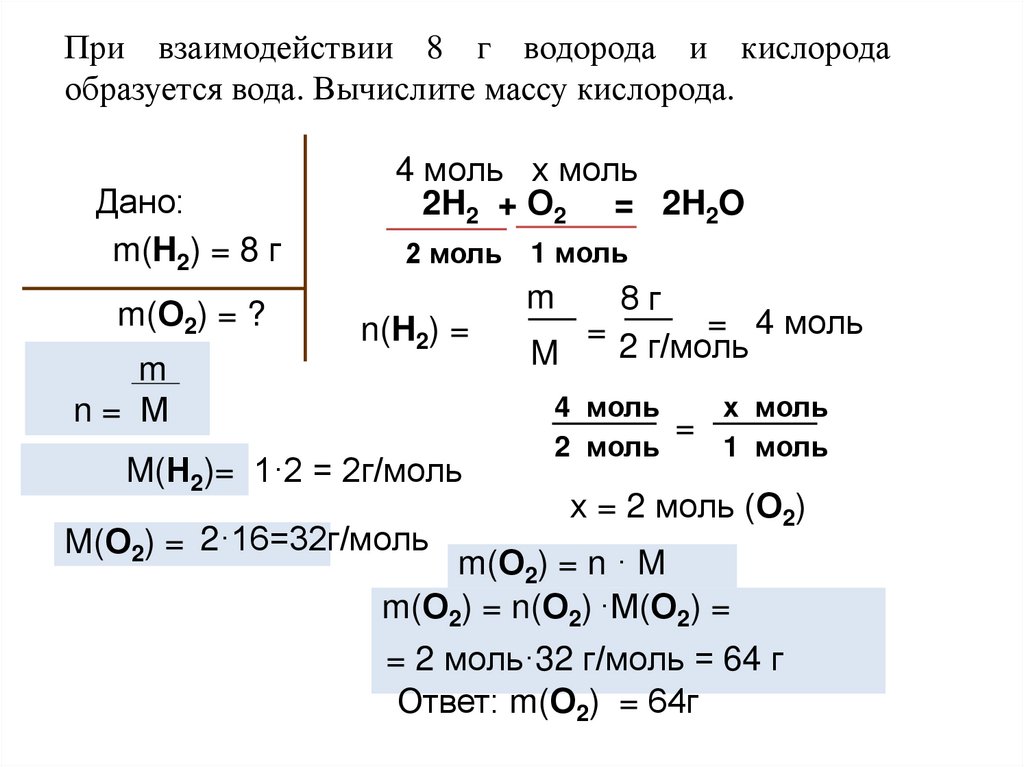
При взаимодействии 8 г водорода и кислородаобразуется вода. Вычислите массу кислорода.
Дано:
m(H2) = 8 г
m(О2) = ?
4 моль х моль
2H2 + О2 = 2H2O
2 моль 1 моль
8г
= 4 моль
= 2 г/моль
M
m
n(H2) =
m
n= М
M(Н2)= 1·2 = 2г/моль
M(О2) = 2·16=32г/моль
4 моль
х моль
=
2 моль
1 моль
х = 2 моль (О2)
m(О2) = n · M
m(О2) = n(О2) ·M(О2) =
= 2 моль·32 г/моль = 64 г
Ответ: m(О2) = 64г
5.
Для закрепления:1. При разложении 200 г карбоната кальция (CaCO3),
образуется оксид кальция и углекислый газ. Вычислите
массу образовавшегося оксида кальция.
2. 5 г цинка опустили в раствор хлороводорода, при этом
образовалась соль хлорида цинка и выделился водород.
Вычислите массу образовавшейся соли.



 Химия
Химия








