Похожие презентации:
алкены
1. АЛКЕНЫ химические свойства и получение
2.
Алкены (олефины) — непредельные углеводороды, в молекулахкоторых содержится одна двойная связь между атомами углерода.
Общая формула — CnH2n
3. Химические свойства
РЕАКЦИИ ПРИСОЕДИНЕНИЯДля алкенов характерны реакции присоединения по двойной связи
С=С, при которых протекает разрыв пи-связи в молекуле алкена.
4. Алкены реагируют с водородом при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt, Pd и др.)
Химические свойства1
ГИДРИРОВАНИЕ
Алкены реагируют с водородом при нагревании и под давлением в
присутствии металлических катализаторов (Ni, Pt, Pd и др.)
5. Химические свойства
2ГАЛОГЕНИРОВАНИЕ
Реакция с бромной водой является качественной для непредельных соединений, содержащих
двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает
на присоединение его по кратным связям к органическому веществу.
Условия:
CCl4, комнатная
температура.
6. Химические свойства
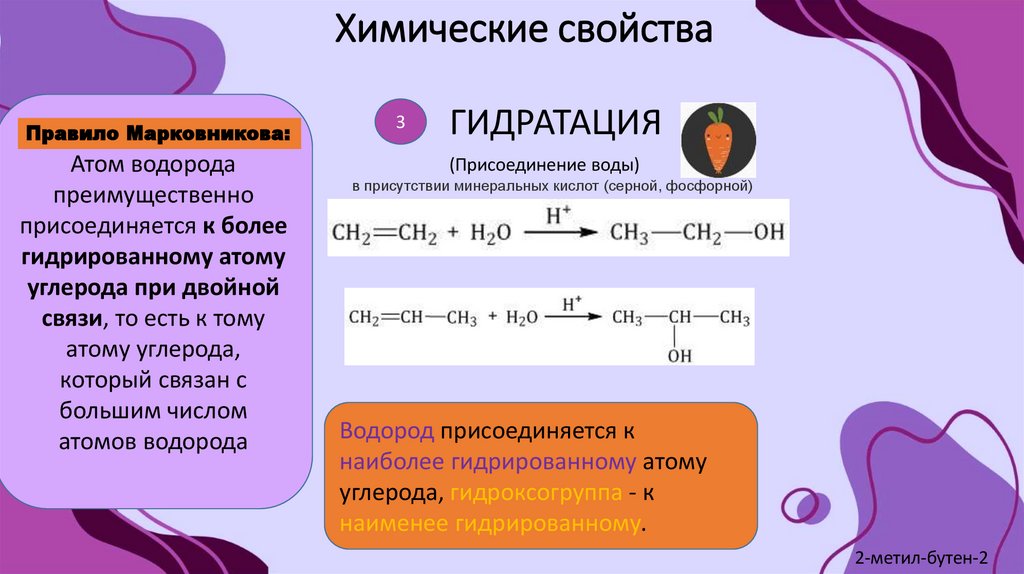
Правило Марковникова:Атом водорода
преимущественно
присоединяется к более
гидрированному атому
углерода при двойной
связи, то есть к тому
атому углерода,
который связан с
большим числом
атомов водорода
3
ГИДРАТАЦИЯ
(Присоединение воды)
в присутствии минеральных кислот (серной, фосфорной)
Водород присоединяется к
наиболее гидрированному атому
углерода, гидроксогруппа - к
наименее гидрированному.
2-метил-бутен-2
7. Химические свойства
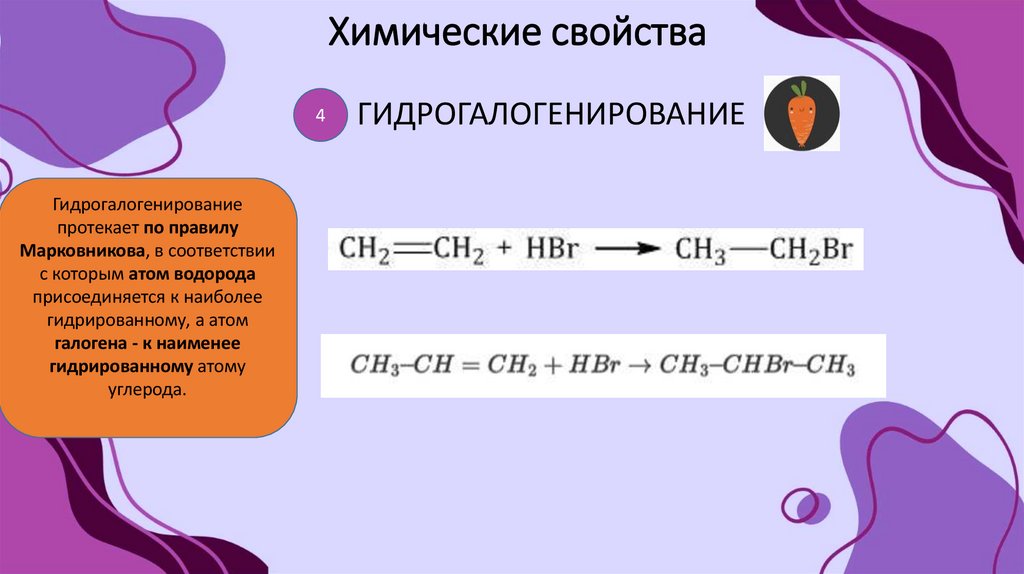
4Гидрогалогенирование
протекает по правилу
Марковникова, в соответствии
с которым атом водорода
присоединяется к наиболее
гидрированному, а атом
галогена - к наименее
гидрированному атому
углерода.
ГИДРОГАЛОГЕНИРОВАНИЕ
8. Химические свойства
5ПОЛИМЕРИЗАЦИЯ
Реакции полимеризации — соединение одинаковых молекул за счет разрыва п-связей
nM → Mn
9.
РЕАКЦИИ ОКИСЛЕНИЯ10. Химические свойства
6 • Полное окисление (горение)7 • Неполное окисление (каталитическое)
11. Химические свойства
8МЯГКОЕ ОКИСЛЕНИЕ
Мягкое окисление протекает при низкой температуре в присутствии перманганата калия. При этом
раствор перманганата обесцвечивается.
В молекуле алкена разрывается только π-связь и окисляется каждый атом углерода при двойной связи.
При этом образуются двухатомные спирты (диолы).
12.
ПОЛУЧЕНИЕ13.
Алкены получают несколькими способами:1. Крекинг нефти
В результате крекинга нефти образуется один алкан и один алкен.
C12H26 → C6H12 + C6H14
14.
2. Дегидрирование алкановПри наличии катализатора и повышенной температуры от молекул
алканов отщепляется водород. Наиболее легко водород отдает
третичный атом, чуть труднее - вторичный и заметно труднее первичный.
15.
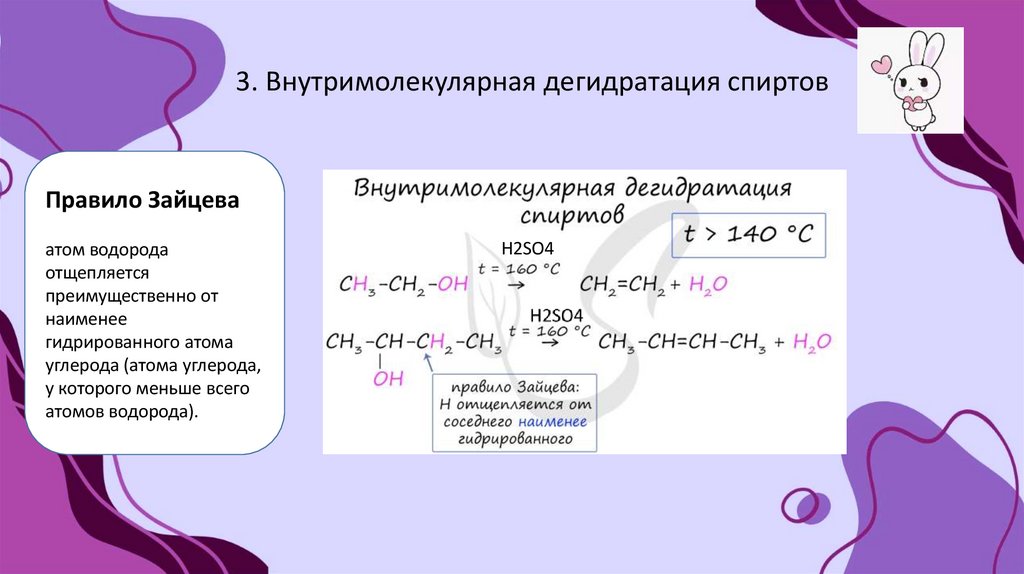
3. Внутримолекулярная дегидратация спиртовПравило Зайцева
атом водорода
отщепляется
преимущественно от
наименее
гидрированного атома
углерода (атома углерода,
у которого меньше всего
атомов водорода).
H2SO4
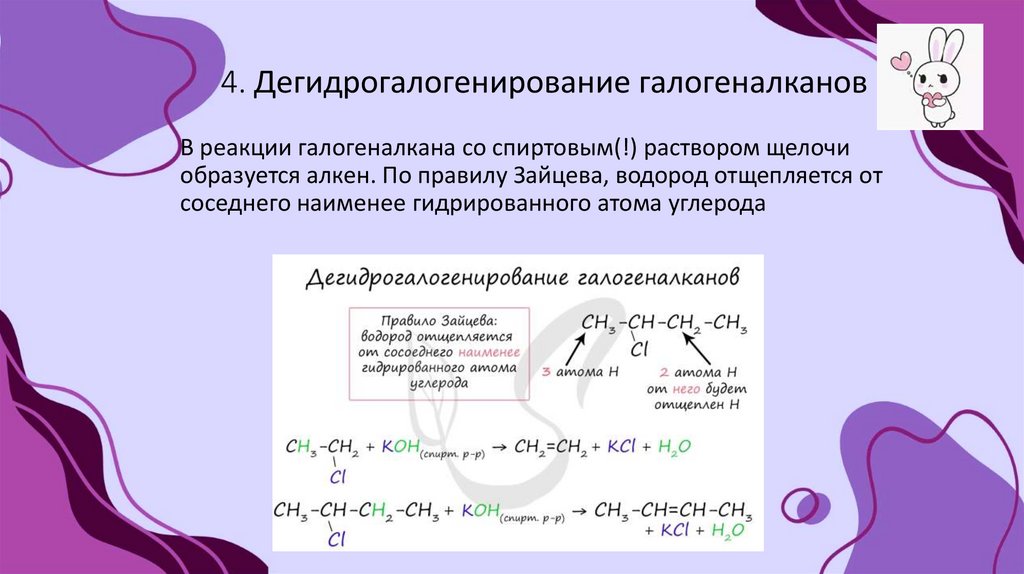
16. 4. Дегидрогалогенирование галогеналканов
В реакции галогеналкана со спиртовым(!) раствором щелочиобразуется алкен. По правилу Зайцева, водород отщепляется от
соседнего наименее гидрированного атома углерода
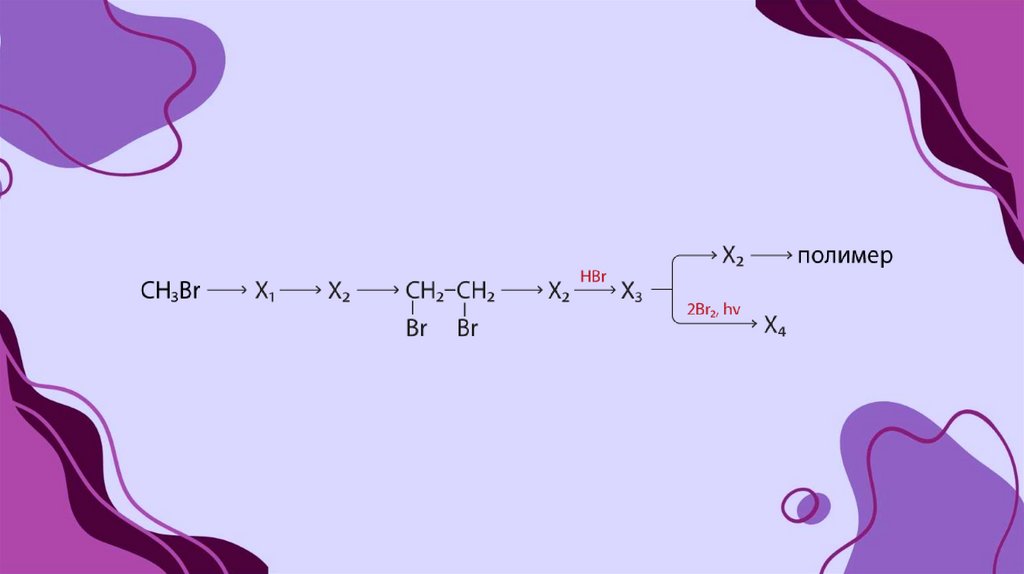
17. 5. Дегалогенирование дигалогеналканов
В подобных реакциях применяется цинк (цинковая пыль) - двухвалентный металл,который связывает расположенные рядом атомы галогенов. Между атомами
углерода, которым принадлежали галогены, завязывается двойная связь.














 Химия
Химия








