Похожие презентации:
Хімічні властивості кислот
1.
Підготувала:вчитель хімії
Корвегіна В.А.
2. Завдання уроку:
Закріпитиі узагальнити знання про
властивості класів неорганічних
сполук;
Вивчати хімічні властивості кислот;
Удосконалювати вміння
узагальнювати вивчений матеріл та
робити висновки.
3. Запитання для повторення:
Щоназивається кислотами?
Які види класифікації кислот ви
знаєте?
Які фізичні властивості
притаманні кислотам?
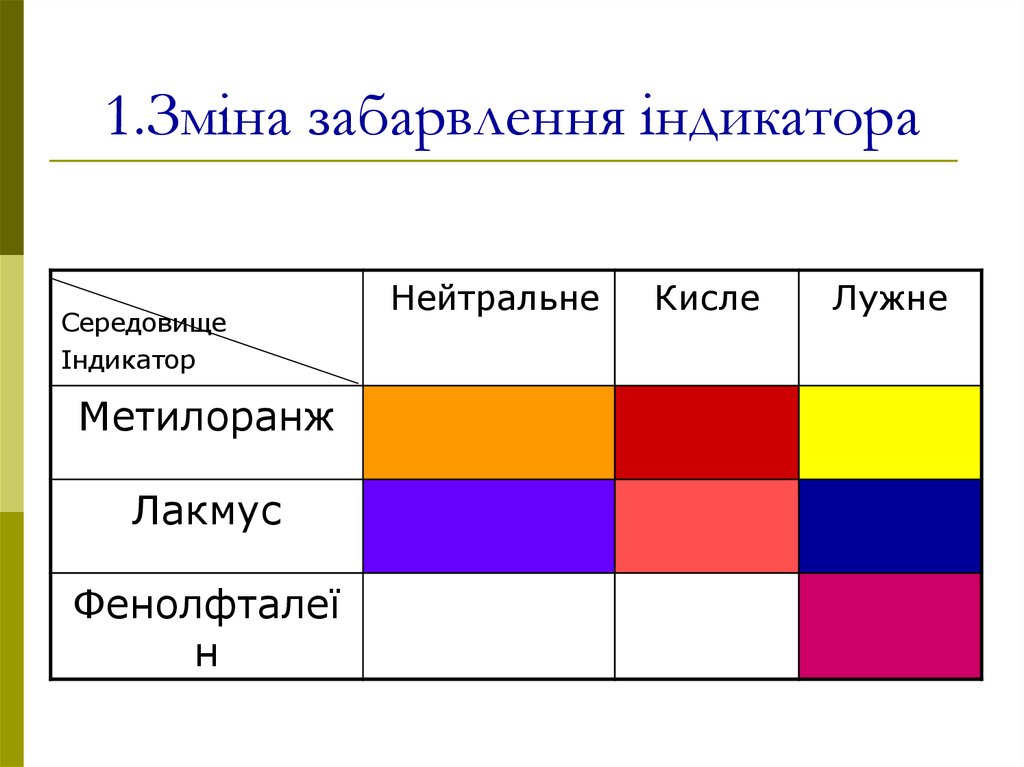
4. 1.Зміна забарвлення індикатора
СередовищеІндикатор
Метилоранж
Лакмус
Фенолфталеї
н
Нейтральне
Кисле
Лужне
5. 2.Взаємодія з металами
При взаємодії кислот з металамивиділяється водень та утворюється
сіль.
Неактивні метали водень з кислот не
витісняють, їх можна визначити за
таблицею активності металів.
Zn
+ H2SO4 → H2↑ + ZnSO4
Cu
+ HCl ≠неактивний метал не
реагує.
6. 3. Взаємодія кислот з лугами:
Привзаємодії кислот з основами
утворюється сіль та вода
(обов'язковий продукт) реакція
проходить в присутності
індикатора.
NaOH
+ HCl → NaCl + H2O
7. 4. Взаємодія кислот з солями:
Привзаємодії кислот з солями
утворюється нова сіль та кислота
(слабка, яка іноді розкладається).
Na2CO3+HCl
→NaCl +
+CO2↑+H2O
8. 5. Взаємодія кислот з оксидами металів:
При взаємодії кислот з оксидамиметалів (основними), утворюється сіль
та вода (обов'язковий продукт), реакція
відбувається при нагріванні.
CuO
+ H2SO4 t→ CuSO4 + H2O
9. Виконати завдання :
Визначити масу солі, що утворюєтьсяпри взаємодії цинку масою 130 г з
хлоридною кислотою.








 Химия
Химия








