Похожие презентации:
Аутоімунні захворювання
1. Аутоімунні захворювання
2. Нормальні аутоантитіла
У 40-х роках ХХ ст. було встановлено, що аутоантитіла
виявляють не лише при захворюваннях (інфекційних, гострих
запальних, у хворих з інфарктом міокарда), але й при багатьох
фізіологічних станах здорових людей і навіть у сироватці
новонароджених дітей.
Нормальні аутоантитіла – це низькоафінні Ig М, а у
хворих з АІЗ продукуються високоафінні Ig G.
Функції нормальних аутоантитіл:
- видалення продуктів клітинного метаболізму і деструкції;
- фактори регуляції імунного гомеостазу;
- участь у тканинній репарації;
- функція транспортних білків
3. Аутоімунні процеси – це такий стан організму, за якого відбувається продукування антитіл або сенсибілізованих лімфоцитів до нормальних а
Аутоімунні процеси – це такий стан організму, за якоговідбувається продукування антитіл або
сенсибілізованих лімфоцитів до нормальних антигенів
власного організму.
• Ж. Борде – показав можливість появи ізоантитіл, що
аглютинують еритроцити, у морських свинок.
• В. Ліндеман у 1900 р. помітив аутоімунну реакцію у
дослідах з утворенням нефро- та сперматотоксинів у
тварин після введення їм гомологічних тканин.
• Мазугі – автор вчення про імунопатогенез нефриту
(1933 р.).
• Донат, Ландштейнер – виявили утворення АТ проти
еритроцитів власного організму (1904 р.).
• Ріверс, Швенткер – вперше описали аутоімунне
захворювання.
4. Системний червоний вовчак
5. Ревматичні захворювання
6. Тиреоїдит Хашімото
7. Пародонтоз Колагеноз
8. За А.Д.Адо аутоантигени (ендоантигени чи ендоалергени) поділяють на групи:
• -природні, первинні – АГ імунологічнозабар’єрованих органів (тканин),
• -набуті, вторинні (патологічні тканини):
-неінфекційні ауто-АГ (утворюються
під впливом фізичних факторів: тепло, холод,
іонізуюче випромінення),
-інфекційні (виникають в результаті
впливу на тканини мікробних токсинів).
9. За механізмами імунних процесів, залучених у розвиток аутоімунної патології, АІЗ поділяють на:
• захворювання, зумовлені патогенною дієюаутоантитіл до аутоантигенів клітин або
міжклітинного матриксу (аутоімунна гемолітична
анемія),
• захворювання, зумовлені патогенною дією
імунних комплексів (системний червоний
вовчак),
• захворювання, зумовлені патогенною дією
аутоспецифічних
Т-лімфоцитів
(інсулінзалежний цукровий діабет)
10. Ауто-АТ зустрічаються при багатьох синдромах і хворобах:
1-хвороби серця і кровоносних судин: ревмокардит,
алергічний васкуліт;
2-хвороби крові і кровотворних органів: аутоімунна
гемолітична анемія, гемолітична жовтяниця новонароджених,
злоякісна анемія;
3-хвороби дихальних органів та нервової системи:
розсіяний склероз, міастенія;
4-хвороби очей: анафілактичний ендофтальміт;
5-хвороби сполучної тканини: ревматоїдний артрит,
системний червоний вовчак, колагенози, склеродермія;
6-хвороби ендокринної системи: цукровий діабет,
первинна мікседема;
7-хвороби шкіри: контактний дерматит, дитяча екзема;
8-інфекційні хвороби – стрептококова ангіна, скарлатина.
11. ПРИКЛАДИ АУТОІМУНІЗАЦІЇ ЧЕРЕЗ ПЕРЕХРЕСНІ РЕАКЦІЇ
Перехресно реагуючі АГКлінічні
прояви
Гетероантигени
Аутоантигени
АГ
мембран Субсарколема
серцевого Ревмокардит
стрептококів
м’яза
-гемолітичний
стрептокок типу А
АГ ниркових клубочків, Післяінфекційні
тканин суглобів
ревматизм
нефропатії,
Тканини
головного Тканина головного мозку Післявакцинальний енцефаліт
мозку
тварин людини
(виробництво вакцин)
Мембранні АГ E. сoli, Ацетилхолінові рецептори
Proteus vulgaris
Нуклеїнові
вірусів
M. tuberculosis
кислоти Нуклеїнова
людини
Міастенія гравіс
кислота Системний червоний вовчак,
гепатит
АГ суглобового хряща
Артрити
12. СПЕКТР АУТОІМУННИХ ЗАХВОРЮВАНЬ
ОРГАНОСПЕЦИФІЧНІ
Тиреоїдит Хасімото
Первинна мікседема
Тиреотоксикоз
Перніціозна анемія
Аутоімунний атрофічний гастрит
Хвороба Адісона
Інсулін-залежний цукровий діабет
Синдром Гудпасчера
Злоякісна міастенія
Чоловіче безпліддя (деякі випадки)
Симпатична офтальмія
Рзсіяний склероз
Аутоімунна гемолітична анемія
Ідіопатична тромбоцитопенічна пурпура
Ідіопатична лейкопенія
Активний хронічний гепатит (при відсутності антигенів вірусу гепатиту В)
Криптогенний цироз печінки
Виразковий коліт
Синдром Шегрена
Ревматоїдний артрит
Дерматоміозит
Склеродермія
Дискоїдний еритематозний вовчак
Системний червоний вовчак
ОРГАНОНЕСПЕЦИФІЧНІ
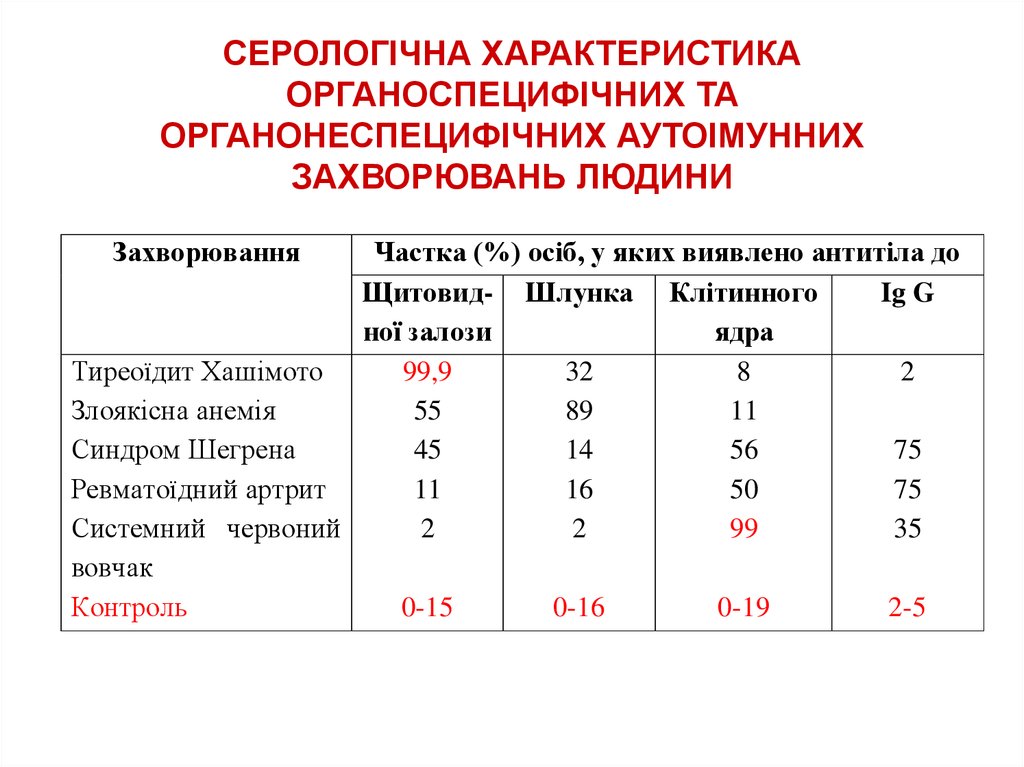
13. СЕРОЛОГІЧНА ХАРАКТЕРИСТИКА ОРГАНОСПЕЦИФІЧНИХ ТА ОРГАНОНЕСПЕЦИФІЧНИХ АУТОІМУННИХ ЗАХВОРЮВАНЬ ЛЮДИНИ
ЗахворюванняЧастка (%) осіб, у яких виявлено антитіла до
Щитовид- Шлунка Клітинного
Ig G
ної залози
ядра
Тиреоїдит Хашімото
99,9
32
8
2
Злоякісна анемія
55
89
11
Синдром Шегрена
45
14
56
75
Ревматоїдний артрит
11
16
50
75
Системний червоний
2
2
99
35
вовчак
Контроль
0-15
0-16
0-19
2-5
14. Аутоімунна гемолітична анемія
• Набуте хронічне захворювання зпочерговими
загостреннями
та
ремісіями,
що
характеризується
зниженням кількості еритроцитів на
фоні нормального стану кісткового
мозку. Патологія зустрічається з
частотою 1:80000. Частіше хворіють
жінки. В основі захворювання –
утворення аутоантитіл до зрілих
еритроцитів чи їхніх попередників на
ранніх стадіях дозрівання.
• Клінічна симптоматика зумовлена
недостатністю транспорту кисню
еритроцитами внаслідок їхнього
підвищеного руйнування.
15. Системний червоний вовчак
• Системний червоний вовчак (СЧВ) хронічне полісиндромне захворюванняпереважно молодих жінок і дівчат, що
розвивається на фоні генетично зумовленої
недосконалості
імунорегуляторних
процесів,
що
призводить
до
неконтрольованої продукції антитіл до
власних клітин та їх компонентів, з
розвитком
імунокомплексного
та
аутоімунного
хронічного
запалення
(В.А.Насонова,
1989).
Захворювання
перебігає з непрогнозованими періодами
загострення і ремісій, проявляється
полісимптомністю.
• СЧВ уражає головним чином жінок і
дівчаток-підлітків, співвідношення між
дорослими чоловіками і жінками становить
1:10-15.
16. Системний червоний вовчак
• СЧВ – одне з найбільш розповсюджених і важкихзахворювань сполучної тканини. В останнє десятиріччя
повсюдно відзначається тенденція до зростання
захворюваності на СЧВ, а її поширеність у різних
клімато-географічних зонах становить від 4 до 250 (в
Україні – 16,5) випадків на 100 тис. населення,
переважно
у
жінок
репродуктивного
віку.
При
цьому
зростання
захворюваності
відбувається за рахунок розширення вікового діапазону
дебюту хвороби: все частіше він зміщується до 14-15
років, а також долає 40-річний рубіж, особливо у
чоловіків, питома вага яких серед хворих на СЧВ уже
досягла 15%.
17. Системний червоний вовчак
• Причини. Тригерними пусковими факторами є інсоляція,охолодження, гострі інфекції, психічні та фізичні травми, вагітність,
пологи, щеплення, медикаментозна непереносимість (гідралазин,
антибіотики, сульфаніламіди, вітаміни, сироватки, оральні
контрацептиви тощо). Так, ультрафіолетове опромінення стимулює
апоптоз клітин шкіри, що призводить до появи деяких
внутрішньоклітинних аутоантигенів на мембрані «апоптозних»
клітин, інфікуючи тим самим розвиток аутоімунного процесу у
генетично схильних осіб.
• На роль статевих гормонів у розвитку СЧВ вказує значне
превалювання захворювання у жінок репродуктивного віку.
• Патогенез. У патогенезі СЧВ важлива роль належить імунним
механізмам, особливо Т-клітинним дефектам та гіперреактивності
В-лімфоцитів; при цьому відзначається найбільш істотне зниження
рівня СD8+-клітин, що корелює з клінічною активністю
захворювання. Зниження показника СD4+/СD8+ насамперед має
місце у хворих з ушкодженням нирок і тромбоцитопенією.
18. Про генетичну схильність до виникнення СЧВ свідчать:
підвищений ризик розвитку СЧВ у хворих, які мають дефіцит
комплементу, особливо компонентів СІ, С2, С4, а також в осіб із
псевдопозитивною реакцією Васермана;
частий розвиток захворювання за наявності антигенів HLA-А1, В8,
В35, DR2, DR3, а також селективних В-клітинних алоантигенів;
генетична гетерогенність, що зумовлює клінічний поліморфізм СЧВ;
сімейний характер захворювання, який відзначають у 5-10% хворих
на СЧВ; як правило, СЧВ виявляють в обох монозиготних близнят,
при цьому у здорових членів сім'ї часто спостерігають названі вище
імунні аномалії;
виражені асоціативні зв'язки між носійством HLA-Cw6, HLA-Cw7 і
хронічним характером перебігу СЧВ, високим ступенем системності;
велика ймовірність швидкого прогресування вовчакового нефриту в
чоловіків із фенотипом HLA-A6 і HLA-B18
19. Міастенія гравіс
Щорічна захворюваністьстановить близько 0,4 на 100 тисяч
населення, поширеність
коливається в межах 10–24 на 100
тисяч.
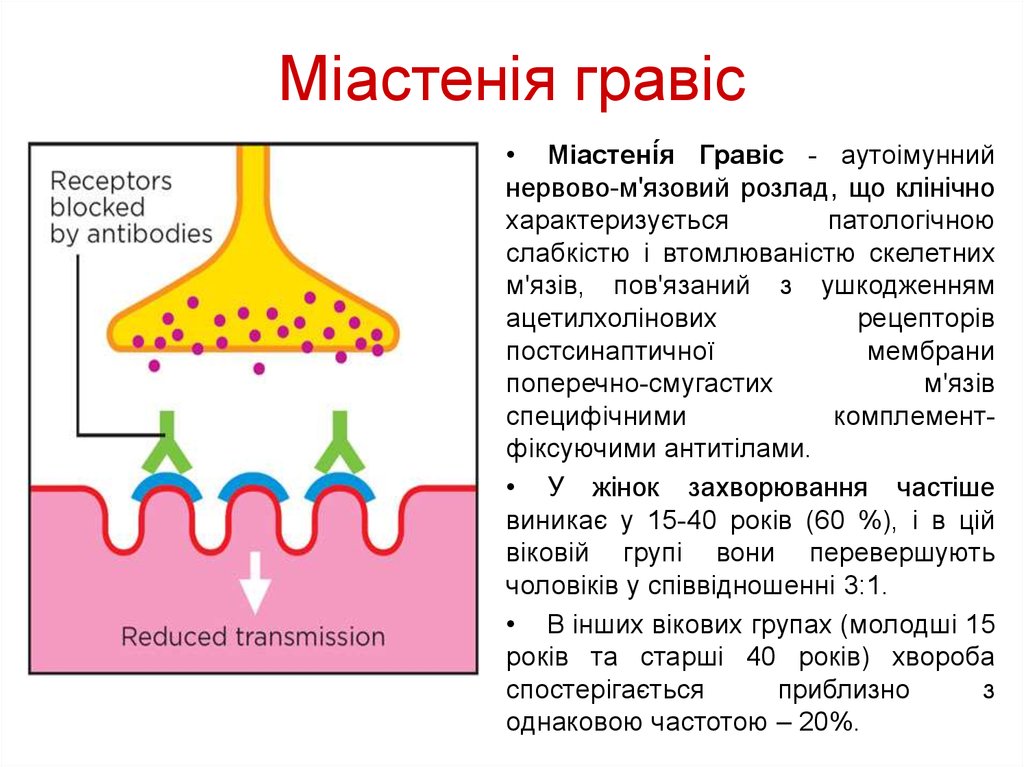
20. Міастенія гравіс
• Міастені́я Гравіс - аутоімуннийнервово-м'язовий розлад, що клінічно
характеризується
патологічною
слабкістю і втомлюваністю скелетних
м'язів, пов'язаний з ушкодженням
ацетилхолінових
рецепторів
постсинаптичної
мембрани
поперечно-смугастих
м'язів
специфічними
комплементфіксуючими антитілами.
• У жінок захворювання частіше
виникає у 15-40 років (60 %), і в цій
віковій групі вони перевершують
чоловіків у співвідношенні 3:1.
• В інших вікових групах (молодші 15
років та старші 40 років) хвороба
спостерігається
приблизно
з
однаковою частотою – 20%.
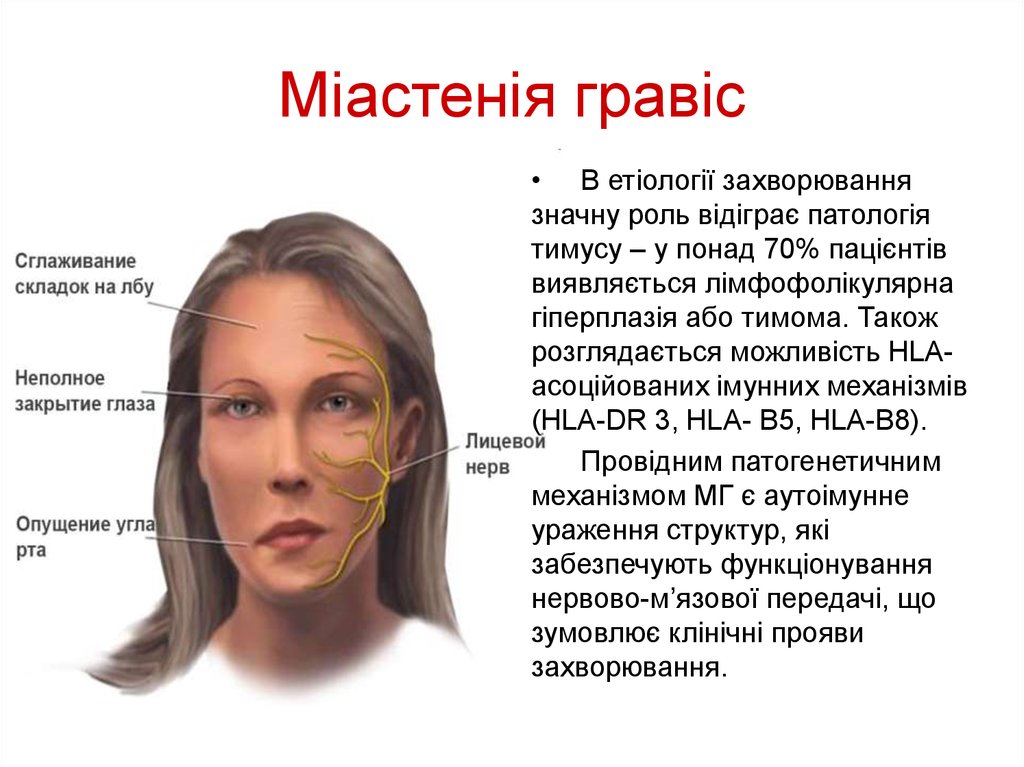
21. Міастенія гравіс
• В етіології захворюваннязначну роль відіграє патологія
тимусу – у понад 70% пацієнтів
виявляється лімфофолікулярна
гіперплазія або тимома. Також
розглядається можливість HLAасоційованих імунних механізмів
(HLA-DR 3, HLA- B5, HLA-B8).
Провідним патогенетичним
механізмом МГ є аутоімунне
ураження структур, які
забезпечують функціонування
нервово-м’язової передачі, що
зумовлює клінічні прояви
захворювання.
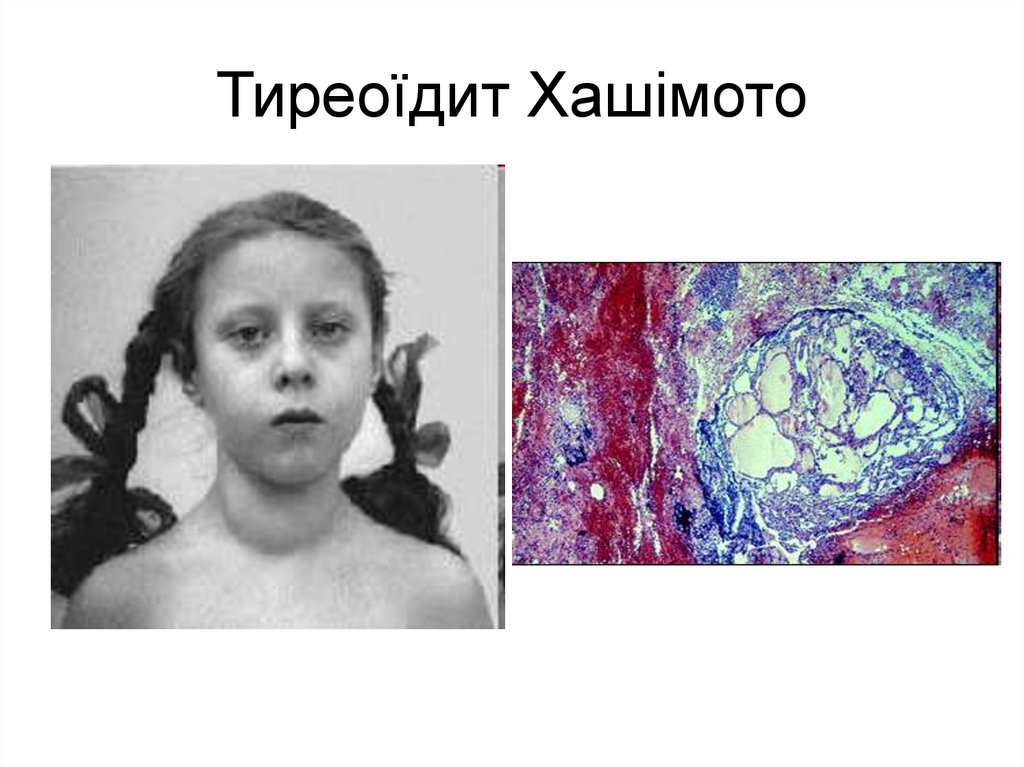
22. Тиреоїдит Хашімото
• ТиреоїдитХашімото
характеризується функціональною
неповноцінністю
щитоподібної
залози.
Залоза
збільшена,
спостерігається
інфільтрація
функціонально активної тканини
лімфоцитами і подальша заміна
паренхіми
залози
сполучною
тканиною.
Захворювання
розвивається повільно.
• Частіше хворіють жінки похилого
віку.
• Доведено зв’язок
хвороби з
генами HLA I класу (A2, B16, B35,
B46, B51, B54, C3) в II класу (HLADR3, HLA-DR4, HLA-DQw7 и HLADR5).
23. Тиреоїдит Хашімото
• Вперше аутоімунний тиреоїдит(АІТ) як окрему нозологічну одиницю у
1912 р. виділив H. Hashimoto на основі
спостереження ураження щитовидної
залози у 4 жінок. Цю хворобу H.
Hashimoto назвав struma
lymphomatosa. АІТ у дітей описано
вперше у 1938 р.
• На АІТ страждають 1–3 %
населення Землі. Виникнення АІТ у
дітей можливе з дошкільного віку.
Поширеність АІТ серед дітей і підлітків
становить від 0,2 до 4 %. Максимальна
частота розвитку АІТ – у пре- і
пубертатному періоді, причому частота
виявлення АІТ у дівчаток майже на
порядок вища, ніж у хлопчиків.
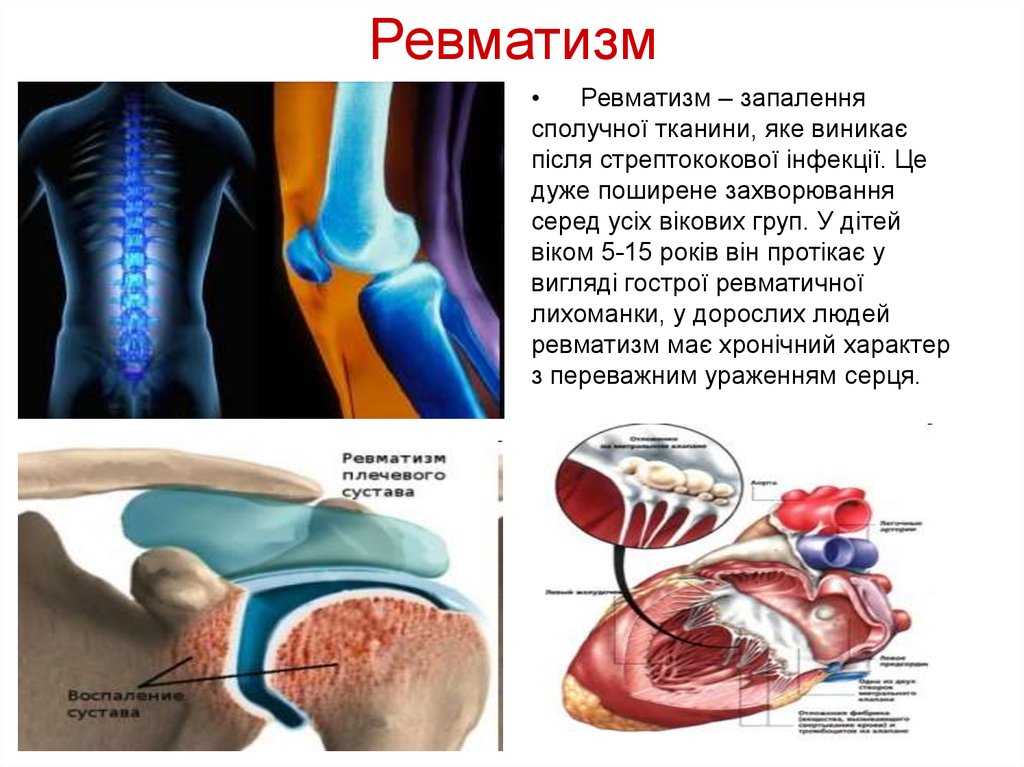
24. Ревматизм
Ревматизм – запалення
сполучної тканини, яке виникає
після стрептококової інфекції. Це
дуже поширене захворювання
серед усіх вікових груп. У дітей
віком 5-15 років він протікає у
вигляді гострої ревматичної
лихоманки, у дорослих людей
ревматизм має хронічний характер
з переважним ураженням серця.
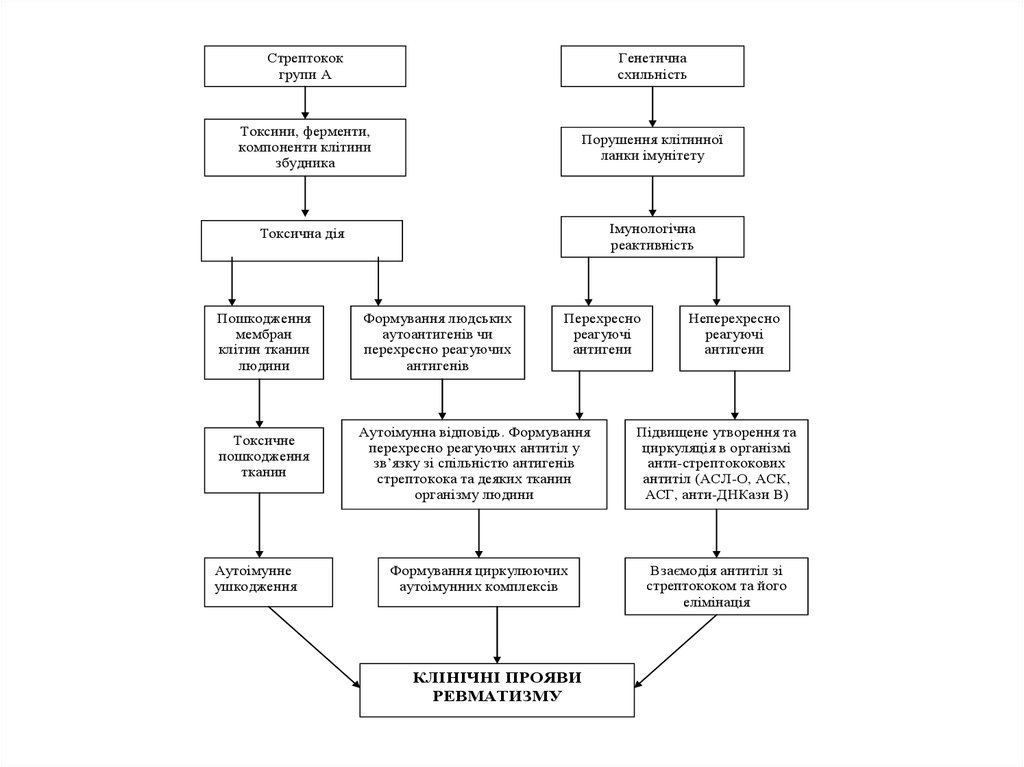
25.
Стрептококгрупи А
Генетична
схильність
Токсини, ферменти,
компоненти клітини
збудника
Порушення клітинної
ланки імунітету
Токсична дія
Імунологічна
реактивність
Пошкодження
мембран
клітин тканин
людини
Токсичне
пошкодження
тканин
Аутоімунне
ушкодження
Формування людських
аутоантигенів чи
перехресно реагуючих
антигенів
Перехресно
реагуючі
антигени
Аутоімунна відповідь. Формування
перехресно реагуючих антитіл у
зв’язку зі спільністю антигенів
стрептокока та деяких тканин
організму людини
Формування циркулюючих
аутоімунних комплексів
КЛІНІЧНІ ПРОЯВИ
РЕВМАТИЗМУ
Неперехресно
реагуючі
антигени
Підвищене утворення та
циркуляція в організмі
анти-стрептококових
антитіл (АСЛ-О, АСК,
АСГ, анти-ДНКази В)
Взаємодія антитіл зі
стрептококом та його
елімінація
26. У розвитку АІЗ беруть участь кілька генетичних факторів:
• -гени,що
визначають
загальну
схильність до розвитку аутоімунної
патології,
органоспецифічної
чи
неспецифічної,
• -інші гени, які визначають конкретну
мішень – антиген чи антигени, проти яких
направлена аутоімунна реакція.
27. Роль генетичних факторів у розвитку АІЗ :
Серед хворих на ревматизм частіше зустрічаються особи з
групами крові А(II) та В(III).
Припускають зв’язок ревматизму з антигенами гістосумісності HLA
A8, B5, B7, BW 35. У хворих росіян переважають HLA A11, BW 35, DR
5, DR 7, CW 2, CW 3.
У хворих з клапанними ураженнями серця підвищена частота
носійства HLA-А3, при ураженні аортального клапану – В15.
Існує схильність до ревматизму, в якій визначається комплекс
порушень в системі специфічного та неспецифічного захисту. Ще
С.Б.Боткін в 1885 р. відмітив, що на ревматизм частіше хворіють люди,
в яких батько й мати також хворіли на ревматизм.
Пізніше було показано, що частота ревматизму в сім’ях
коливається від 10% до 50%, що значно перевищує його поширеність в
популяції (1,5%). Частота випадків ревматизму через родичів першого
ступеня спорідненості не перевищує 15-20%
Тиреоїдит Хашімото: доведеним є зв’язок з HLA-DR3 і HLA-DR5
Хвороба Адісона (недостатність наднирників) – зв’язок з HLA-В8
28. Ознаки АІЗ
• наявність в сироватці крові і в тканинах АТ, щореагують in vitro та in vivo з АГ певного органу чи
системи тканин,
• підвищений вміст гама-глобулінів у сироватці крові
(гіпергамаглобулінемія),
• активація проліферативних процесів у лімфовузлах
та селезінці,
• дифузна лімфоїдно-плазмоклітинна інфільтрація
ураженого органу чи системи тканин,
• гіперплазія епітелію і утворення лімфоїдних фолікул
із зародковими центрами в мозковій речовині тимусу,
• імунодепресивні засоби призупиняють розвиток
патологічного процесу.
29. ДІАГНОСТИКА АУТОІМУННИХ ЗАХВОРЮВАНЬ
• Точна діагностика аутоагресії можлива принаявності таких критеріїв:
• прямого доказу циркулюючих або зв’язаних
аутоантитіл
чи
сенсибілізованих
лімфоцитів,
спрямованих проти антигену, асоційованого з даним
захворюванням.
• ідентифікації аутоантигену, проти якого спрямована
імунна відповідь.
• переносу аутоімунного процесу з допомогою
сироватки, що містить антитіла, чи лімфоцитами.
• можливості створення експериментальної моделі
захворювання
з
відповідними
морфологічними
порушеннями
шляхом
переносу
сироватки
чи
лімфоцитів.
30. ЛІКУВАННЯ АУТОІМУННИХ ЗАХВОРЮВАНЬ
• Елімінація “заборонених” клонів сенсибілізованих лімфоцитів.• Видалення імуногену чи ад’юванту.
• Імуносупресорна терапія повинна бути диференційованою і по
можливості короткою.
• Блокада медіаторів
імунних
реакцій
антигістамінними
препаратами, зміїною отрутою, що руйнує комплемент і т.д.
• Замісна терапія необхідними метаболітами (при перніціозній
анемії – вітаміном В 12, при мікседемі – тироксином.
• Протизапальні засоби: кортикостероїди, препарати саліцилової
кислоти.
• Імунотерапія: десенсибілізація причинними алергенами, при
наявності гіперчутливості негайного типу – стимуляція синтезу Ig G
(чи його введення), що конкурує з Ig E.
• Імунокорекція дефіциту чи функціонального дефекту Тсупресорів.
























 Медицина
Медицина








