Похожие презентации:
Реакционная способность карбоновых кислот
1. Реакционная способность карбоновых кислот
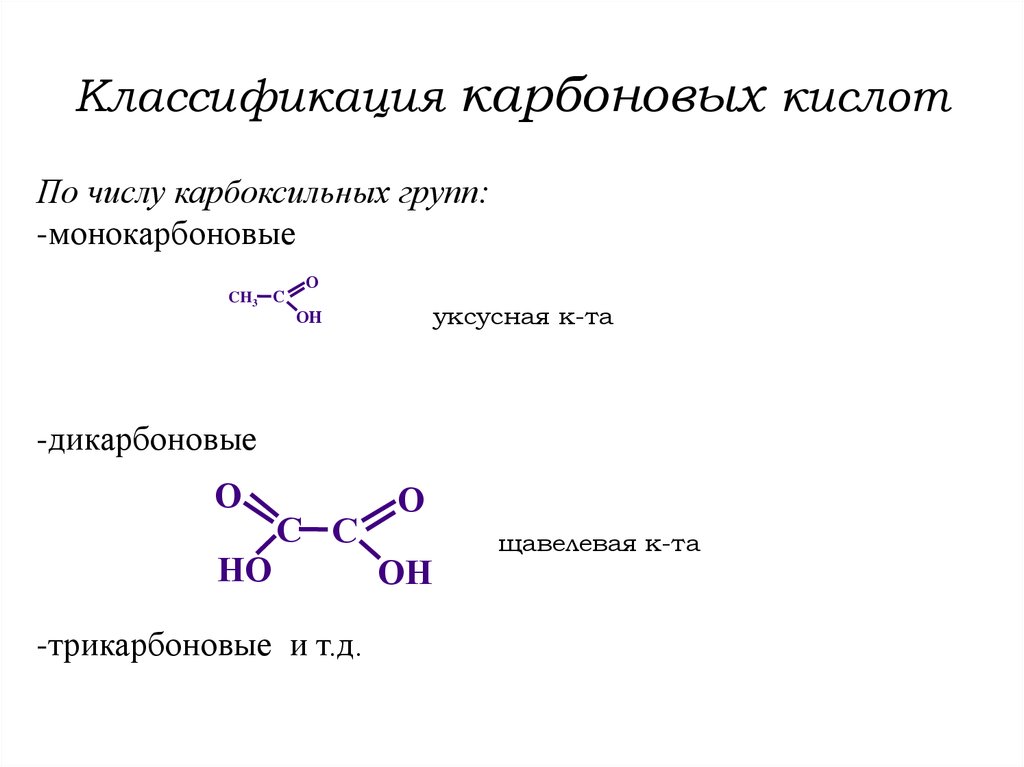
2. Классификация карбоновых кислот
По числу карбоксильных групп:-монокарбоновые
CH3
C
O
уксусная к-та
OH
-дикарбоновые
O
HO
C C
-трикарбоновые и т.д.
O
OH
щавелевая к-та
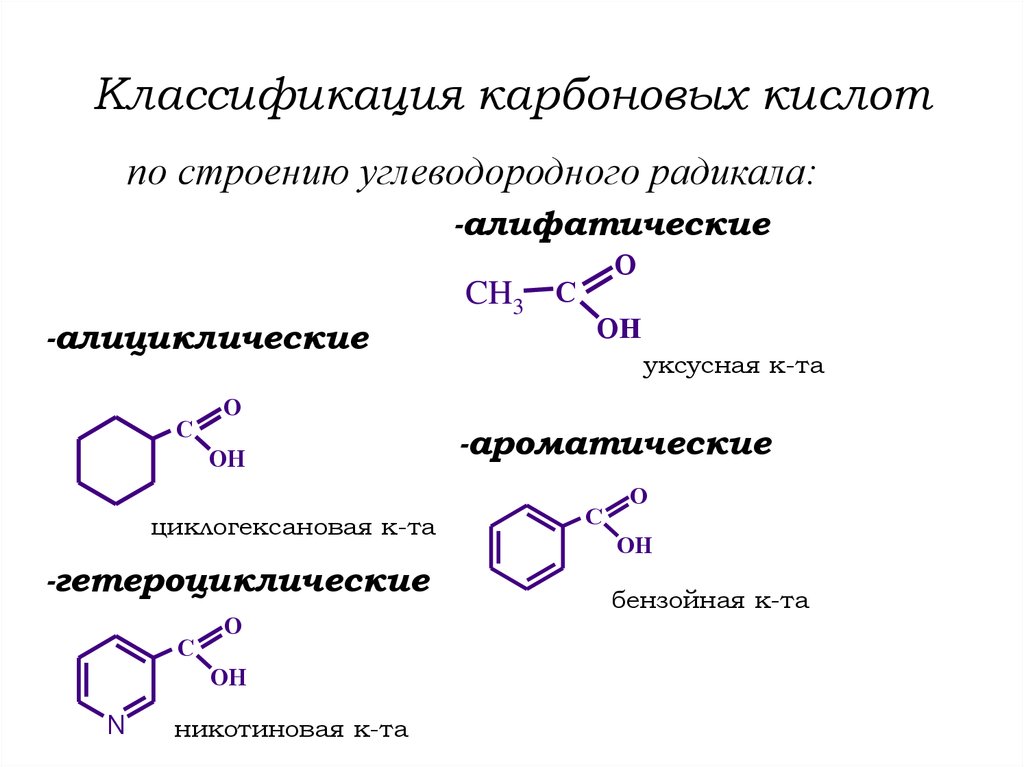
3. Классификация карбоновых кислот
по строению углеводородного радикала:-алифатические
-алициклические
C
циклогексановая к-та
-гетероциклические
O
OH
N
OH
уксусная к-та
O
OH
C
CH3 C
O
никотиновая к-та
-ароматические
C
O
OH
бензойная к-та
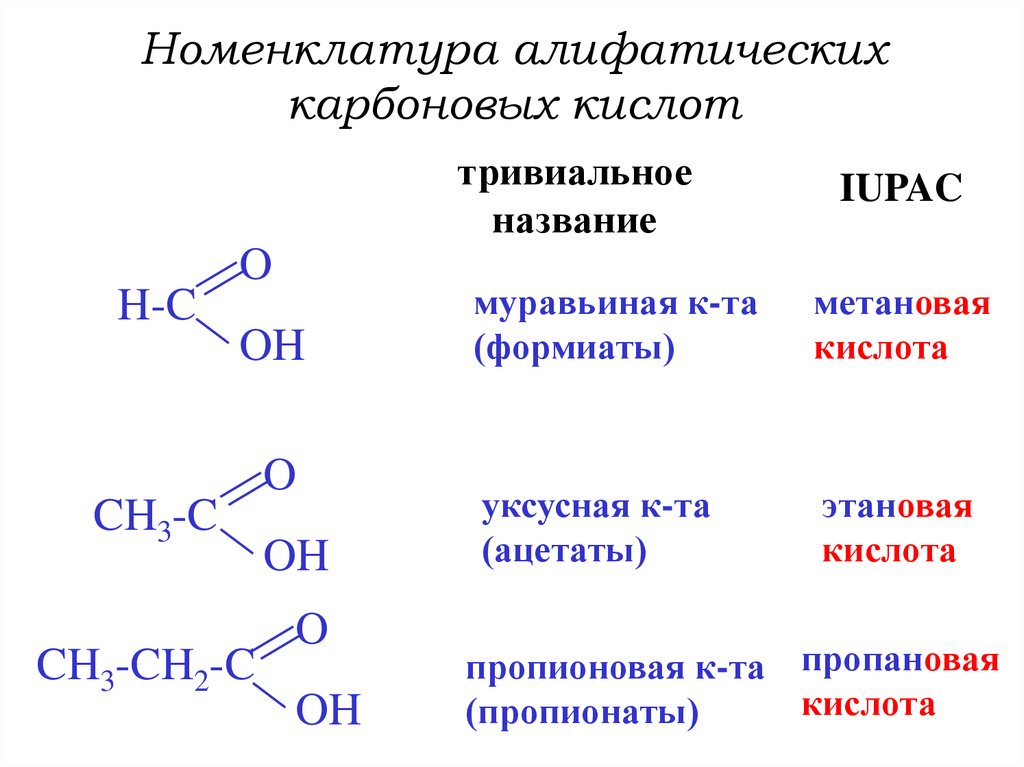
4. Номенклатура алифатических карбоновых кислот
тривиальноеназвание
H-C
O
OH
CH3-C
CH3-CH2-C
O
OH
O
OH
IUPAC
муравьиная к-та
(формиаты)
метановая
кислота
уксусная к-та
(ацетаты)
этановая
кислота
пропионовая к-та пропановая
кислота
(пропионаты)
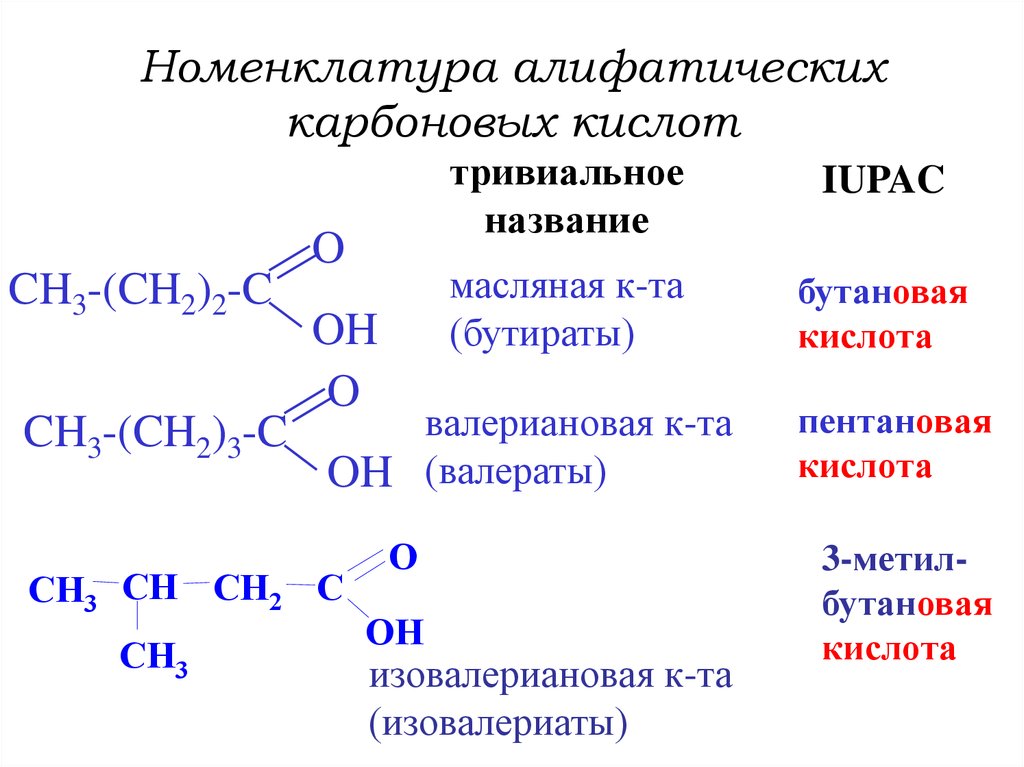
5. Номенклатура алифатических карбоновых кислот
CH3-(CH2)2-CCH3-(CH2)3-C
O
OH
O
IUPAC
масляная к-та
(бутираты)
бутановая
кислота
валериановая к-та
OH (валераты)
CH3 CH CH2 C
CH3
тривиальное
название
O
OH
изовалериановая к-та
(изовалериаты)
пентановая
кислота
3-метилбутановая
кислота
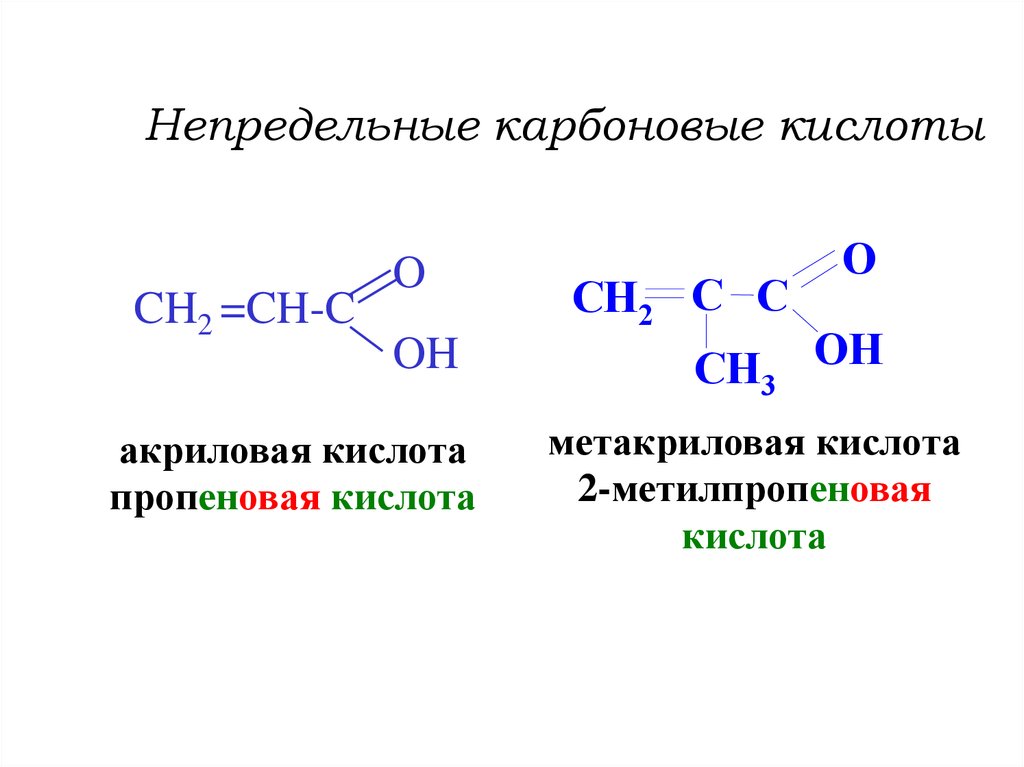
6. Непредельные карбоновые кислоты
CH2 =CH-CO
OH
акриловая кислота
пропеновая кислота
CH2 C C
O
CH3 OH
метакриловая кислота
2-метилпропеновая
кислота
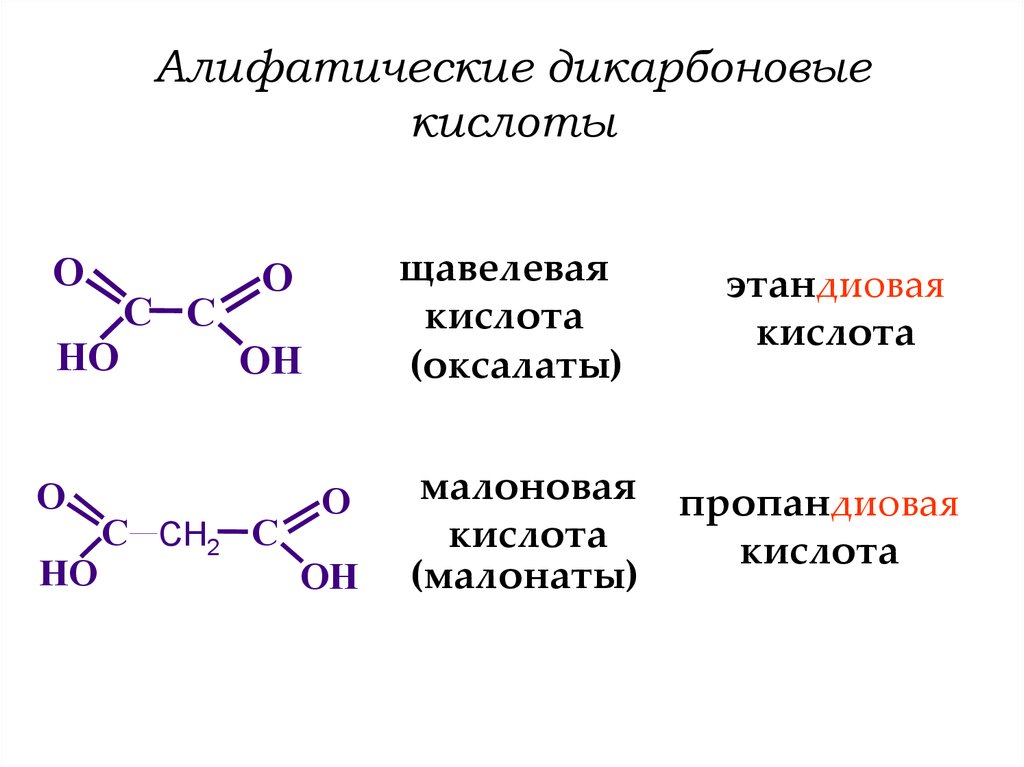
7. Алифатические дикарбоновые кислоты
OHO
O
HO
C C
щавелевая
кислота
(оксалаты)
O
OH
C CH2 C
O
OH
малоновая
кислота
(малонаты)
этандиовая
кислота
пропандиовая
кислота
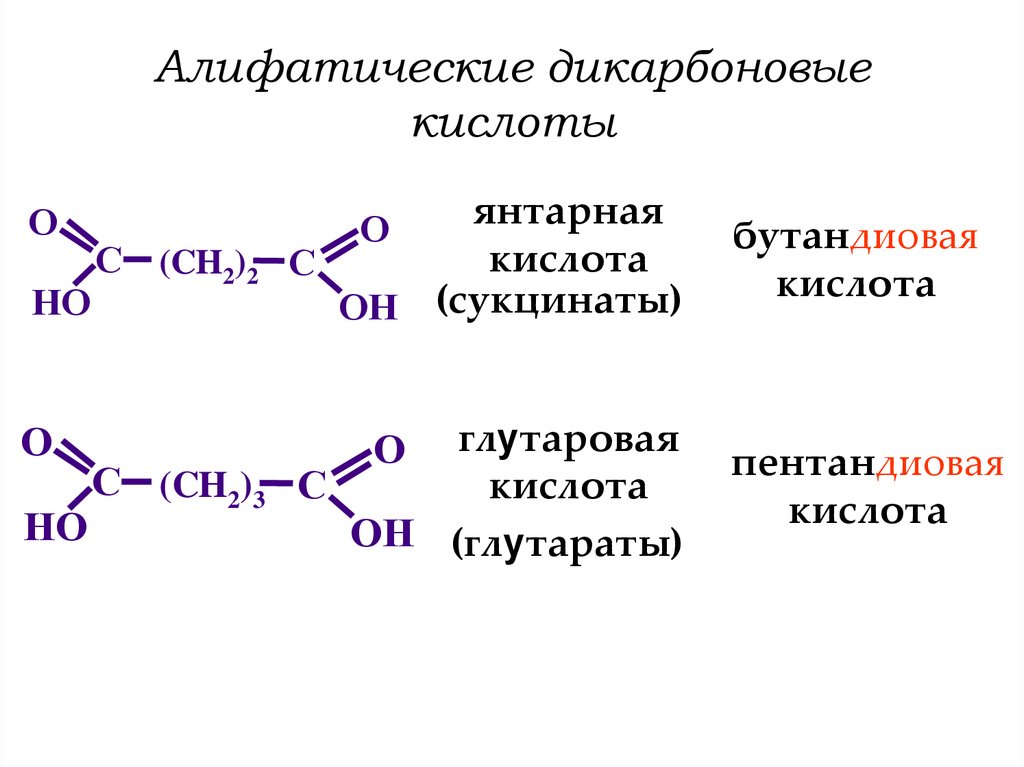
8. Алифатические дикарбоновые кислоты
OHO
O
HO
C (CH2)2
янтарная
кислота
C
OH (сукцинаты)
бутандиовая
кислота
C (CH2)3
глутаровая
C
кислота
OH (глутараты)
пентандиовая
кислота
O
O
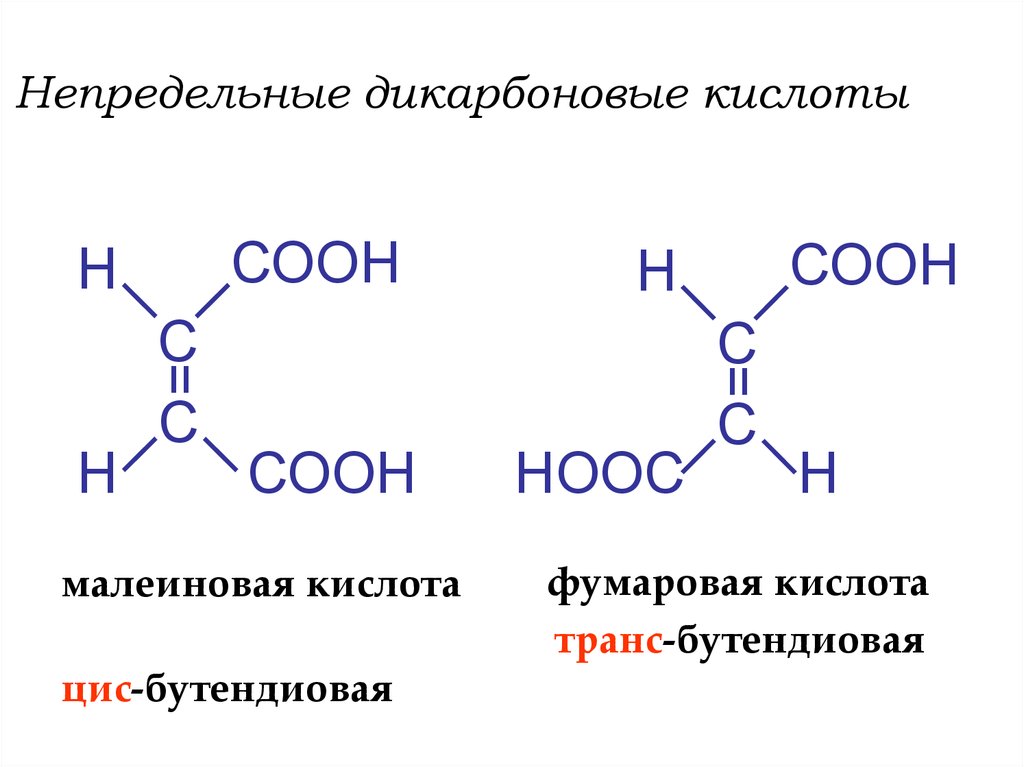
9. Непредельные дикарбоновые кислоты
СООНН
Н
С
С
=
=
С
С
СООН
Н
СООН
малеиновая кислота
цис-бутендиовая
НООС
Н
фумаровая кислота
транс-бутендиовая
10. Реакционные центры в молекулах карбоновых кислот
δ-H
δ' +
R
C
δ+
C
O:
..
O
основный центр
H
H
OH-кислотный центр
CH-кислотный
электрофильный
центр
центр
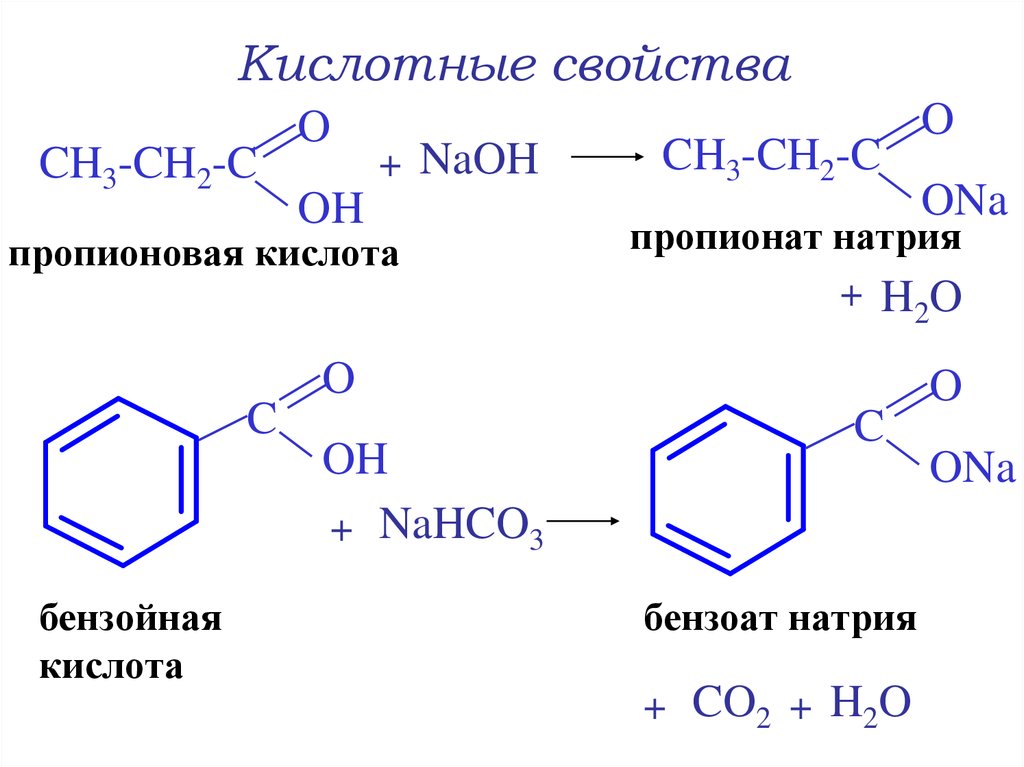
11. Кислотные свойства
CH3-CH2-CO
+ NaOH
OH
пропионовая кислота
C
бензойная
кислота
CH3-CH2-C
ONa
пропионат натрия
+ H 2O
O
OH
+ NaHCO3
O
C
бензоат натрия
+ CO2 + H2O
O
ONa
12. Кислотные свойства карбоновых кислот
Электроноакцепторные заместители врадикале
карбоновых
кислот
повышают их кислотные свойства,
электронодонорные
–
понижают.
В гомологическом ряду предельных
алифатических карбоновых кислот
кислотность понижается.
13. Реакции нуклеофильного замещения
О+ E+ NuR–С
ОН
+
-E
OE+
OE
R– С – Nu
OH
R– С – Nu
присоединение
OH
E+
замещение
R–С
О
Nu
+ E+ OH-
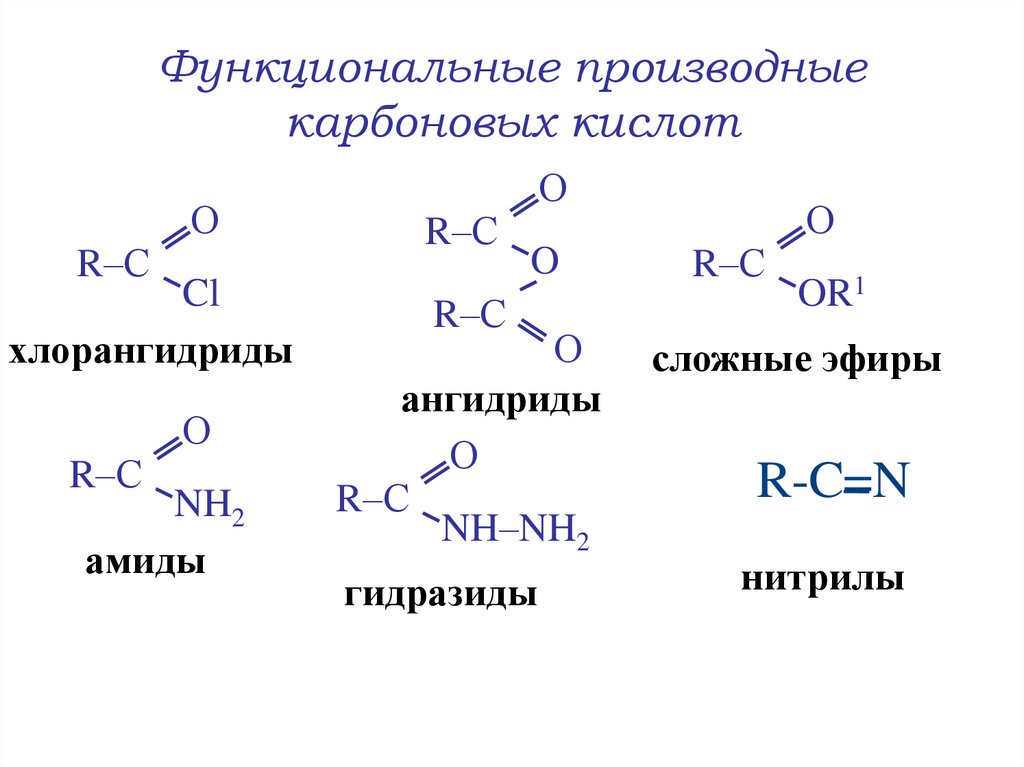
14. Функциональные производные карбоновых кислот
R–СCl
хлорангидриды
О
R–С
NH2
амиды
R–С
O
R–С
О
О
О
ангидриды
О
R–С
NH–NH2
гидразиды
О
R–С
OR1
сложные эфиры
R-C=N
нитрилы
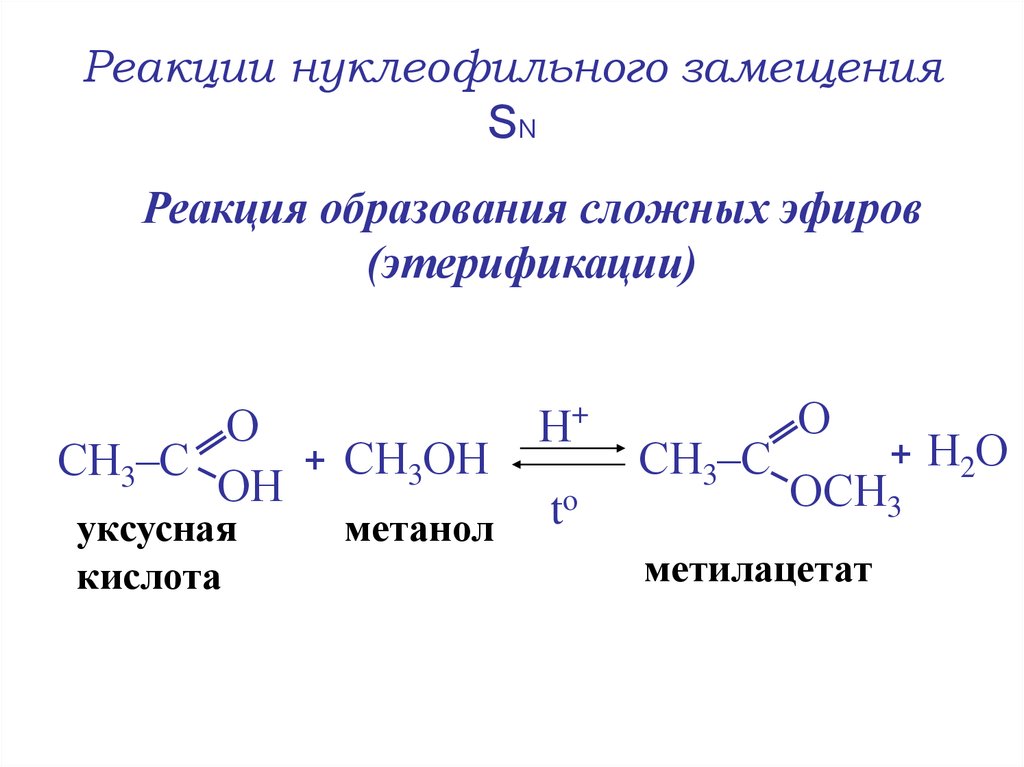
15. Реакции нуклеофильного замещения SN
Реакция образования сложных эфиров(этерификации)
О
+ СН3ОН
СН3–С
ОН
уксусная
кислота
метанол
Н+
to
СН3–С
О
+ Н2О
ОСН3
метилацетат
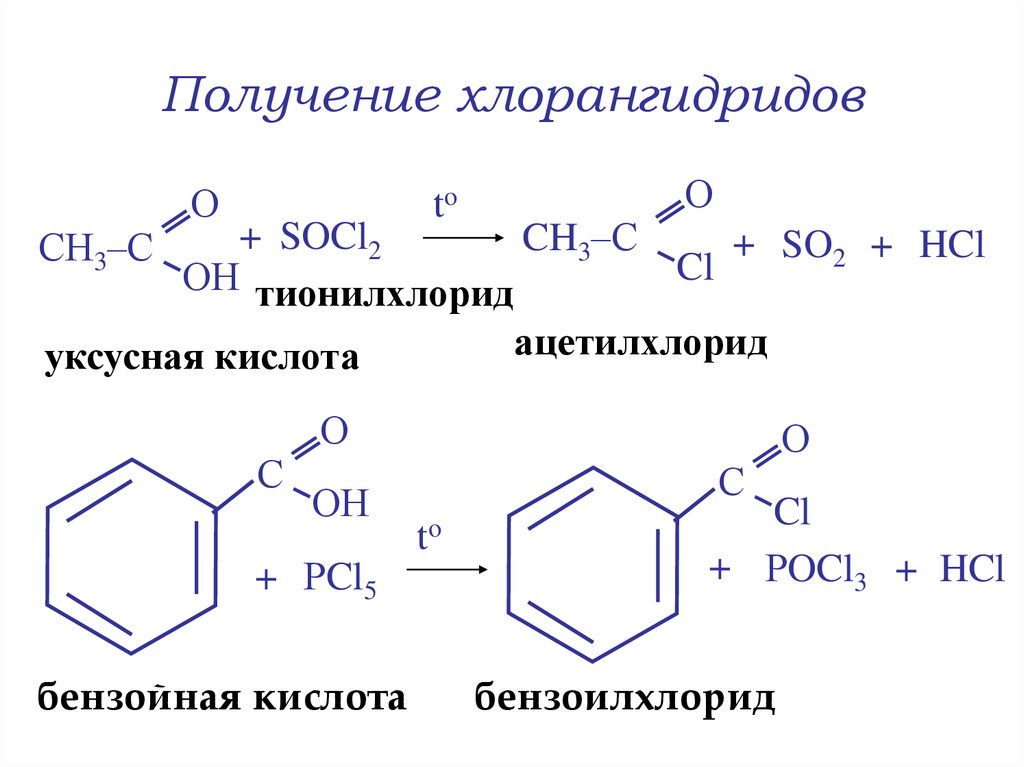
16. Получение хлорангидридов
Оto
О
+ SOCl2
CH3–С
+ SO2 + HCl
Cl
ОН тионилхлорид
ацетилхлорид
уксусная кислота
СН3–С
С
О
ОН
+ РCl5
бензойная кислота
С
to
О
Cl
+ РOCl3 + HCl
бензоилхлорид
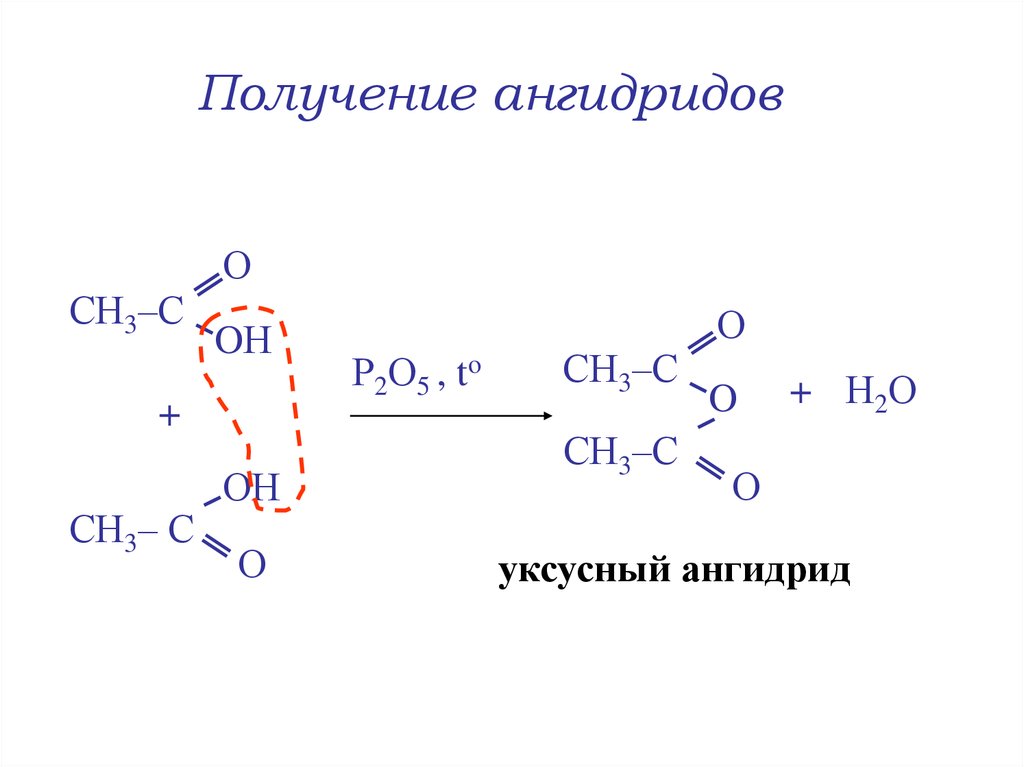
17. Получение ангидридов
ОOН
+
О
СН3– С
ОН
Р2О5 , to
СН3–С
СН3–С
О
O
+ Н2О
О
СН3–С
уксусный ангидрид
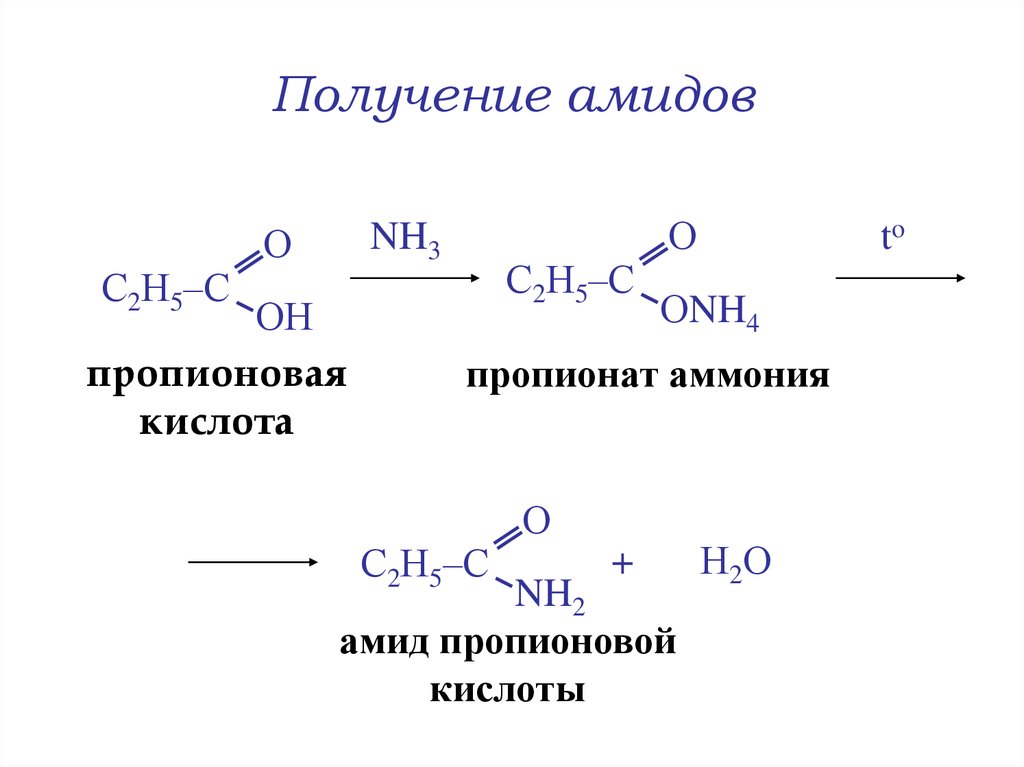
18. Получение амидов
С2Н5–СО
NH3
ОН
пропионовая
кислота
С2Н5–С
О
to
ОNH4
пропионат аммония
С2Н5–С
О
+
NH2
амид пропионовой
кислоты
Н2О
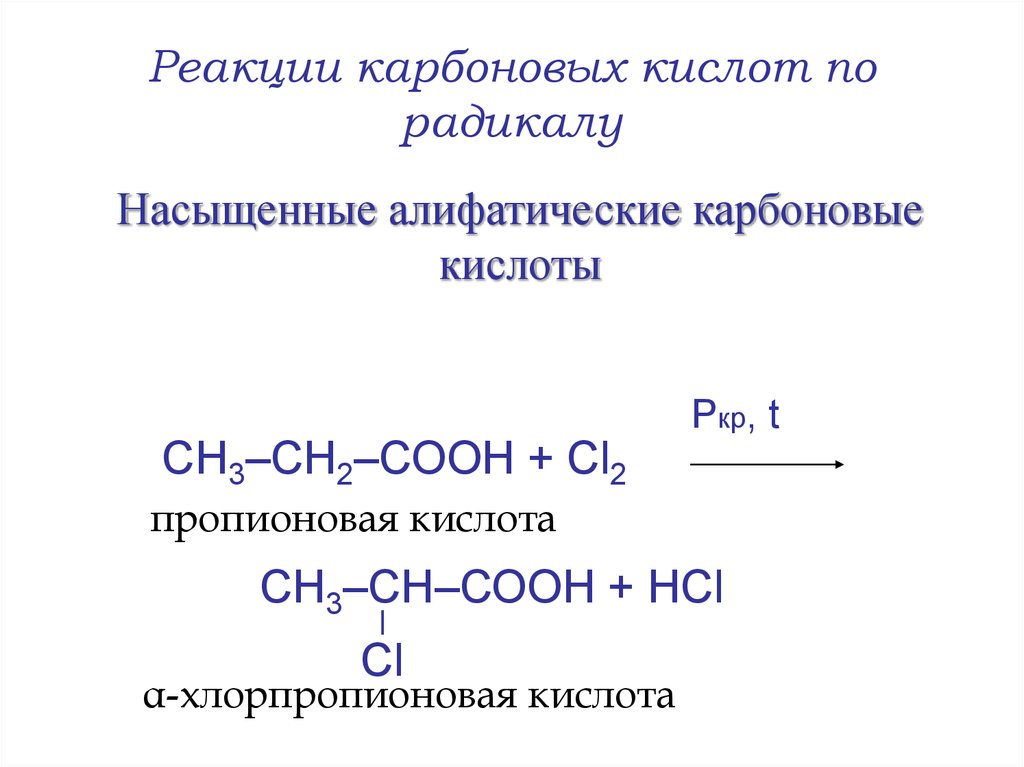
19. Реакции карбоновых кислот по радикалу
Насыщенные алифатические карбоновыекислоты
СН3–СН2–СООН + Cl2
Ркр, t
пропионовая кислота
СН3–СН–СООН + НCl
Cl
α-хлорпропионовая кислота
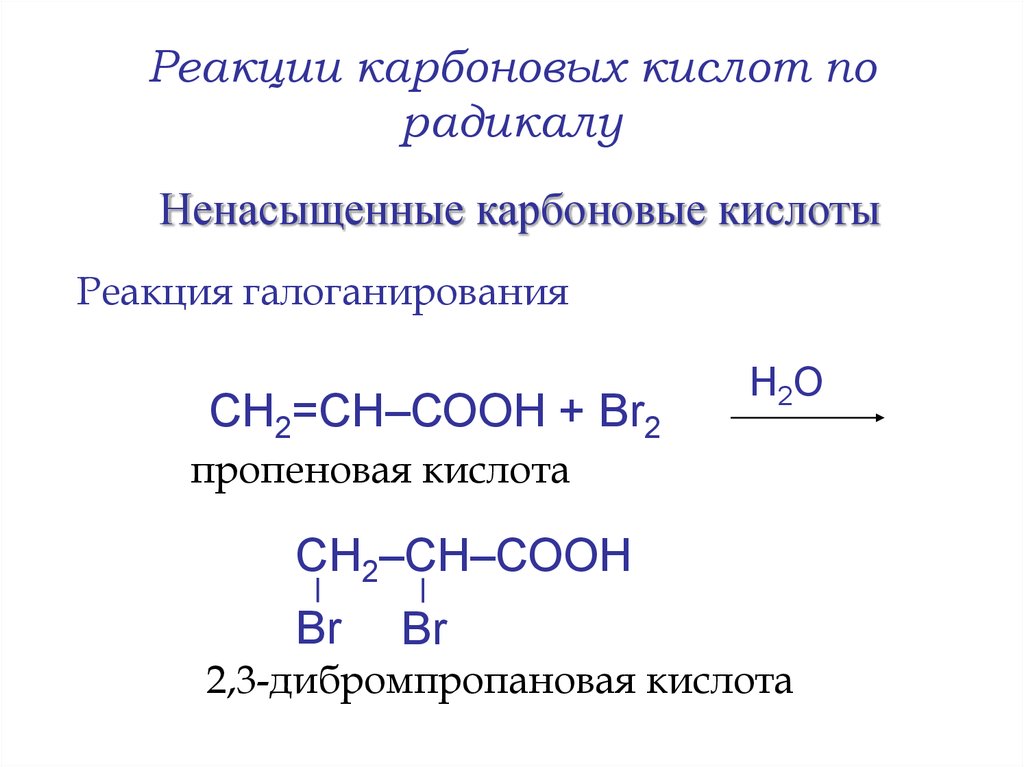
20. Реакции карбоновых кислот по радикалу
Ненасыщенные карбоновые кислотыРеакция галоганирования
СН2=СН–СООН + Br2
H2 O
пропеновая кислота
СН2–СН–СООН
Br
Br
2,3-дибромпропановая кислота
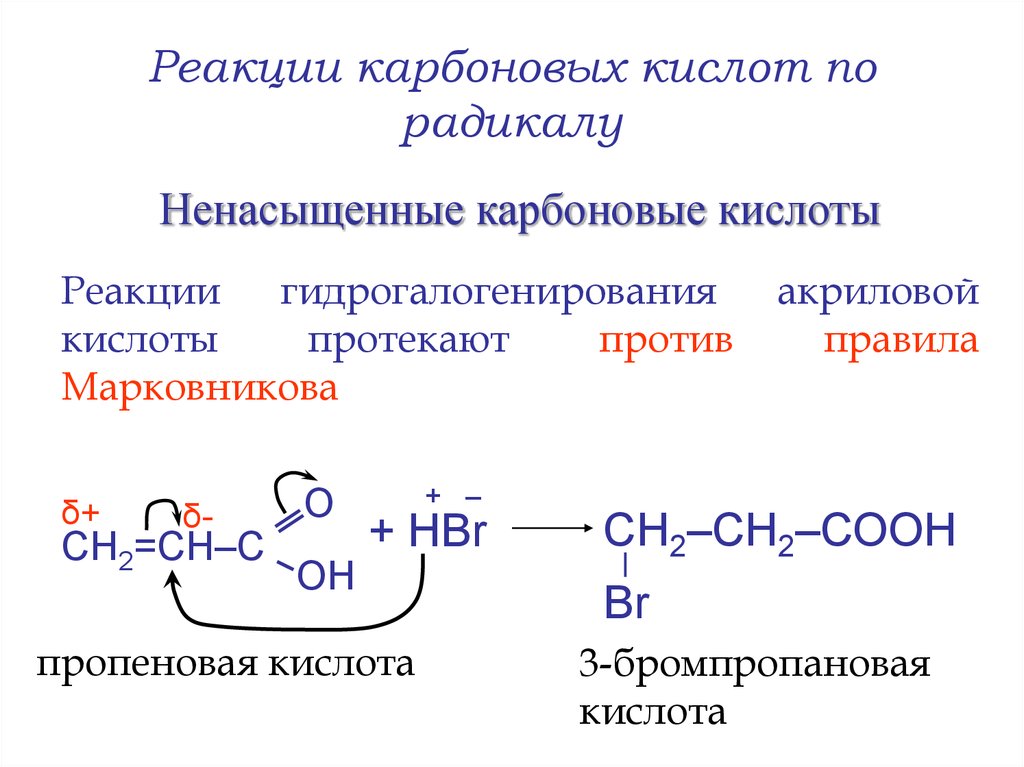
21. Реакции карбоновых кислот по радикалу
Ненасыщенные карбоновые кислотыРеакции
гидрогалогенирования
кислоты
протекают
против
Марковникова
δ+
δ-
СН2=СН–С
О
ОН
+ –
+ НBr
пропеновая кислота
акриловой
правила
СН2–СН2–СООН
Br
3-бромпропановая
кислота
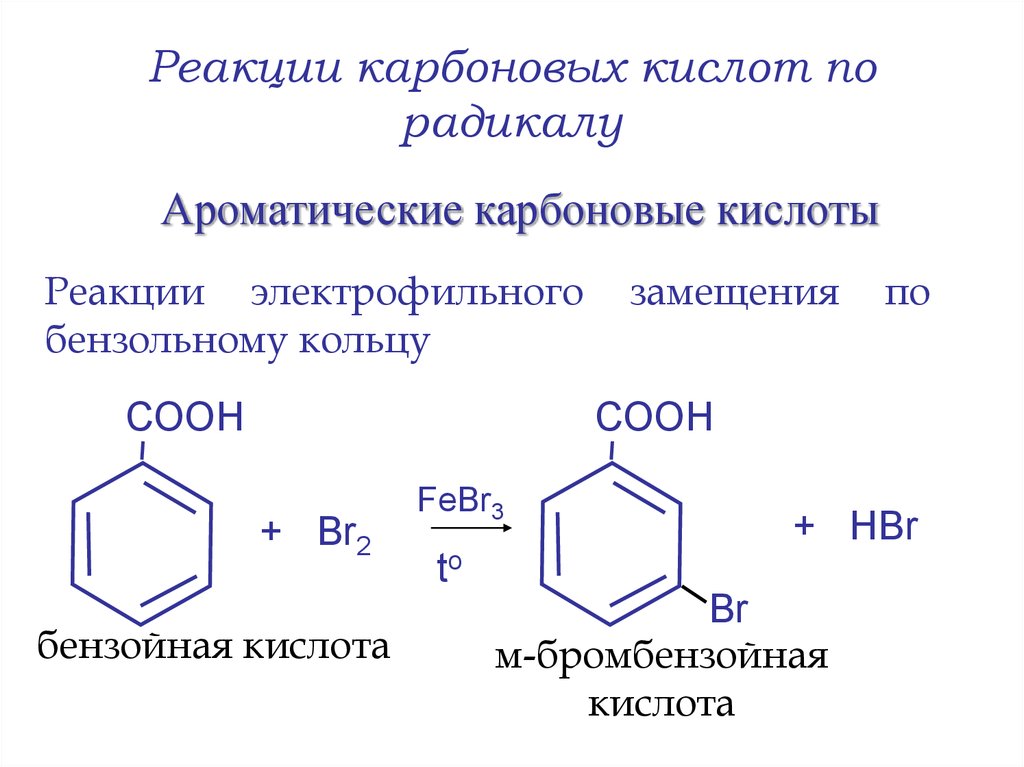
22. Реакции карбоновых кислот по радикалу
Ароматические карбоновые кислотыРеакции электрофильного
бензольному кольцу
СООН
замещения
по
СООН
+ Br2
бензойная кислота
FeBr3
+ НBr
to
Br
м-бромбензойная
кислота
23. Дикарбоновые кислоты
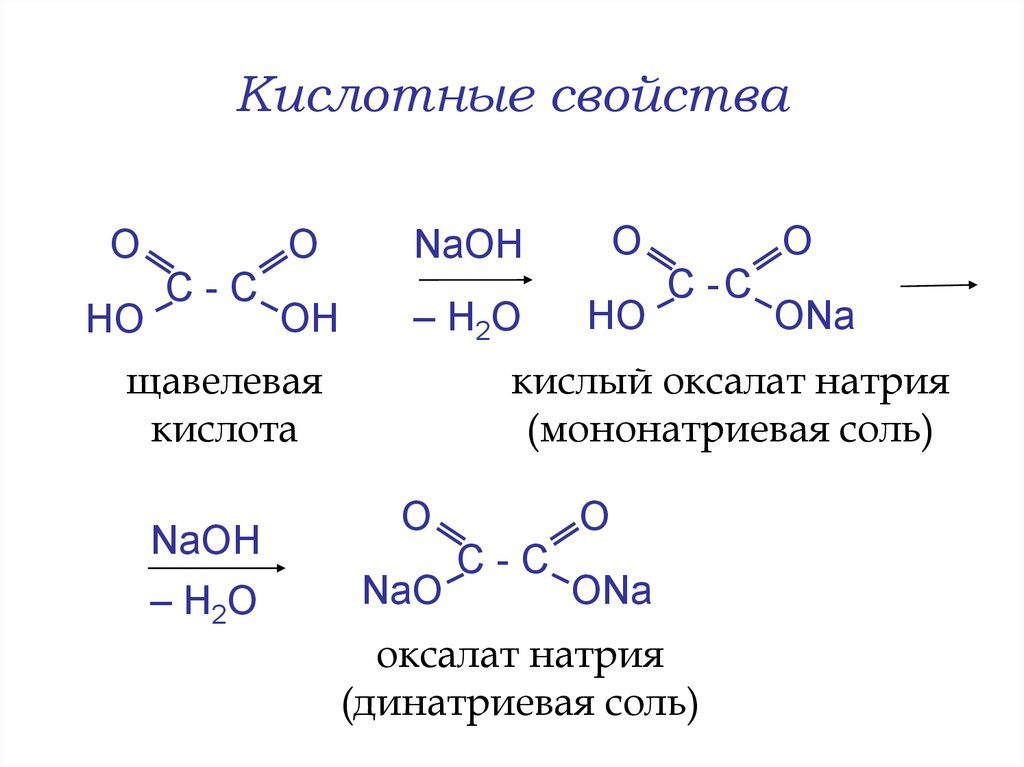
24. Кислотные свойства
ОHO
С-С
О
NaOH
О
ОН
– Н2O
HO
щавелевая
кислота
NaOH
– Н2O
С -С
О
ОNa
кислый оксалат натрия
(мононатриевая соль)
О
NaO
С-С
О
ОNa
оксалат натрия
(динатриевая соль)
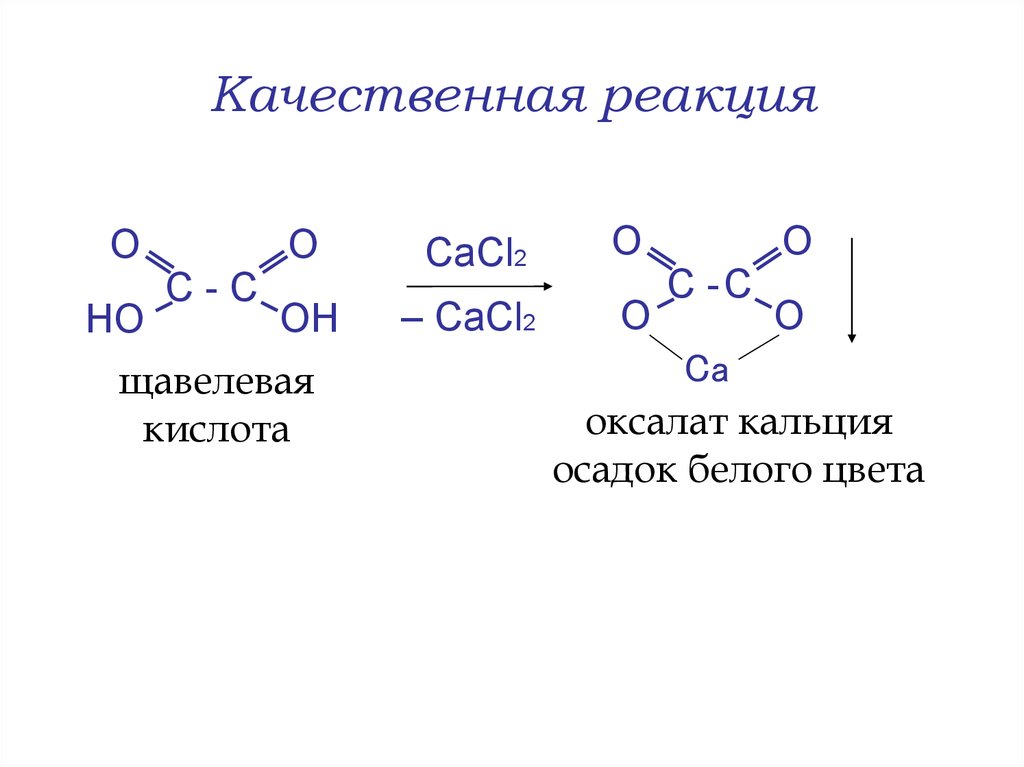
25. Качественная реакция
ОHO
С-С
О
СaСl2
О
ОН
– СaCl2
O
щавелевая
кислота
С -С
О
О
Ca
оксалат кальция
осадок белого цвета
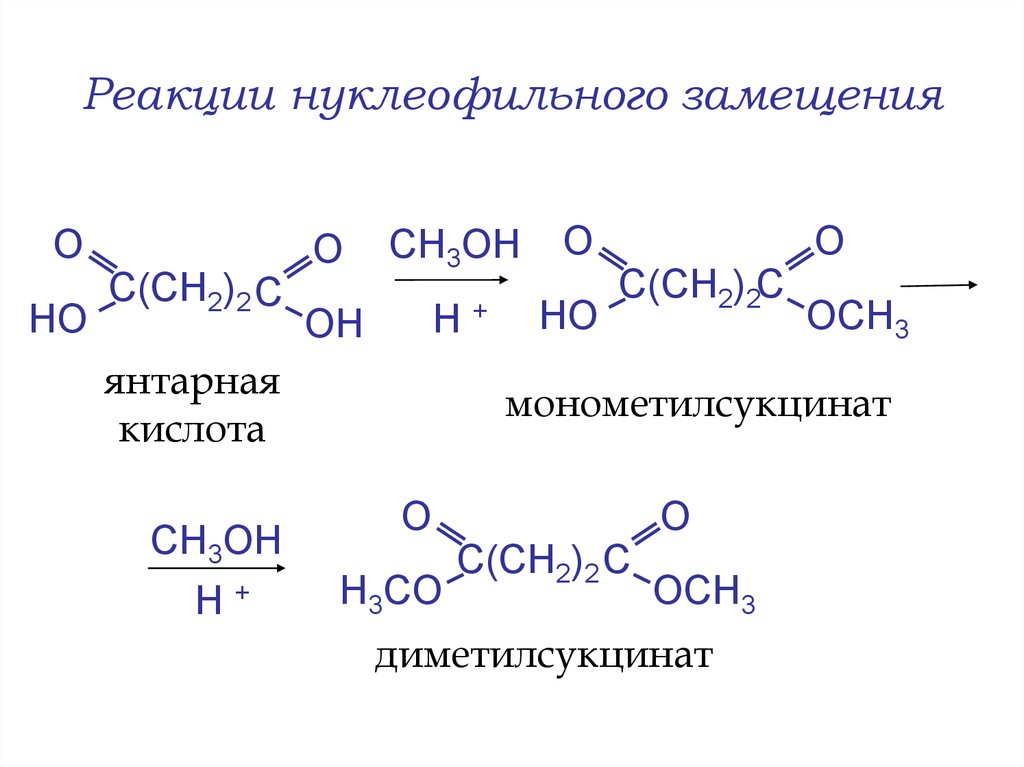
26. Реакции нуклеофильного замещения
ОHO
С(СН2)2 С
О
СН3OH
О
ОН
Н+
HO
янтарная
кислота
СН3OH
Н+
С(СН2)2С
О
ОСН3
монометилсукцинат
О
Н3СO
С(СН2)2 С
О
ОСН3
диметилсукцинат
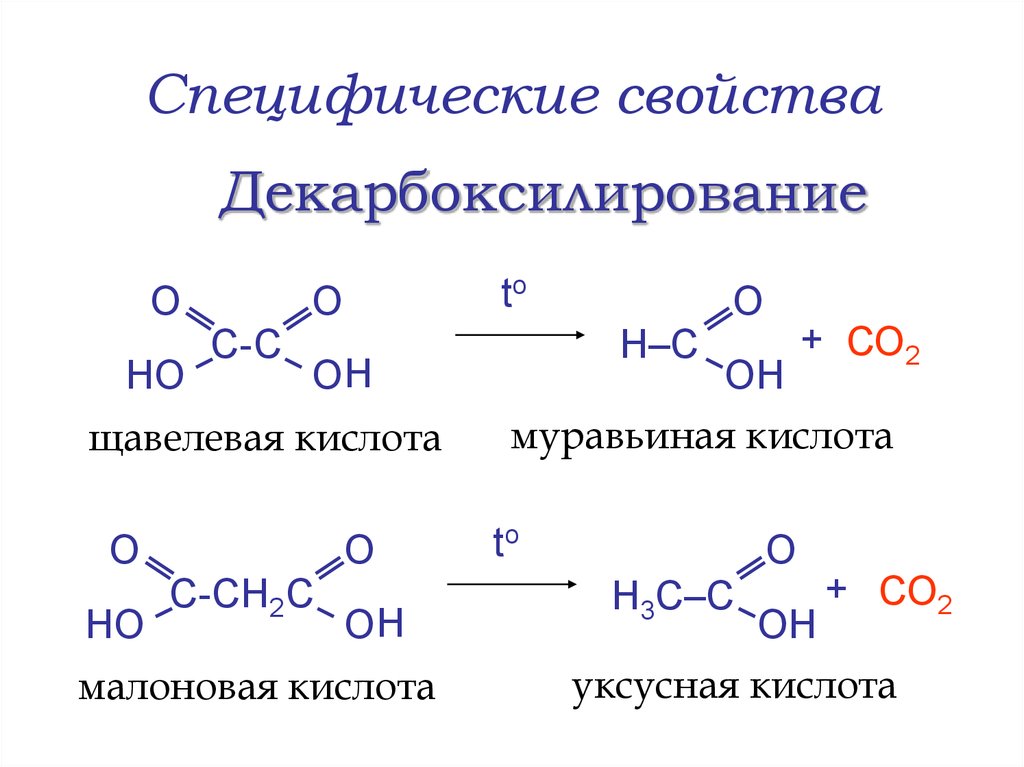
27. Специфические свойства
ДекарбоксилированиеО
HO
С- С
О
to
ОН
ОН
муравьиная кислота
щавелевая кислота
О
HO
С-СН2 С
О
ОН
малоновая кислота
Н–С
О
to
+ СО2
О
Н3С–С
+ СО2
ОН
уксусная кислота
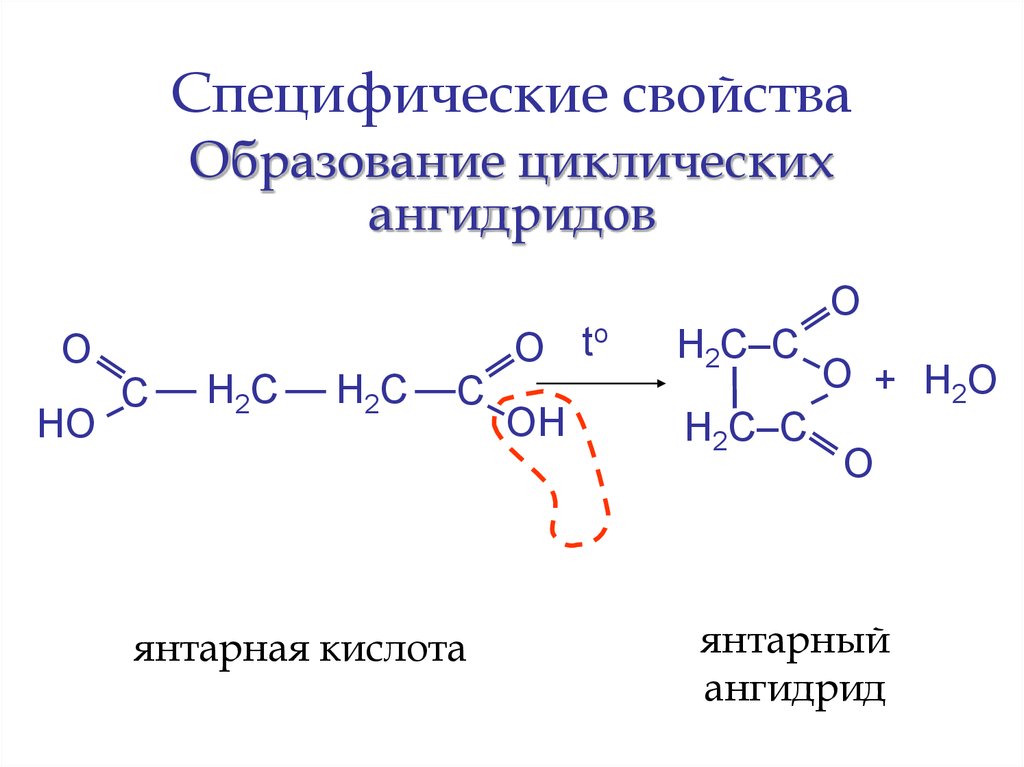
28. Специфические свойства
Образование циклическихангидридов
HO
С
Н2С
Н2С
С
янтарная кислота
О to
Н2С–С
ОН
Н2С–С
O + Н2О
О
О
О
янтарный
ангидрид





 Химия
Химия








