Похожие презентации:
Генетическая связь между основными классами органических соединений
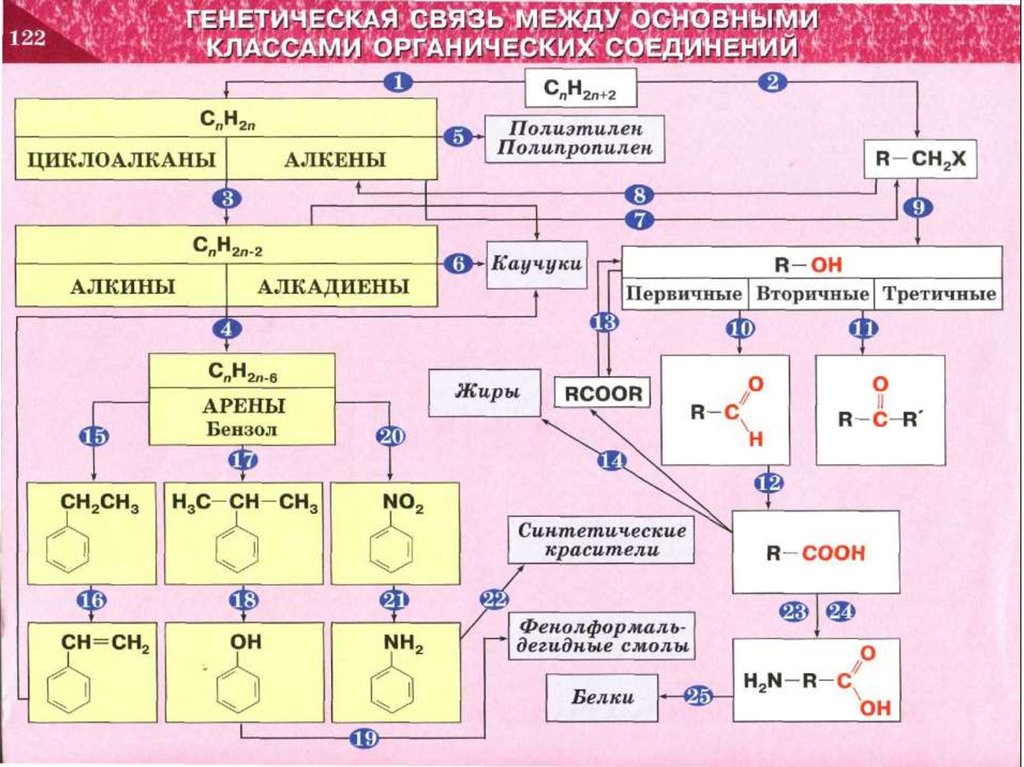
1. Генетическая связь между основными классами органических соединений
Санкт-Петербургский государственный университетГенетическая связь между
основными классами
органических соединений
профессор СПбГУ,
доктор химических наук
Карцова Анна Алексеевна
Санкт-Петербург
2011
2.
Алиса (в Стране Чудес Чеширскому коту):– Скажите, а куда мне отсюда
идти?
Чеширский кот:
– Это зависит от того, куда Вы
хотите придти?
2
3.
От простого – к сложномуСостав
Строение
Свойства
3
4.
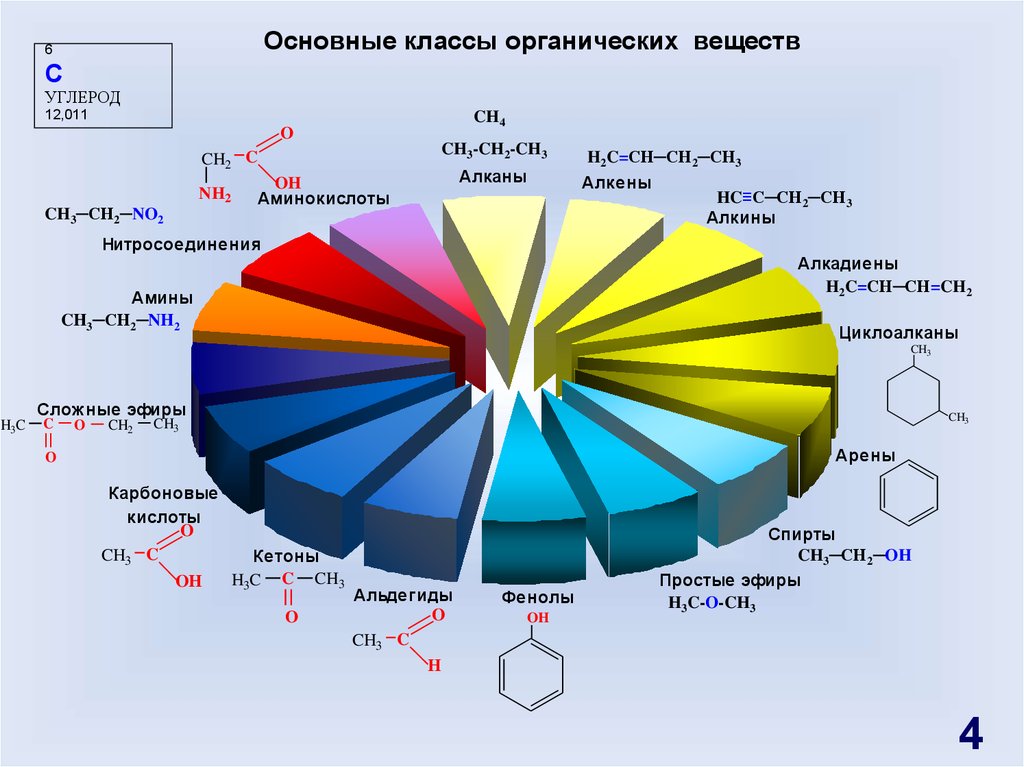
Основные классы органических веществ6
C
УГЛЕРОД
12,011
CH4
O
CH3-CH2-CH3
CH2 C
NH2
CH3─CH2─NO2
OH
Аминокислоты
Алканы
Нитросоединения
H2C=CH─CH2─CH3
Алкены
HC≡C─CH2─CH3
Алкины
Алкадиены
H2C=CH─CH=CH2
Амины
CH3─CH2─NH2
Циклоалканы
CH3
Слож ные эфиры
H3C
C
O
CH2
CH3
CH3
Арены
O
Карбоновые
кислоты
O
CH3 C
OH
Кетоны
H3C C CH3
O
Альдегиды
O
CH3 C
H
Фенолы
OH
Спирты
CH3─CH2─OH
Простые эфиры
H3C-O-CH3
4
5.
Стратегия синтезаВыбор исходного сырья
Построение углеродного остова молекулы
Введение, удаление или замена
функциональной группы
Защита группы
Стереоселективность
«Я хочу воспеть хвалу сотворению молекул
– химическому синтезу…
…Я глубоко убежден, что он и есть
искусство. И в то же время синтез – это
логика».
Роальд Хоффман
(Нобелевская премия по химии 1981 г)
5
6.
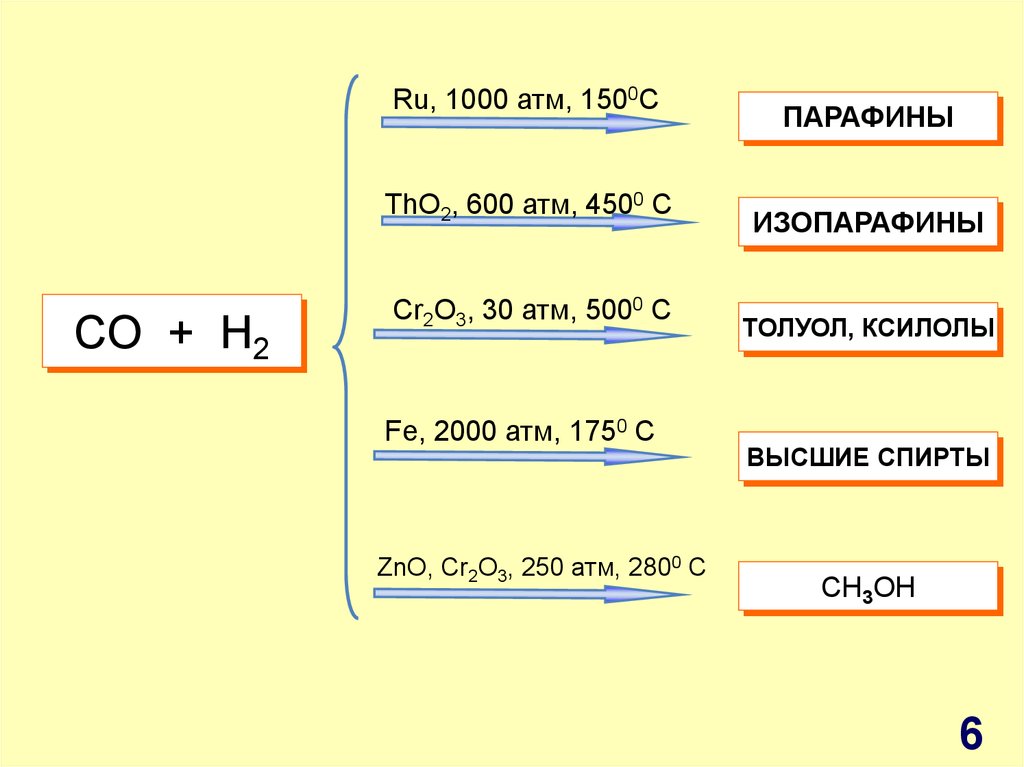
Ru, 1000 атм, 1500CThO2, 600 атм, 4500 C
СO + H2
Cr2O3, 30 атм, 5000 C
Fe, 2000 атм, 1750 C
ZnO, Cr2O3, 250 атм, 2800 C
ПАРАФИНЫ
ИЗОПАРАФИНЫ
ТОЛУОЛ, КСИЛОЛЫ
ВЫСШИЕ СПИРТЫ
СH3OH
6
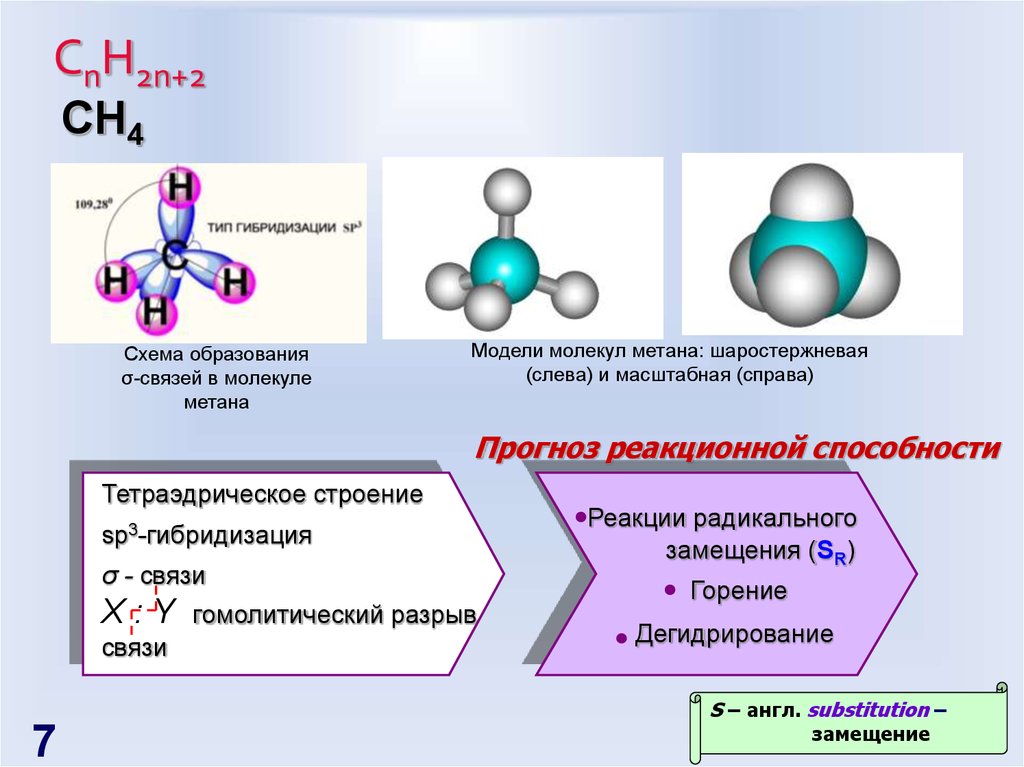
7. СnH2n+2
СH4Схема образования
σ-связей в молекуле
метана
Модели молекул метана: шаростержневая
(слева) и масштабная (справа)
Прогноз реакционной способности
Тетраэдрическое строение
sp3-гибридизация
σ - связи
X:Y
связи
гомолитический разрыв
Реакции радикального
замещения (SR)
Горение
Дегидрирование
S – англ. substitution –
7
замещение
8. СИНТЕЗЫ НА ОСНОВЕ МЕТАНА
8Синтетический
бензин
СИНТЕЗ ГАЗ
СO + H2
СCl3NO2
хлорпикрин
Н2О, Ni, 9000 C
Конверсия
СH3OH – МЕТАНОЛ
HCHO – МЕТАНАЛЬ
HCOOH муравьиная кислота
О2,
Окисление
CH4
МЕТАН
СH3NH2
метиламин
СH3NO2 – НИТРОМЕТАН
HNO3, 4750 C
Нитрование
15000С
пиролиз
Сl2, hγ
Хлорирование
Бензол
С2Н2 – АЦЕТИЛЕН
Н2 – ВОДОРОД
С – САЖА
СH3Cl – МЕТИЛХЛОРИД
СH2Cl2 – ДИХЛОРМЕТАН
растворители
СHCl3 – ТРИХЛОРМЕТАН
СCl4 – ТЕТРАХЛОРМЕТАН
СHFCl2 фреон
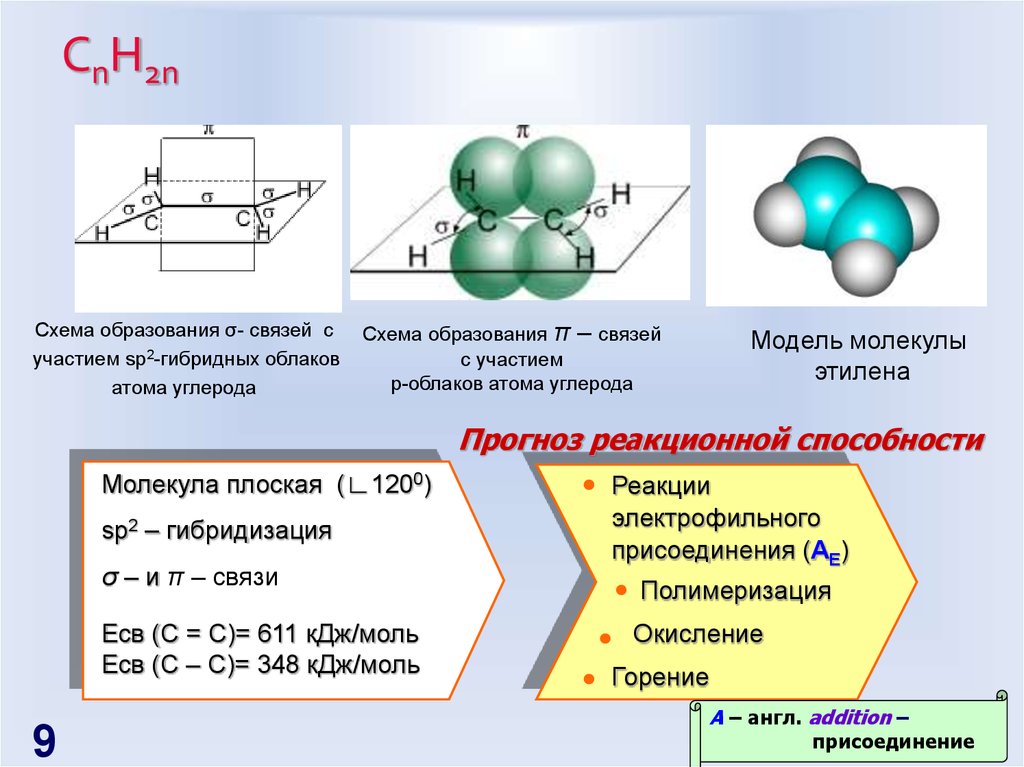
9. СnH2n
Схема образования σ- связей сучастием sp2-гибридных облаков
атома углерода
Схема образования π – связей
с участием
p-облаков атома углерода
Модель молекулы
этилена
Прогноз реакционной способности
Молекула плоская (∟1200)
sp2 – гибридизация
σ – и π – связи
Есв (С = С)= 611 кДж/моль
Есв (С – С)= 348 кДж/моль
9
Реакции
электрофильного
присоединения (AE)
Полимеризация
Окисление
Горение
A – англ. addition –
присоединение
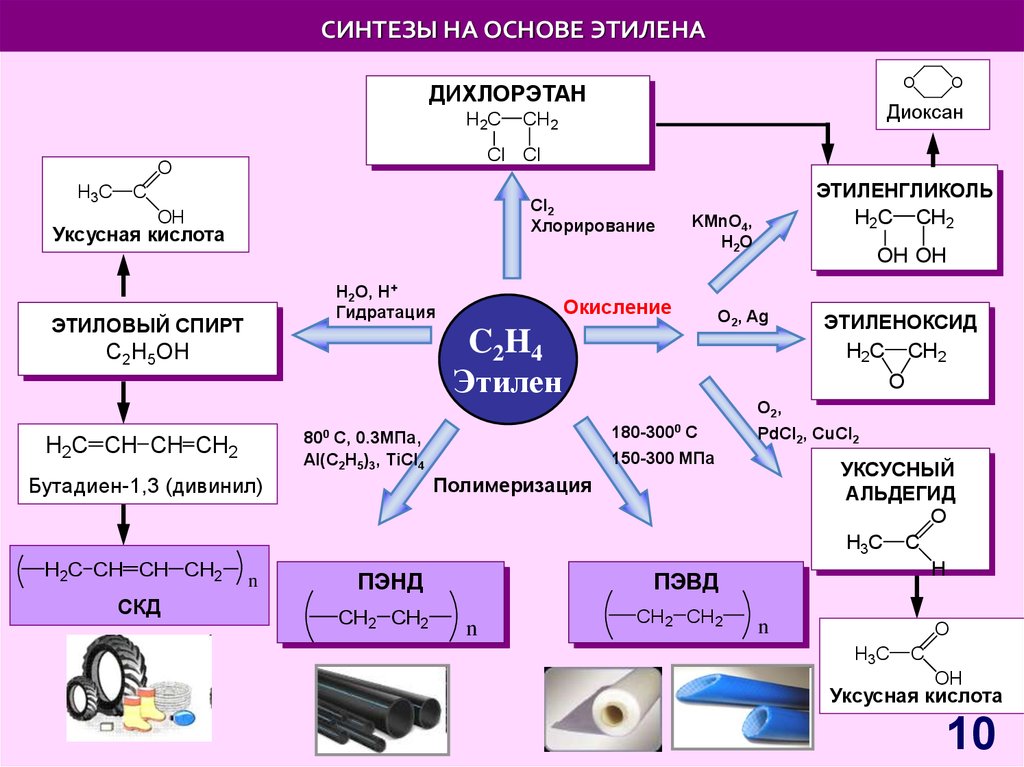
10. СИНТЕЗЫ НА ОСНОВЕ ЭТИЛЕНА
OДИХЛОРЭТАН
H2C
Диоксан
CH2
Cl Cl
O
H3C
O
C
Cl2
Хлорирование
OH
Уксусная кислота
H2O, H+
Гидратация
ЭТИЛОВЫЙ СПИРТ
ЭТИЛЕНГЛИКОЛЬ
H2C CH2
KMnO4,
H2O
Окисление
OH OH
O2, Ag
C2H4
Этилен
С2Н5OH
ЭТИЛЕНОКСИД
H2C CH2
O
O2,
Бутадиен-1,3 (дивинил)
H2C CH CH CH2
СКД
180-3000 С
800 С, 0.3МПа,
Al(C2H5)3, TiCl4
H2C CH CH CH2
n
PdCl2, CuCl2
150-300 МПа
УКСУСНЫЙ
АЛЬДЕГИД
O
H3C C
H
Полимеризация
ПЭНД
CH2 CH2
ПЭВД
n
CH2 CH2
n
O
H3C
C
OH
Уксусная кислота
10
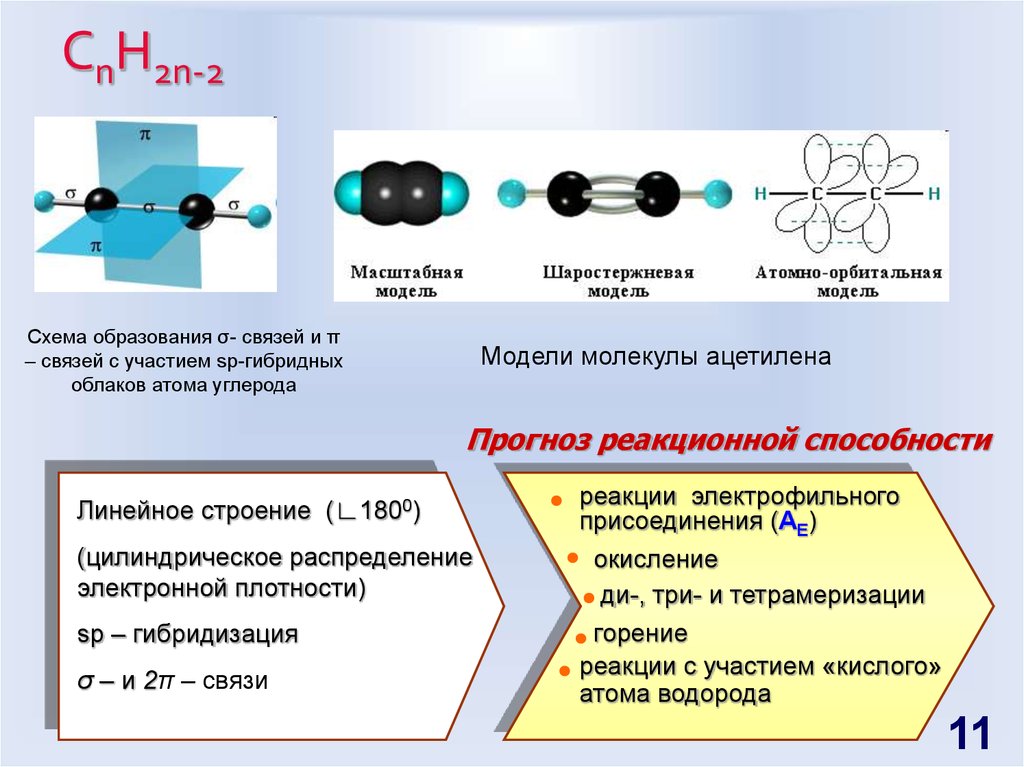
11. СnH2n-2
Схема образования σ- связей и π– связей с участием sp-гибридных
облаков атома углерода
Модели молекулы ацетилена
Прогноз реакционной способности
Линейное строение (∟1800)
(цилиндрическое распределение
электронной плотности)
sp – гибридизация
σ – и 2π – связи
реакции электрофильного
присоединения (AE)
окисление
ди-, три- и тетрамеризации
горение
реакции с участием «кислого»
атома водорода
11
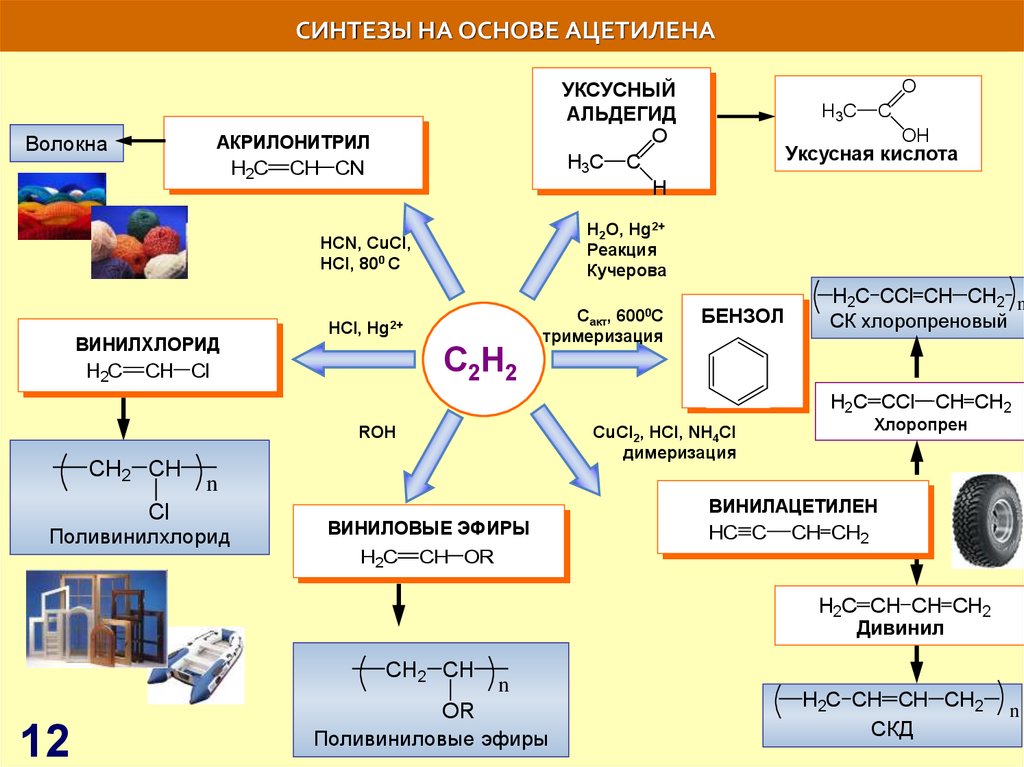
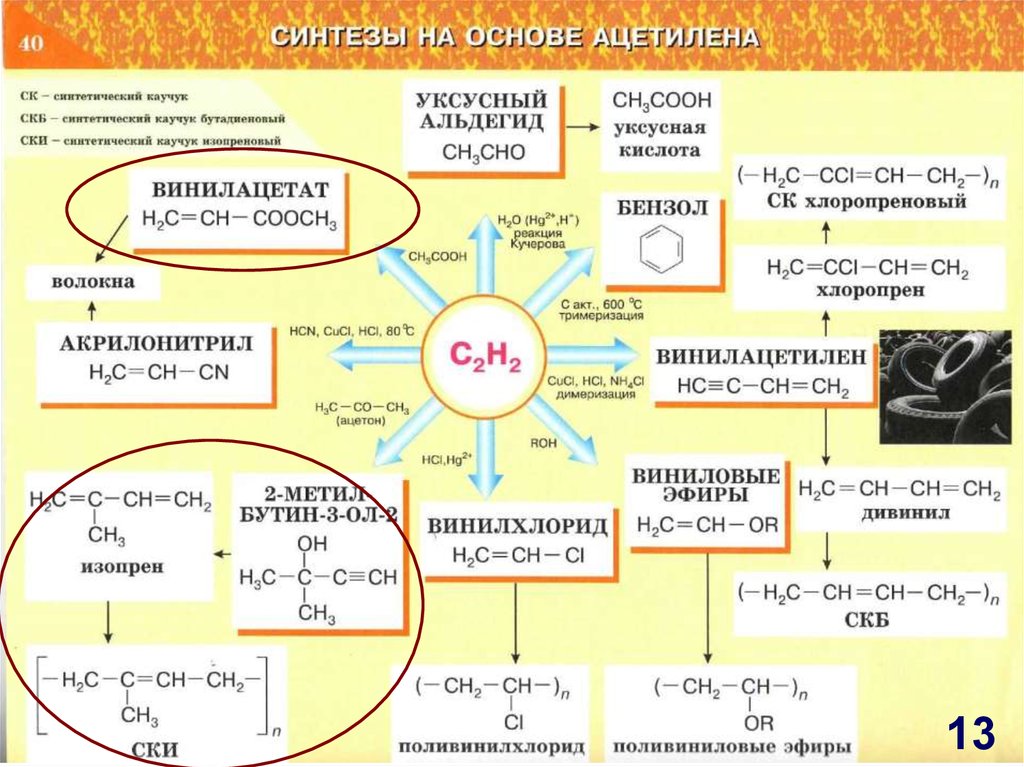
12. СИНТЕЗЫ НА ОСНОВЕ АЦЕТИЛЕНА
ВолокнаУКСУСНЫЙ
АЛЬДЕГИД
O
H3C C
H
АКРИЛОНИТРИЛ
H2C
CH CN
H2C
H3C
C
OH
Уксусная кислота
H2O, Hg2+
Реакция
Кучерова
HCN, СuCl,
HCl, 800 C
ВИНИЛХЛОРИД
O
Сакт, 6000С
тримеризация
HСl, Hg2+
БЕНЗОЛ
H2C CCl CH CH2 n
СК хлоропреновый
C2H2
CH Cl
H2C CCl
CH2 CH
Хлоропрен
СuCl2, HCl, NH4Cl
димеризация
ROH
CH CH2
n
Cl
Поливинилхлорид
ВИНИЛАЦЕТИЛЕН
ВИНИЛОВЫЕ ЭФИРЫ
H2C
HC C
CH CH2
CH OR
H2C CH CH CH2
Дивинил
CH2 CH
12
n
OR
Поливиниловые эфиры
H2C CH CH CH2
СКД
n
13.
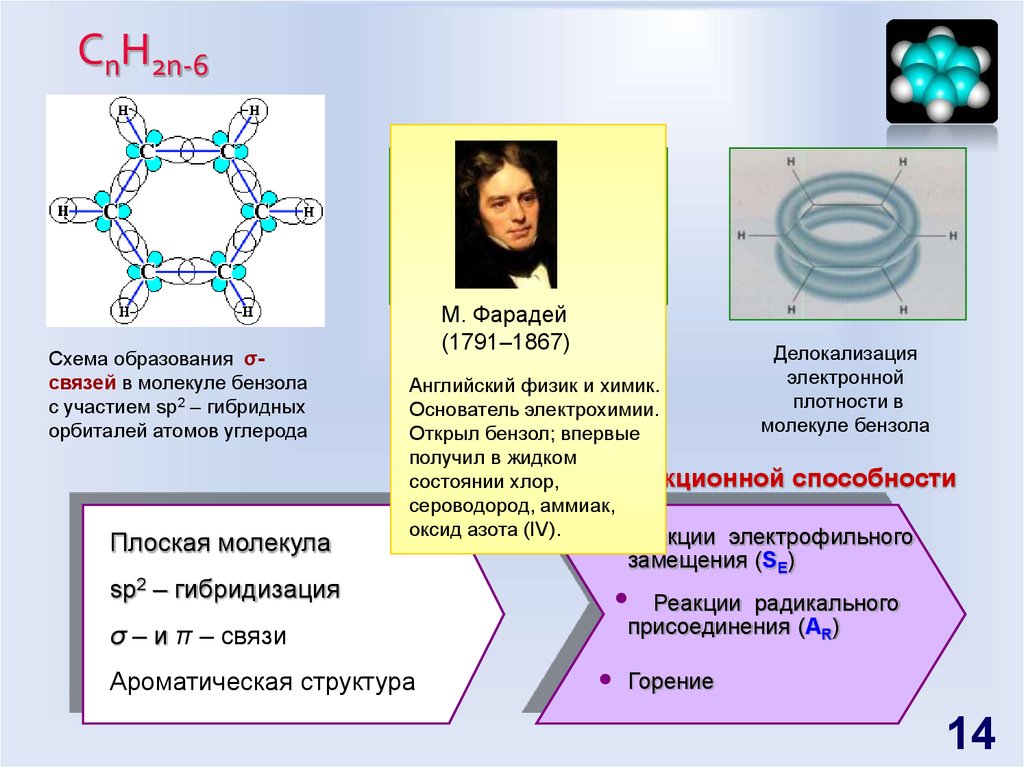
1314. СnH2n-6
Схема образования σсвязей в молекуле бензолас участием sp2 – гибридных
орбиталей атомов углерода
Плоская молекула
М. Фарадей
(1791–1867)
Схема образования
Английский
и химик.
π-связей вфизик
молекуле
Основатель
электрохимии.
бензола
Делокализация
электронной
плотности в
молекуле бензола
Открыл бензол; впервые
получил в жидком
реакционной способности
состоянии Прогноз
хлор,
сероводород, аммиак,
оксид азота (IV).
Реакции электрофильного
sp2 – гибридизация
замещения (SE)
σ – и π – связи
Реакции радикального
присоединения (АR)
Ароматическая структура
Горение
14
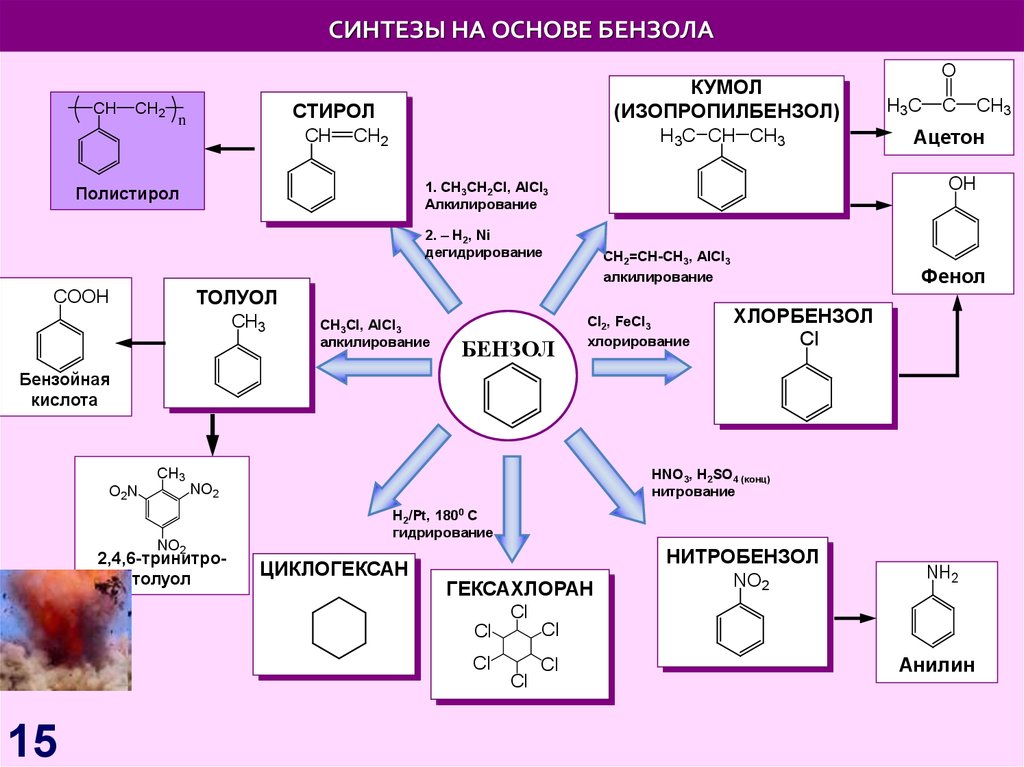
15. СИНТЕЗЫ НА ОСНОВЕ БЕНЗОЛА
CHCH2
КУМОЛ
(ИЗОПРОПИЛБЕНЗОЛ)
СТИРОЛ
n
CH
H3C CH CH3
CH2
2. – H2, Ni
дегидрирование
СH2=CH-CH3, AlCl3
алкилирование
ТОЛУОЛ
COOH
CH3
CH3Cl, AlCl3
алкилирование
БЕНЗОЛ
H3C
C
Ацетон
Сl2, FeCl3
хлорирование
Фенол
ХЛОРБЕНЗОЛ
Cl
Бензойная
кислота
CH3
O2N
NO2
HNO3, H2SO4 (конц)
нитрование
NO2
2,4,6-тринитротолуол
H2/Pt, 1800 C
гидрирование
ЦИКЛОГЕКСАН
НИТРОБЕНЗОЛ
ГЕКСАХЛОРАН
NO2
NH2
Cl
Cl
Cl
Cl
Cl
15
Cl
CH3
OH
1. СH3CH2Cl, AlCl3
Алкилирование
Полистирол
O
Анилин
16. СИНТЕЗЫ НА ОСНОВЕ МЕТАНОЛА
ФОРМАЛЬДЕГИДO
H
H
МЕТИЛТИОЛ
СН3SH
C
H2S, t
МЕТИЛХЛОРИД
СН3Сl
СuO, t
HCl
ДИМЕТИЛАНИЛИН
С6H5NH2
C6H5N(CH3)2
СH3OH
СН3NH2
HC CH
ВИНИЛМЕТИЛОВЫЙ
ЭФИР
МЕТИЛАМИН
NH3
H+, t<1400C
ДИМЕТИЛОВЫЙ ЭФИР
HC CH
+ CO
CH3–O–CH3
H2C CH O CH3
ВИНИЛАЦЕТАТ
H2C CH O C
CH3
O
16
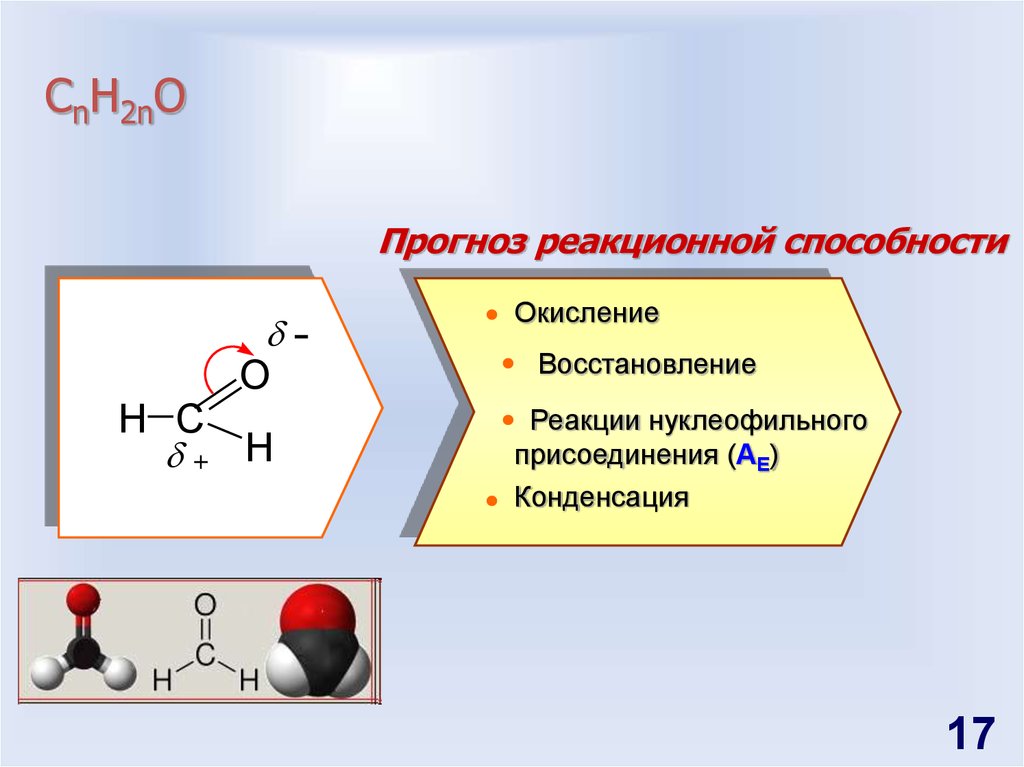
17. СnH2nO
Прогноз реакционной способности-
O
H C
+
H
Окисление
Восстановление
Реакции нуклеофильного
присоединения (AE)
Конденсация
17
18. СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДА
КАРБАМИДНЫЕСМОЛЫ
CH2 NH OC NH n
ФЕНОЛФОРМАЛЬДЕГИДНЫЕ
СМОЛЫ
OH
...
OH
CH2
CH2
МУРАВЬИНАЯ КИСЛОТА
...
O
H
C
[O]
O
ПАРАФОРМ
CH2 O
H
n
[H]
C
H
O
УРОТРОПИН
(ГЕКСМЕТИЛЕНТЕТРАМИН)
N
O 2N
N
NO2
Гексоген
CH2OH
ТРИОКСАН
СH3OH
N
ПЕРВИЧНЫЕ СПИРТЫ
R
МЕТАНОЛ
NO2
OH
N
H2C
CH2
H2C
N
N
N
H2C
CH2
C
H2
O
O
1861 г.
А.М. Бутлеров
18
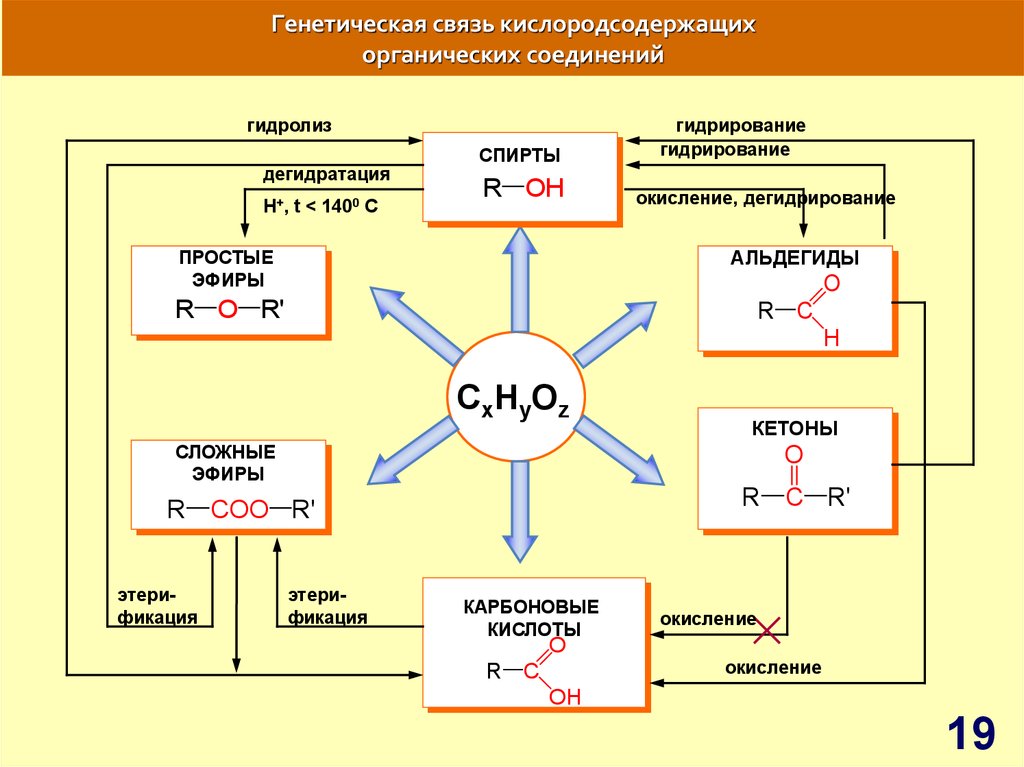
19. Генетическая связь кислородсодержащих органических соединений
гидролиздегидратация
H+, t < 1400 C
СПИРТЫ
R OH
гидрирование
гидрирование
окисление, дегидрирование
АЛЬДЕГИДЫ
ПРОСТЫЕ
ЭФИРЫ
O
R O R'
R C
H
CxHyOz
КЕТОНЫ
СЛОЖНЫЕ
ЭФИРЫ
O
R C R'
R COO R'
этерификация
этерификация
КАРБОНОВЫЕ
КИСЛОТЫ
окисление
O
окисление
R C
OH
19
20.
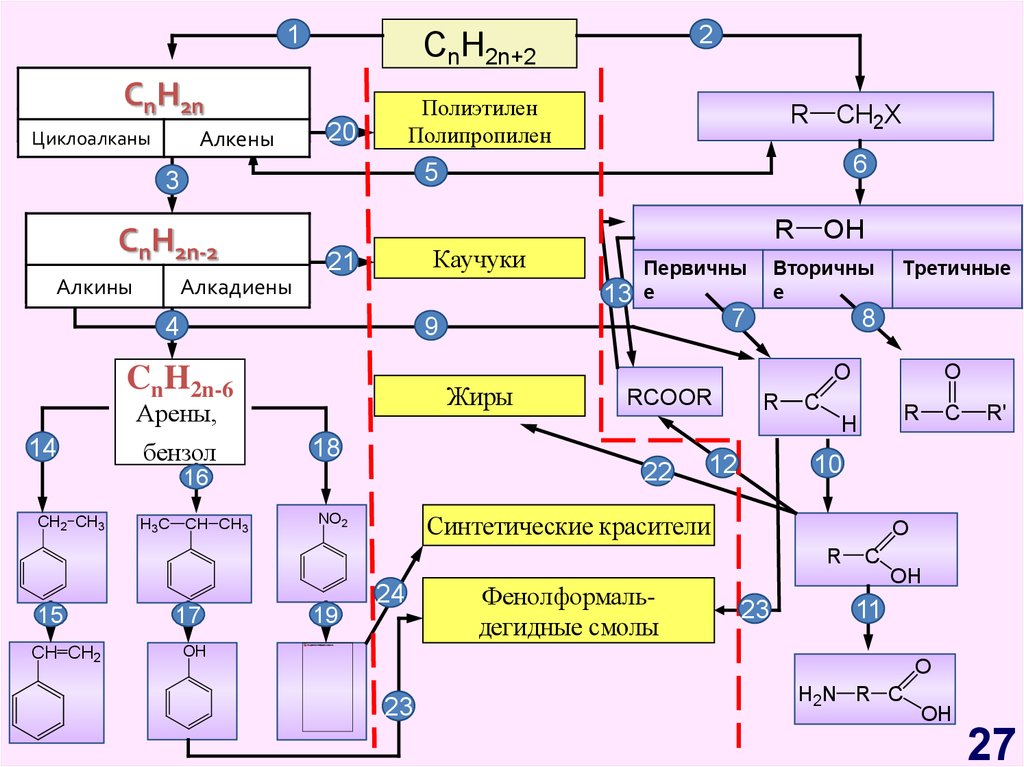
ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ ОСНОВНЫМИКЛАССАМИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
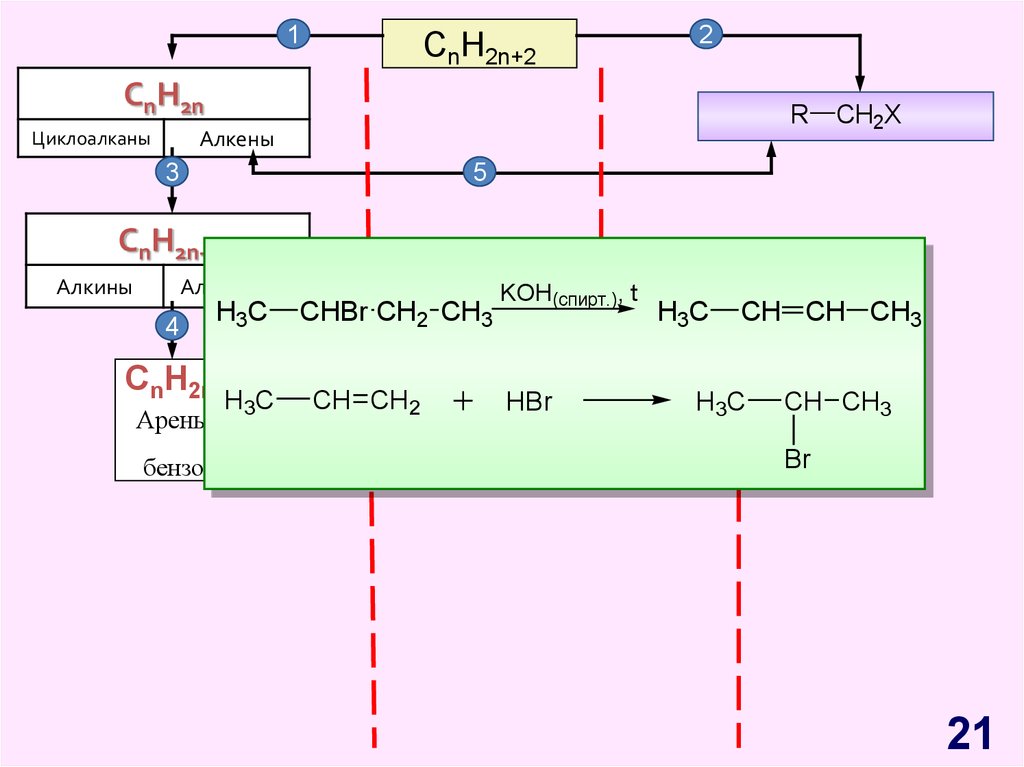
21.
1CnH2n+2
2
CnH2n
R
Алкены
Циклоалканы
3
CH2X
5
CnH2n-2
Алкины
Алкадиены
4
H3C
CnH2n-6
Арены,
бензол
H3C
CHBr CH2 CH3
CH CH2
KOH(cпирт.), t
HBr
H3C
CH CH CH3
H3C
CH CH3
Br
21
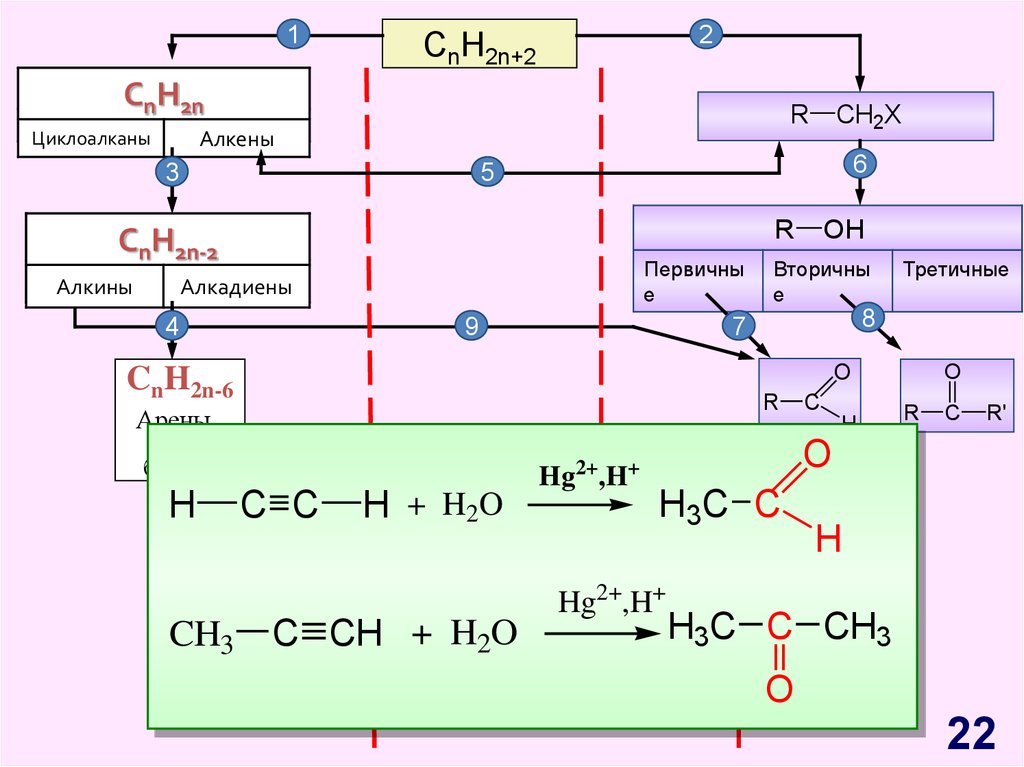
22.
1H2n
CCnnH
2n
Циклоалканы
2
CnH2n+2
R
Алкены
Алкены
Циклоалканы
3
6
5
R
H2n-2
CCnnH
2n-2
Алкины
Алкины
CH2X
Алкадиены
Алкадиены
4
Первичны
е
Вторичны
е
7
8
9
R
Арены,
C
H
бензол
C C
H + H2O
Hg2+,H+
O
C CH + H2O
R
C
R'
O
H3 C C
Hg2+,H+
CH3
Третичные
O
CnH2n-6
H
OH
H
H3C C CH3
O
22
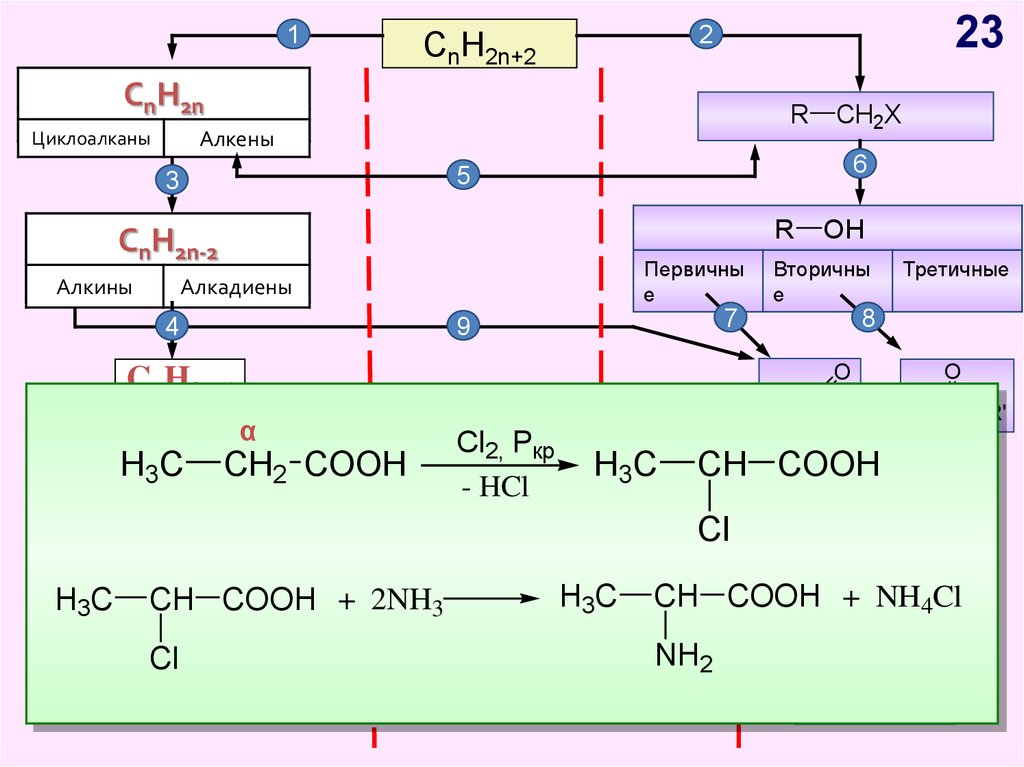
23.
1H2n
CCnnH
2n
Циклоалканы
23
2
CnH2n+2
R
Алкены
Алкены
Циклоалканы
6
5
3
R
H2n-2
CCnnH
2n-2
Алкины
Алкины
CH2X
Первичны
е
Алкадиены
Алкадиены
4
Вторичны
е
7
9
8
O
R
COOH
Cl2, Pкр
- HCl
C
R
H
H3C
O
R
CH COOH + 2NH3
Cl
H3C
C
CH COOH
10
Cl
H3C
Третичные
O
CnH2n-6
Арены, α
Hбензол
CH2
3C
OH
C
OH
CH COOH + NH4Cl
11
NH2
O
H2N R C
OH
R'
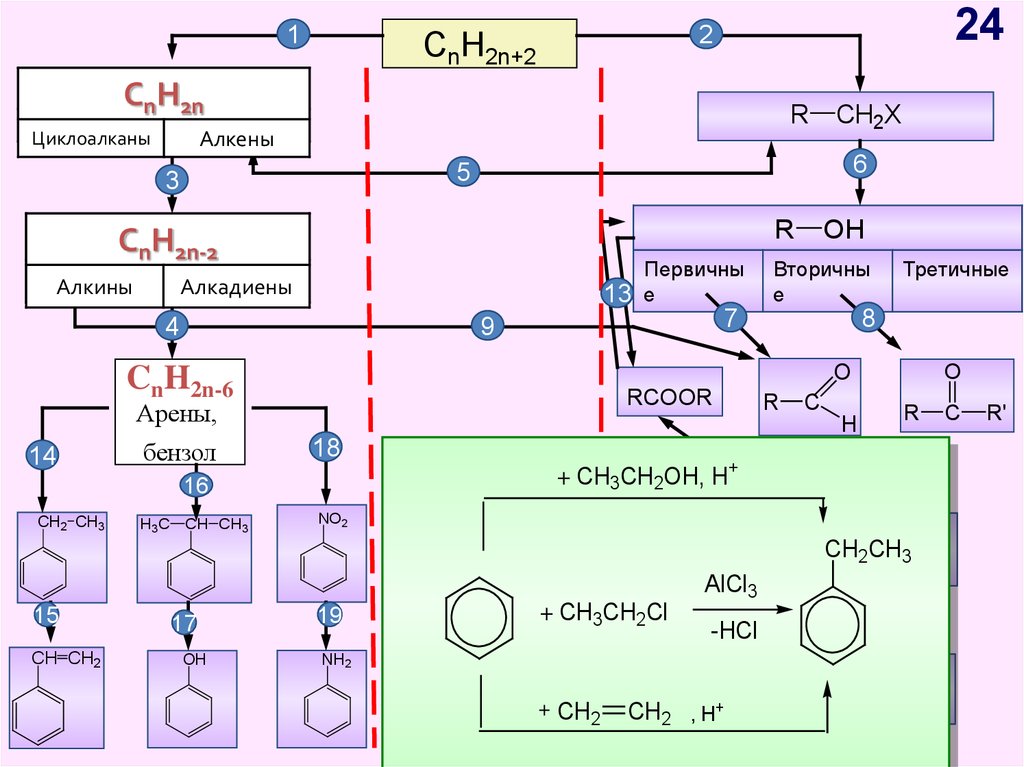
24.
1H2n
CCnnH
2n
Циклоалканы
R
Алкены
Алкены
Циклоалканы
6
R
H2n-2
CCnnH
2n-2
Алкины
Алкины
Алкадиены
Алкадиены
13
4
бензол
Вторичны
е
Третичные
8
O
O
RCOOR
R
C
R
H
18
16
CH CH3
OH
7
Арены,
H 3C
Первичны
е
9
CnH2n-6
CH2 CH3
CH2X
5
3
14
24
2
CnH2n+2
+ CH3CH2OH, 12
H+
C
10
NO2
O
CH
CH3
R 2C
OH
AlCl3
15
CH CH2
17
OH
19
+ CH3CH2Cl
-HCl
11
NH2
O
+ CH2
CH2 , H+
H2N R C
OH
R'
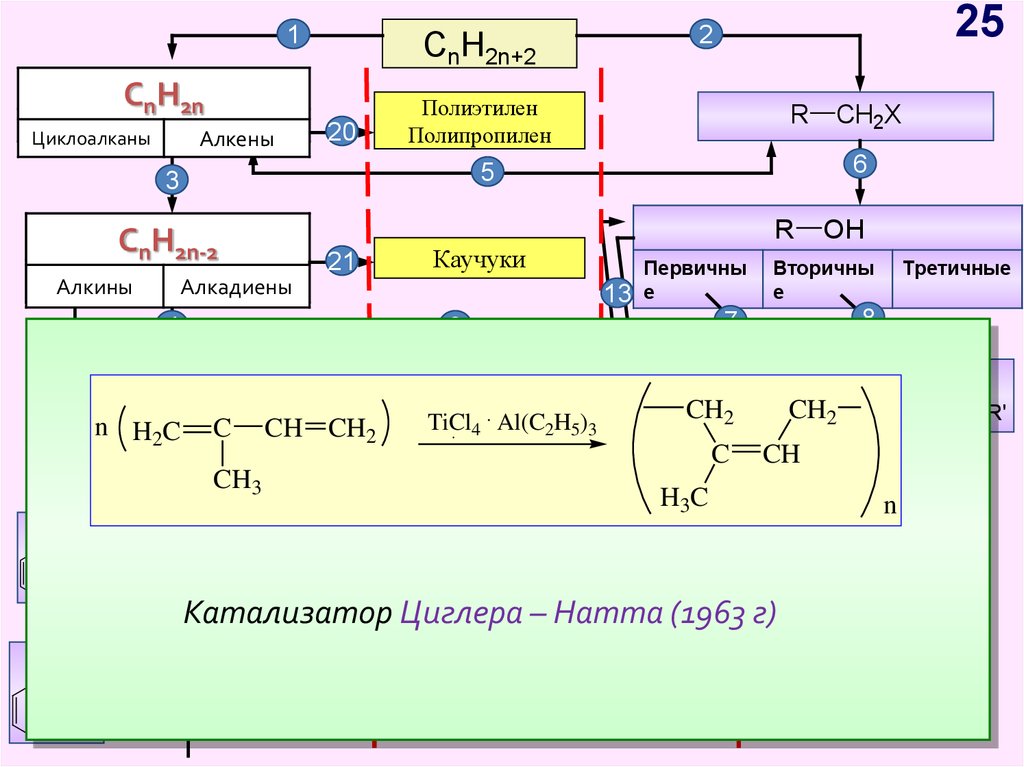
25.
1H2n
CCnnH
2n
Циклоалканы
Алкены
Алкены
Циклоалканы
CnH2n+2
20
Полиэтилен
Полипропилен
Алкадиены
Алкадиены
21
Каучуки
13
4
Арены,
n H2C
C
бензол
CH CH3
OH
Вторичны
е
Третичные
8
7
O
O
CH 18CH2
16 CH3
H 3C
Первичны
е
9
CnH2n-6
CH2 CH3
CH2X
6
R
H2n-2
CCnnH
2n-2
14
R
5
3
Алкины
Алкины
25
2
NO2
.
TiCl4 Al(C2H5)3
RCOOR
CH2
C
12
R
C
CH
2H
R
C
CH 10
H3C
n
O
R
C
OH
15
CH CH2
17
19
Катализатор
OH
Циглера – Натта (1963 г)
11
NH2
O
H2N R C
OH
R'
26.
1H2n
CCnnH
2n
Циклоалканы
Алкены
20
Алкены
Циклоалканы
OH 3
H
H2n-2
CCnH
+
n
2n-2
Алкины
Алкины
H
+
Алкадиены
Алкадиены
Каучуки
21
13
бензол
Жиры
15
CH CH2
H 3C
CH CH3
17
OH
Вторичные
CH2
CHRCOOR
2
R
22
NO2
12
Фенолформальдегидные смолы
OH
O
C
H
O
CH2 ...
R
R'
O
R
C
OH
11
NH2
23
C
10
23
19
Третичные
8
OH
18
16
CH2 CH3
OH
CH2
Арены,
OH
+ H2O
7
OH
...
6
R
Первичн
ые
9
CnH2n-6
CH2X
OH
OH
CH2
4
14
R
H
C
H
Полиэтилен
Полипропилен
OH 5
O
2
CnH2n+2
O
H2N R C
OH
26
27.
1H2n
CCnnH
2n
Циклоалканы
Алкены
Алкены
Циклоалканы
Полиэтилен
Полипропилен
20
H2n-2
CCnnH
2n-2
Алкадиены
Алкадиены
13
Жиры
бензол
Вторичны
е
7
8
CH CH2
17
O
O
RCOOR
R
C
18
22
12
R
Синтетические красители
NO2
19
24
Фенолформальдегидные смолы
C
R'
10
O
R
15
Третичные
H
16
CH CH3
OH
Первичны
е
9
Арены,
H 3C
6
Каучуки
21
CnH2n-6
CH2 CH3
CH2X
R
4
14
R
5
3
Алкины
Алкины
2
CnH2n+2
C
OH
23
11
OH
O
23
H2N R C
OH
27
28.
28Применение анилина
NH 2
Взрывчатые
вещества
Красители
NH NO 2
NO 2
O 2N
N N
АНИЛИН
NH2
Анилиновый желтый
Вариаминовый голубой
NO 2
Лекарственные вещества
Парацетамол
Cтрептоцид
Фталазол
Норсульфазол
H2N
п-Аминобензойная
кислота (ПАБК)
Получение анилина –
реакция Зинина
Н.Н. Зинин
(1812 – 1880)
Fe, HCl
+ 6H
- 2 H2O
Нитробензол
C
OH
O
O
H 2N
NO 2
NH2
NH
CH3O
Тетрил
S
OH
O
Сульфаниловая кислота
NH 2
O
H
C
N
N
C
H
O
индиго
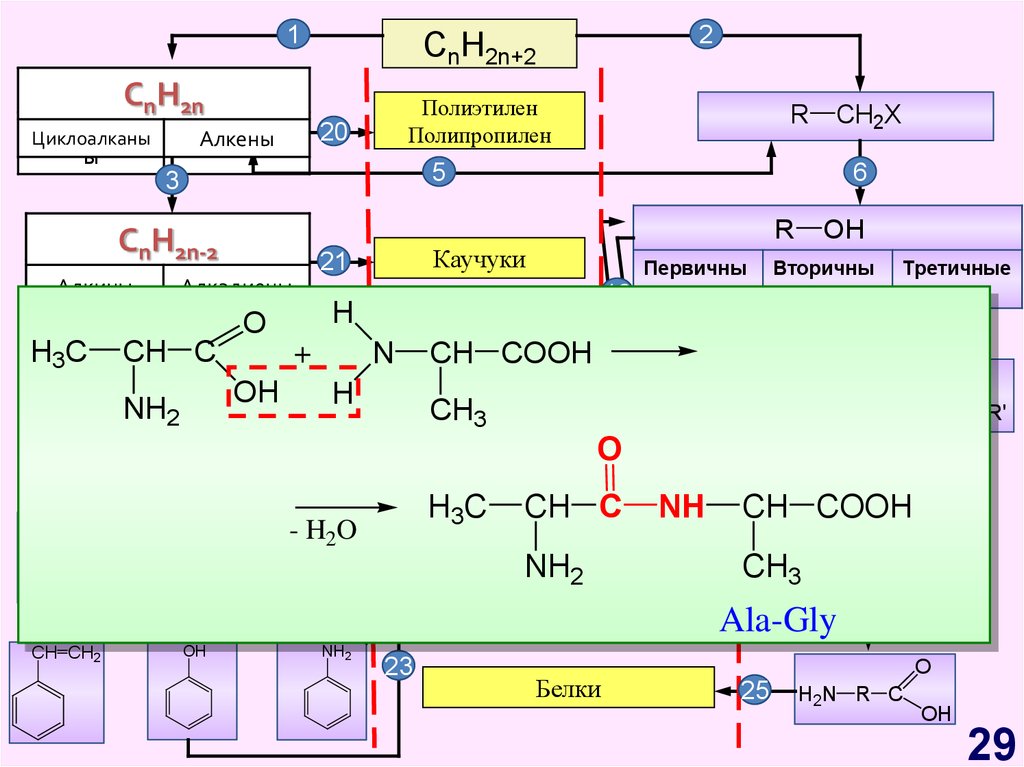
29.
1CnnH
H2n
C
2n
Циклоалкан
Циклоалканы
ы
Полиэтилен
Полипропилен
20
Алкены
14
Алкадиены
Алкадиены
CH C
CnH2n-6OH
NH
Арены,
2
бензол
H 3C
CH CH3
Каучуки
21
13
H
O
4
16
CH2 CH3
N
+
CH CH2
17
OH
H
Жиры
H C
19
23
Третичные
8
O
O
RCOOR
R
C
R
H
C
R'
O 22 12
10
CH C NH CH COOH
3
Синтетические
красители
- H2O
Вторичны
е
CH COOH
CH3
NO2
OH
7
18
NH2
Первичны
е
9
24
15
CH2X
6
R
H2n-2
CCnnH
2n-2
H3C
R
5
3
Алкины
Алкины
2
CnH2n+2
NH2
Фенолформальдегидные смолы
Белки
O
23
CH3
R
Ala-Gly
C
OH
11
O
25
H2N R C
OH
29











 Химия
Химия








