Похожие презентации:
Биологически важные окислительно-восстановительные реакции органических соединений
1.
©© Негребецкий
Негребецкий 1995
1995 –– 2016
2016
Лекция №9
Биологически важные
окислительновосстановительные реакции
органических соединений
2. Краткий путеводитель.
К РАТ К И Й П У Т Е В ОД И Т Е Л ЬК РАТ К И Й П У Т Е В ОД И Т Е Л Ь
Краткий путеводитель.
1. Обмен веществ, метаболизм.
2. Окисление - восстановление.
3. Кислород – главный окислитель в живом организме.
4. Окислительно-восстановительная система ФАД – ФАДН2.
5. Окислительно-восстановительная система НАД+ - НАДН
(НАДФ+ - НАДФН).
6. Окислительно-восстановительная система дисульфид - тиол.
7. Окислительно-восстановительная система хинон - гидрохинон.
8. Реакции окисления с участием молекулярного кислорода.
9. Реакции гидроксилирования.
3.
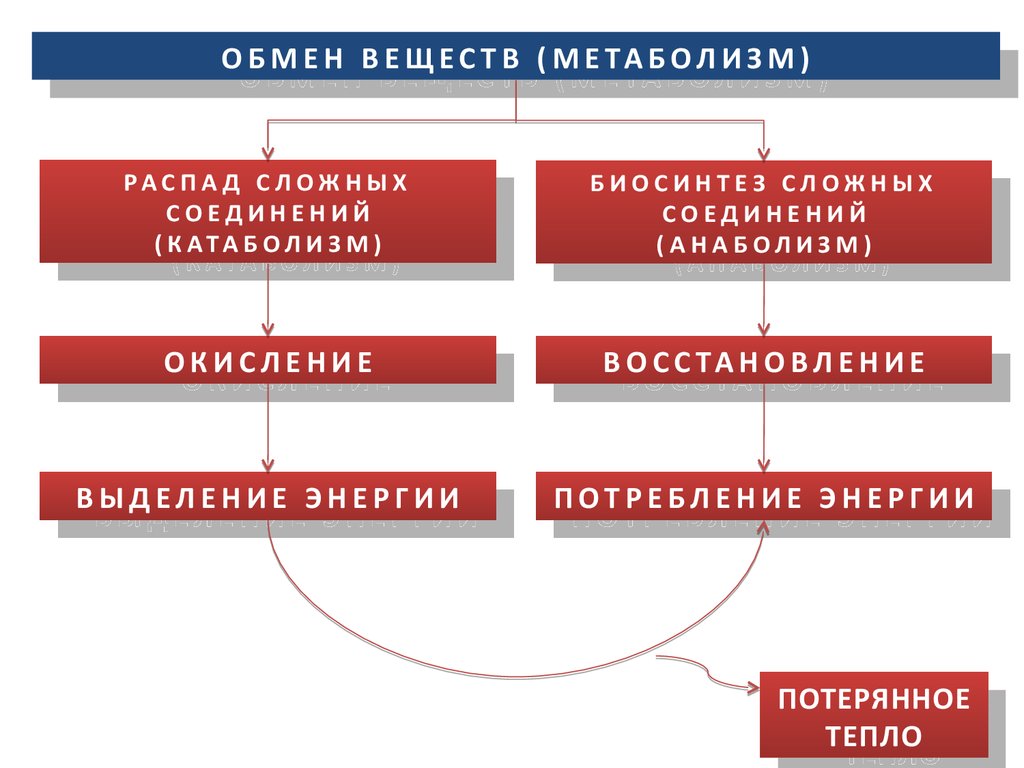
О Б М Е Н В Е Щ Е С Т В ( М Е ТА Б О Л И З М )О Б М Е Н В Е Щ Е С Т В ( М Е ТА Б О Л И З М )
РАС П А Д С Л ОЖ Н Ы Х
Р АССОПЕАДДИ НС ЕЛНОИЖЙН Ы Х
ДО
И ЛН И
ЕН
ИЙ
( К САО
Т АЕ Б
ЗМ
)
( К АТА Б О Л И З М )
БИОСИНТЕЗ СЛОЖНЫХ
Б И ОССОИЕНДТИЕНЗ ЕСНЛИОЙЖ Н Ы Х
И )Й
( АСНОАЕБДОИЛНИЕЗНМ
(АНАБОЛИЗМ)
ОКИСЛЕНИЕ
ОКИСЛЕНИЕ
В О С С ТА Н О В Л Е Н И Е
В О С С ТА Н О В Л Е Н И Е
ВЫДЕЛЕНИЕ ЭНЕРГИИ
ВЫДЕЛЕНИЕ ЭНЕРГИИ
ПОТРЕБЛЕНИЕ ЭНЕРГИИ
ПОТРЕБЛЕНИЕ ЭНЕРГИИ
ПОТЕРЯННОЕ
ПОТЕРЯННОЕ
ТЕПЛО
ТЕПЛО
4.
Окисление процесс удаления водорода с образованием кратнойОкисление процесс удаления водорода с образованием кратной
связи или новой связи между атомом углерода и гетероатомом,
связи или новой связи между атомом углерода и гетероатомом,
более электро-отрицательным, чем водород, например, атомами
более электро-отрицательным, чем водород, например, атомами
O, N, S и т. д.
O, N, S и т. д.
е–
субстрат + окислитель
ОкисленВосстановленная
ный продукт +
форма
окислителя
Восстановление процесс, обратный окислению, сопровождается
Восстановление процесс, обратный окислению, сопровождается
образованием новых связей с водородом
образованием новых связей с водородом
е–
субстрат + восстановитель
ВосстановленОкисленная
+
ный продукт
форма
восстановителя
5.
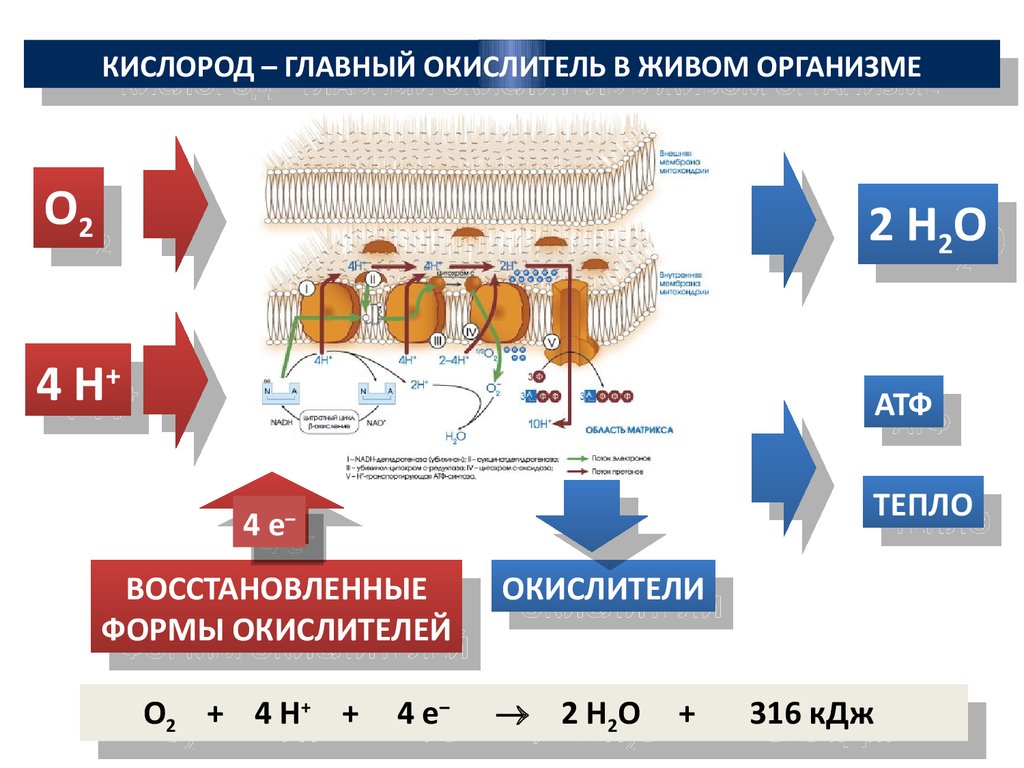
КИСЛОРОД – ГЛАВНЫЙ ОКИСЛИТЕЛЬ В ЖИВОМ ОРГАНИЗМЕКИСЛОРОД – ГЛАВНЫЙ ОКИСЛИТЕЛЬ В ЖИВОМ ОРГАНИЗМЕ
ОО2
2
22НН2ОО
2
44НН+ +
АТФ
АТФ
4е –
4е
ВОССТАНОВЛЕННЫЕ
ОКИСЛИТЕЛИ
ВОССТАНОВЛЕННЫЕ
ОКИСЛИТЕЛИ
ФОРМЫ ОКИСЛИТЕЛЕЙ
ФОРМЫ ОКИСЛИТЕЛЕЙ
–
О2 + 4 Н+ + + 4 е– – 2 Н2О +
О2 + 4 Н + 4 е
2 Н2О +
ТЕПЛО
ТЕПЛО
316 кДж
316 кДж
6.
Реактивные формы кислорода (РФК) или активные формыРеактивные формы кислорода (РФК) или активные формы
кислорода (АФК) — включают ионы кислорода, свободные
кислорода (АФК) — включают ионы кислорода, свободные
радикалы и перекиси как неорганического, так
радикалы и перекиси как неорганического, так
и органического происхождения
и органического происхождения
Î
Î 2 (ñóï åðî êñèä àí èî í -ðàäèêàë)
Î 2 + åÎ
Î
-
Î
-
Î Í
Î
àêòèâí ûå
+ Í +
Î
Î Í
Î
+ å
(ãèäðî ï åðî êñèä ðàäèêàë)
Î Í
(ãèäðî ï åðî êñèä àí èî í )
ô î ðì û
êèñëî ðî äà
Î
Î Í
+ Í +
Í 2Î 2 (ï åðî êñèä âî äî ðî äà)
Í 2Î 2
Í 2Î
+
(ÀÔÊ)
1/ Î
2 2
Î 2 < HOO < H2O2 < HO
-
Î 2 + H2O2
HO + HO- + O2; H2O2 + Fe2+
HO + HO- + Få3+
7.
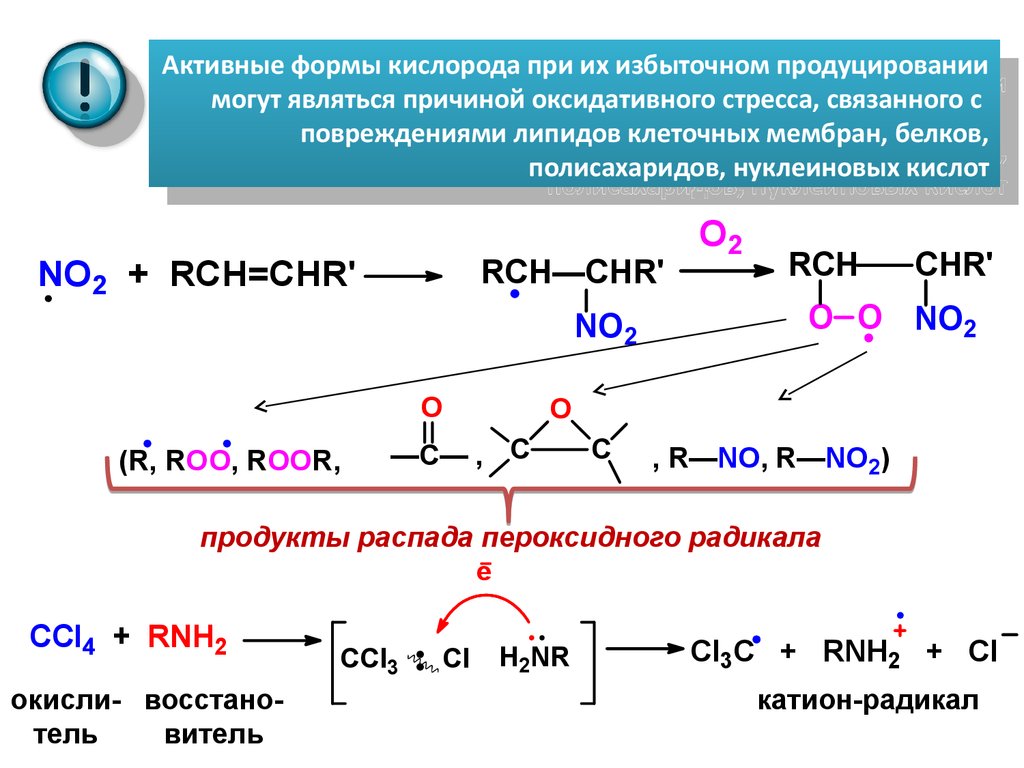
Активные формы кислорода при их избыточном продуцированииАктивные формы кислорода при их избыточном продуцировании
могут являться причиной оксидативного стресса, связанного с
могут являться причиной оксидативного стресса, связанного с
повреждениями липидов клеточных мембран, белков,
повреждениями липидов клеточных мембран, белков,
полисахаридов, нуклеиновых кислот
полисахаридов, нуклеиновых кислот
NO2 + RCH=CHR'
RCH—CHR'
NO2
O
(R, ROO, ROOR,
O2
RCH
CHR'
O O NO2
O
—C— , C
C
, R—NO, R—NO2)
продукты распада пероксидного радикала
e
CCl4 + RNH2
окисли- восстанотель
витель
CCl3
Cl
H2NR
Cl3C + RNH2 + Cl
катион-радикал
8.
Внутрибольничные инфекции.Медико-социальная значимость
инвалидизации
инвалидизации
летальность
летальность
Высокая стоимость
Высокая стоимость
лечения и профилактики
лечения и профилактики
Staphylococcus aureus
Pseudomonas aeruginosa
9. Инновационность предлагаемого подхода к лечению
Простые и низкозатратные способы антимикробного воздействияПростые и низкозатратные способы антимикробного воздействия
на основе ФС имеют высокое народно-хозяйственное значение
на основе ФС имеют высокое народно-хозяйственное значение
10.
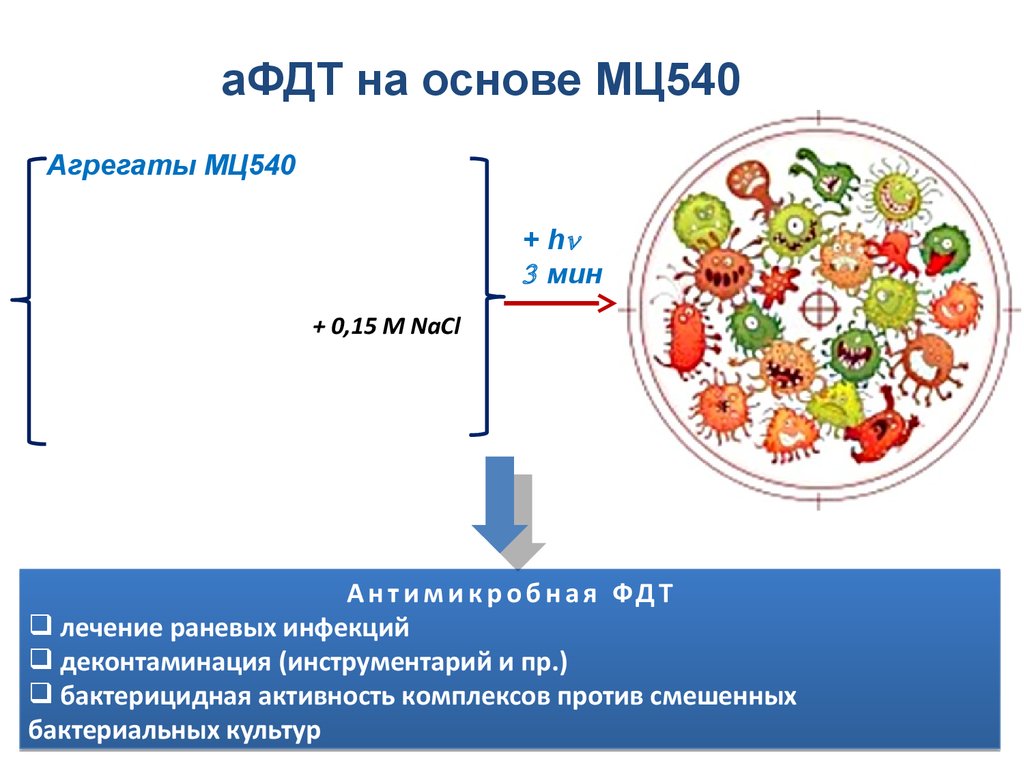
аФДТ на основе МЦ540Агрегаты МЦ540
+ hn
3 мин
+ 0,15 M NaCl
А н т и м и к р о б н а я ФДТ
лечение раневых инфекций
деконтаминация (инструментарий и пр.)
бактерицидная активность комплексов против смешенных
бактериальных культур
11.
Преимущества предлагаемого подхода клечению
12.
Антимикробныесредства
2011, 2013
гг.
16-33-00970
13.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА ФАД – ФАДН2ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА ФАД – ФАДН2
Х
Х
Х
Х
флавинадениндинуклеотид
ФАД
ФАДН2
окислитель
восстановитель
O
N
N
R
N
N
H
O
+
2H
+
H
N
O
N
R
N
H
N
H
O
14.
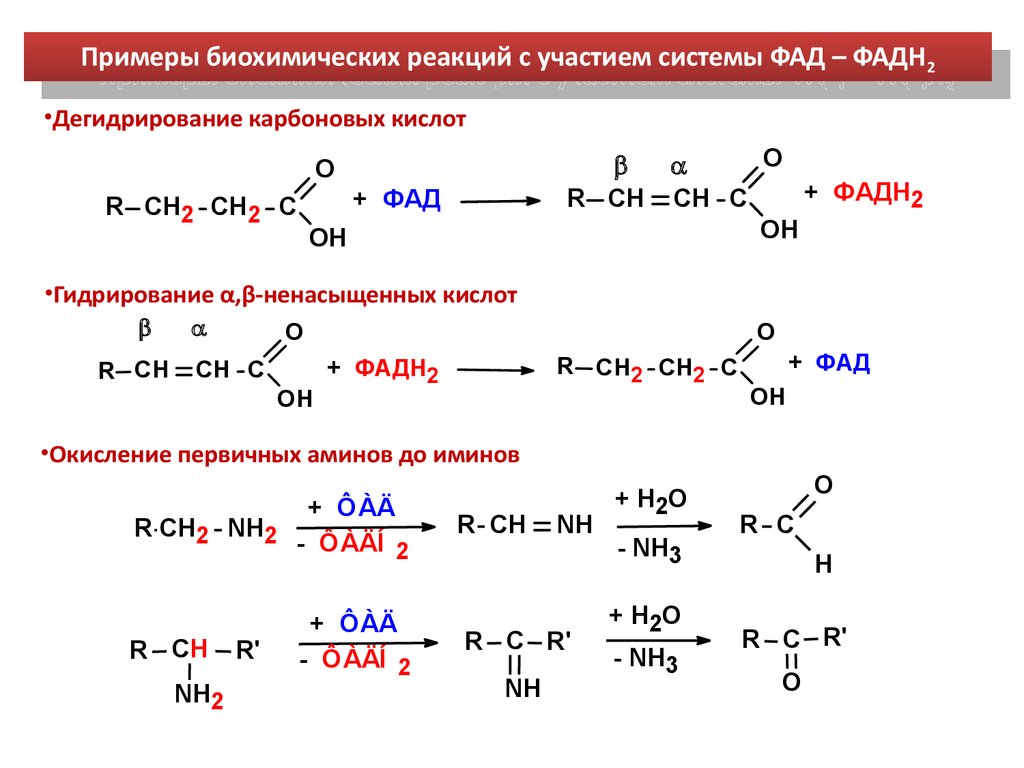
Примеры биохимических реакций с участием системы ФАД – ФАДН 2Примеры биохимических реакций с участием системы ФАД – ФАДН 2
•Дегидрирование карбоновых кислот
R CH
О
+ ФАД
R CH2 CH2 C
OH
О
+ ФАДН2
CH C
OH
•Гидрирование α,β-ненасыщенных кислот
R CH
О
CH C
OH
О
R CH2 CH2 C
+ ФАДН2
+ ФАД
OH
•Окисление первичных аминов до иминов
+ ÔÀÄ
R CH2 NH2
- ÔÀÄÍ 2
R CH
NH2
R'
+ ÔÀÄ
- ÔÀÄÍ 2
R CH
NH
R C R'
NH
+ H2O
- NH3
+ H2O
- NH3
O
R C
H
R C R'
O
15.
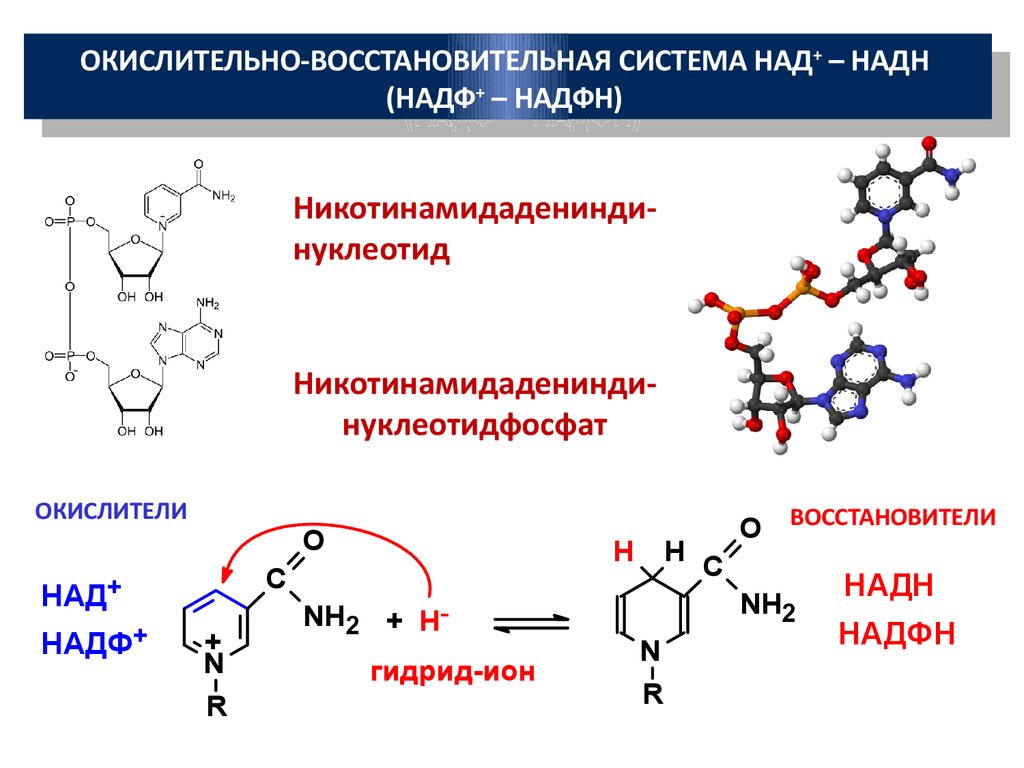
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА НАД+ –+ НАДНОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ
СИСТЕМА НАД – НАДН
(НАДФ+ –+ НАДФН)
(НАДФ – НАДФН)
Никотинамидадениндинуклеотид
Никотинамидадениндинуклеотидфосфат
ОКИСЛИТЕЛИ
O
C
НАД+
НАДФ+
H
+
N
R
NH2 + Hгидрид-ион
H
O ВОССТАНОВИТЕЛИ
C
NH2
N
R
НАДН
НАДФН
16.
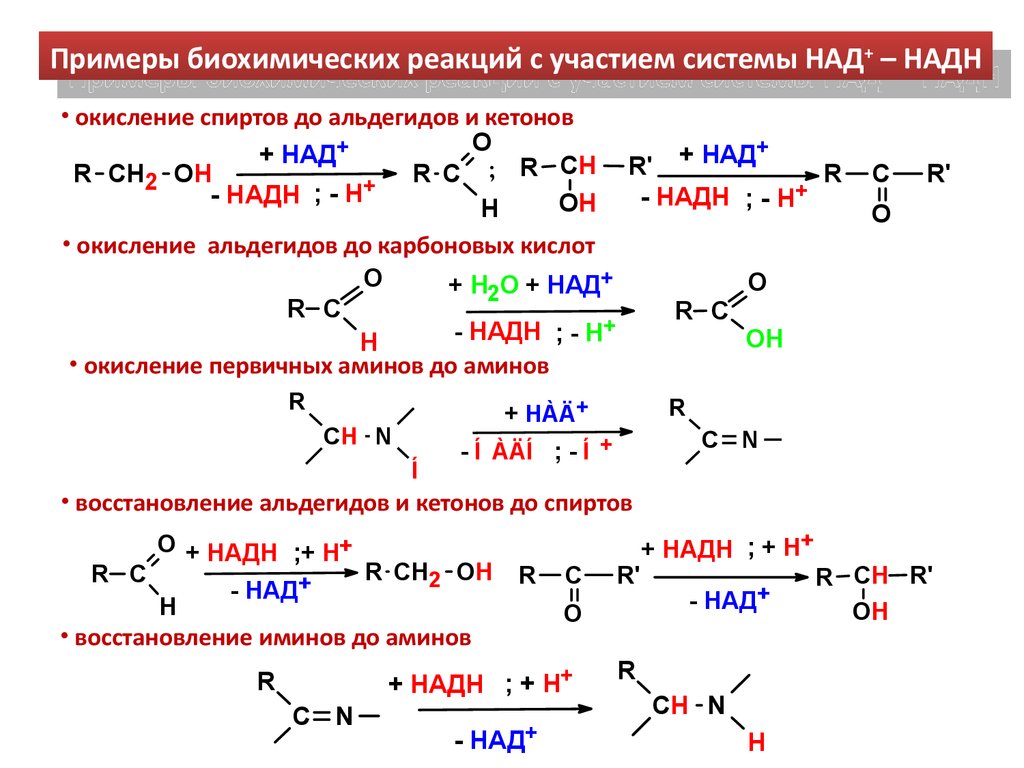
Примеры биохимических реакций с участием системы НАД+ –+ НАДНПримеры биохимических реакций с участием системы НАД – НАДН
• окисление спиртов до альдегидов и кетонов
O
+ HАД+
+ HАД+
CH
R'
R CH2 OH
R C ; R
R
+
+
- НАДН ; - Н
- НАДН ; - Н
OH
H
• окисление альдегидов до карбоновых кислот
O
O
+ Н2О + HАД+
R C
R C
+
НАДН
;-Н
ОH
H
• окисление первичных аминов до аминов
R
Í
R'
O
R
+ HÀÄ+
CH N
C
C N
- Í ÀÄÍ ; - Í +
• восстановление альдегидов и кетонов до спиртов
R C
O + НАДН ;+ Н+
- HАД+
R CH2 OH
R
H
• восстановление иминов до аминов
C
O
+ НАДН ; + Н+
R
C N
- HАД+
R'
+ НАДН ; + Н+
- HАД+
R
CH N
Н
R CH R'
OH
17.
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА ДИСУЛЬФИД – ТИОЛОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА ДИСУЛЬФИД – ТИОЛ
R S S R + 2 H+ + 2 e-
SH
2 R
дисульфид
тиол
окислитель
восстановитель
Примеры биохимических реакций с участием системы
Примеры биохимических реакций с участием системы
дисульфид – тиол
дисульфид – тиол
• восстановление гидропероксидов до спиртов
R O O H +
2 R SH
R O H + R S S R
• образование и разрыв дисульфидных мостиков в молекулах белков
2 R SH
глутатион
R S S R
+ H2O
18.
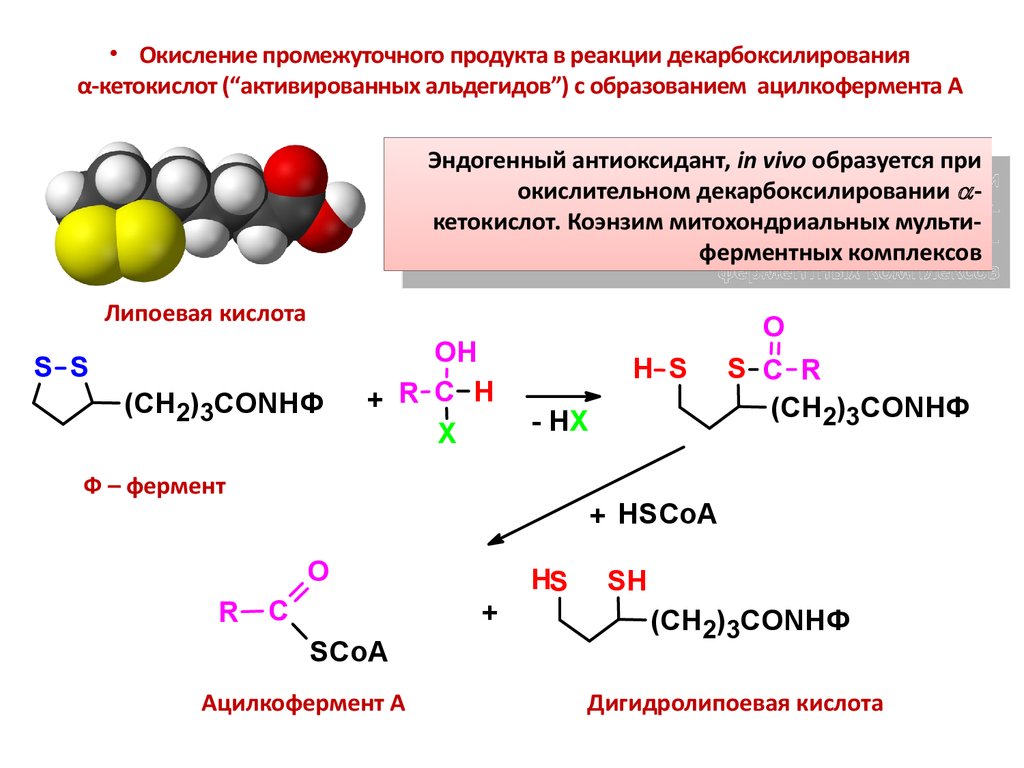
• Окисление промежуточного продукта в реакции декарбоксилированияα-кетокислот (“активированных альдегидов”) с образованием ацилкофермента А
Эндогенный антиоксидант, in vivo образуется при
Эндогенный
антиоксидант,
in vivo образуется
при
окислительном
декарбоксилировании
окислительном
декарбоксилировании
кетокислот.
Коэнзим митохондриальных
мульти- кетокислот. Коэнзим митохондриальных
мультиферментных комплексов
ферментных комплексов
Липоевая кислота
S S
(CH2)3CONHФ
OH
+ R C H
X
H S
- HX
Ф – фермент
O
S C R
(CH2)3CONHФ
+ HSСoA
O
R C
+
SСoA
Ацилкофермент А
HS
SН
(CH2)3CONHФ
Дигидролипоевая кислота
19.
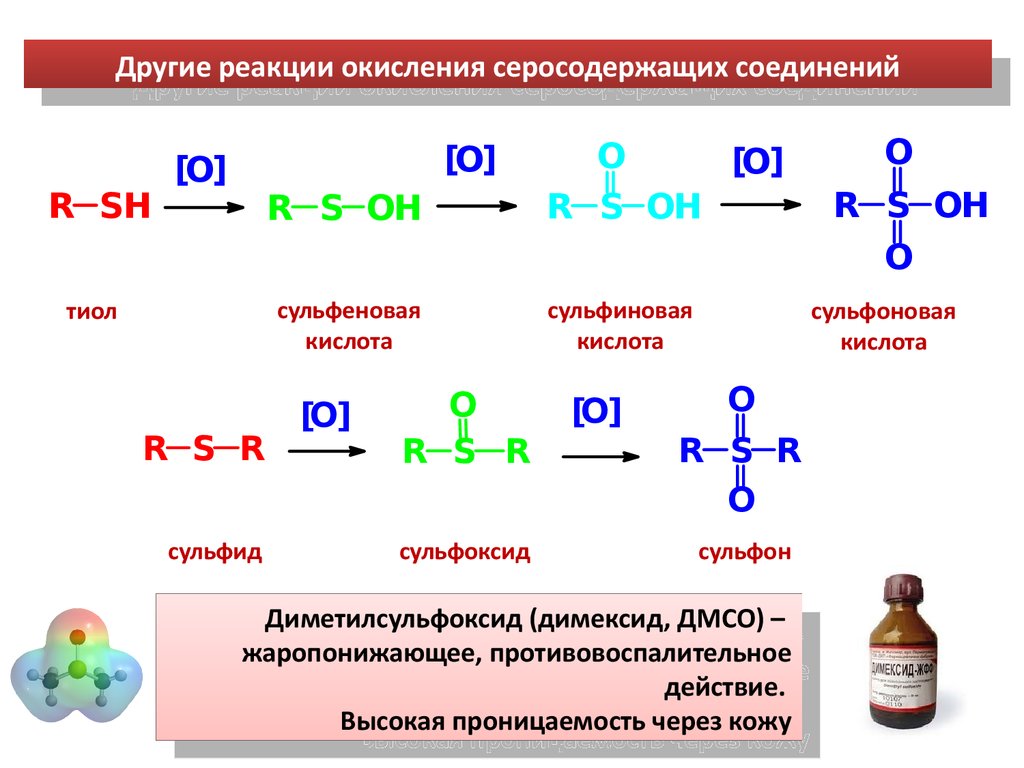
Другие реакции окисления серосодержащих соединенийДругие реакции окисления серосодержащих соединений
R SH
[O]
[O]
R S OH
сульфеновая
кислота
тиол
R S R
сульфид
[O]
O
R S R
сульфоксид
O
[O]
R S OH
сульфиновая
кислота
[O]
O
R S OH
O
сульфоновая
кислота
O
R S R
O
сульфон
Диметилсульфоксид (димексид, ДМСО) –
Диметилсульфоксид (димексид, ДМСО) –
жаропонижающее, противовоспалительное
жаропонижающее, противовоспалительное
действие.
действие.
Высокая проницаемость через кожу
Высокая проницаемость через кожу
20.
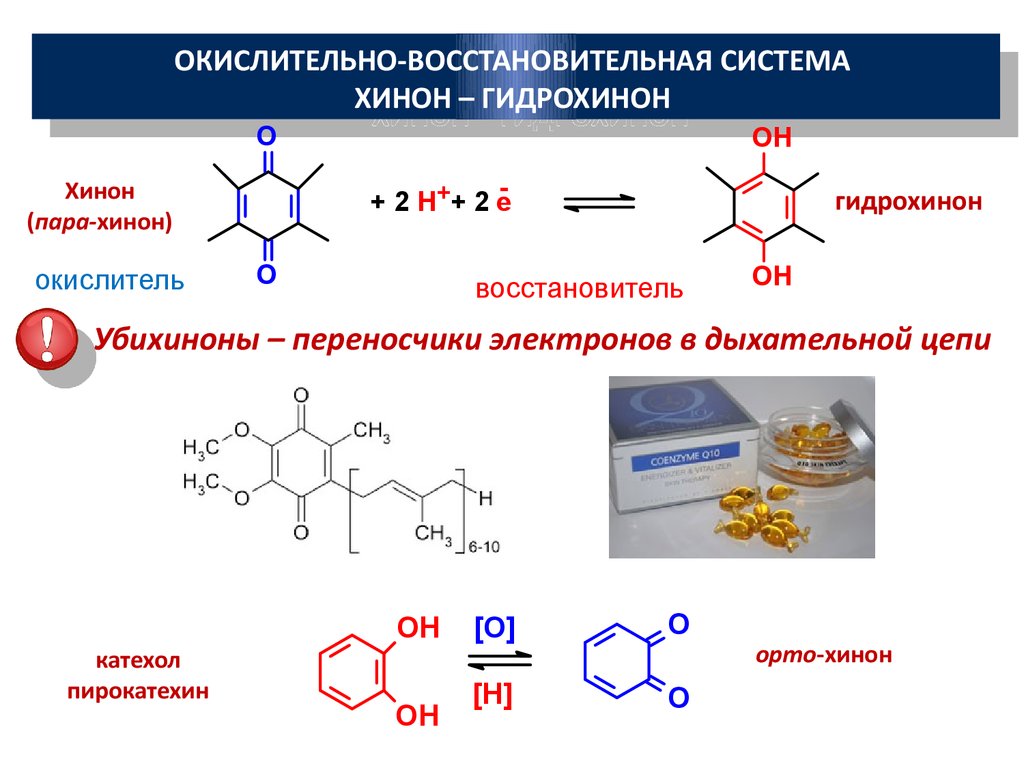
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМАОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНАЯ СИСТЕМА
ХИНОН – ГИДРОХИНОН
ХИНОН – ГИДРОХИНОН
О
+ 2 Н++ 2 е
Хинон
(пара-хинон)
окислитель
ОН
О
гидрохинон
восстановитель
ОН
Убихиноны – переносчики электронов в дыхательной цепи
катехол
пирокатехин
ОН
ОН
[O]
О
[H]
О
орто-хинон
21.
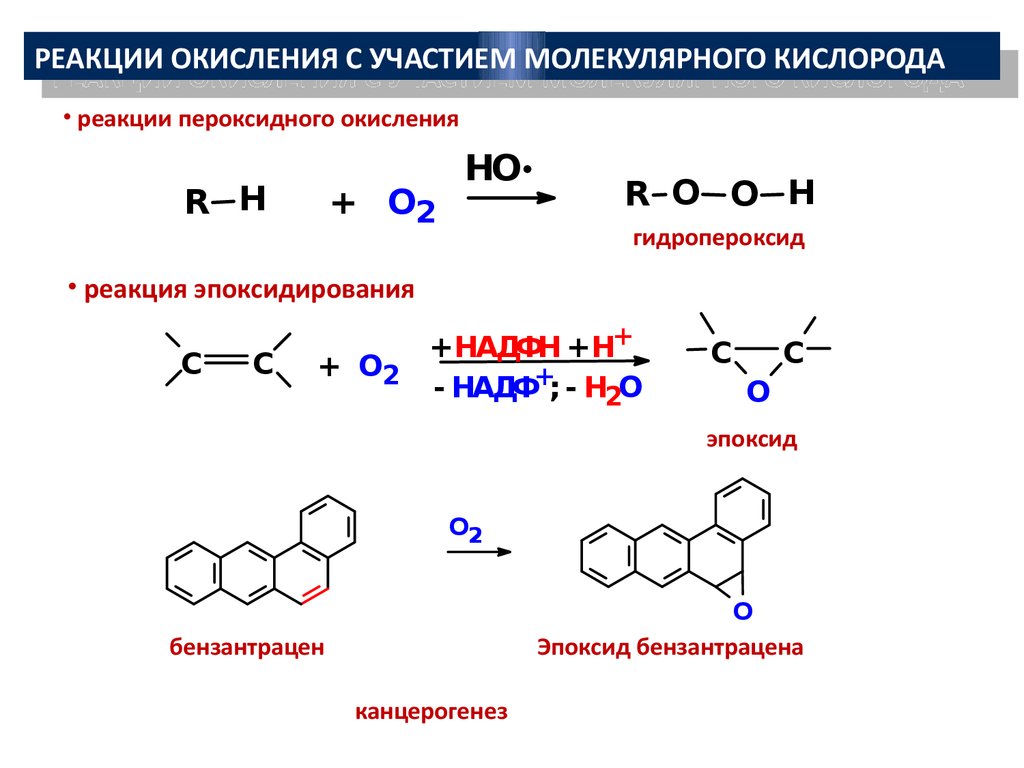
РЕАКЦИИ ОКИСЛЕНИЯ С УЧАСТИЕМ МОЛЕКУЛЯРНОГО КИСЛОРОДАРЕАКЦИИ ОКИСЛЕНИЯ С УЧАСТИЕМ МОЛЕКУЛЯРНОГО КИСЛОРОДА
• реакции пероксидного окисления
R Н
+ O2
НО
R О О Н
гидропероксид
• реакция эпоксидирования
С
С
+НАДФН + Н+
+ О2
- НАДФ+; - Н2О
С
С
О
эпоксид
О2
О
Эпоксид бензантрацена
бензантрацен
канцерогенез
22.
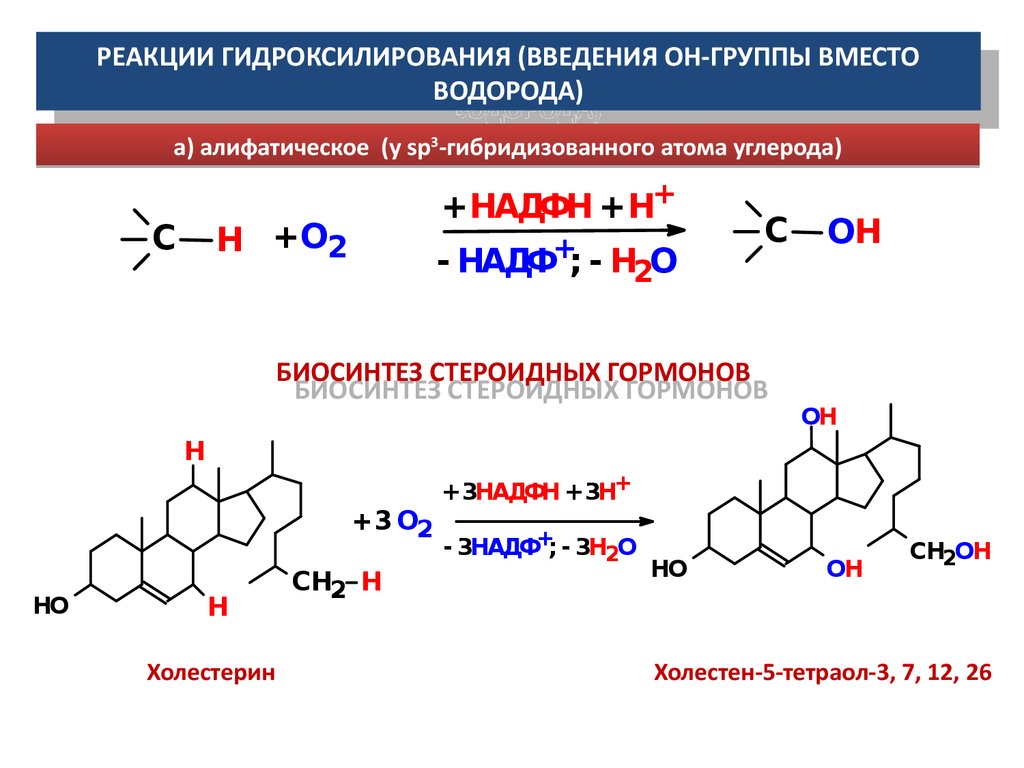
РЕАКЦИИ ГИДРОКСИЛИРОВАНИЯ (ВВЕДЕНИЯ ОН-ГРУППЫ ВМЕСТОРЕАКЦИИ ГИДРОКСИЛИРОВАНИЯ (ВВЕДЕНИЯ ОН-ГРУППЫ ВМЕСТО
ВОДОРОДА)
ВОДОРОДА)
а) алифатическое (у sp3-гибридизованного атома углерода)
+НАДФН + Н+
Н + О2
С
- НАДФ+; - Н2О
С
БИОСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ
БИОСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ
ОН
ОН
Н
+ 3НАДФН + 3Н+
+ 3 О2
НО
Н
Холестерин
СН2 Н
- 3НАДФ+; - 3Н2О
НО
ОН
СН2ОН
Холестен-5-тетраол-3, 7, 12, 26
23.
б) гидроксилирование фрагментов аминокислот в белке – коллагенеНО
O
О2; витамин С
C
N
O
C
N
OH
H
H
OH
4-гидроксипролин
пролин
O
NН2 СН2
СН2 СН2 СН2 CH C
лизин
O2
NH2
витамин С
OH
O
NН2
СН2 СН СН2 СН2 CH C
ОН
5-гидроксилизин
NH2
OH
24.
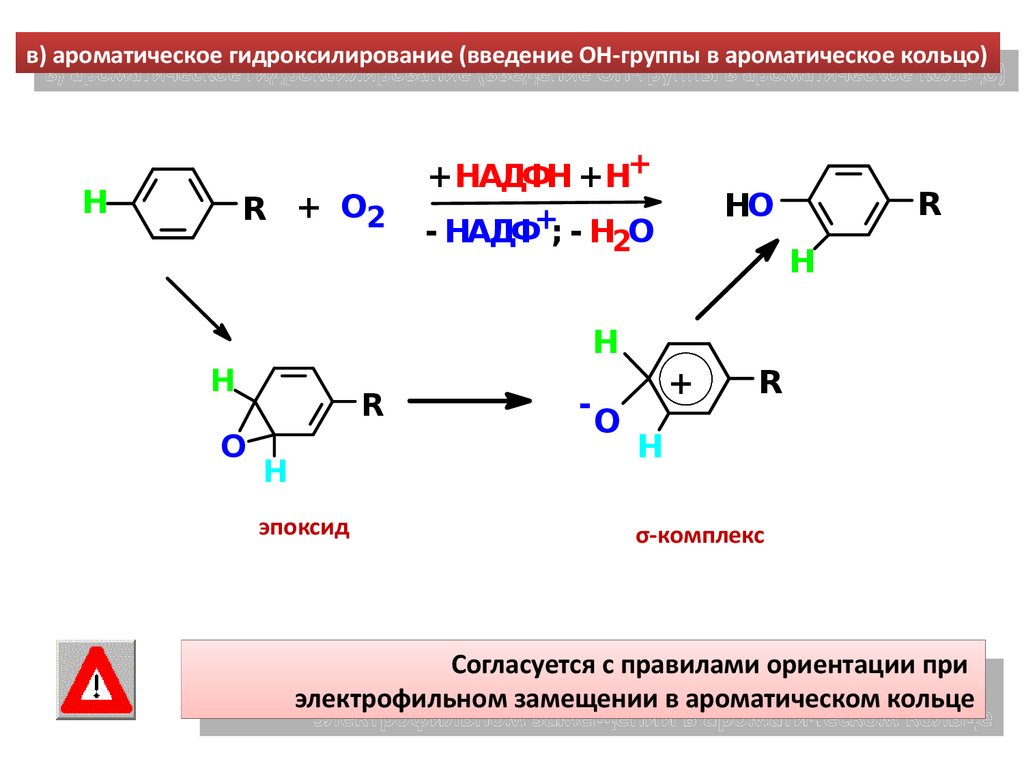
в) ароматическое гидроксилирование (введение ОН-группы в ароматическое кольцо)в) ароматическое гидроксилирование (введение ОН-группы в ароматическое кольцо)
Н
R + O2
+ НАДФН + Н+
R
HO
- НАДФ+; - Н2О
Н
H
Н
O
R
Н
эпоксид
-
+
O
R
Н
σ-комплекс
Согласуется с правилами ориентации при
Согласуется с правилами ориентации при
электрофильном замещении в ароматическом кольце
электрофильном замещении в ароматическом кольце
25.
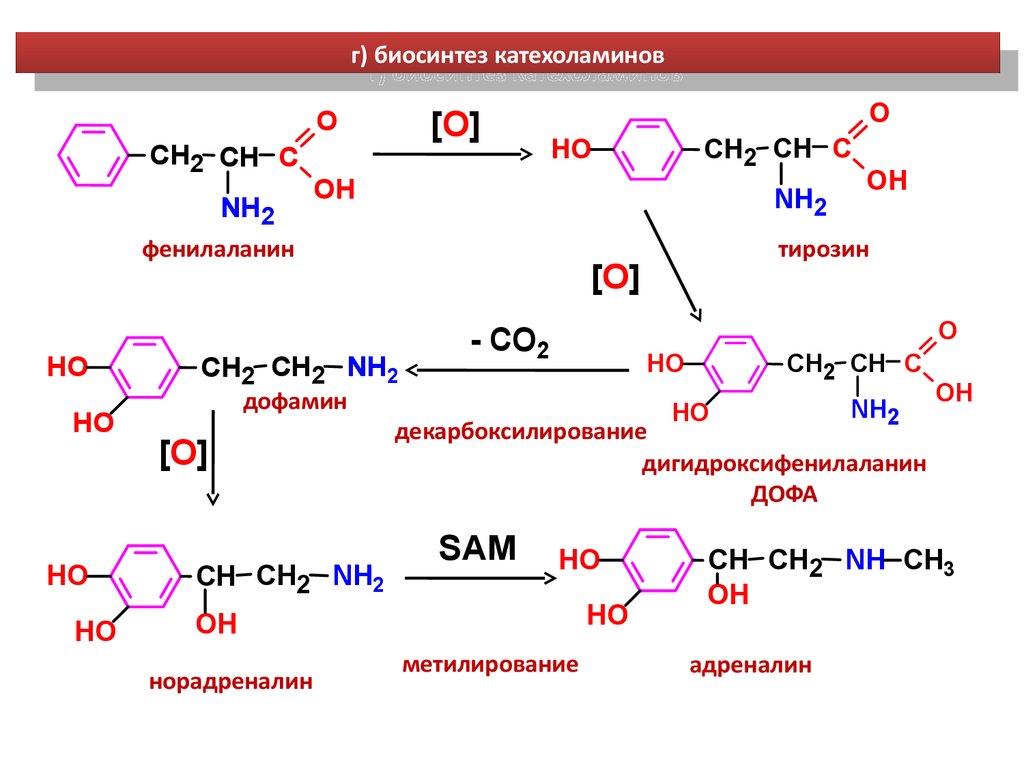
г) биосинтез катехоламиновг) биосинтез катехоламинов
O
СН2 CH C
NH2
[O]
O
OH
NH2
фенилаланин
НО
НО
НО
HO
дофамин
[O]
СН CH2 NH2
OH
OH
тирозин
[O]
СН2 CH2 NH2
норадреналин
СН2 CH C
НО
O
- CO2
НО
СН2 CH C
NH2
НО
декарбоксилирование
дигидроксифенилаланин
ДОФА
SAM
НО
HO
метилирование
OH
СН CH2 NH CH3
OH
адреналин












 Химия
Химия








