Похожие презентации:
Хромосомные болезни (эпидемиология, классификация, методы профилактики и предупреждения рождения детей с хромосомной патологией)
1. Медицинская генетика
Хромосомные болезни(эпидемиология, классификация, цитогенетические формы,
методы профилактики и предупреждения рождения детей с
хромосомной патологией)
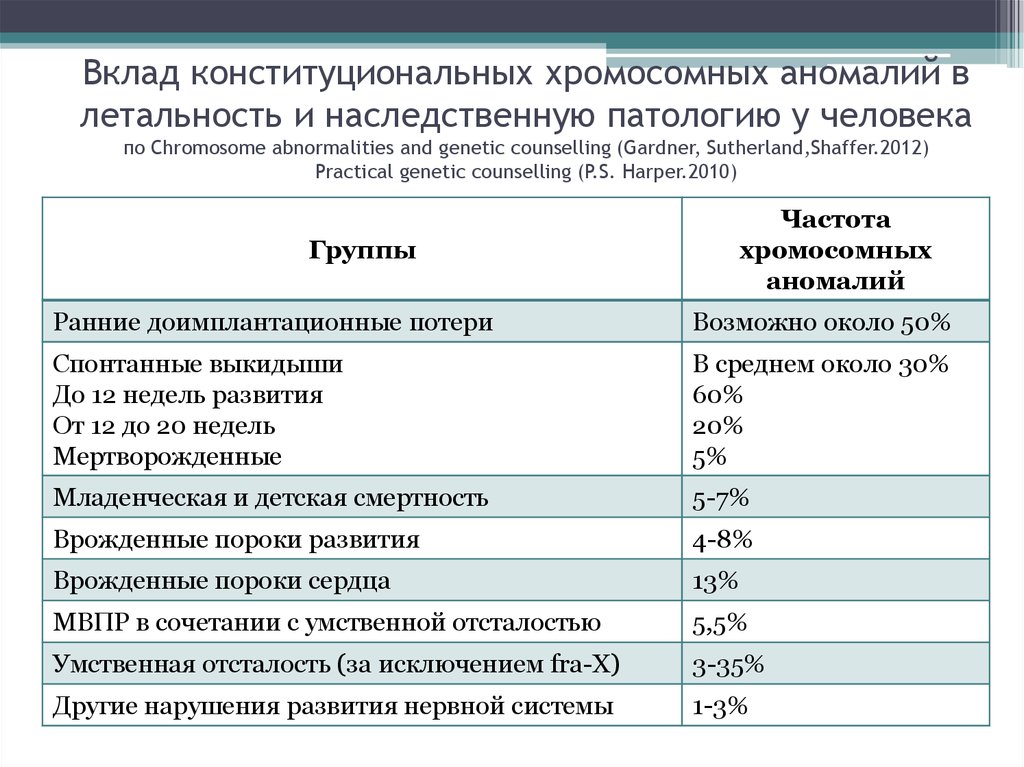
2. Вклад конституциональных хромосомных аномалий в летальность и наследственную патологию у человека по Chromosome abnormalities
and genetic counselling (Gardner, Sutherland,Shaffer.2012)Practical genetic counselling (P.S. Harper.2010)
Частота
хромосомных
аномалий
Группы
Ранние доимплантационные потери
Возможно около 50%
Спонтанные выкидыши
До 12 недель развития
От 12 до 20 недель
Мертворожденные
В среднем около 30%
60%
20%
5%
Младенческая и детская смертность
5-7%
Врожденные пороки развития
4-8%
Врожденные пороки сердца
13%
МВПР в сочетании с умственной отсталостью
5,5%
Умственная отсталость (за исключением fra-X)
3-35%
Другие нарушения развития нервной системы
1-3%
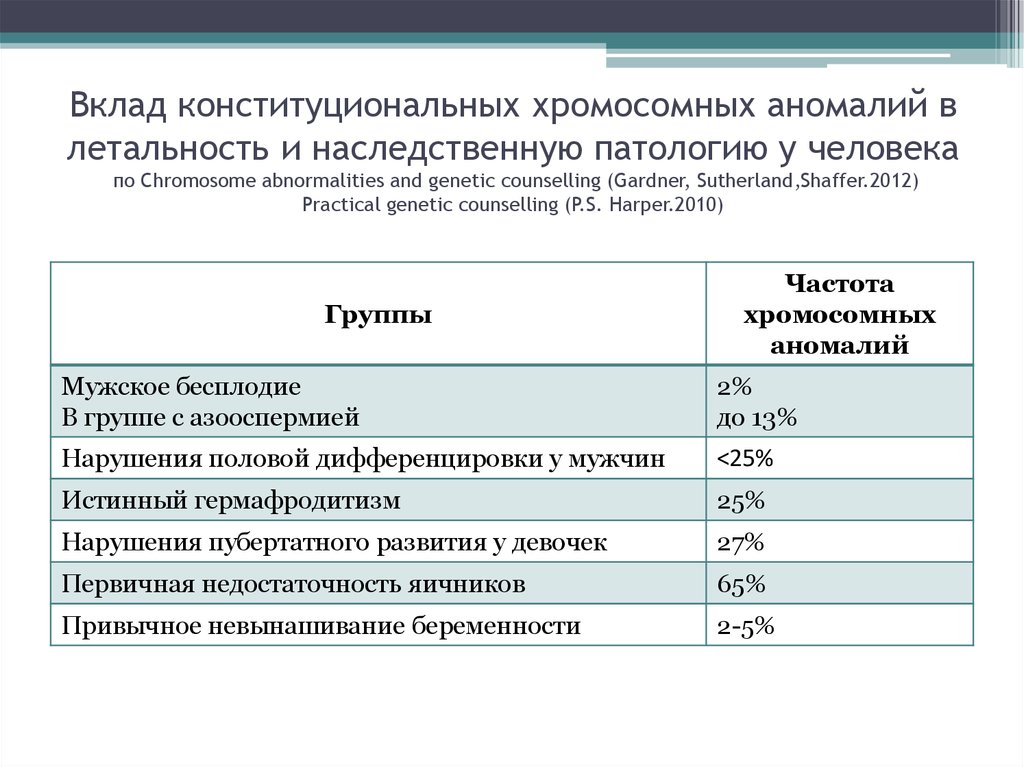
3. Вклад конституциональных хромосомных аномалий в летальность и наследственную патологию у человека по Chromosome abnormalities
and genetic counselling (Gardner, Sutherland,Shaffer.2012)Practical genetic counselling (P.S. Harper.2010)
Группы
Частота
хромосомных
аномалий
Мужское бесплодие
В группе с азооспермией
2%
до 13%
Нарушения половой дифференцировки у мужчин
˂25%
Истинный гермафродитизм
25%
Нарушения пубертатного развития у девочек
27%
Первичная недостаточность яичников
65%
Привычное невынашивание беременности
2-5%
4. Классификация аномалий кариотипа
По типу мутации• Синдромы, обусловленные
аномалиями числа хромосом:
▫ тетраплоидии, триплоидии
▫ трисомии
▫ моносомия
• Синдромы, обусловленные
структурными перестройками
хромосом:
▫ синдромы частичных
трисомий (дупликации)
▫ синдромы частичных
моносомий (делеции)
• Однородительская дисомия
По типу задействованной
хромосомы
• Аутосомные синдромы
• Гоносомные синдромы
(аномалии половых хромосом)
По происхождению
• Гаметические мутации (ХБ)
• Соматические мутации
• ранний эмбриогенез (ХБ)
• постнатальный период
(онкологические болезни)
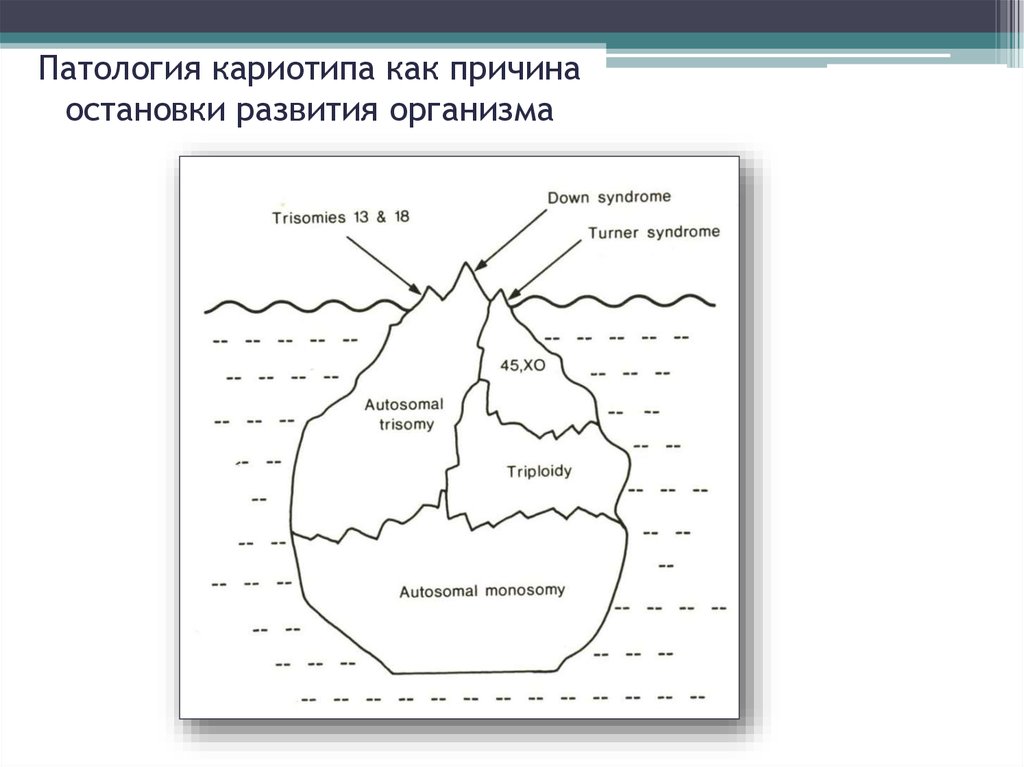
5. Патология кариотипа как причина остановки развития организма
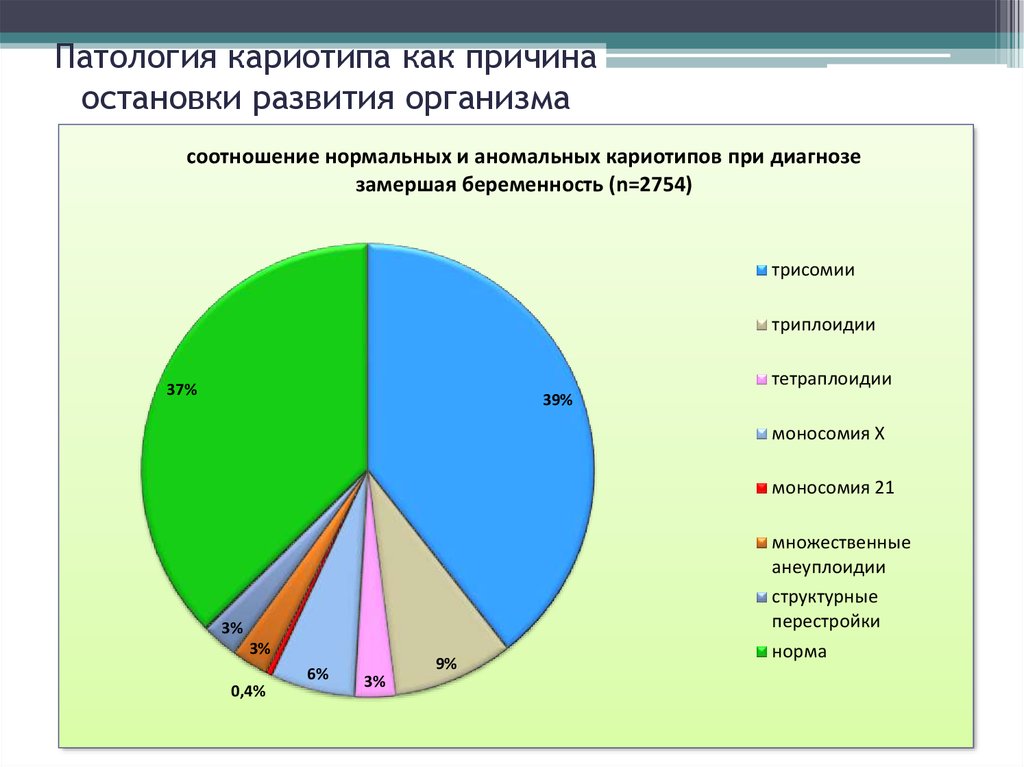
6. Патология кариотипа как причина остановки развития организма
соотношение нормальных и аномальных кариотипов при диагнозезамершая беременность (n=2754)
трисомии
триплоидии
тетраплоидии
37%
39%
моносомия Х
моносомия 21
3%
3%
6%
0,4%
9%
3%
множественные
анеуплоидии
структурные
перестройки
норма
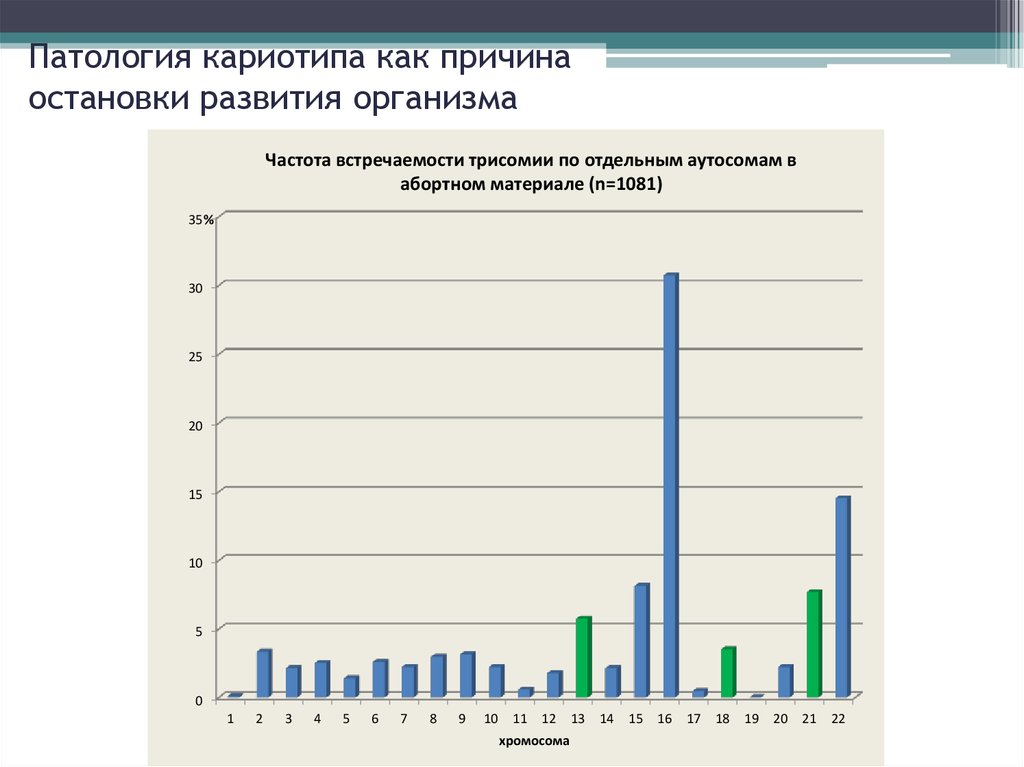
7. Патология кариотипа как причина остановки развития организма
Частота встречаемости трисомии по отдельным аутосомам вабортном материале (n=1081)
35 %
30
25
20
15
10
5
0
1
2
3
4
5
6
7
8
9
10
11
12
хромосома
13
14
15
16
17
18
19
20
21
22
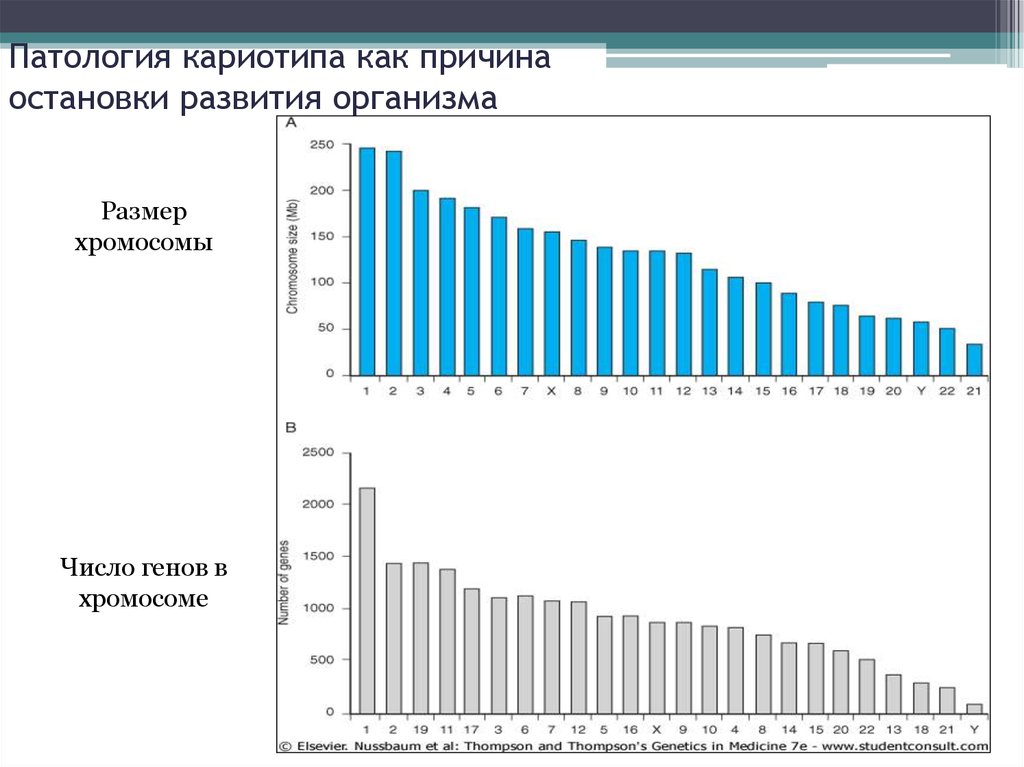
8. Патология кариотипа как причина остановки развития организма
Размерхромосомы
Число генов в
хромосоме
9.
Частота хромосомных аномалий в популяцииноворожденных детей
Practical genetic counselling (P.S. Harper.2010)
Аномалия кариотипа
Частота
(на 1000)
Все аномалии
9.1
Трисомии аутосом
1.4
Сбалансированные перестройки аутосом
5.2
Несбалансированные перестройки аутосом
0.6
Аномалии половых хромосом:
при мужском фенотипе
при женском фенотипе
1.2
0.75
10. Хромосомные болезни
Наследственное заболевание (этиологический фактор – мутация)Изменение конститутивного кариотипа
Фенотипические проявления:
•летальность
•врожденные пороки развития
АУТОСОМНЫЕ СИНДРОМЫ
ГОНОСОМНЫЕ СИНДРОМЫ
Множественные врожденные
пороки развития
•Отсутствие тяжелых пороков развития
Резкое снижение
продолжительности жизни
•Нормальная продолжительность
жизни
Многочисленные микроаномалии
Задержка психомоторного
развития, умственная отсталость
•Нерезкая задержка психомоторного
развития/нормальный интеллект
Ранняя диагностика
•Диагностика в период полового
созревания
11.
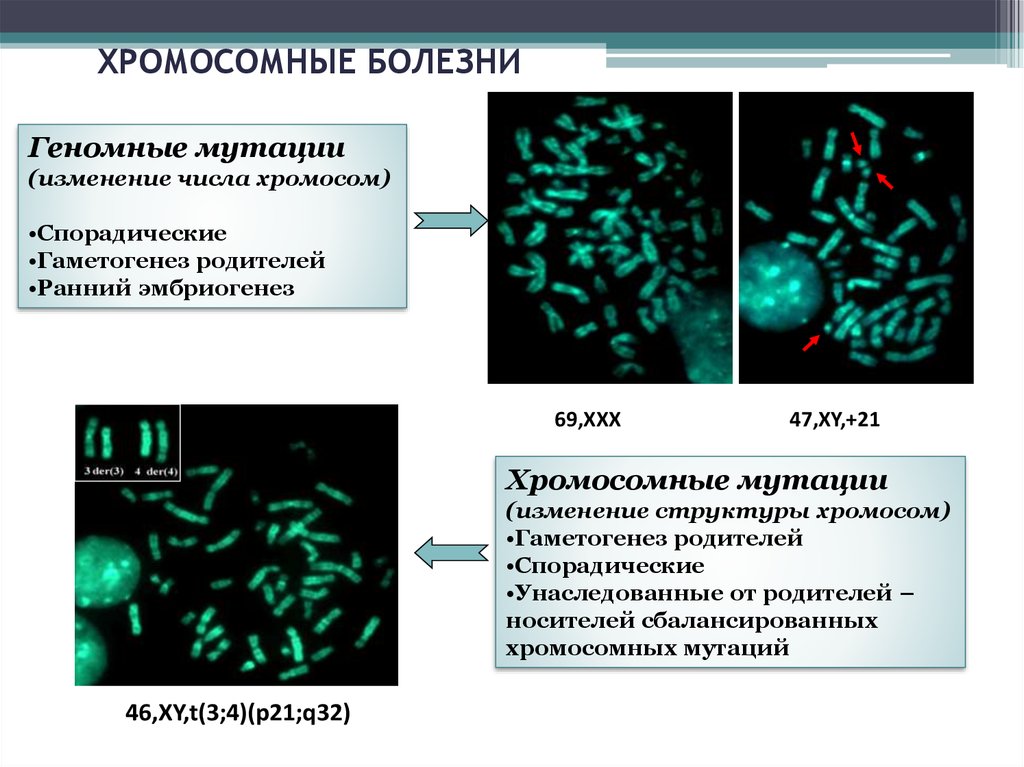
ХРОМОСОМНЫЕ БОЛЕЗНИГеномные мутации
(изменение числа хромосом)
•Спорадические
•Гаметогенез родителей
•Ранний эмбриогенез
69,ХХХ
47,ХY,+21
Хромосомные мутации
(изменение структуры хромосом)
•Гаметогенез родителей
•Спорадические
•Унаследованные от родителей –
носителей сбалансированных
хромосомных мутаций
46,XY,t(3;4)(p21;q32)
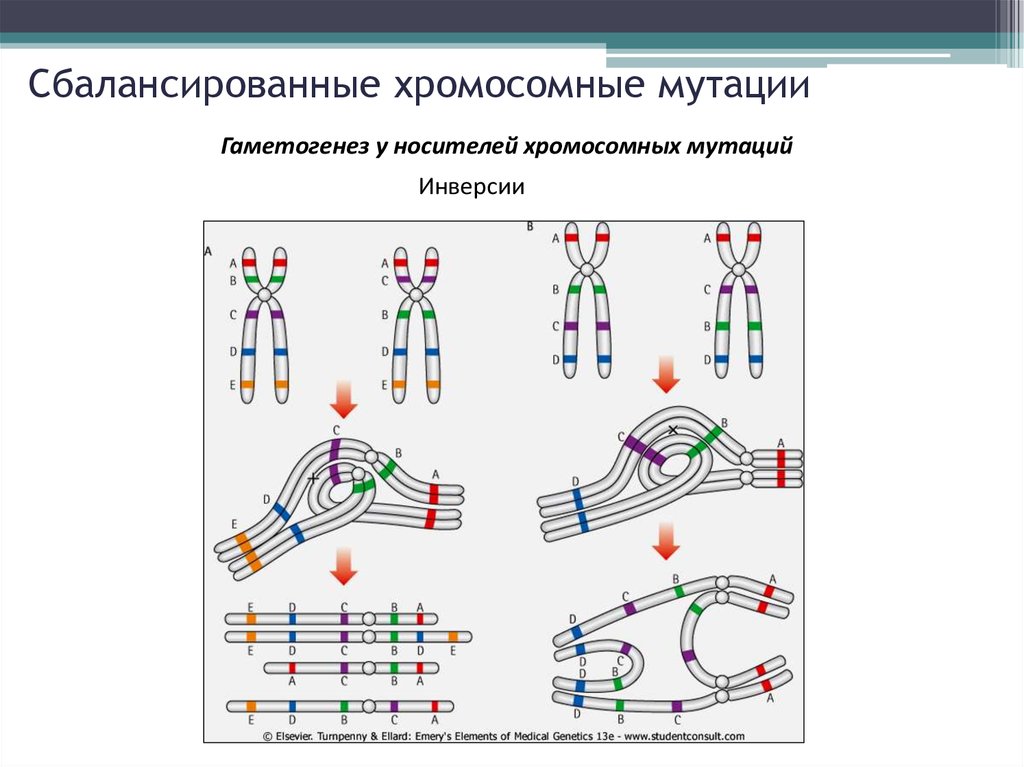
12. Сбалансированные хромосомные мутации
Гаметогенез у носителей хромосомных мутацийИнверсии
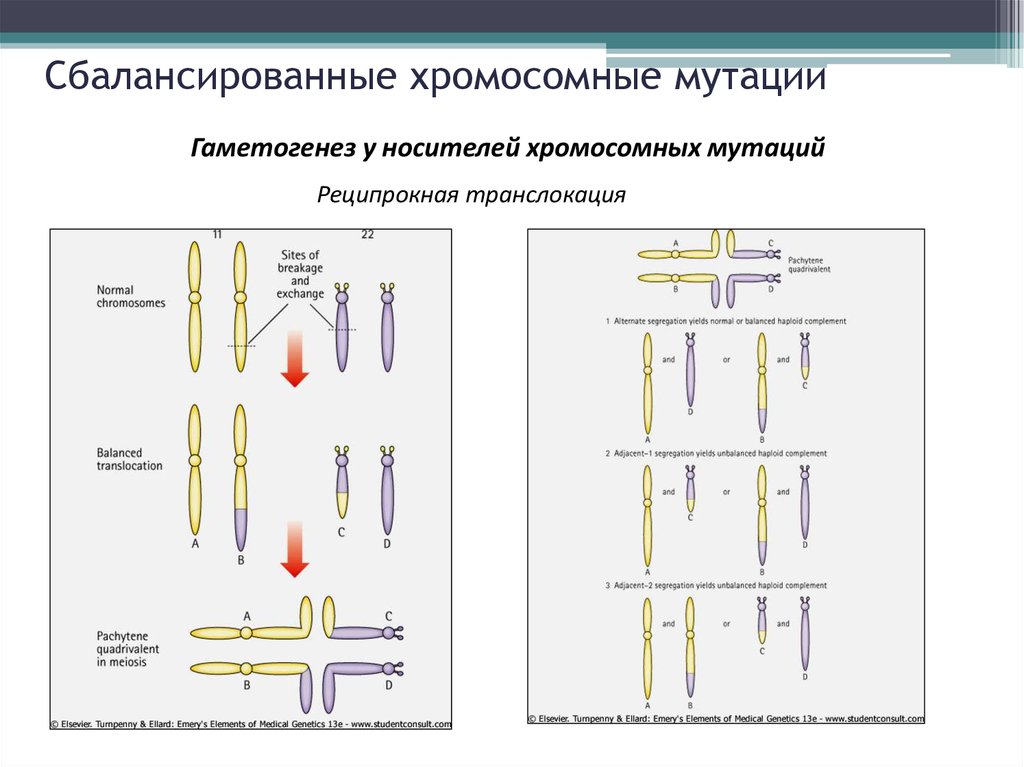
13. Сбалансированные хромосомные мутации
Гаметогенез у носителей хромосомных мутацийРеципрокная транслокация
14.
Частичная моносомия по Tel 7q и частичная трисомия по Tel 2q у ребёнка сЗПМР и микроаномалиями развития
der (7)
der (7)
– Tel 7p
– Tel 7q
– Tel 2p
– Tel 2q
Частичная
трисомия
2qTel
Частичная
моносомия
7qTel
гомологи
гомологи
гомологи
гомологи
хромосомы 2
хромосомы 7
хромосомы 2
хромосомы 7
15.
Сбалансированная реципрокная транслокация между хромосомами 2 и 7 –кариотип 46,XY,t(2;7)(q37;q36) у отца ребенка
der (2)
der (7)
der (7)
der (2)
– Tel 7p
– Tel 7q
– Tel 2p
– Tel 2q
гомологи
гомологи
гомологи
гомологи
хромосомы 2
хромосомы 7
хромосомы 2
хромосомы 7
16.
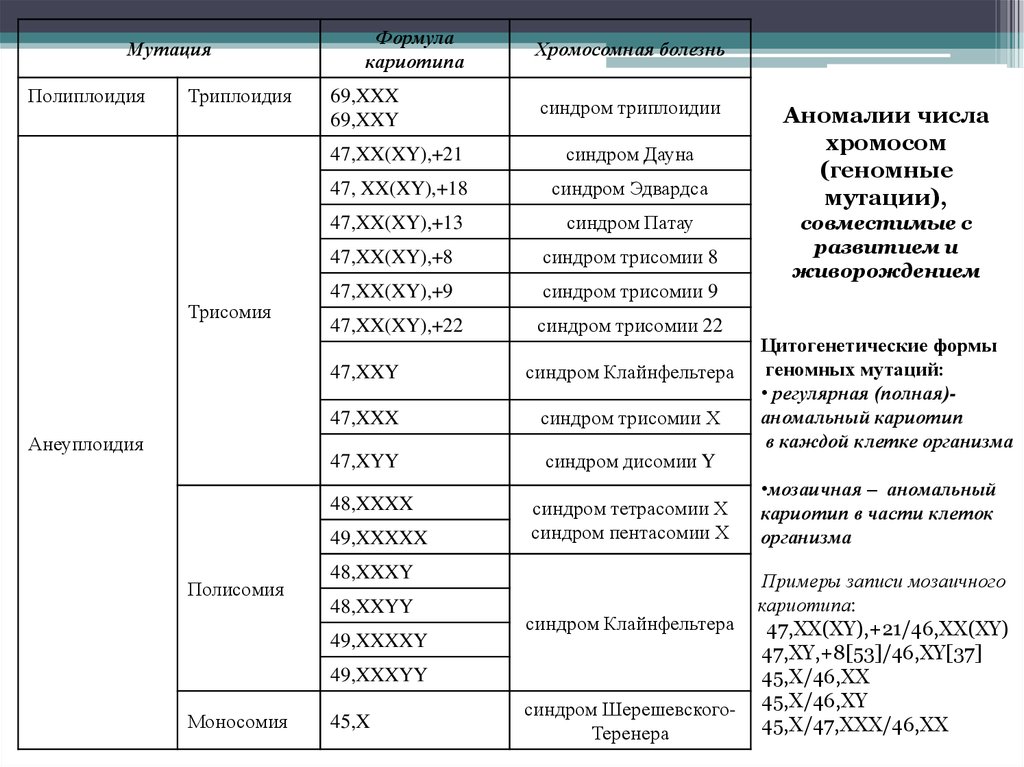
МутацияПолиплоидия
Триплоидия
Трисомия
Анеуплоидия
Формула
кариотипа
69,XXX
69,XXY
синдром триплоидии
47,XX(XY),+21
синдром Дауна
47, XX(XY),+18
синдром Эдвардса
47,XX(XY),+13
синдром Патау
47,XX(XY),+8
синдром трисомии 8
47,XX(XY),+9
синдром трисомии 9
47,XX(XY),+22
синдром трисомии 22
47,XXY
синдром Клайнфельтера
47,XXX
синдром трисомии Х
47,XYY
синдром дисомии Y
48,XXXX
49,XXXXX
Полисомия
Хромосомная болезнь
синдром тетрасомии Х
синдром пентасомии Х
48,XXXY
48,XXYY
49,XXXXY
синдром Клайнфельтера
49,XXXYY
Моносомия
45,X
синдром ШерешевскогоТеренера
Аномалии числа
хромосом
(геномные
мутации),
совместимые с
развитием и
живорождением
Цитогенетические формы
геномных мутаций:
• регулярная (полная)аномальный кариотип
в каждой клетке организма
•мозаичная – аномальный
кариотип в части клеток
организма
Примеры записи мозаичного
кариотипа:
47,XX(XY),+21/46,XX(XY)
47,XY,+8[53]/46,XY[37]
45,X/46,XX
45,X/46,XY
45,X/47,XXX/46,XX
17.
Зарегистрированы тысячиструктурных перестроек по всем
хромосомам человека.
К хромосомным болезням
приводят несбалансированные
структурные перестройки (делеции,
дупликации, изохромосомы,
кольцевые хромосомы, маркерные
хромосомы).
18.
Микроделеционные синдромы19.
20. Историческая справка
Down JLH. Observations on an Ethnic Classification ofIdiots. Clinical Lecture Reports, London Hospital, 1866, 3:
259-262.
Классификация умственной отсталости по
этническим стандартам (кавказцы, эфиопы,
малайцы, американские индейцы, монголы). Первое
клиническое описание умственно отсталых детей,
объединяемых в настоящее время термином
«синдром Дауна»
John Langdon Haydon
Down
21. Историческая справка
MartheGautier
Jerome
Lejeune
Raymond
Turpin
Lejeune J, Gautier M and Turpine R (1959) Etude des chromosomes somatiquesde
neuf enfants mongoliens. C. R. Acad. Sci. 248,1721-1722.
Проведено исследование метафазных хромосом из
культивированных фибробластов девяти детей с
монголоидной идиотией (пяти мальчиков и четырех
девочек). Выявлено 47 хромосом, сверхчисленной
оказалась маленькая телоцентрическая хромосома.
Впервые показано, что причиной болезни является
нарушение в кариотипе.
22. Историческая справка
Polani PE, Briggs JH, Ford CE, Clarke CM and Berg JM (1960).A Mongol girl with 46 chromosomes. Lancet 1, 721-724.
Penrose LS, Ellis JR and Delhanty JDA (1960). Chromosomal
translocations in mongolism and in normal relatives. Lancet 2, 409-410.
Первые описания транслокационной формы синдрома
Дауна.
Lionel Penrose
Paul Polani
Clarke CM, Edwards JH and Smallpiece V (1961).
Trisomy/nomal Mosaicism, in an intelligent child with some
Mongoloid characters. Lancet 1, 1028-1030. Описана
John H Edwards мозаичная форма синдрома Дауна.
23. Синдром Дауна
Синонимы: синдром трисомии по хромосоме 21,G1-трисомияOMIM: 190685
Популяционная частота: 1:700 новорожденных
Соотношение по полу 1:1
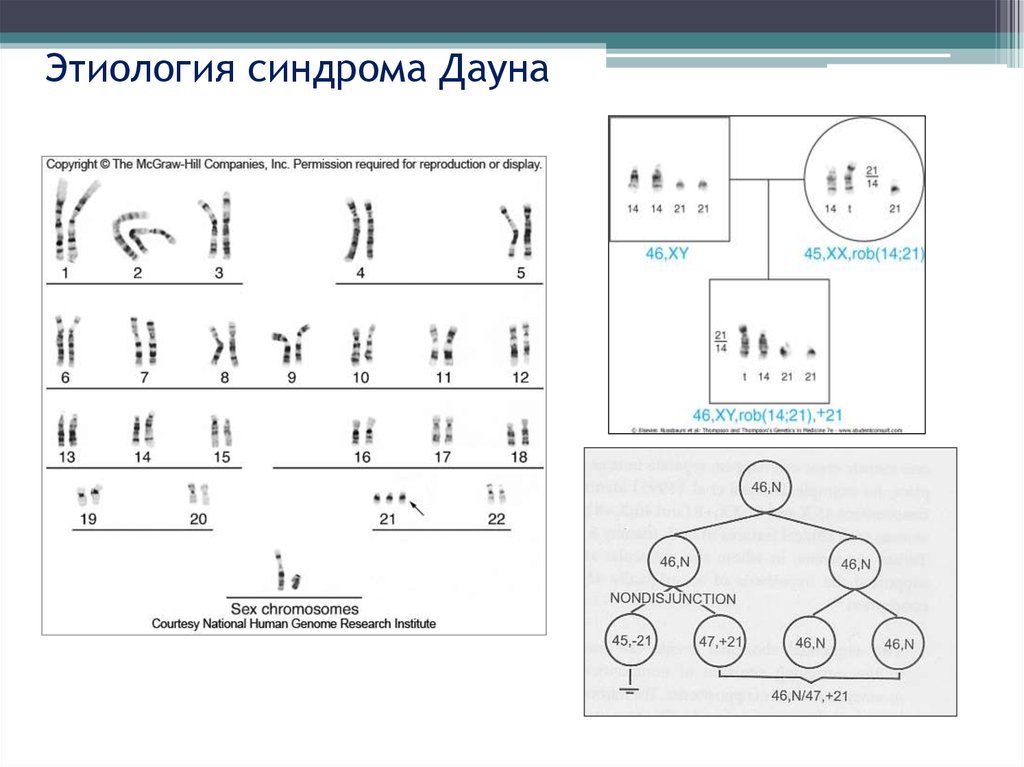
Цитогенетические формы:
90-95% - простая регулярная трисомия - 47,XX,+21 или
47,XY,+21
3-5% - мозаичная форма – 47,XX,+21/46,XX или
47,XY,+21/46,XY
4 % - транслокационная форма – 46,XX,der(14;21),+21
46,XY,der(14;21),+21
робертсоновская транлокация может быть между любой из
акроцентрических хромосомом (13, 14, 15, 21, 22) и хромосомой 21
1% - частичная трисомия по хромосоме 21 (результат
мутации de novo или сегрегации перестроенных хромосом
родителя)
24. Этиология синдрома Дауна
25. Этиология синдрома Дауна
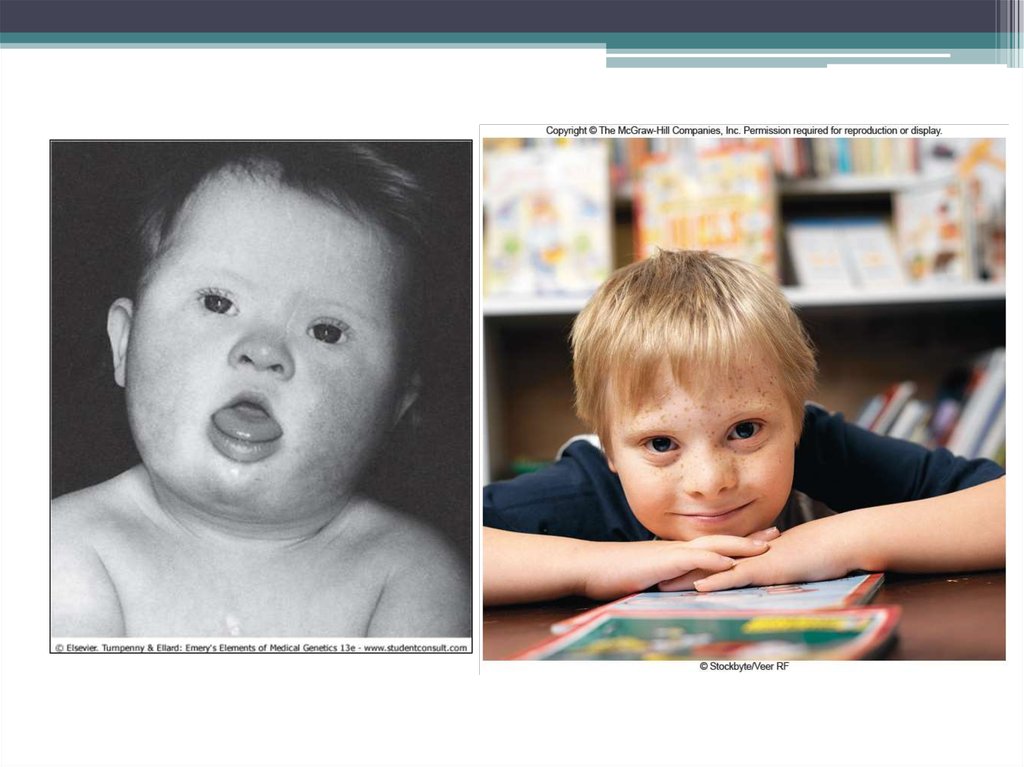
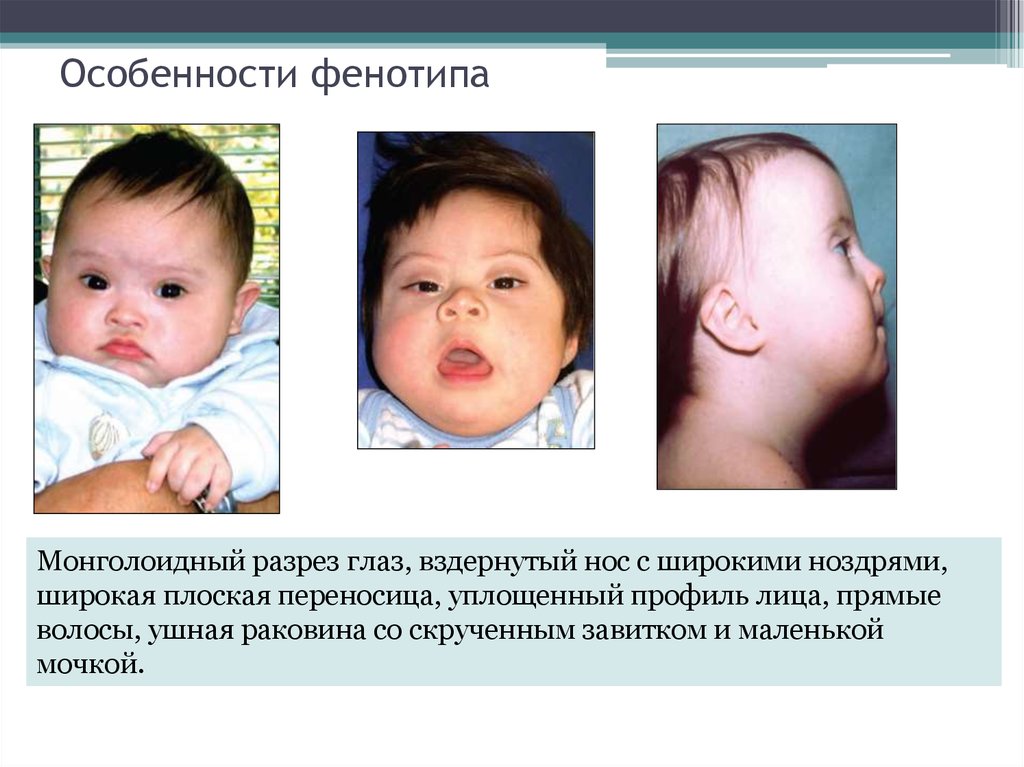
26. Особенности фенотипа
Монголоидный разрез глаз, вздернутый нос с широкими ноздрями,широкая плоская переносица, уплощенный профиль лица, прямые
волосы, ушная раковина со скрученным завитком и маленькой
мочкой.
27. Особенности фенотипа
Короткая шея с «воротниковой» складкой, мышечнаягипотония, полуоткрытый рот, макроглоссия
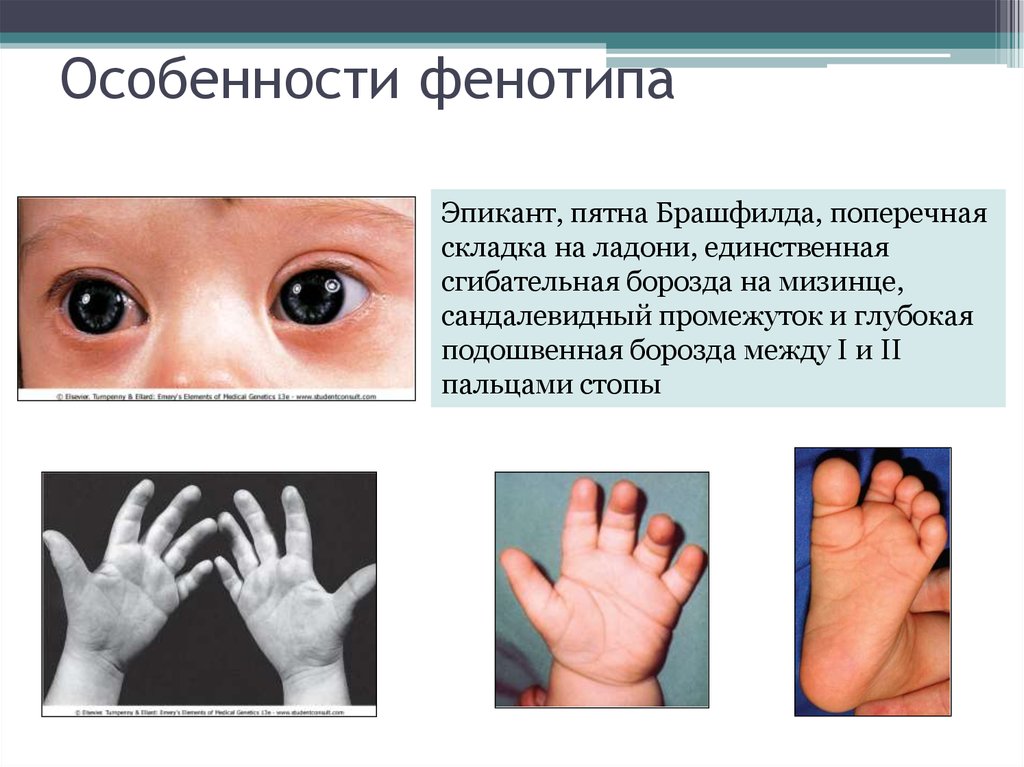
28. Особенности фенотипа
Эпикант, пятна Брашфилда, поперечнаяскладка на ладони, единственная
сгибательная борозда на мизинце,
сандалевидный промежуток и глубокая
подошвенная борозда между I и II
пальцами стопы
29. Клиническая характеристика
Умственная отсталостьНарушение зрения (близорукость, косоглазие, катаракта)
Нейросенсорная или смешанная тугоухость
Аномалии зубов
Низкий рост, брахидактилия, изменение дерматоглифики
Врожденные пороки сердца
Гипогонадизм, снижение фертильности, бесплодие
Раннее старение
Аномалии развития ЖКТ (стенозы, атрезии, болезнь Гиршспрунга)
Лейкозы
Ослабленный иммунитет (частые инфекционные заболевания)
50% больных умирает до 10 лет, 44% доживают до 60-68
лет.
В 1997 г. средняя продолжительность жизни составила 49
лет.
Ежегодно в России рождается около 2400 детей с синдромом
Дауна.
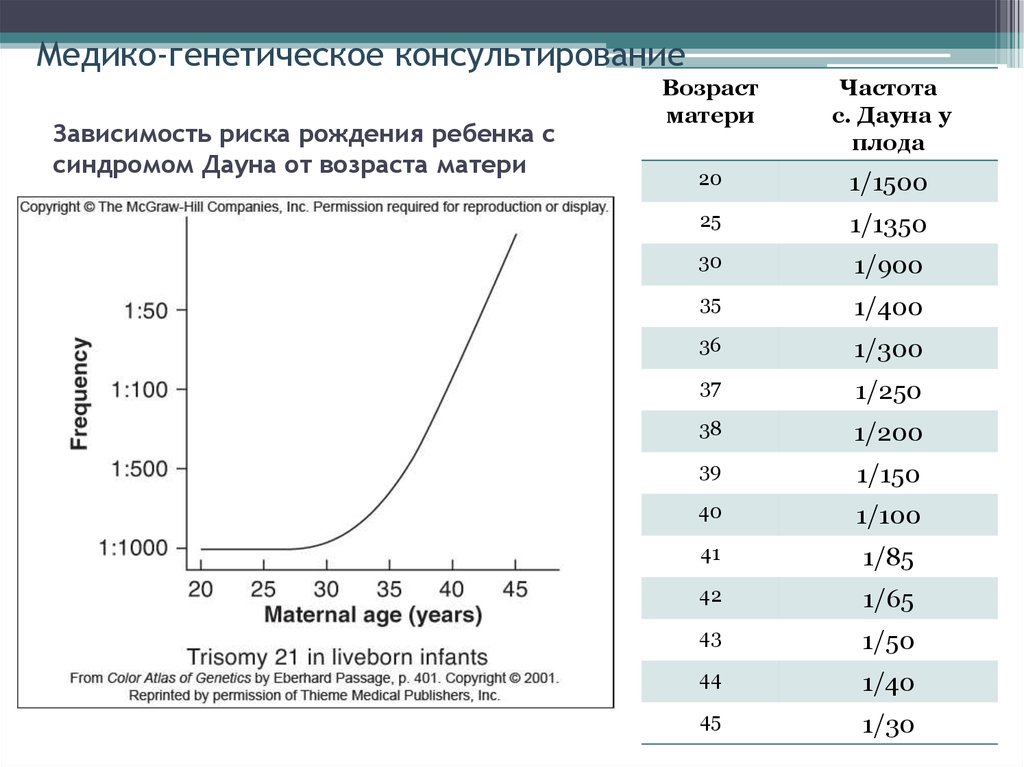
30. Зависимость риска рождения ребенка с синдромом Дауна от возраста матери
Медико-генетическое консультированиеЗависимость риска рождения ребенка с
синдромом Дауна от возраста матери
Возраст
матери
Частота
с. Дауна у
плода
20
1/1500
25
1/1350
30
1/900
35
1/400
36
1/300
37
1/250
38
1/200
39
1/150
40
1/100
41
1/85
42
1/65
43
1/50
44
1/40
45
1/30
31. Медико-генетическое консультирование
Клинический диагноз болезни Дауна необходимоподтверждать цитогенетическим исследованием
(ведущий признак хромосомной болезни – аномалия
кариотипа).
Вероятность рецидива простой регулярной трисомии у
следующего ребенка в семье составляет 1-2%, что
несколько выше среднего популяционного риска (0,5% )
и зависит от возраста матери.
Повторное рождение ребенка с простой трисомией в
семье может быть результатом скрытого соматического
или гонадного мозаицизма у родителя, или возможной
«предрасположенности» к нерасхождению хромосом.
Родителям может быть назначено кариотипирование и
тестирование генов «предрасположенности»
32. Медико-генетическое консультирование
При обнаружении у ребенка транслокационной формы болезниДауна, необходимо провести кариотипирование родителей. При
нормальном кариотипе родителей, повторный риск рождения
больного ребенка приближается к популяционному (1%)
При выявлении сбалансированной транслокации у одного из
родителей риск рождения больного ребенка определяется типом
перестройки и полом носителя:
Тип транслокации
(14;21)
(21;22)
(21;21)
Носитель
Риск для
потомства (%)
мать
10
отец
2,5
никто из родителей
˂1
один из родителей
возможно как для
(14;21), статистика
недостаточна
никто из родителей
низкий (возможно˂1)
любой из родителей
100
никто из родителей
низкий (возможно˂1)
33.
Методы оценки состояния плодаПРЯМЫЕ
(обследование плода)
НЕПРЯМЫЕ
(обследование беременной)
Клиническое
Медико-генетическое
консультирование
НЕИНВАЗИВНЫ
Е
ИНВАЗИВНЫЕ
Анализ
эмбрионспецифически
х белков:
•α–фетопротеин
• хорионический гонадотропин
• РАРРА
Цитогенетическая,
биохимическая
и молекулярная
пренатальная диагностика
Ультразвуковое
сканирование
Методы
лабораторной
генетики
34. Показания для проведения инвазивной пренатальной диагностики с целью исключения хромосомной патологии
• Возраст матери от 35 лет и старше• Наличие в анамнезе ребенка или плода с
хромосомной патологией или МВПР
• Установленное семейное носительство
хромосомной аномалии
• Выявление у плода УЗ-маркеров хромосомных
болезней
• Высокий риск хромосомной болезни у плода по
отклонению уровня сывороточных белков



















 Медицина
Медицина








