Похожие презентации:
Молекулярно-цитогенетическая диагностика острых лейкозов
1.
Молекулярно-цитогенетическаядиагностика острых лейкозов
2. Хромосомные нарушения
• ключевая роль в патогенезе опухолей• критерии для классификации гематологических опухолей
• цитогенетические маркеры опухолей
• цитогенетические факторы прогноза
• стратификация больных к терапии
• «прицельня терапия» - коррекция имеющихся нарушений на
генетическом или биохимическом уровне
• оценка эффективности терапии и контроль минимальной
резидуальной болезни
3.
Материал для исследованияКлетки:
костного мозга
крови
лимфоузла
селезенки
любой опухолевой ткани
4.
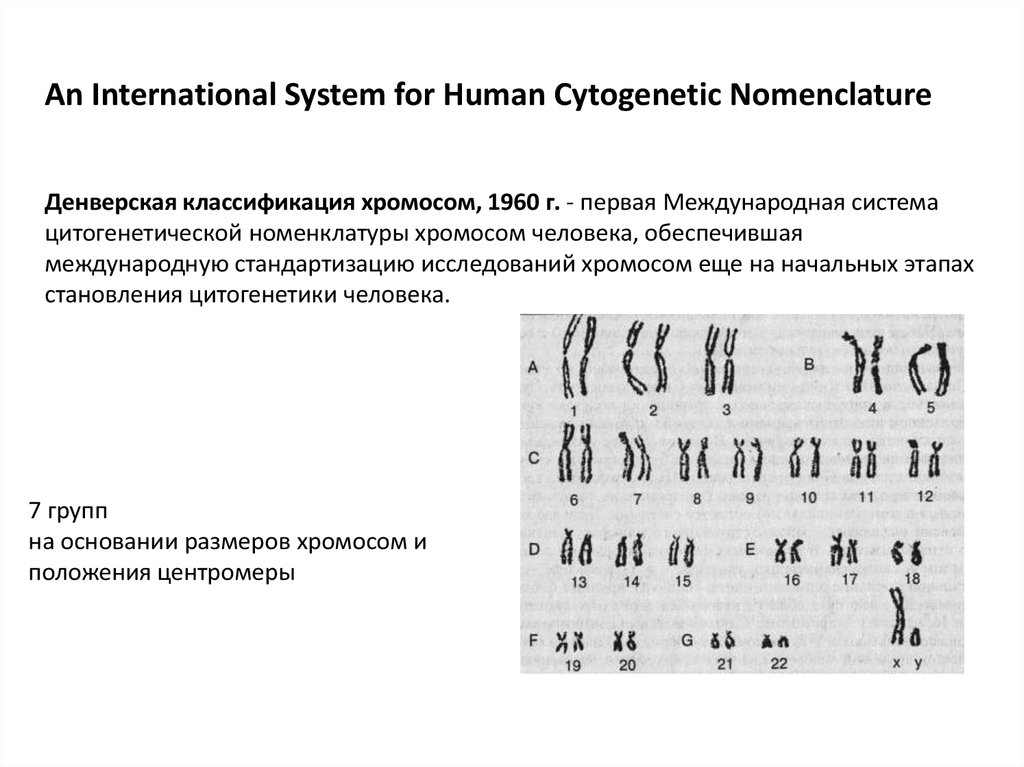
An International System for Human Cytogenetic NomenclatureДенверская классификация хромосом, 1960 г. - первая Международная система
цитогенетической номенклатуры хромосом человека, обеспечившая
международную стандартизацию исследований хромосом еще на начальных этапах
становления цитогенетики человека.
7 групп
на основании размеров хромосом и
положения центромеры
5.
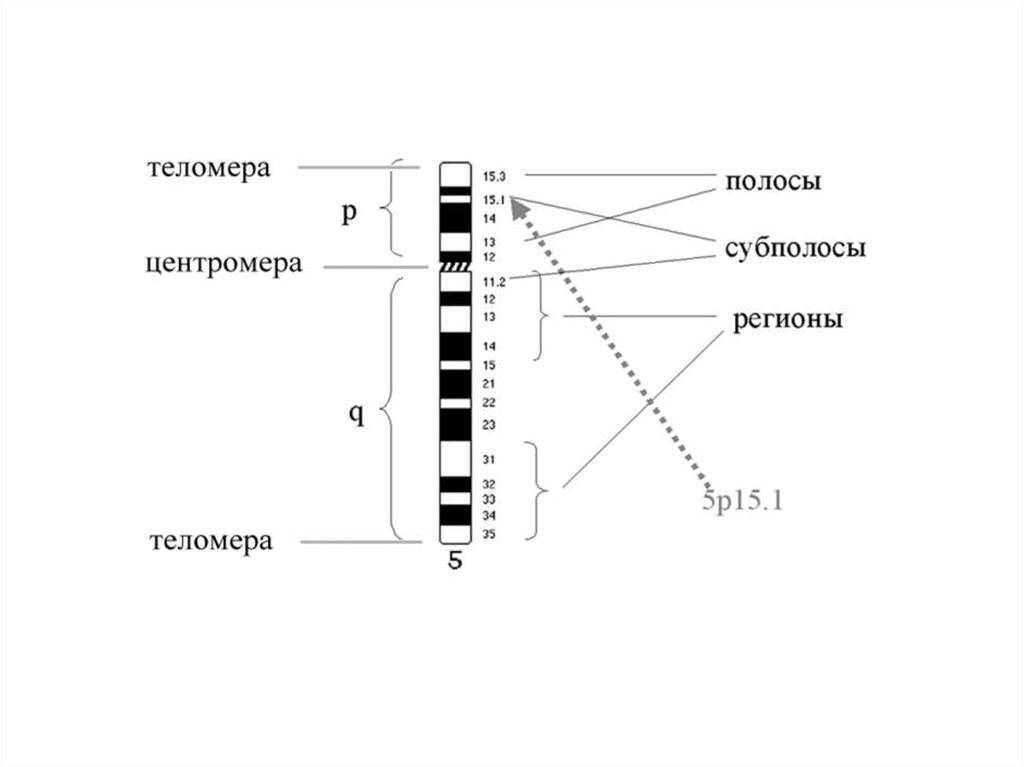
дифференциальная окраска хромосом(chromosome banding)
позволяет выявлять закономерно расположенные и
закрепленные наследственно участки плотной конденсации
вещества хромосом и, на основе их расположения,
идентифицировать хромосомы, не различающиеся по
признакам, видимым без такой окраски.
1968 г. - Torbjörn Caspersson
Q-окраска (Quinacrine – акрихин)
6.
1971 г. - Marina SeabrightG-окраска (Giemsa – Гимза)
Парижская классификация хромосом, 1971
7.
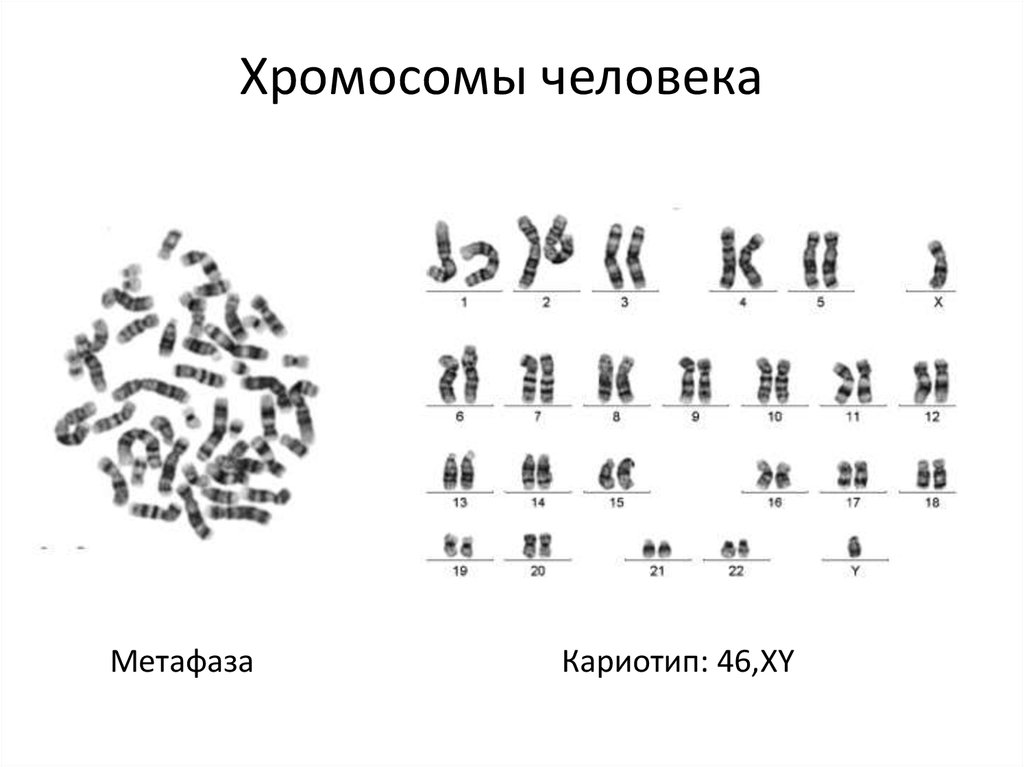
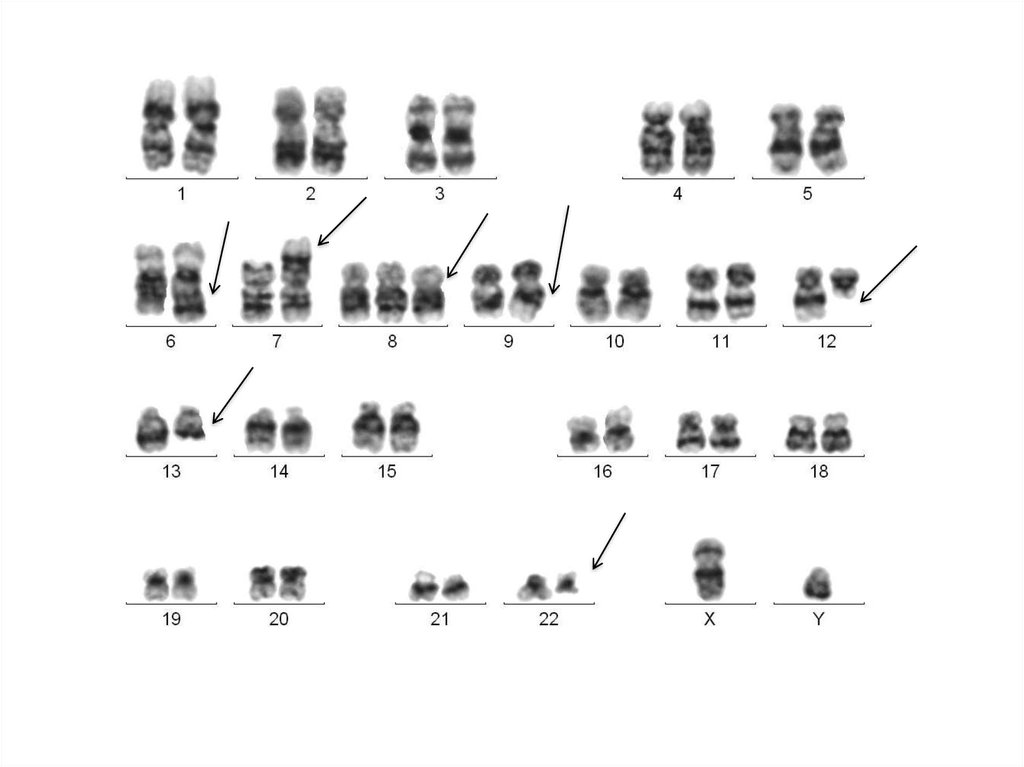
Хромосомы человекаМетафаза
Кариотип: 46,XY
8.
9.
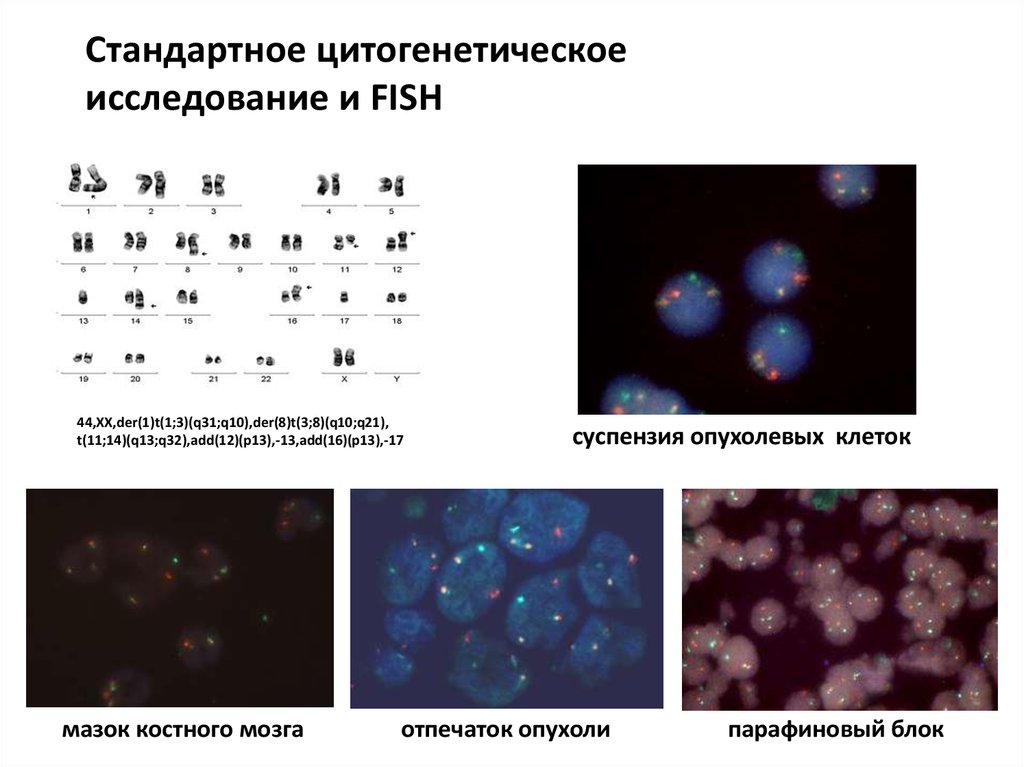
Стандартное цитогенетическоеисследование и FISH
44,XX,der(1)t(1;3)(q31;q10),der(8)t(3;8)(q10;q21),
t(11;14)(q13;q32),add(12)(p13),-13,add(16)(p13),-17
мазок костного мозга
суспензия опухолевых клеток
отпечаток опухоли
парафиновый блок
10.
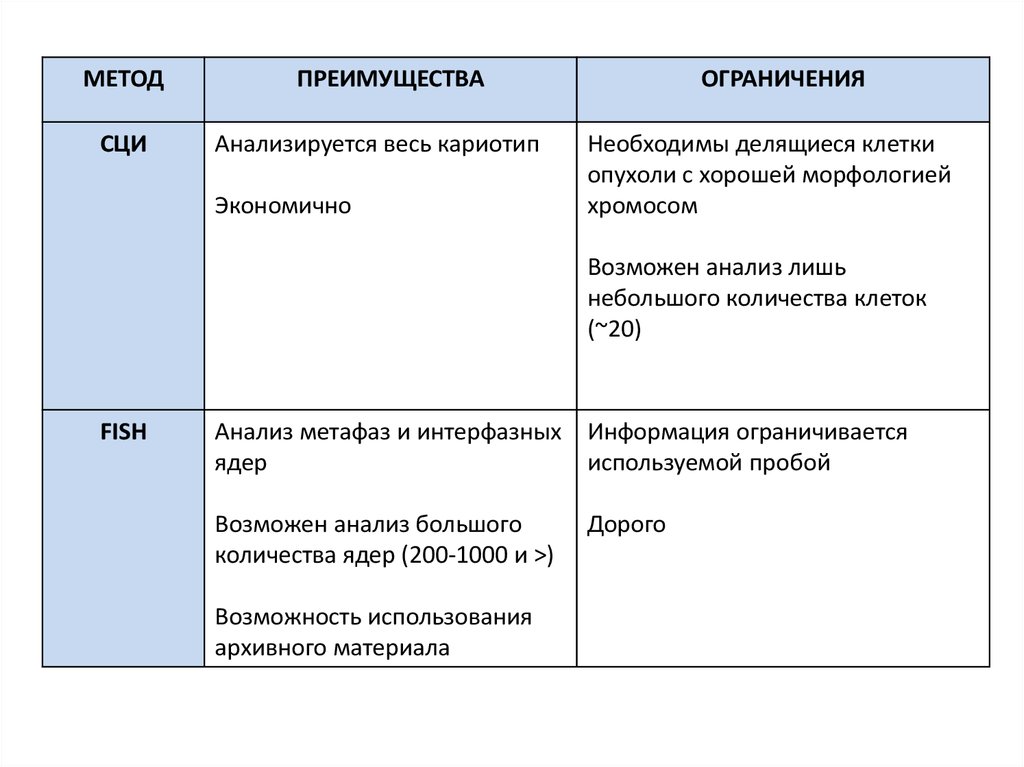
МЕТОДСЦИ
ПРЕИМУЩЕСТВА
Анализируется весь кариотип
Экономично
ОГРАНИЧЕНИЯ
Необходимы делящиеся клетки
опухоли с хорошей морфологией
хромосом
Возможен анализ лишь
небольшого количества клеток
(~20)
FISH
Анализ метафаз и интерфазных Информация ограничивается
ядер
используемой пробой
Возможен анализ большого
количества ядер (200-1000 и >)
Возможность использования
архивного материала
Дорого
11.
12.
Стандартное цитогенетическое исследованиекультивирование клеток
17-24 ч
прямая проба
задержка митоза (колхицин/колцемид)
обработка гипотоническим раствором KCl
фиксация (метанол+ледяная уксусная кислота)
приготовление препаратов и окраска хромосом
кариотипирование
13.
Количественные изменения кариотипатрисомия
дополнительная хромосома
в двух и более метафазах –
гипердиплоидия
моносомия
отсутствие хромосомы
в трех и более метафазах –
гиподиплоидия
14.
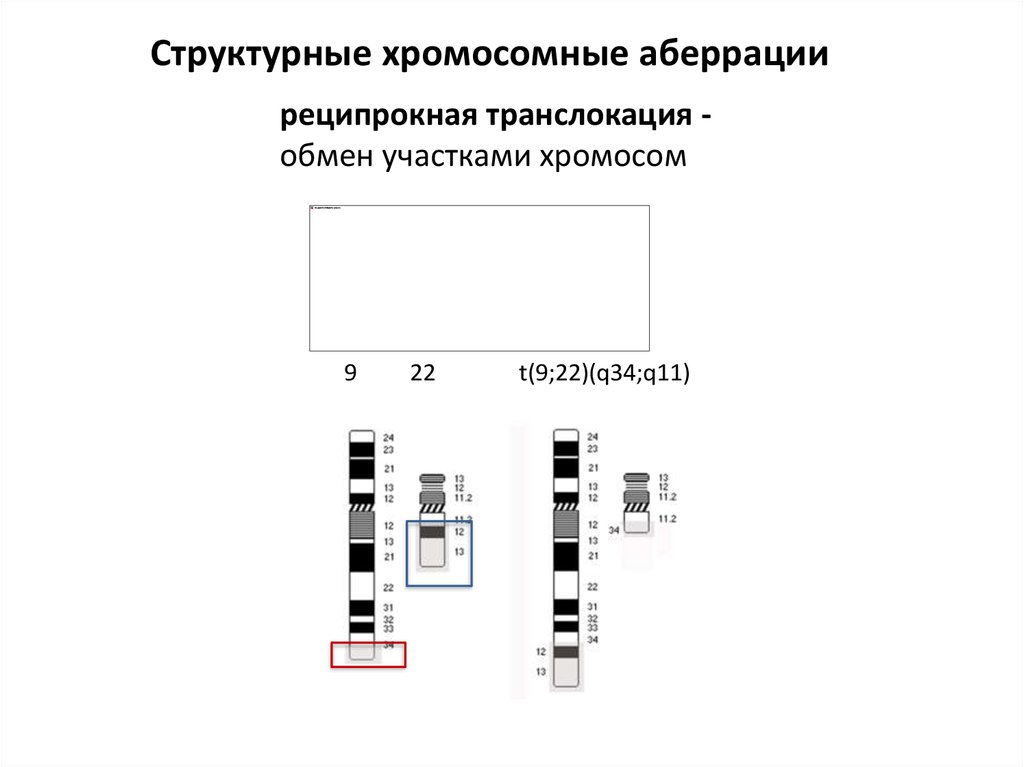
Структурные хромосомные аберрацииреципрокная транслокация обмен участками хромосом
9
22
t(9;22)(q34;q11)
15.
Инверсии3
inv(3)(q21q26)
перицентрическая инверсия
поворот участка хромосомы
на 1800 внутри плеча
16 inv(16)(p13q22)
парацентрическая инверсия
поворот участка хромосомы
на 1800 вокруг центромеры
16.
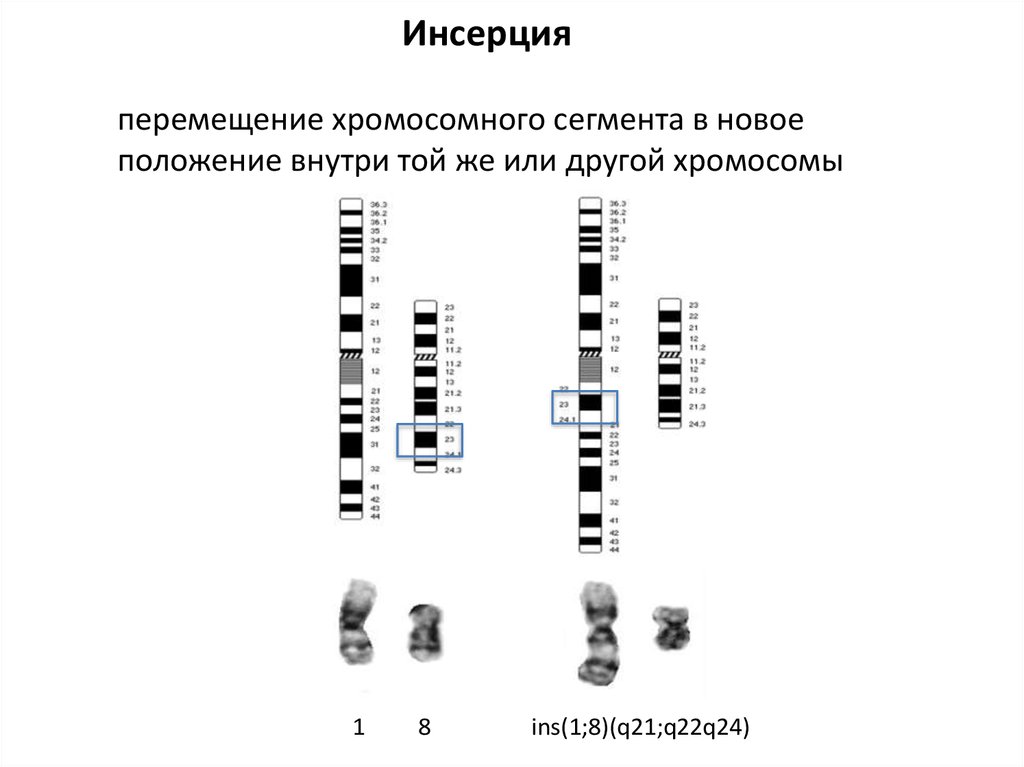
Инсерцияперемещение хромосомного сегмента в новое
положение внутри той же или другой хромосомы
1
8
ins(1;8)(q21;q22q24)
17.
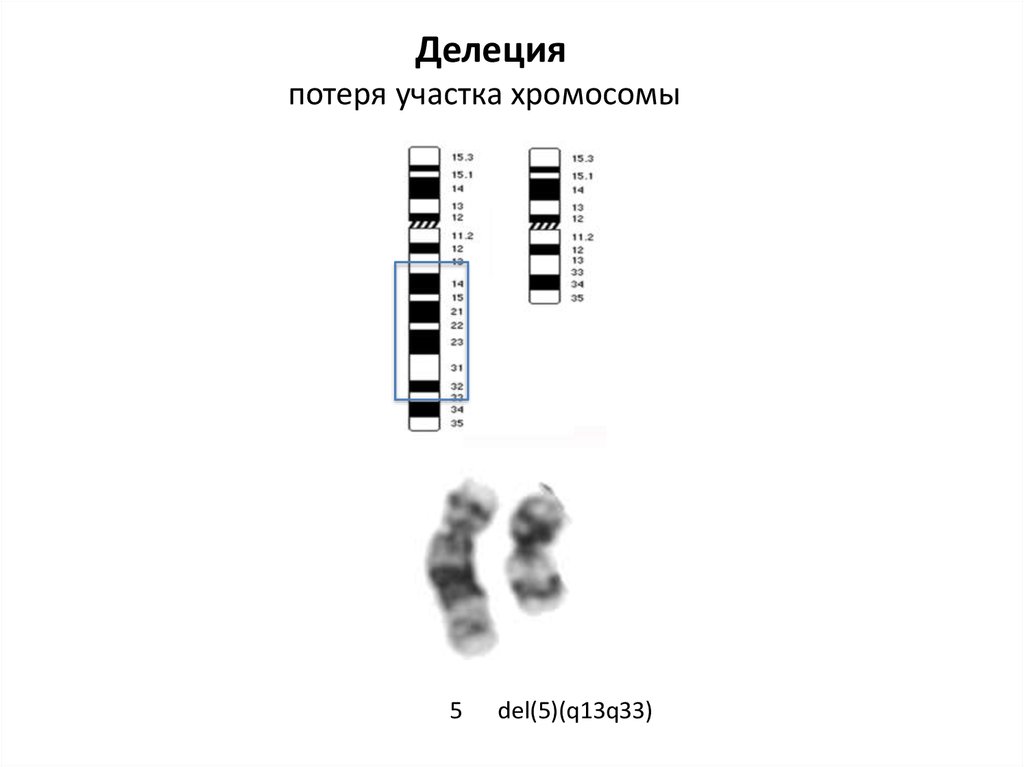
Делецияпотеря участка хромосомы
5
del(5)(q13q33)
18.
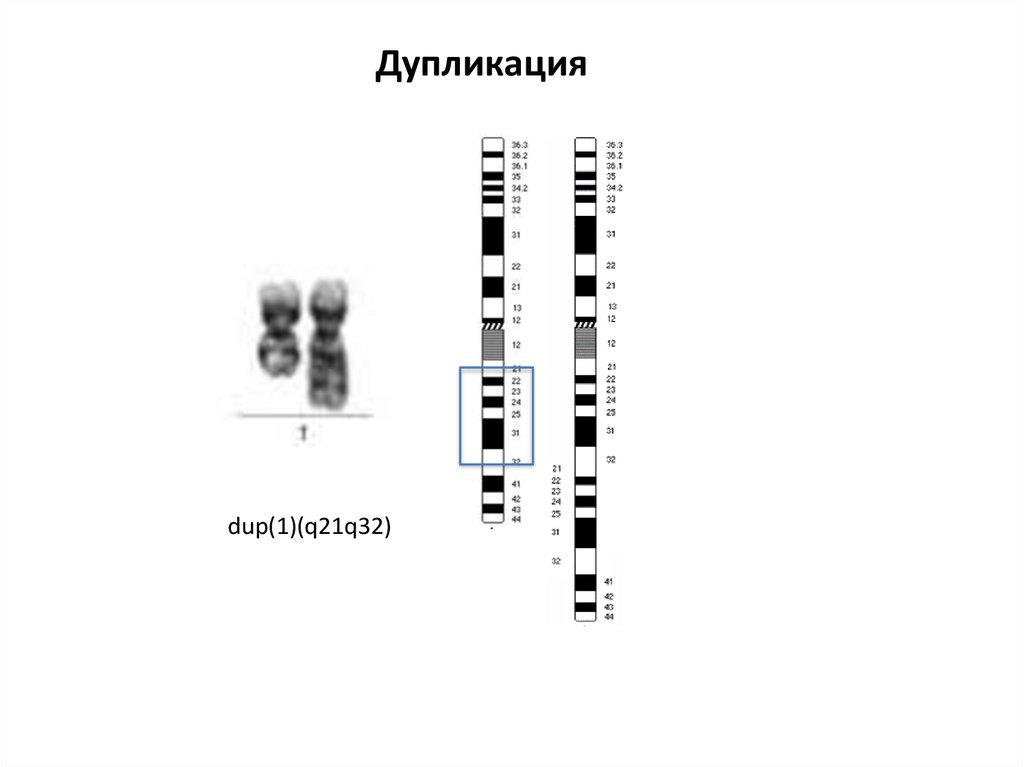
Дупликацияdup(1)(q21q32)
19.
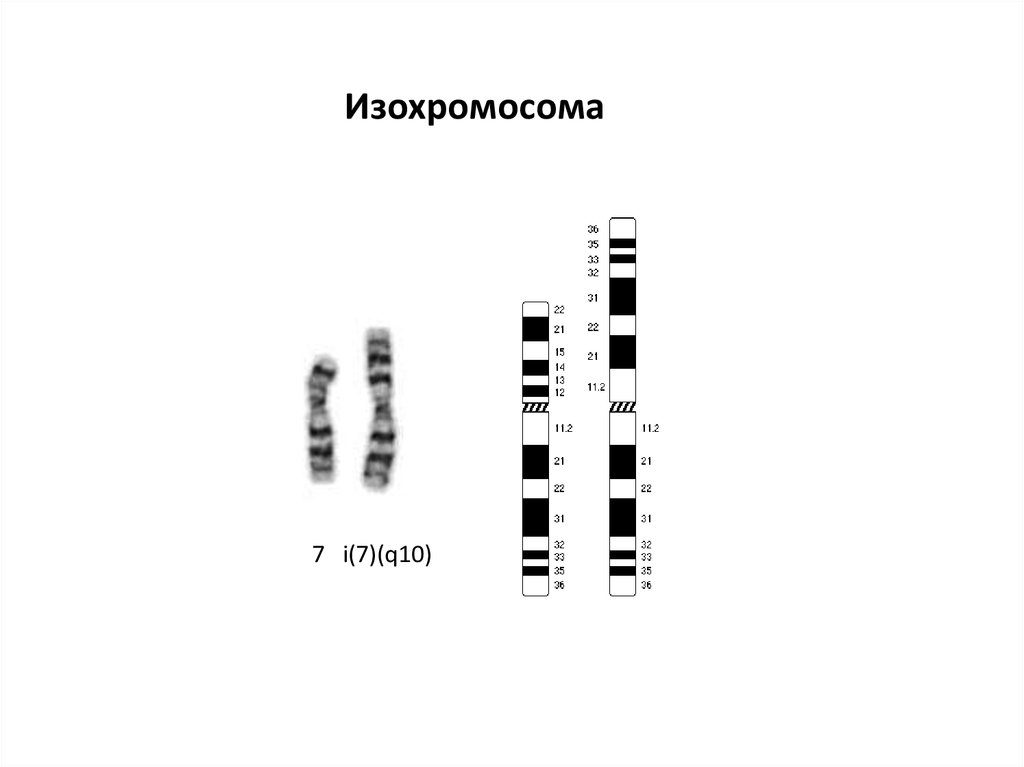
Изохромосома7 i(7)(q10)
20.
Дицентрическая хромосомаdic
21.
Кольцевая хромосомаr
22.
Дополнительный хромосомный материалнеизвестного происхождения
add
23.
Дериват хромосомы73~77<4n>XX,t(Y;13)(q10;q10)x2,t(1;5)(p22;q14~15),-2x2,add(2)(q37)or t(1;2)(q31;q37),-3,-4,
add(4)(p16)x2,+add(5) (p22;q14~15)or t(1;5)(p22;q14~15),add(6)(p23~25),add(7)(q36),-9,-10x2,
del(11)(p12),-12,add(12)(?q23),del(13)(q22),-14,add(14)(q32),-15,-17x2,add(20)(p13),-21,add(22)(p11),
+add(22)(p11)or t(9;22)(q10;q10),+3 mar
der
24.
Маркерная хромосома45,XX,add(2)(p21),-3,der(3)inv(3)(q21q26),-5,del(5)(q13q33),del(6)(q13),-7,-8,
del(12)(p12),der(12)del(12)(q22),+5mar[4]/ 45,XX,add(2)(p21) ,del(3)( q26),der(4),
-5,del(6)(q13),-7,-8,-11,der(11),del(12)(p12),der(12)del(12)(q22),-15,-18,+5mar[6]
mar
25.
Комплексные (множественные) перестройкитри и более аберрации
26.
An International System for Human Cytogenetic Nomenclature, 2013Кариотип: 46,XY [20]
Кариотип: 46,XX,t(15;17)(q22;q21) [20]
Кариотип: 47,XY,t(9;22)(q34;q11),+8 [16]/46,XY [4]
Кариотип: 46,XX,t(9;22)(q34;q11) [6]/47,idem,+8 [14]
Кариотип: 46,XX,t(9;22)(q34;q11) [12]/46,XX,del(13)(q14) [15]
Кариотип: 43-47,XX,add(2)(p21),inv(3)(q21q26),der(4),-5,del(6)(q13),-7,-8,der(11),
del(12)(p?12),-15,-18,+5mar [cp10]
27.
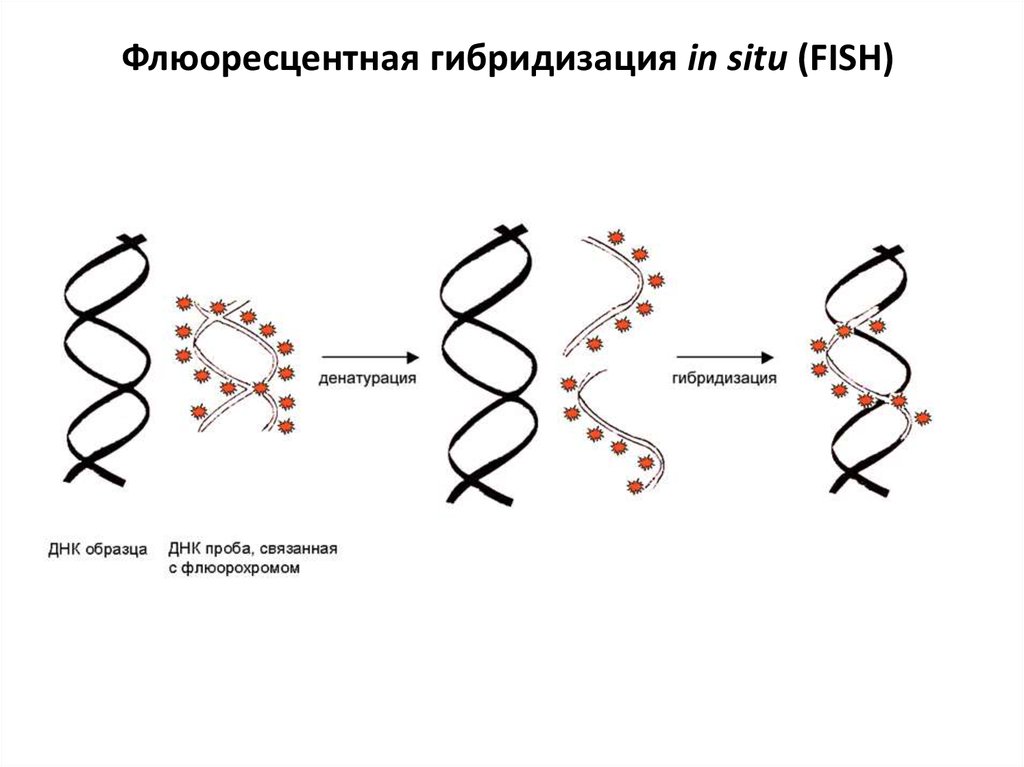
Fluorescence in situ hybridization (FISH)окраска флюорохромами участков комплементарной ДНК
прицельный поиск определенных хромосомных нарушений
интерфазная и метафазная
28.
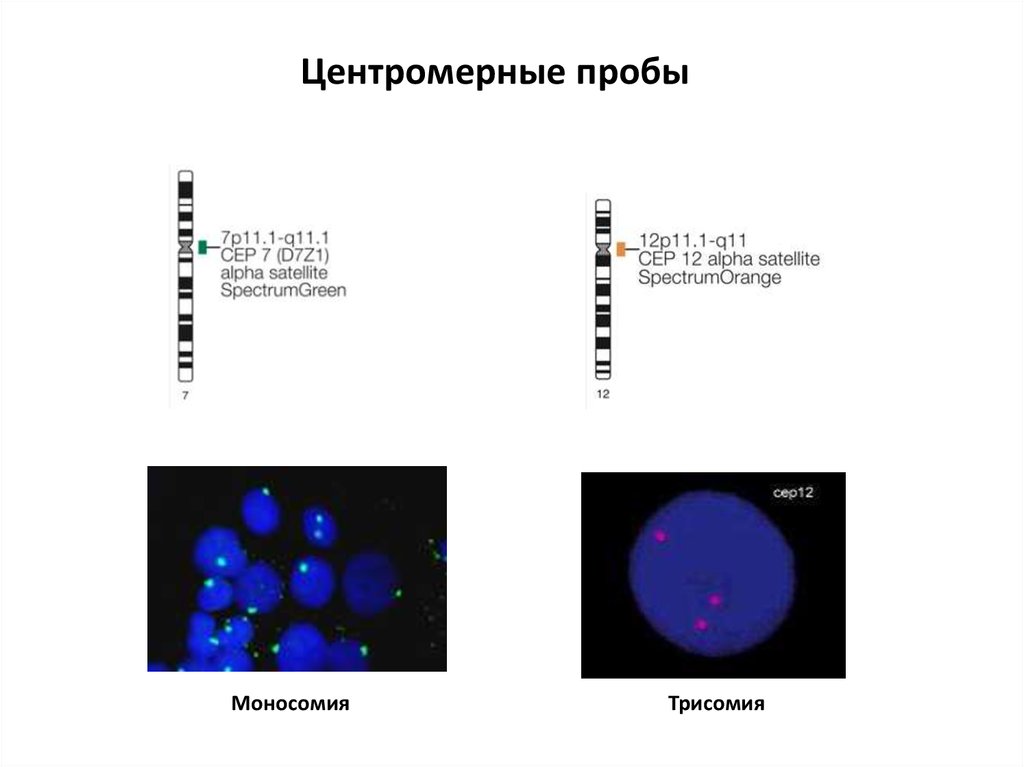
Флюоресцентная гибридизация in situ (FISH)29.
Центромерные пробыМоносомия
Трисомия
30.
Пробы для выявления транслокацийDual Fusion Translocation Probe
t(14;18)(q32;q21)
Break Apart Probe
t(18q21)/BCL2
31.
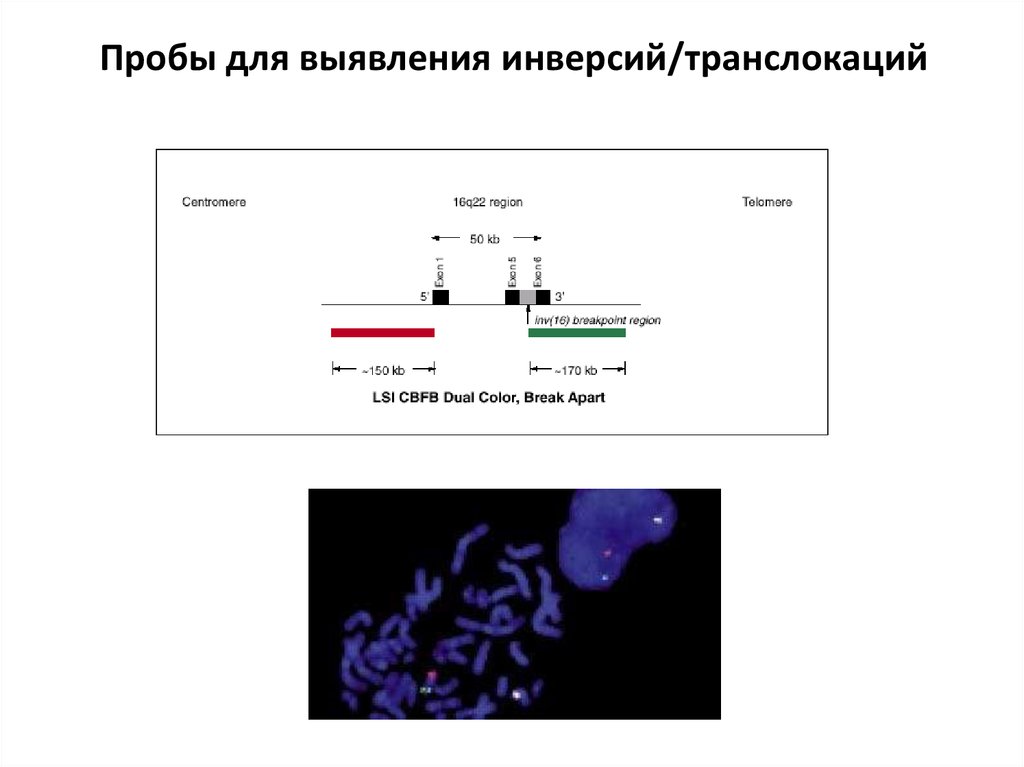
Пробы для выявления инверсий/транслокаций32.
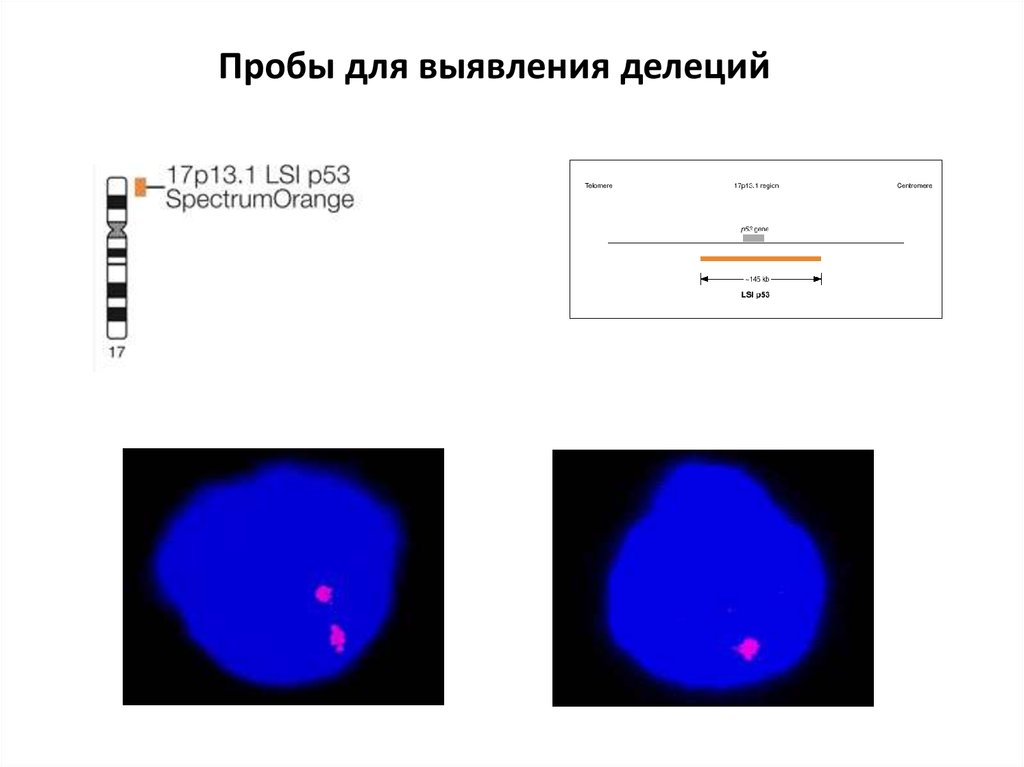
Пробы для выявления делеций33.
Пробы для выявления делеций и моносомийделеция 17р13/р53
моносомия 17
34.
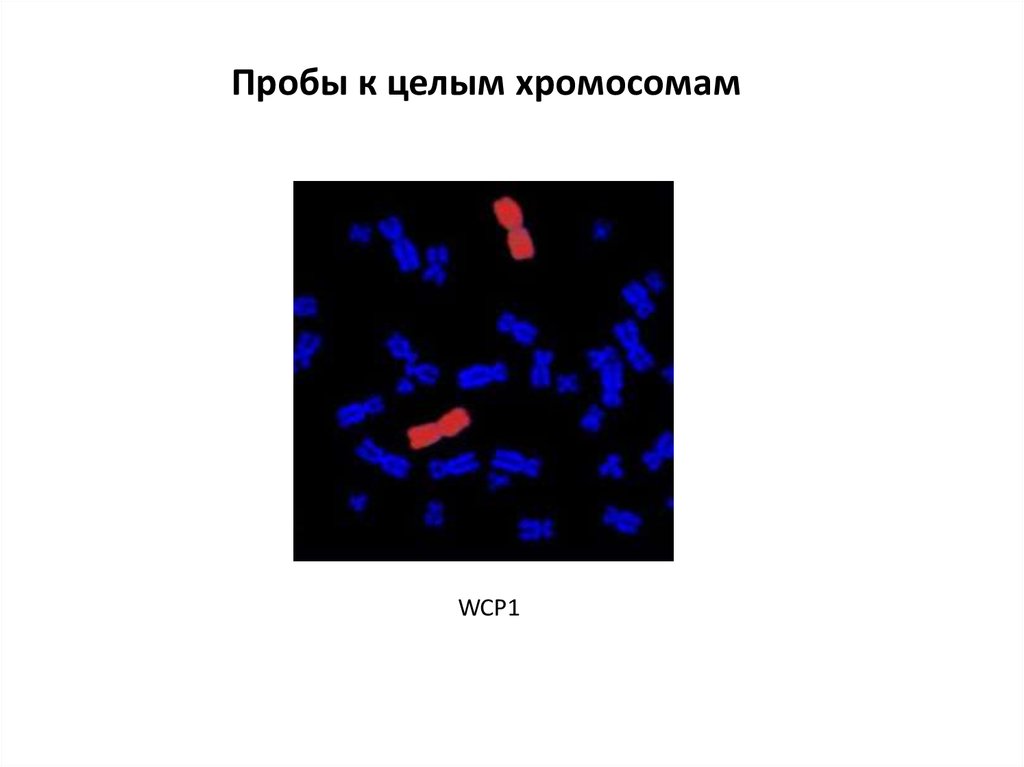
Пробы к целым хромосомамWCP1
35.
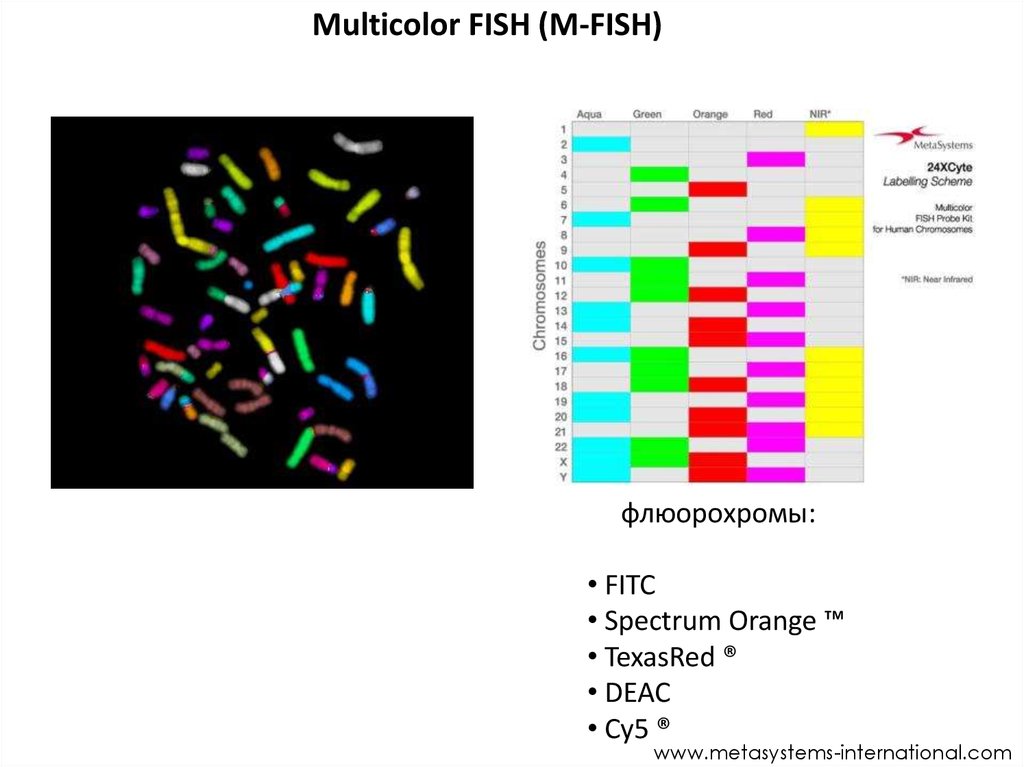
Мulticolor FISH (M-FISH)флюорохромы:
• FITC
• Spectrum Orange ™
• TexasRed ®
• DEAC
• Cy5 ®
www.metasystems-international.com
36.
• раздельная цифровая регистрация сигнала всех используемыхфлюорохромов при последовательной смене набора фильтров
• специальное ПО переводит информацию об уровне сигналов
флюорохромов в каждой точке изображения в псевдоцвета
• не позволяет выявлять внутрихромосомные аномалии и перестройки
между гомологичными хромосомами
37.
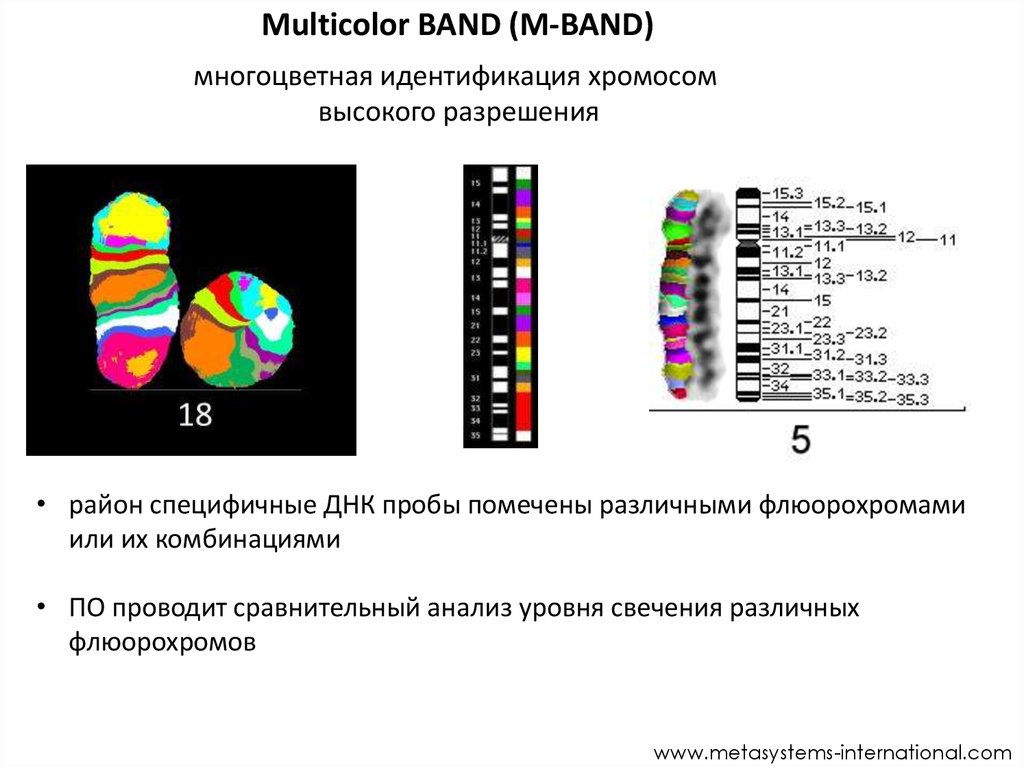
Multicolor BAND (M-BAND)многоцветная идентификация хромосом
высокого разрешения
• район специфичные ДНК пробы помечены различными флюорохромами
или их комбинациями
• ПО проводит сравнительный анализ уровня свечения различных
флюорохромов
www.metasystems-international.com
38.
An International System for Human Cytogenetic Nomenclature, 2013nuc ish: (D7Z1,D7S522)x2 [200]
nuc ish: (D7Z1x2,D7S522x1) [62/200]
nuc ish: (ABL,BCR)x2 [200]
nuc ish: (ABL,BCR)x3(ABL con BCRx2) [198/200]
nuc ish: (MYCx2)[200]
nuc ish: (MYCx2) (5’MYC sep 3’MYCx1)[180/200]
39.
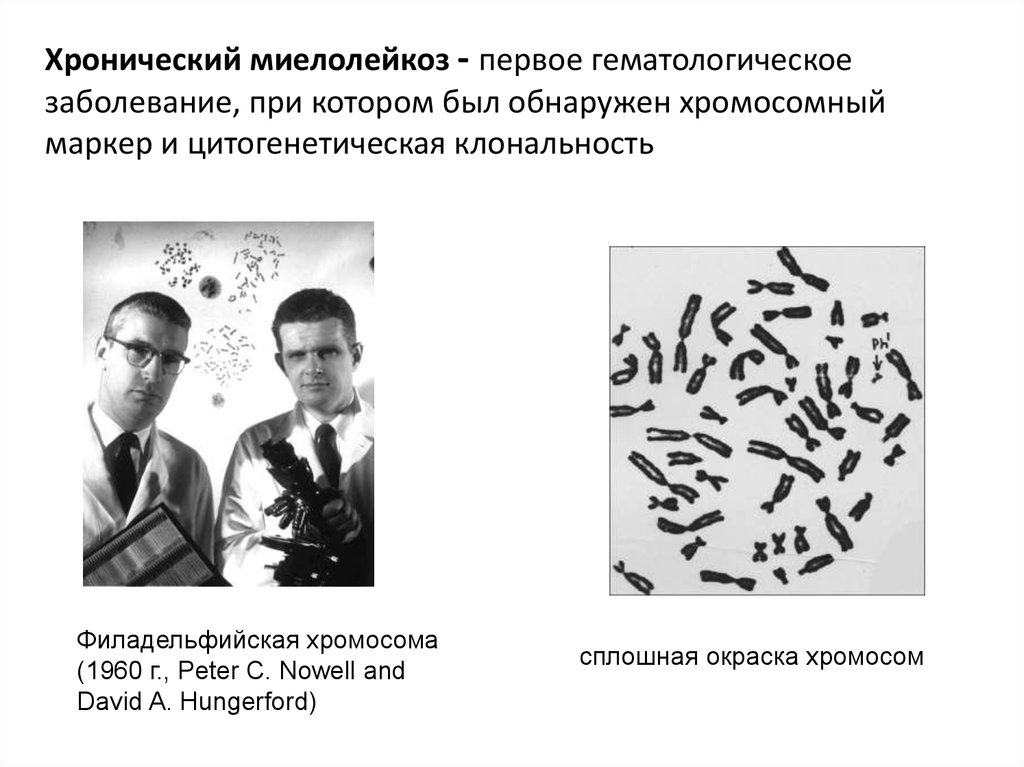
Хронический миелолейкоз - первое гематологическоезаболевание, при котором был обнаружен хромосомный
маркер и цитогенетическая клональность
Филадельфийская хромосома
(1960 г., Peter C. Nowell and
David A. Hungerford)
сплошная окраска хромосом
40.
Lore Zech______________________________
9
22
t(9;22)(q34;q11)
(1973 г., Janet Rowley)
41.
Миелодиспластический синдромХромосомные аберрации - ~50% случаев
наиболее характерные
менее характерные
другие
del(5q)
-7/del(7q)
+8
-Y
del(20)(q11q13)
i(17)(q10)
del(12p)
30%
10%
1q, inv(3)(q21q26), t(1;7)(q10;p10),
+6, +11,del(11q), +13, -21, +21
42.
WHO Classification of Tumoursof Haematopoietic and Lymphoid Tissues, 2008
43.
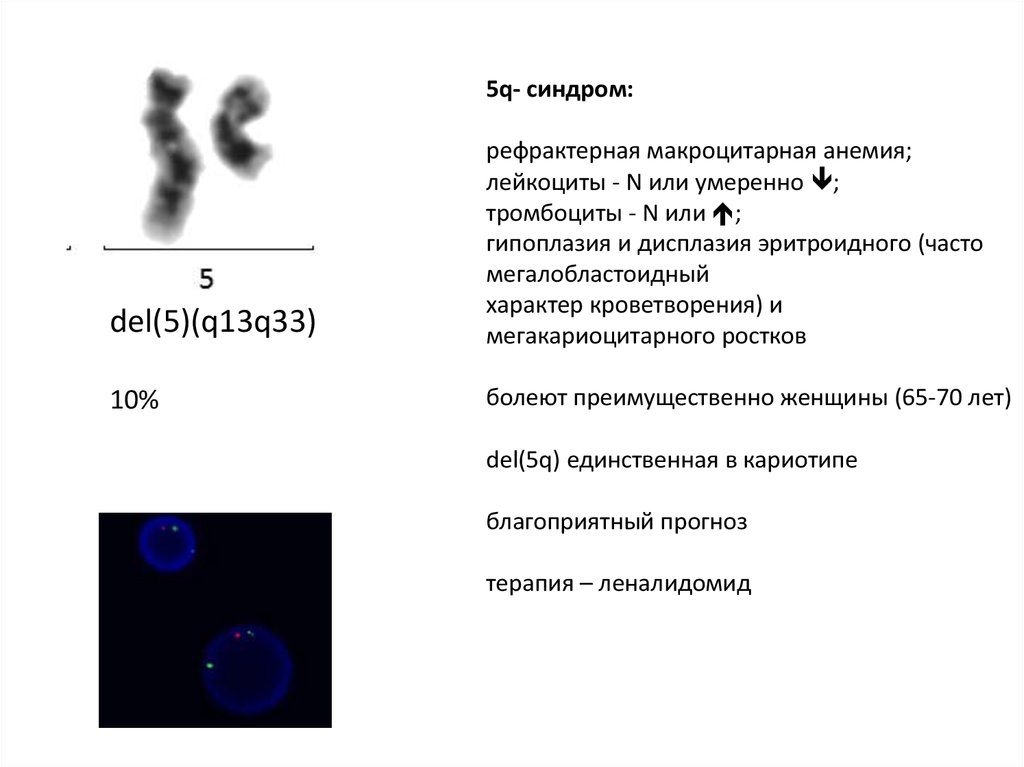
5q- синдром:del(5)(q13q33)
рефрактерная макроцитарная анемия;
лейкоциты - N или умеренно ;
тромбоциты - N или ;
гипоплазия и дисплазия эритроидного (часто
мегалобластоидный
характер кроветворения) и
мегакариоцитарного ростков
10%
болеют преимущественно женщины (65-70 лет)
del(5q) единственная в кариотипе
благоприятный прогноз
терапия – леналидомид
44.
чаще в составе комплексного кариотипахарактерна для вторичного МДС
риск трансформации в ОМЛ
7
del(7)(q22)
10%
45.
2%EVI1/3q26
3
inv(3)(q21q26)
или t(3;3)(q21;q26)
N или уровень Тр
гиперклеточный к/м
выраженная трехростковая дисплазия,
особенно мегакариоциоцитарного
ростка
высокий риск трансформации в ОМЛ
46.
потеря хромосомы Y5%
трисомия 8
может быть возрастная
10%
20
del(20)(q11)
5-8%
единственное нарушение в кариотипе –
дисплазия эритроидного и
мегакариоцитарного ростков
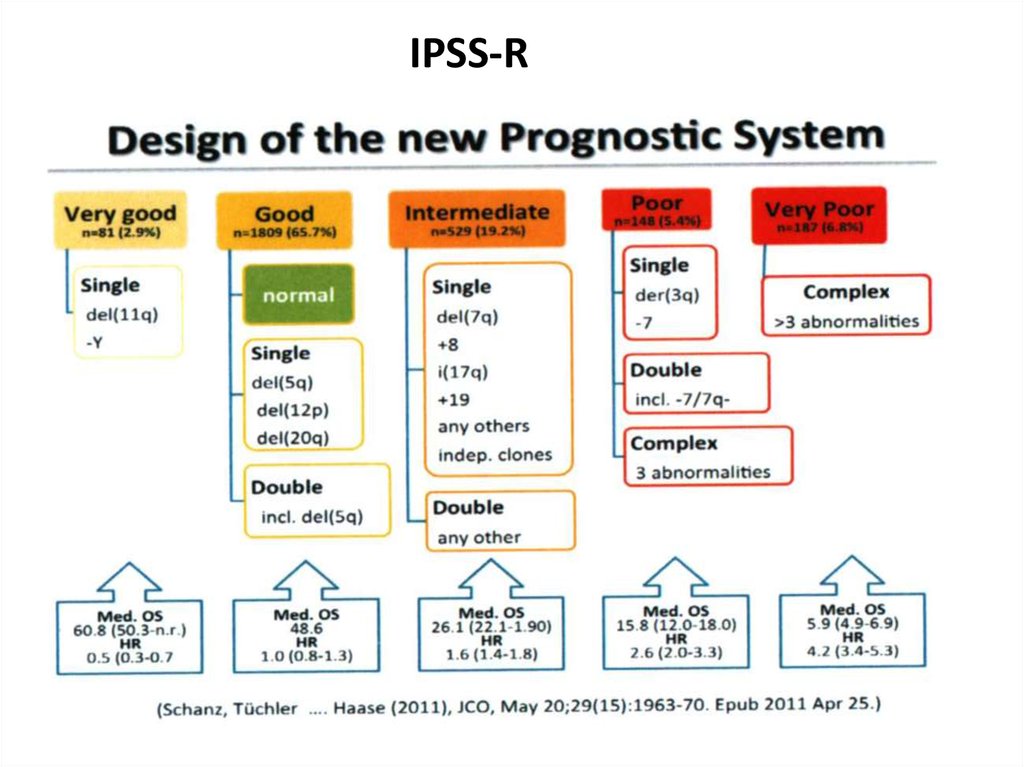
47. Прогностические группы (IPSS prognostic index, 1997; WHO, 2008)
Хорошийнормальный кариотип,
-Y, del(5q), del(20q)
Средний
все другие
Плохой
комплексные перестройки (≥3),
-7/del(7q)
48.
IPSS-R49.
Острые миелоидные лейкозыХромосомные нарушения –
80-90% случаев ОМЛ
WHO Classification of Tumours
of Haematopoietic and Lymphoid Tissues, 2008
50.
t(15;17)(q22;q21)Острый промиелоцитарный лейкоз
t(15;17)(q22;q21)
5-8% ОМЛ
химерный ген PML-RARα
прицельная терапия – (АТРА) + ХТ
51.
вариантные:t(11;17)(q23;q21) - ZBTB16;
t(11;17)(q13;q21) - NUMA1;
t(5;17)(q32;q21) - NPM1;
t(17;17)(q11;q21) - STATSB
52.
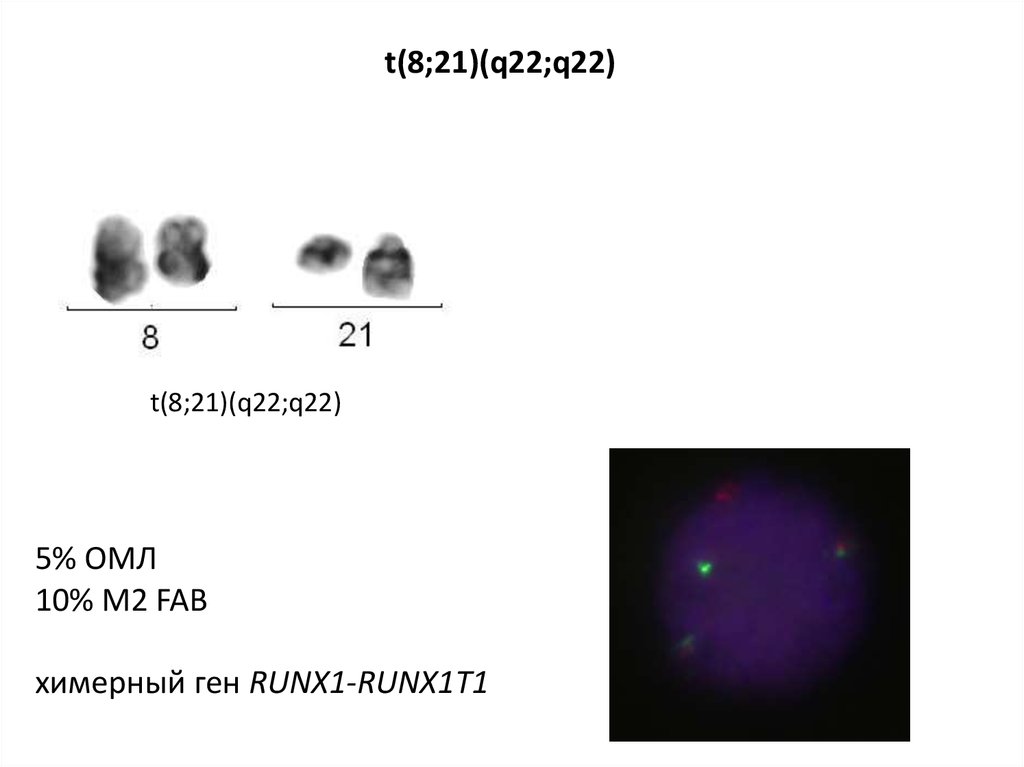
t(8;21)(q22;q22)t(8;21)(q22;q22)
5% ОМЛ
10% M2 FAB
химерный ген RUNX1-RUNX1T1
53.
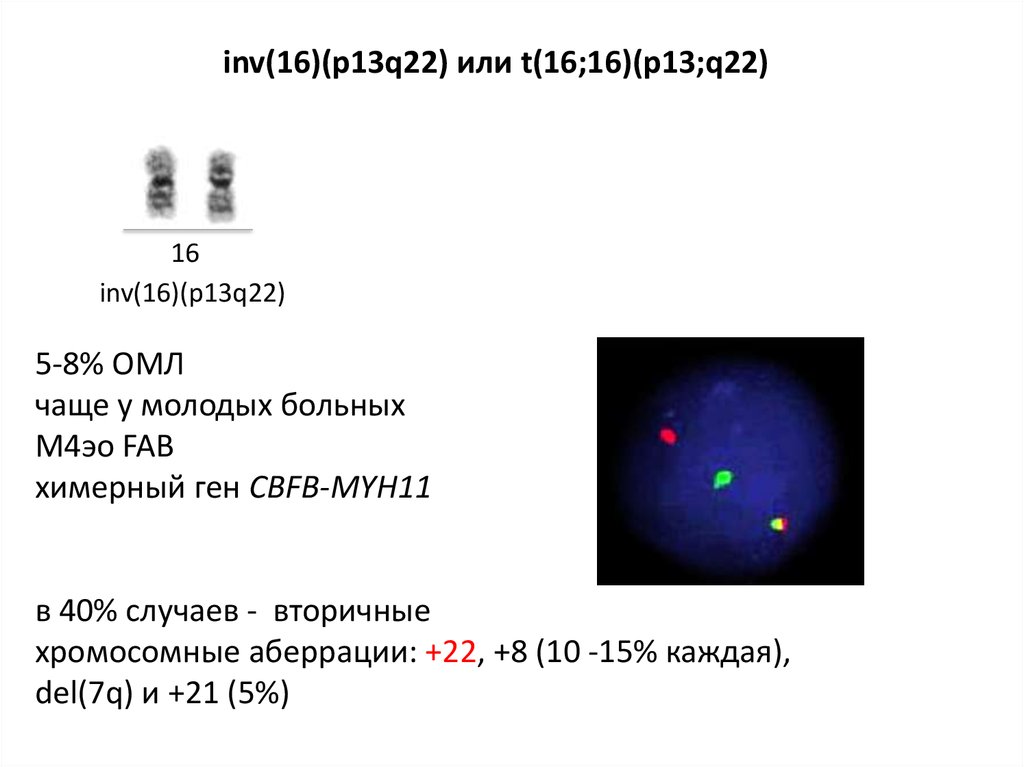
inv(16)(p13q22) или t(16;16)(p13;q22)16
inv(16)(p13q22)
5-8% ОМЛ
чаще у молодых больных
M4эо FAB
химерный ген CBFB-MYH11
в 40% случаев - вторичные
хромосомные аберрации: +22, +8 (10 -15% каждая),
del(7q) и +21 (5%)
54.
t(15;17)(q22;q21)t(8;21)(q22;q22)
inv(16)(p13q22) или t(16;16)(p13;q22)
Высокоспецифичны для ОМЛ
Диагноз ОМЛ вне зависимости от количества БК
55.
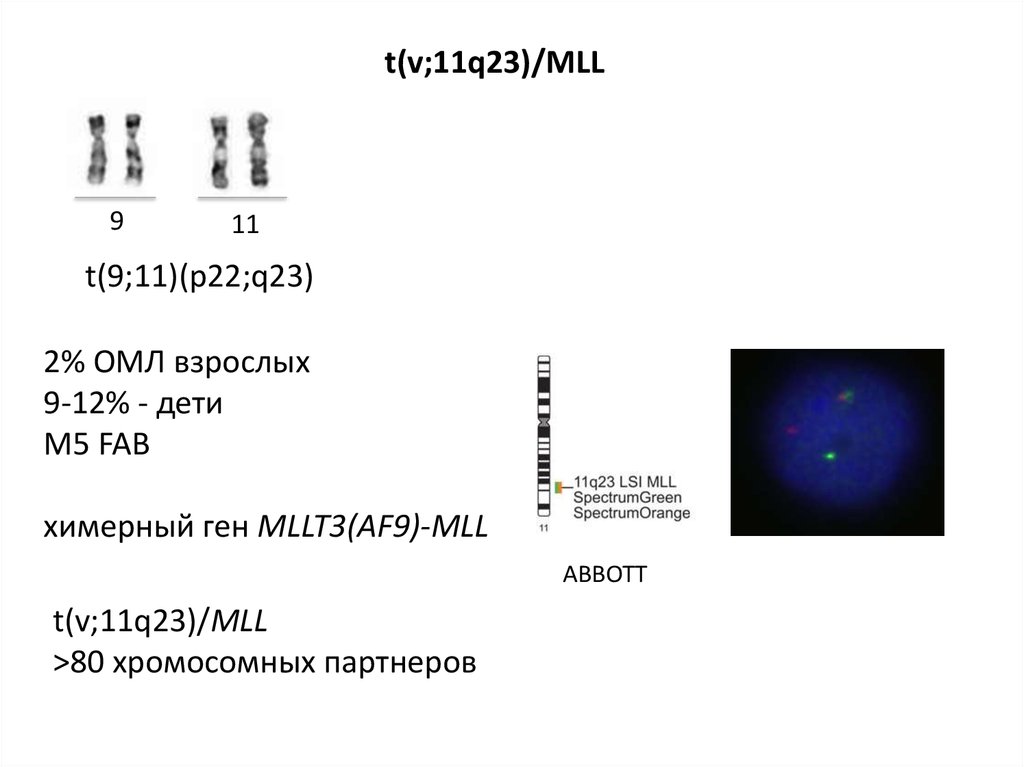
t(v;11q23)/MLL9
11
t(9;11)(p22;q23)
2% ОМЛ взрослых
9-12% - дети
M5 FAB
химерный ген MLLT3(AF9)-MLL
ABBOTT
t(v;11q23)/MLL
>80 хромосомных партнеров
56.
вариантные транслокации:t(4;11)(q21;q23) - MLLT2(AF4)
t(11;19)(q23;p13.3) - MLLT1(ENL)
t(10;11)(p12q23) - MLLT1O (AF1O)
t(6;11)(q27;q23) - MLLT4 (AF6)
t(11;19)(q23;p13.1) - ELL
57.
t(6;9)(p23;q34)6
9
t(6;9)(p23;q34)
химерный ген DEK-NUP214
1-2% ОМЛ взрослых и детей
базофилия в к/м и п/к – 50% случаев
трехростковая дисплазия
58.
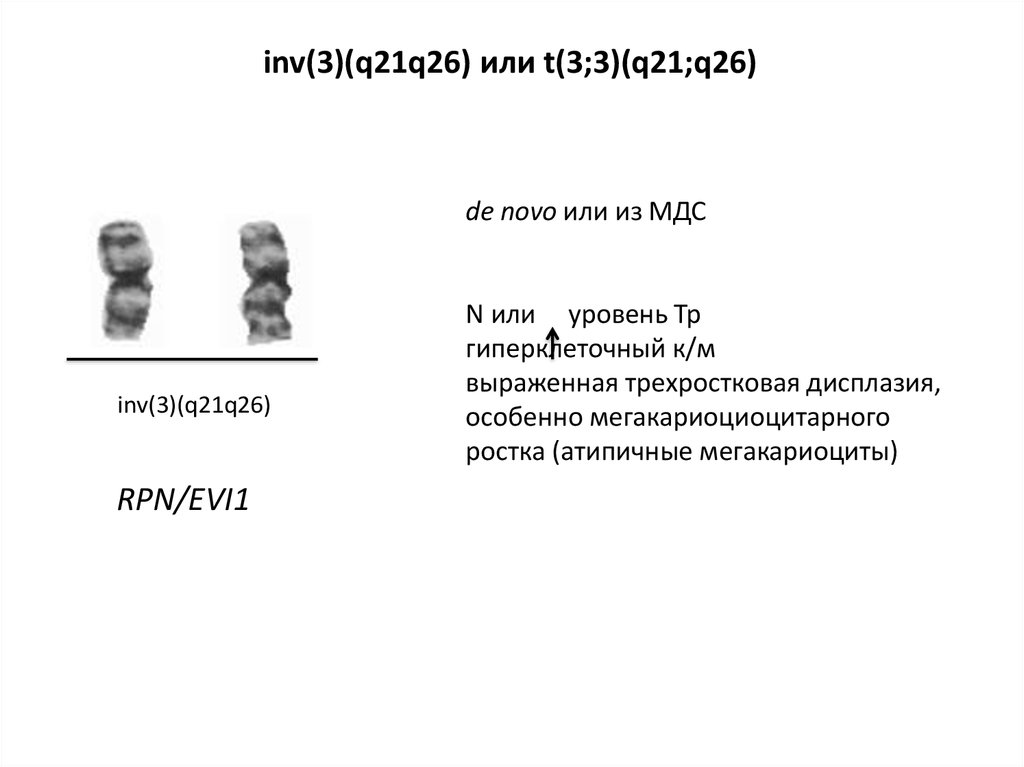
inv(3)(q21q26) или t(3;3)(q21;q26)de novo или из МДС
inv(3)(q21q26)
RPN/EVI1
N или уровень Тр
гиперклеточный к/м
выраженная трехростковая дисплазия,
особенно мегакариоциоцитарного
ростка (атипичные мегакариоциты)
59.
t(1;22)(p13;q13)RBM15-MKL1
de novo
мегакариобластный лейкоз (М7)
дети до 3х лет
органомегалия
60.
другиеdel5q/-5
del7q/-7
+8
del9p21
del11q23
del13q
del17p
-Y
t(9;22)(q34;q11)
61.
Цитогенетические группы прогноза ОМЛБлагоприятный
нормальный кариотип
t(15;17)(q21;q22
t(8;21)(q22;q22)
inv(16)(p13q22)
Средний
t(9;11)(p22;q23)
все другие
Неблагоприятный
t(6;9)(p23;q34)
inv(3)(q21q26)
t(3;3)(q21;q26)
t(v;11q23)
-5, del5q, -7
комплексный кариотип
62.
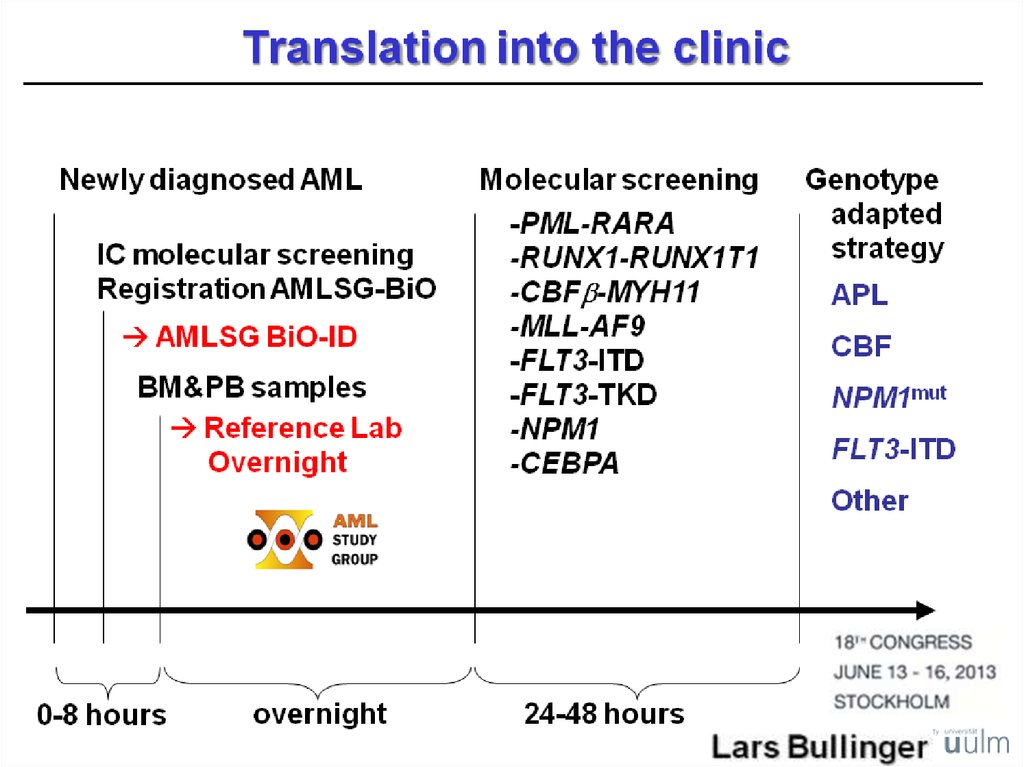
Молекулярно-генетические маркеры прогноза ОМЛFLT3/13q12.2
внутренние тандемные дупликации (ITD)
точечные мутации в тирозинкиназном домене (TKD) ?
NPM1/5q35
de novo М4 или М5 ОМЛ
у пожилых больных с нормальным кариотипом
СЕВРА/ 19q13.1
de novo М1 или М2 ОМЛ, редко М4 или М5
ОМЛ
ОМЛ с
нормальным
кариотипом
Прогноз
FLT3 -ITD
15-25%
25-35%
неблагоприятнй
NPM1
25-35%
45-60%
благоприятный
СЕВРА
5-15%
10-20%
благоприятный
63.
Метод фрагментного анализа(Лаборатория молекулярной гематологии,
зав. лаб. д.б.н. Судариков А.Б.)
Метод основан на разделении меченных флюоресцентным
красителем ПЦР-продуктов в капиллярах, заполненных гелем.
ПЦР с праймерами, меченными флюоресцентной меткой.
При капиллярном электрофорезе денатурированные
ПЦР-продукты разделяются по длине с точностью до одного
нуклеотида, вне зависимости от нуклеотидного состава.
Для исследования используется автоматический анализатор
нуклеиновых кислот.
64.
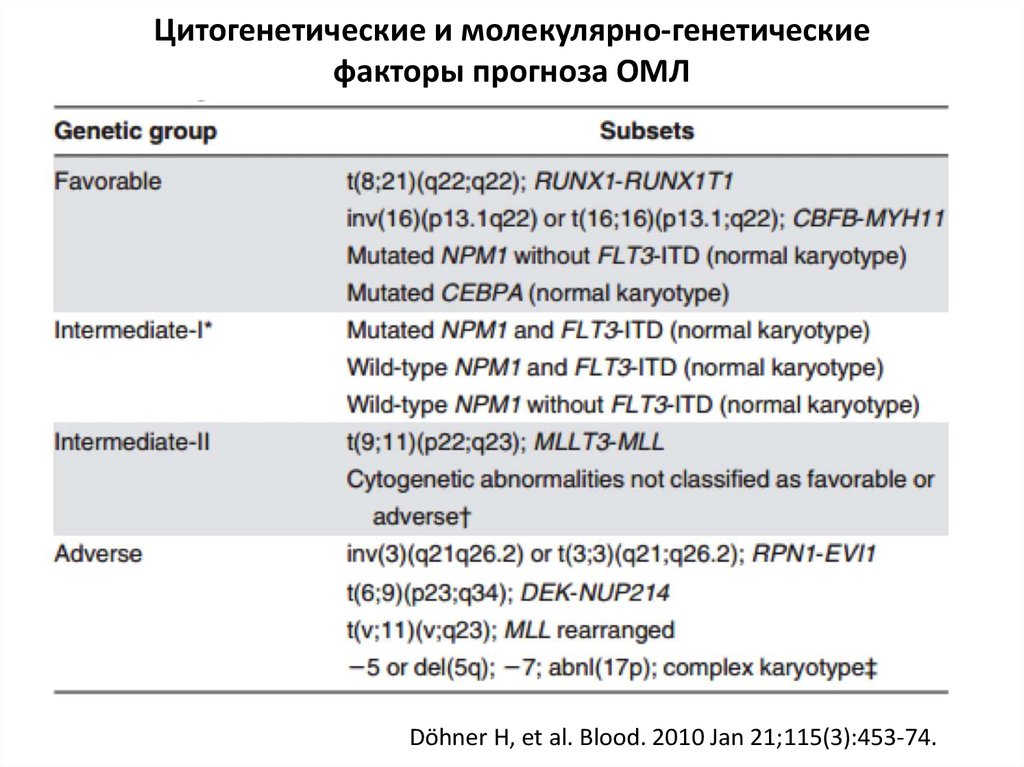
Цитогенетические и молекулярно-генетическиефакторы прогноза ОМЛ
Döhner H, et al. Blood. 2010 Jan 21;115(3):453-74.
65.
66.
Острые В-лимфобластные лейкозыWHO Classification of Tumours
of Haematopoietic and Lymphoid Tissues, 2008
67.
t(9;22)(q34;q11)взрослые – 25%
дети – 3-5%
химерный ген BCR/ABL
Стандартное цитогенетическое исследование + дополнительные
перестройки
68.
t(v;11q23)/MLL5-15%
самая частая t(4;11)(q21;q23)
химерный ген AF4-MLL
>80 хромосомных партнеров
для 35 – гены-партнеры не охарактеризованы
на молекулярном уровне
69.
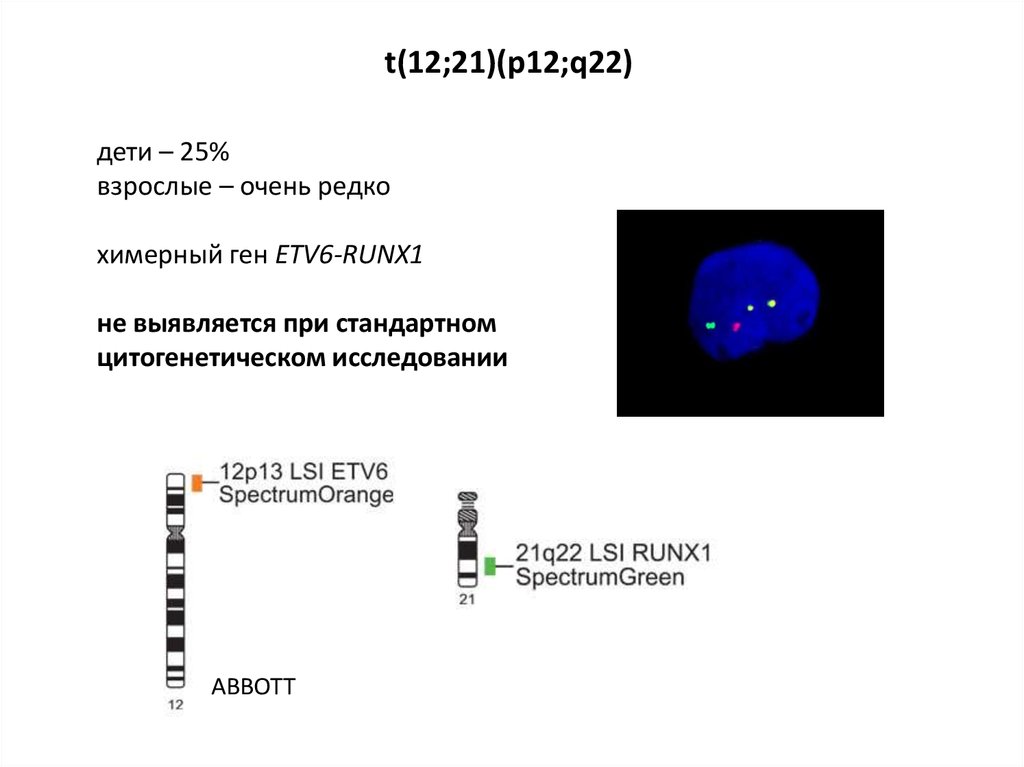
t(12;21)(р12;q22)дети – 25%
взрослые – очень редко
химерный ген ETV6-RUNX1
не выявляется при стандартном
цитогенетическом исследовании
ABBOTT
70.
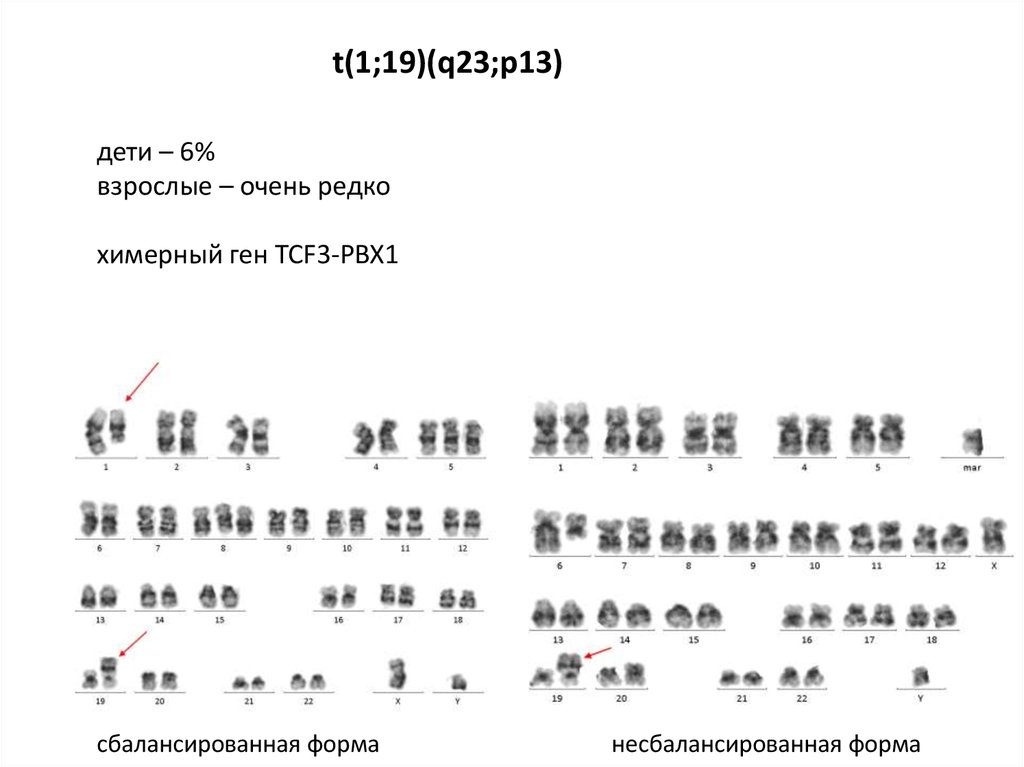
t(1;19)(q23;p13)дети – 6%
взрослые – очень редко
химерный ген TCF3-PBX1
сбалансированная форма
несбалансированная форма
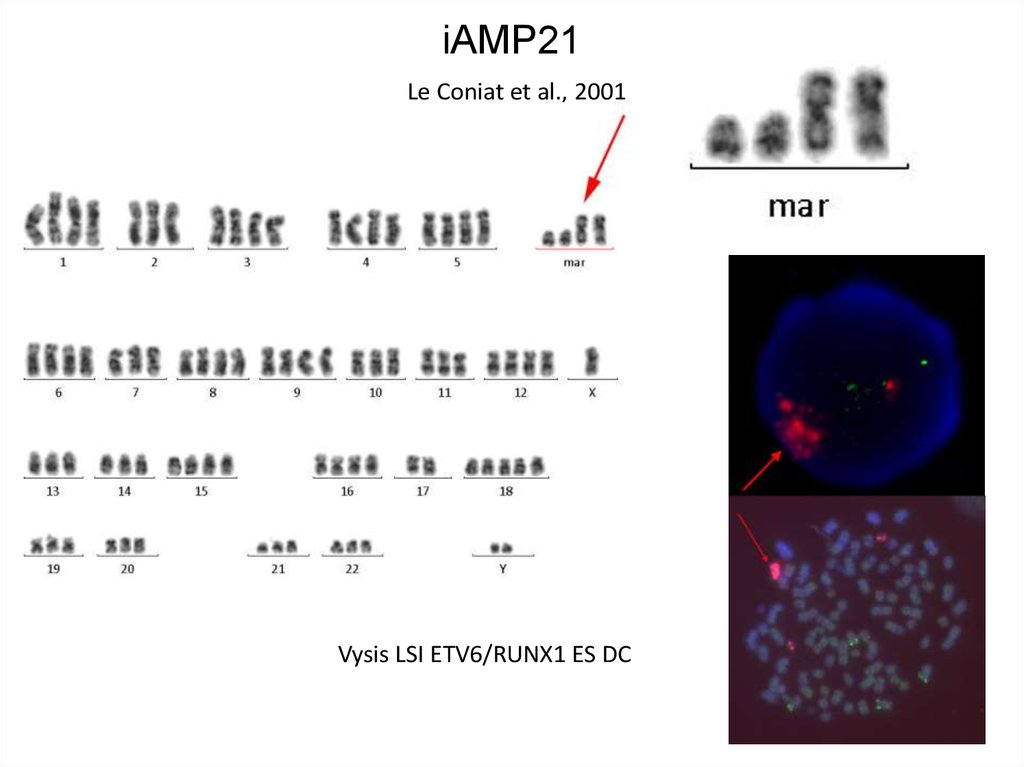
71. iAMP21 Le Coniat et al., 2001
Vysis LSI ETV6/RUNX1 ES DC72.
Количественные изменения кариотипаГипердиплоидия
50-67 хромосом (большая гипердиплоидия)
дети - 20-30%
взрослые – редко
Гиподиплоидия
<45 хромосом – 5%
73.
ПрогнозБлагоприятный
t(12;21)(p13;q22)
большая гипердиплоидия
Средний
t(1;19)(q23;p13)
все другие
Неблагоприятный
t(9;22)(q34;q11)
t(v;11q23)
гиподиплоидия
Обязательно выполнение FISH для выявления
t(9;22)(q34;q11)
t(11q23)/MLL
74.
Острые Т-лимфобластные лейкозыХромосомные нарушения – 50-70% случаев
транслокации TCR a/d - 14q11, TCR β – 7q35 и TCR γ - 7p14- 15
с многочисленными хромосомными партнерами:
HOX 11( TLX1) - 10q24 - 30% случаев
HOX11L2 (TLX3) - 5q35 - 10-15%
С-MYC – 8q24
TAL1 - 1p32
RBTN1 - 11p15
RBTN2 - 11p13
LYL1 - 19p1 3
и др.
75.
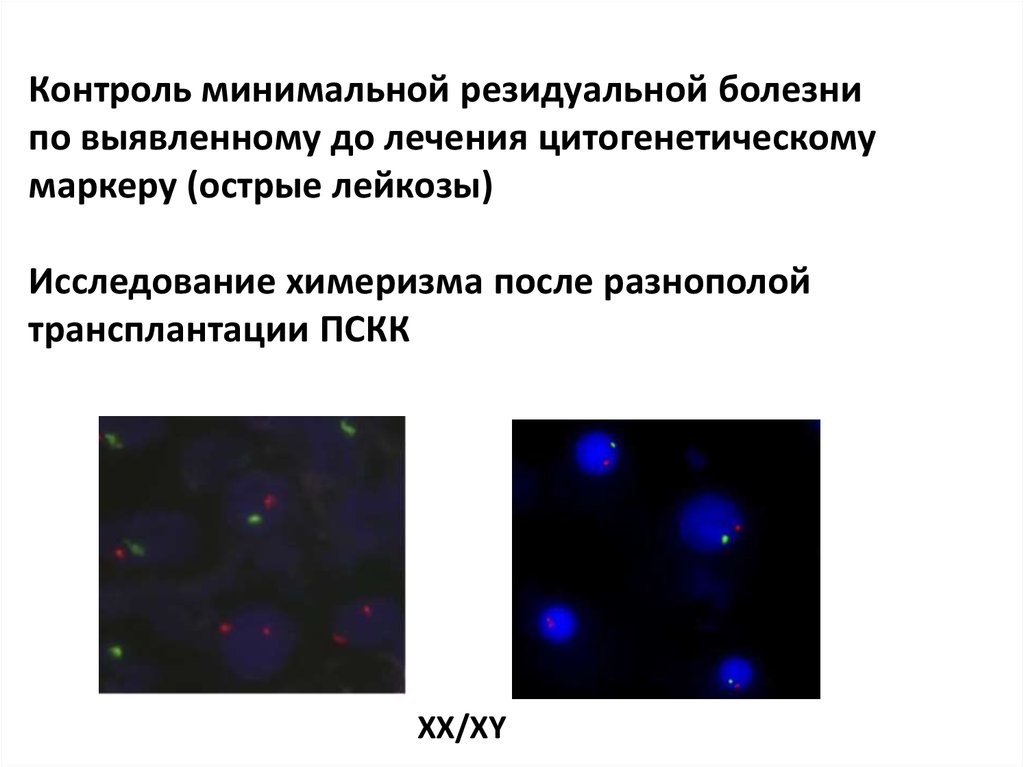
Контроль минимальной резидуальной болезнипо выявленному до лечения цитогенетическому
маркеру (острые лейкозы)
Исследование химеризма после разнополой
трансплантации ПСКК
XX/XY
76.
42-44,XY,del(2)(p21), -5,-7,del(12)(p12),-12,-13,-15,-16,-17,-19,+6-7mar [cp30]
42-44,XY, t(5;15;17;22),del 13,del 15, t(7;13), t(16;17;19;21)
77.
46,XY,add(20)(p?12) [7]/46,XY[13]46,XY,der(11)t(X;11)(?pq;q)t(11;20p;?pq),der(11)t(11;20)(p;?)ins(17;11)














































 Медицина
Медицина








