Похожие презентации:
Дисахариди. Амінокислоти. Пептиди
1.
Лекція 13Дисахариди. Амінокислоти. Пептиди.
2.
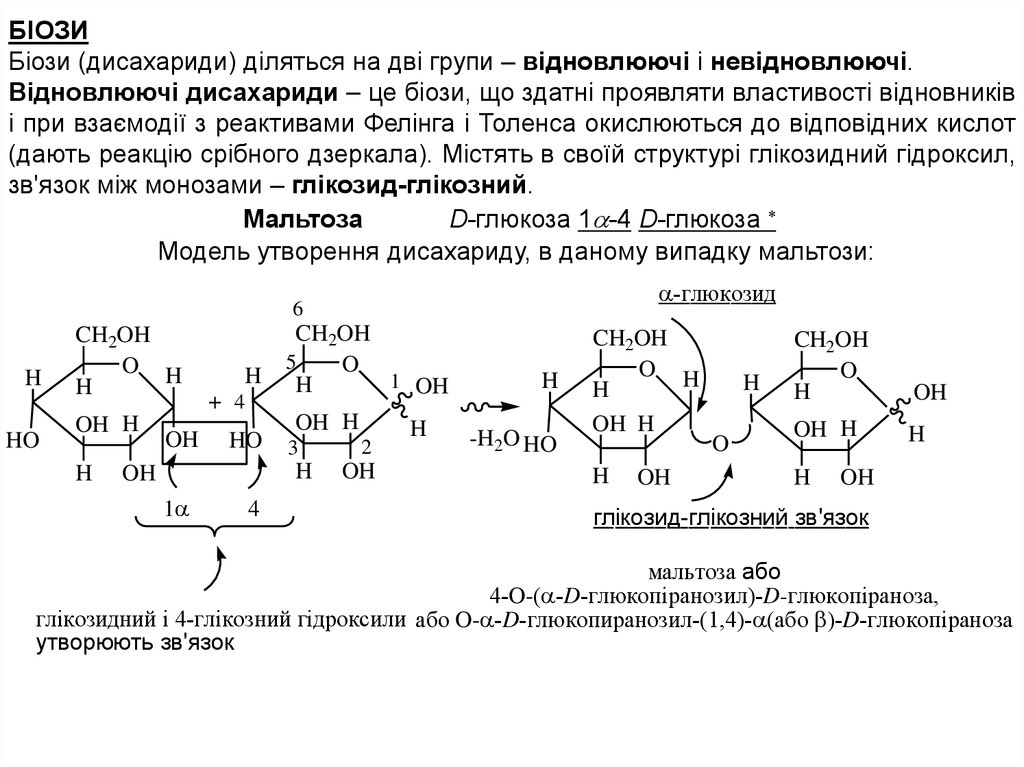
БІОЗИБіози (дисахариди) діляться на дві групи – відновлюючі і невідновлюючі.
Відновлюючі дисахариди – це біози, що здатні проявляти властивості відновників
і при взаємодії з реактивами Фелінга і Толенса окислюються до відповідних кислот
(дають реакцію срібного дзеркала). Містять в своїй структурі глікозидний гідроксил,
зв'язок між монозами – глікозид-глікозний.
Мальтоза
D-глюкоза 1 -4 D-глюкоза
Модель утворення дисахариду, в даному випадку мальтози:
-глюкозид
6
H
HO
CH2OH
O H
H
OH H
H
OH
H
+ 4
HO
CH2OH
5
O
1 OH
H
OH H
3
H
OH
1
4
2
OH
H
H
-H2O HO
CH2OH
O H
H
OH H
H
OH
H
O
CH2OH
O
H
OH
OH H
H
H
OH
глiкозид-глiкозний зв'язок
мальтоза або
4-O-( -D-глюкопіранозил)-D-глюкопіраноза,
глiкозидний i 4-глiкозний гiдроксили або O- -D-глюкопиранозил-(1,4)- або -D-глюкопіраноза
утворюють зв'язок
3.
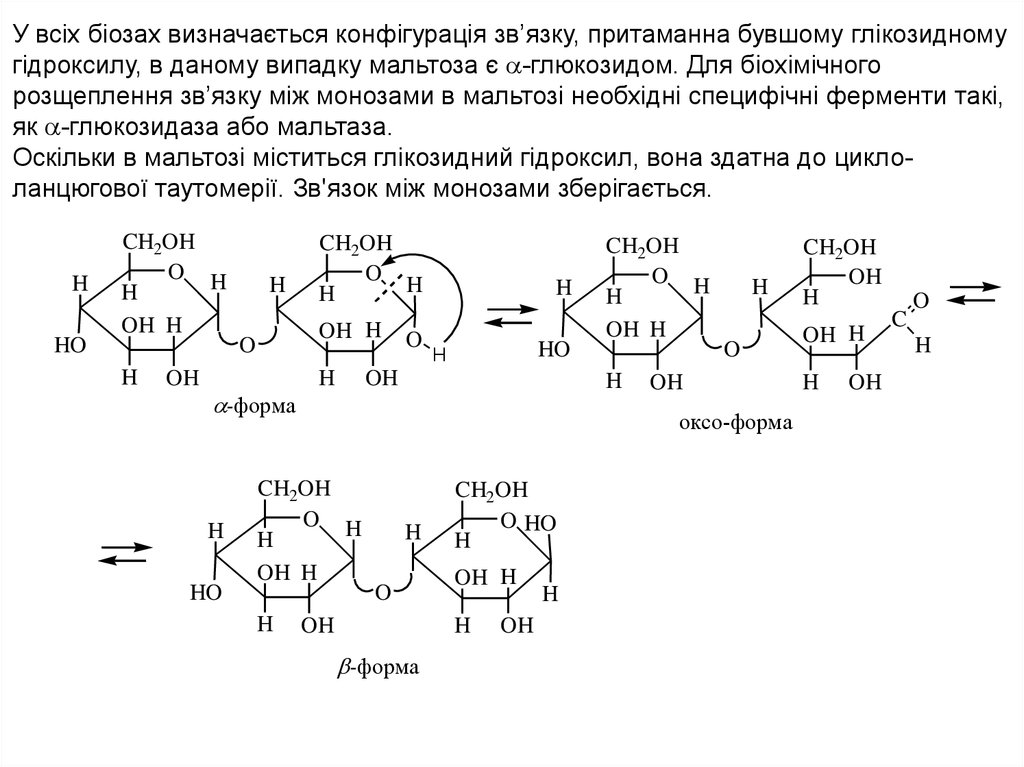
У всіх біозах визначається конфігурація зв’язку, притаманна бувшому глікозидномугідроксилу, в даному випадку мальтоза є -глюкозидом. Для біохімічного
розщеплення зв’язку між монозами в мальтозі необхідні специфічні ферменти такі,
як -глюкозидаза або мальтаза.
Оскільки в мальтозі міститься глікозидний гідроксил, вона здатна до циклоланцюгової таутомерії. Зв'язок між монозами зберігається.
H
HO
CH2OH
O H
H
OH H
H
OH
H
OH H
O
-форма
H
HO
CH2OH
O
H
H
H
HO
H
OH
H
H
O
OH
оксо-форма
CH2OH
O H
H
OH H
H
O
H
CH2OH
O H
H
OH H
H
O
OH
CH2OH
O HO
H
OH H
H
-форма
OH
H
CH2OH
OH
H
OH H
H
OH
C
O
H
4.
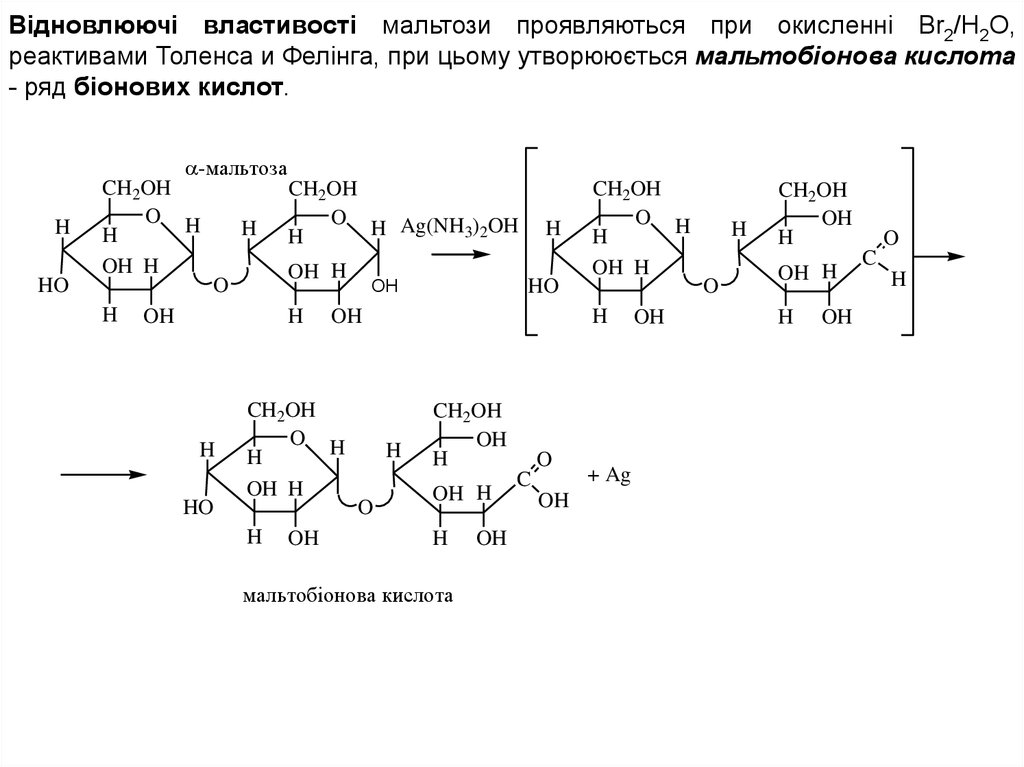
Відновлюючі властивості мальтози проявляються при окисленні Br2/H2O,реактивами Толенса и Фелінга, при цьому утворююється мальтобіонова кислота
- ряд біонових кислот.
-мальтоза
H
HO
CH2OH
O H
H
OH H
H
H
CH2OH
O
H Ag(NH3)2OH
H
OH H
O
OH
H
H
HO
OH
HO
OH
OH
CH2OH
O H
H
OH H
H
H
H
H
O
CH2OH
O H
H
OH H
CH2OH
OH
H
OH H
H
мальтобiонова кислота
OH
O
C
OH
+ Ag
OH
H
O
CH2OH
OH
H
OH H
H
OH
O
C
H
5.
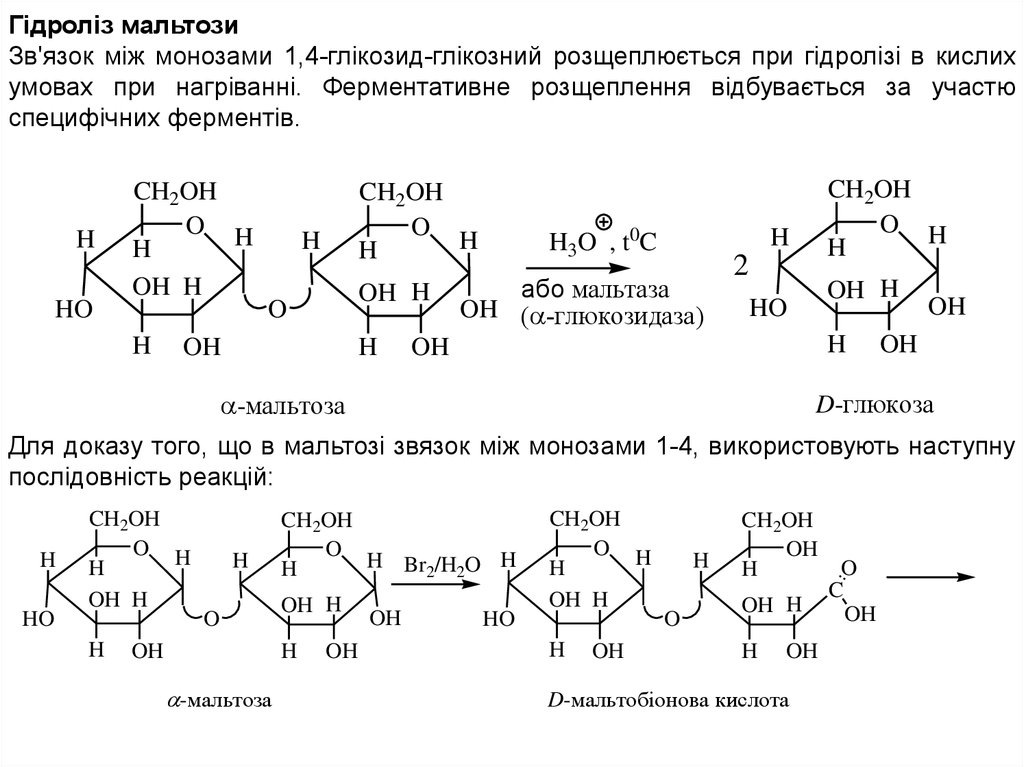
Гідроліз мальтозиЗв'язок між монозами 1,4-глікозид-глікозний розщеплюється при гідролізі в кислих
умовах при нагріванні. Ферментативне розщеплення відбувається за участю
специфічних ферментів.
H
HO
CH2OH
O H
H
OH H
H
CH2OH
O
H
H
H
OH H
O
OH
H
H3O , t0C
CH2OH
O H
H
H
або мальтаза
OH ( -глюкозидаза)
2
OH H
HO
H
OH
-мальтоза
OH
OH
D-глюкоза
Для доказу того, що в мальтозі звязок між монозами 1-4, використовують наступну
послідовність реакцій:
H
HO
CH2OH
O H
H
OH H
H
H
O
OH
CH2OH
O
H Br2/H2O H
H
OH H
H
-мальтоза
OH
OH
HO
CH2OH
O H
H
OH H
H
OH
H
O
CH2OH
OH
H
OH H
H
OH
D-мальтобiонова кислота
O
C
OH
6.
надл.(CH3O)2SO2H
CH2OCH3
O H
H
CH2OCH3
OCH3
O
H
OCH3 H C
OCH3
H
OCH3 H
NaOH
CH3O
O
H
OCH3
H
H3O , t0C
- CH3OH
OCH3
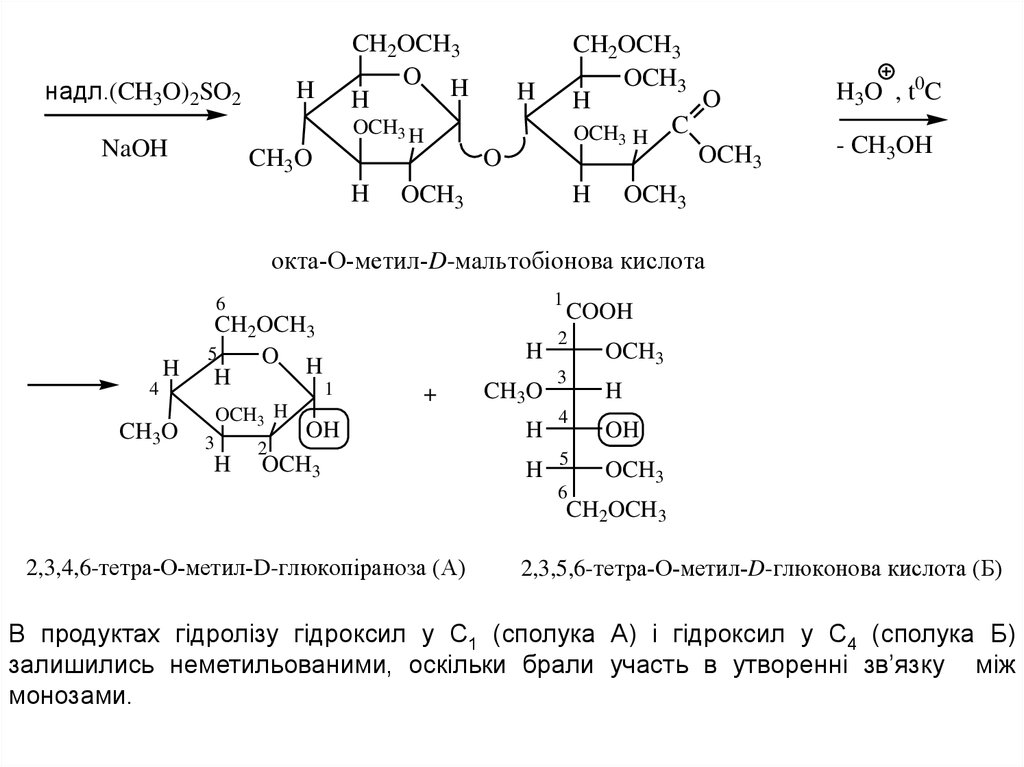
окта-О-метил-D-мальтобiонова кислота
1
6
H
4
CH3O
CH2OCH3
5
O H
H
1
OCH3 H
3
H
H
+
OH
2
OCH3
CH3O
H
H
COOH
2
3
4
5
6
OCH3
H
OH
OCH3
CH2OCH3
2,3,4,6-тетра-О-метил-D-глюкопiраноза (А)
2,3,5,6-тетра-О-метил-D-глюконова кислота (Б)
В продуктах гідролізу гідроксил у С1 (сполука А) і гідроксил у С4 (сполука Б)
залишились неметильованими, оскільки брали участь в утворенні зв’язку між
монозами.
7.
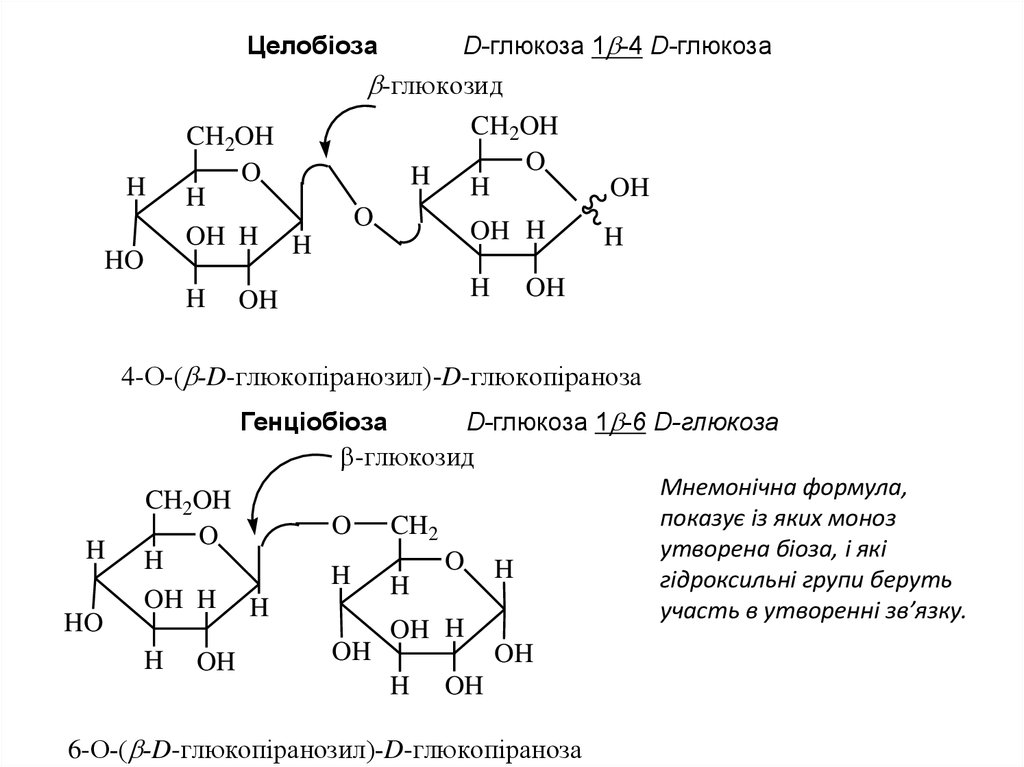
D-глюкоза 1 -4 D-глюкозаЦелобіоза
-глюкозид
H
HO
CH2OH
O
H
OH H H
H
H
O
CH2OH
O
H
OH
OH H
H
H
OH
OH
4-О-( -D-глюкопiранозил)-D-глюкопiраноза
D-глюкоза 1 -6 D-глюкоза
Генціобіоза
-глюкозид
H
HO
CH2OH
O
H
OH H H
H
OH
O
H
OH
CH2
O
H
OH H
H
H
OH
OH
6-О-( -D-глюкопiранозил)-D-глюкопiраноза
Мнемонічна формула,
показує із яких моноз
утворена біоза, і які
гідроксильні групи беруть
участь в утворенні зв’язку.
8.
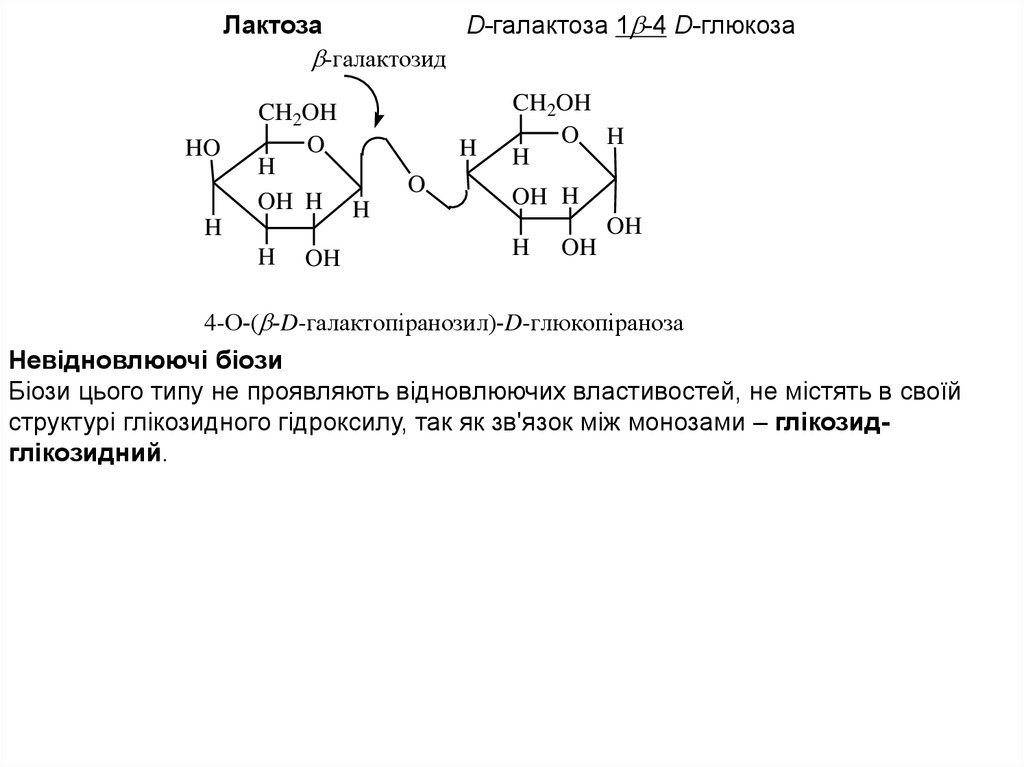
ЛактозаD-галактоза 1 -4 D-глюкоза
-галактозид
HO
H
CH2OH
O
H
OH H H
H
OH
H
O
CH2OH
O H
H
OH H
H
OH
OH
4-О-( -D-галактопiранозил)-D-глюкопiраноза
Невідновлюючі біози
Біози цього типу не проявляють відновлюючих властивостей, не містять в своїй
структурі глікозидного гідроксилу, так як зв'язок між монозами – глікозидглікозидний.
9.
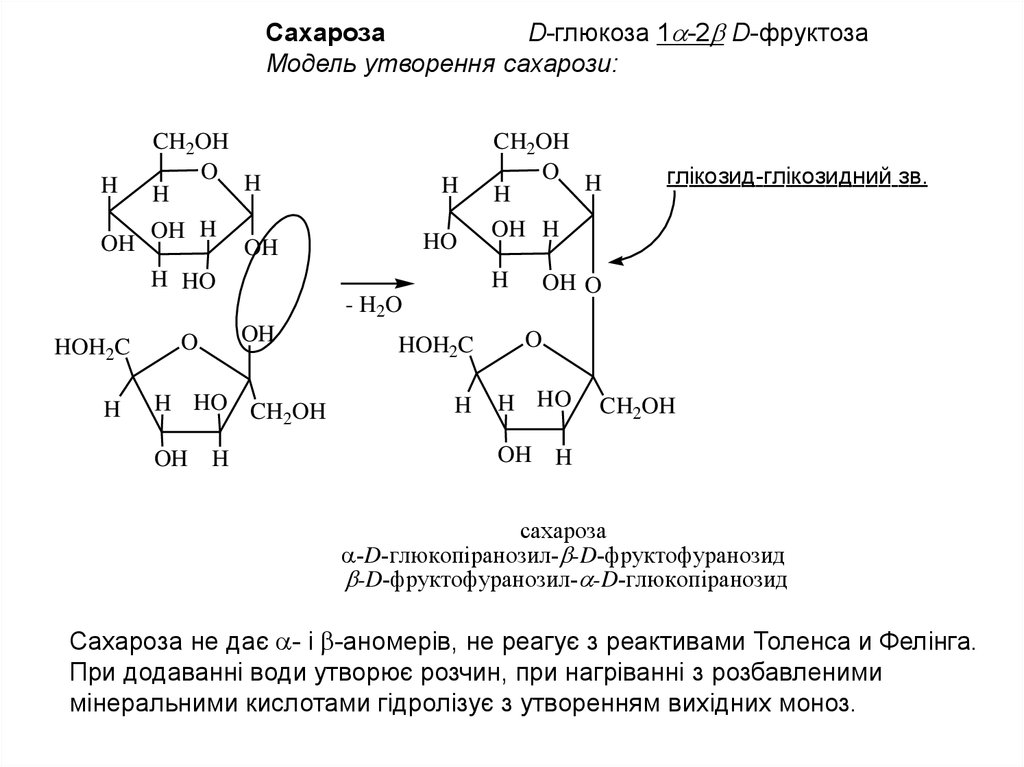
СахарозаD-глюкоза 1 -2 D-фруктоза
Модель утворення сахарози:
CH2OH
O H
H H
OH H
OH
OH
H HO
H
HO
CH2OH
O H
H
OH H
H
OH O
- H2O
HOH2C
H
OH
O
H HO CH OH
2
OH
H
HOH2C
H
глiкозид-глiкозидний зв.
O
H HO
OH
CH2OH
H
сахароза
-D-глюкопiранозил- -D-фруктофуранозид
-D-фруктофуранозил- -D-глюкопiранозид
Сахароза не дає - і -аномерів, не реагує з реактивами Толенса и Фелінга.
При додаванні води утворює розчин, при нагріванні з розбавленими
мінеральними кислотами гідролізує з утворенням вихідних моноз.
10.
Інверсія сахарозиПри кислому гідролизі (+) сахарози або при дії інвертази утворюються рівні
кількості D(+)глюкози і D(-)фруктози. При гідролизі сахарози відбувається зміна
знаку кута обертання [ ] з позитивного на негативний, тому процес називають
інверсією, суміш D(+)глюкози і D(-)фруктози називають інвертним цукром.
цукор
H3O
[ ]20D +66,50
D-глюкоза +
D-фруктоза
( и )
( и )
[ ]20D +52,30
[ ]20D -930
сумарне обертання - 40,70
11.
Амінокислота – це азотовмісна карбонова кислота, тобто — це хімічнаречовина, молекула якої одночасно містить аміногрупу –NH2 (в деяких
випадках – іміногрупу =NH) та карбоксильну групу –СООН, і вуглецевий
скелет. За тим, до якого атому вуглецю приєднана аміно- (або іміно-) група,
амінокислоти поділяються на α, β, γ і т. д При цьому α-амінокислотами
називаються такі, в яких карбоксильна та аміногрупа приєднані до одного і
того ж атому вуглецю; β-амінокислотами – такі, де аміногрупа приєднана до
атому вуглецю, сусіднього з тим, до якого приєднана карбоксильна; γамінокислотами – такі, де аміногрупа приєднана через один атом вуглецю від
карбоксильної, і так далі.
АМІНОКИСЛОТИ
Амінокислотами називають похідні карбонових
кислот, у вуглеводневому радикалі яких один або декілька
атомів водню заміщені на аміногрупу.
12.
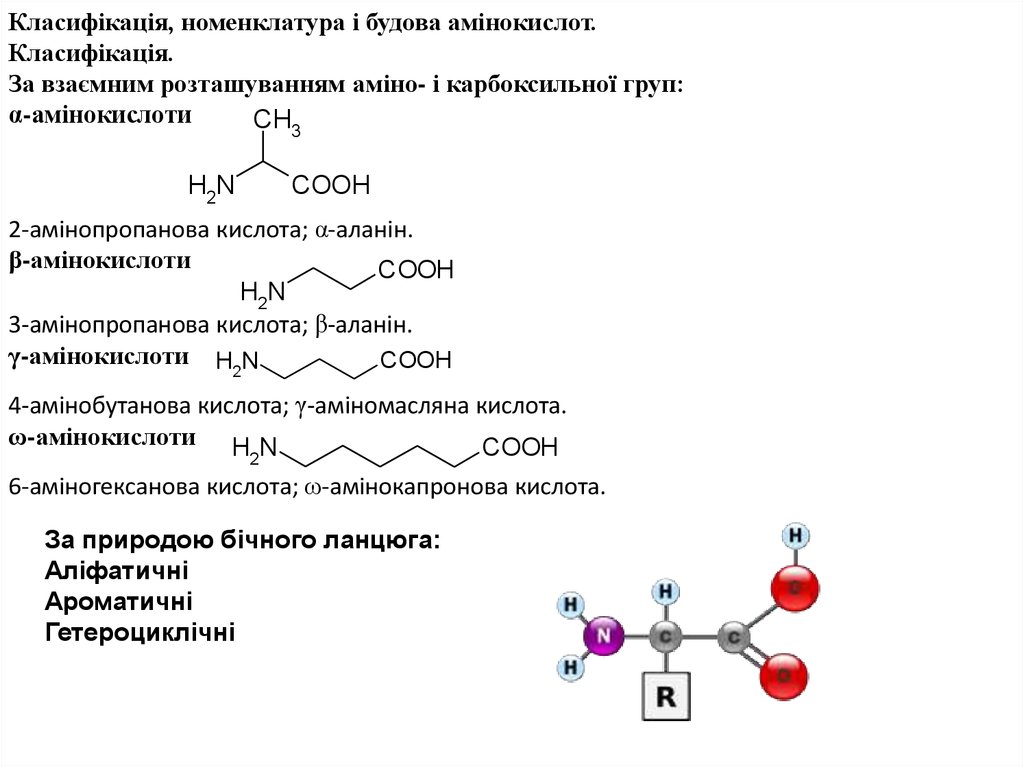
Класифікація, номенклатура і будова амінокислот.Класифікація.
За взаємним розташуванням аміно- і карбоксильної груп:
α-амінокислоти
CH3
COOH
H2N
2-амінопропанова кислота; α-аланін.
β-амінокислоти
COOH
H2N
3-амінопропанова кислота; β-аланін.
γ-амінокислоти H2N
COOH
4-амінобутанова кислота; γ-аміномасляна кислота.
ω-амінокислоти H N
COOH
2
6-аміногексанова кислота; ω-амінокапронова кислота.
За природою бічного ланцюга:
Аліфатичні
Ароматичні
Гетероциклічні
13.
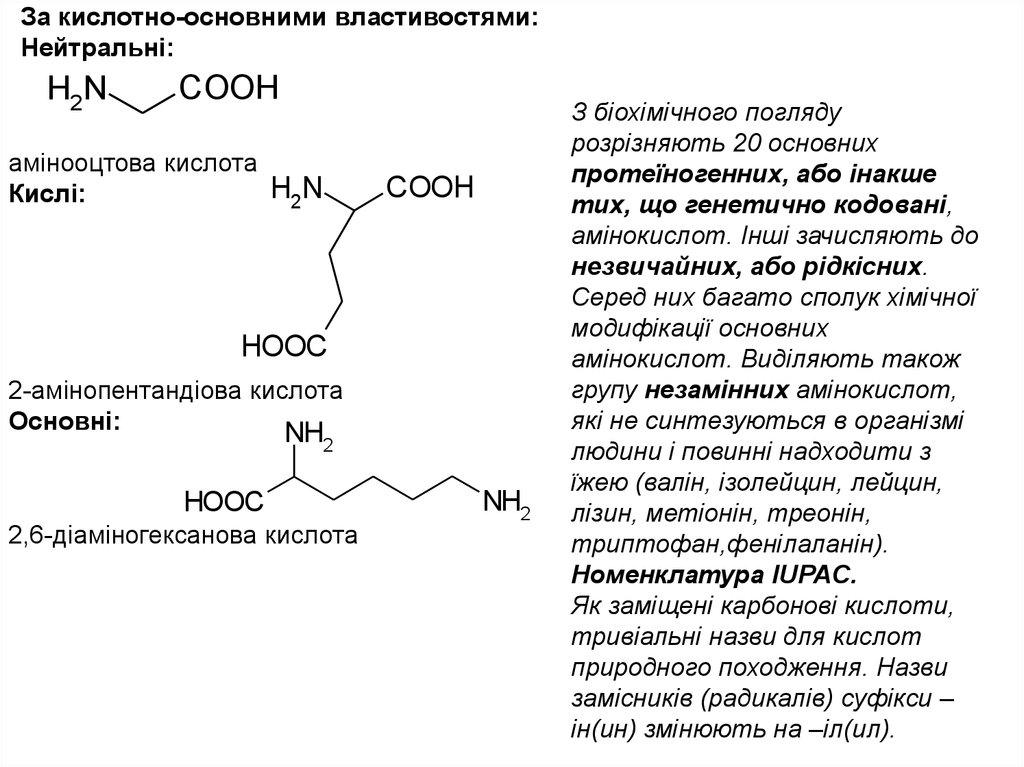
За кислотно-основними властивостями:Нейтральні:
H2N
COOH
амінооцтова кислота
H2N
Кислі:
COOH
HOOC
2-амінопентандіова кислота
Основні:
NH
2
HOOC
2,6-діаміногексанова кислота
NH2
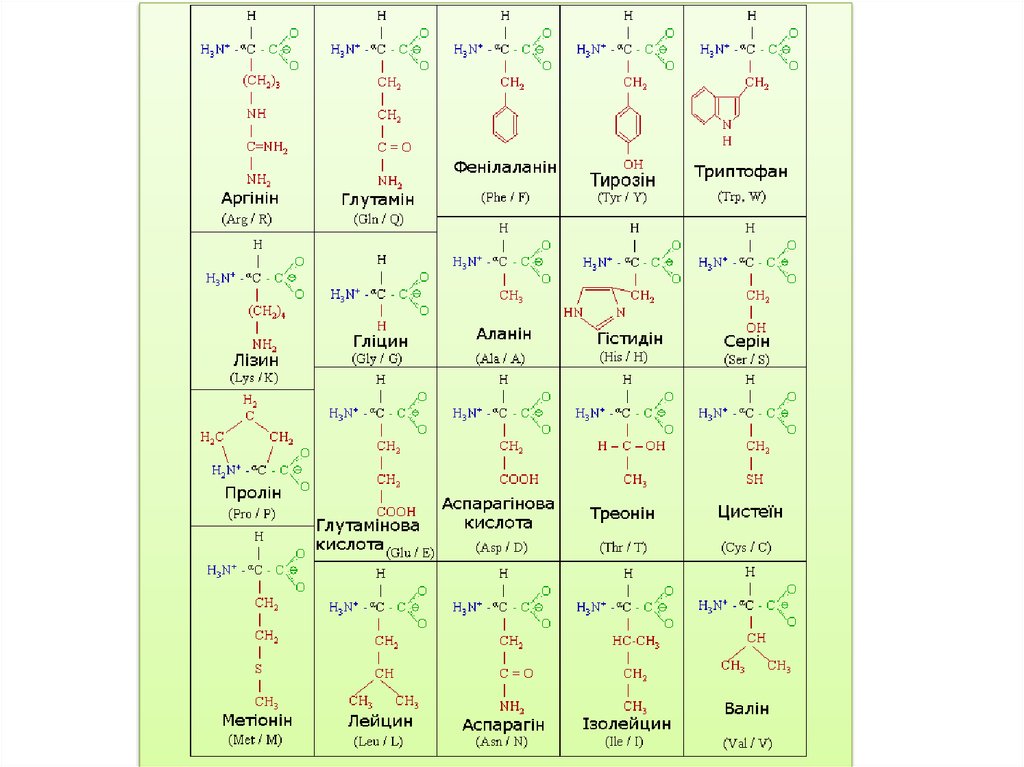
З біохімічного погляду
розрізняють 20 основних
протеїногенних, або інакше
тих, що генетично кодовані,
амінокислот. Інші зачисляють до
незвичайних, або рідкісних.
Серед них багато сполук хімічної
модифікації основних
амінокислот. Виділяють також
групу незамінних амінокислот,
які не синтезуються в організмі
людини і повинні надходити з
їжею (валін, ізолейцин, лейцин,
лізин, метіонін, треонін,
триптофан,фенілаланін).
Номенклатура IUPAC.
Як заміщені карбонові кислоти,
тривіальні назви для кислот
природного походження. Назви
замісників (радикалів) суфікси –
ін(ин) змінюють на –іл(ил).
14.
15.
У залежності від природи вуглеводневого радикала, з яким зв'язанакарбоксильна група, амінокислоти підрозділяють на аліфатичні й
ароматичні. Аліфатичні амінокислоти за взаємним розміщенням
аміногрупи та карбоксильної групи поділяють на -, -, -амінокислоти
і т. д. Найбільш розповсюдженими в природі є -амінокислоти, які
входять до складу білків.
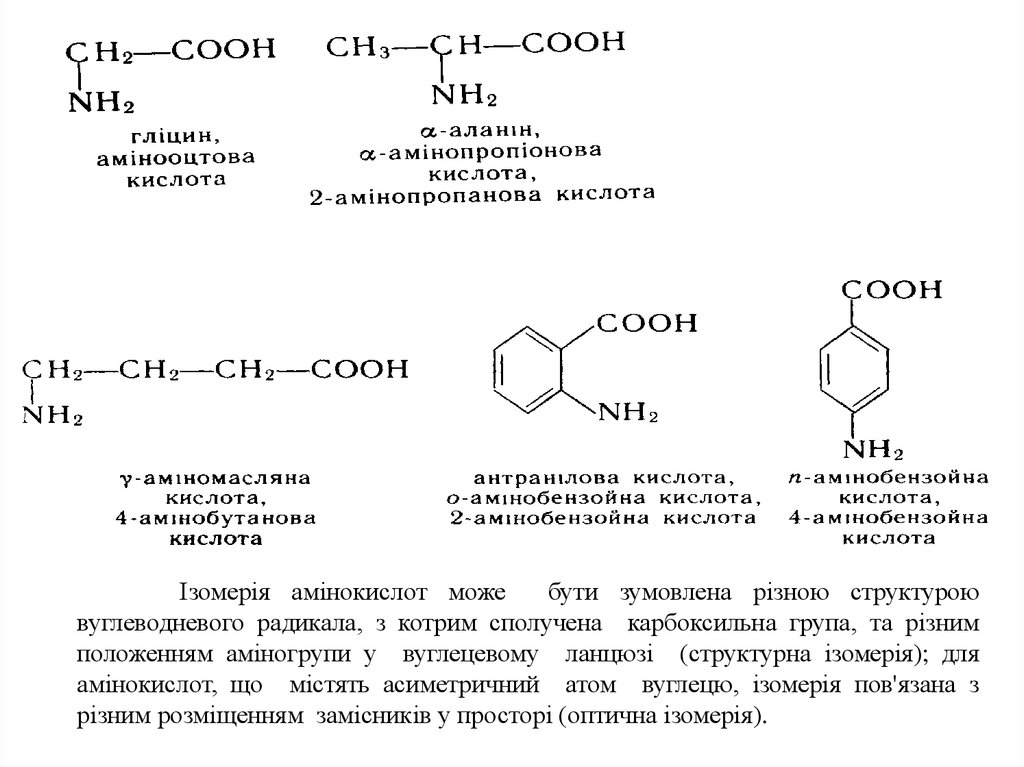
Номенклатура та ізомерія
За замісниковою номенклатурою IUPAC назви амінокислот
утворюють з тривіальних або систематичних назв відповідних
карбонових кислот та префікса аміно-. У випадку тривіальних
карбонових кислот для позначення положення аміногрупи
застосовують букви грецького алфавіту -, -, - і т.д., при
використанні систематичних назв кислот положення аміногрупи
позначають цифровими локантами. Для амінокислот, які входять до
складу білків, найчастіше застосовують тривіальні назви. Ароматичні
амінокислоти бензольного ряду розглядають як похідні бензойної
кислоти:
16.
Ізомерія амінокислот можебути зумовлена різною структурою
вуглеводневого радикала, з котрим сполучена карбоксильна група, та різним
положенням аміногрупи у вуглецевому ланцюзі (структурна ізомерія); для
амінокислот, що містять асиметричний атом вуглецю, ізомерія пов'язана з
різним розміщенням замісників у просторі (оптична ізомерія).
17.
Фізичні та хімічні властивостіАмінокислоти являють собою білі кристалічні речовини з високими
температурами плавлення, добре розчинні у воді. Внаслідок наявності в
структурі кислотного центру (група —СООН) та основного центру
(група —NH2) амінокислоти кристалізуються з нейтральних водних
розчинів у вигляді внутрішніх солей, що дістали назву біполярні іони, або
цвіттер-іони:
У
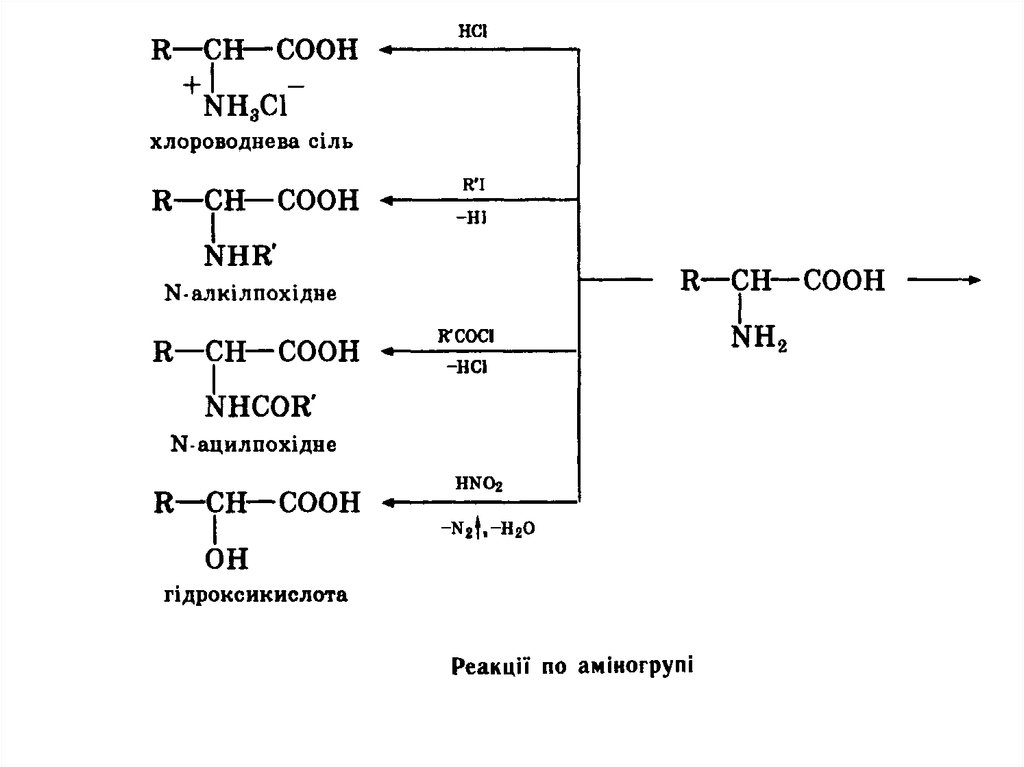
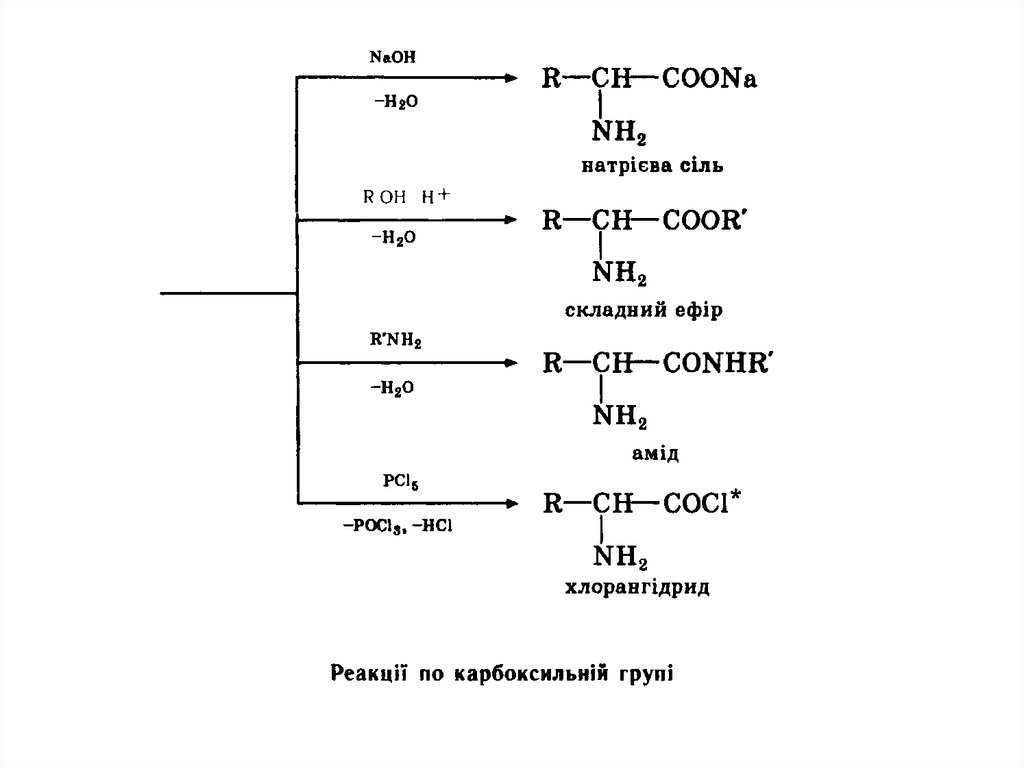
хімічному відношенні амінокислоти виявляють властивості
первинних амінів та карбонових кислот. По карбоксильній групі вони
утворюють функціональні похідні карбонових кислот — солі, складні
ефіри, аміди, галогенангідриди.
За участю аміногрупи амінокислоти утворюють солі з мінеральними
кислотами, вступають в реакції алкілування, ацилування, реагують з
азотистою кислотою, а також дають інші реакції, властиві первинним
амінам. Оскільки амінокислоти утворюють солі як з мінеральними
кислотами, так і з основами, вони є амфотерним речовинами.
18.
19.
20.
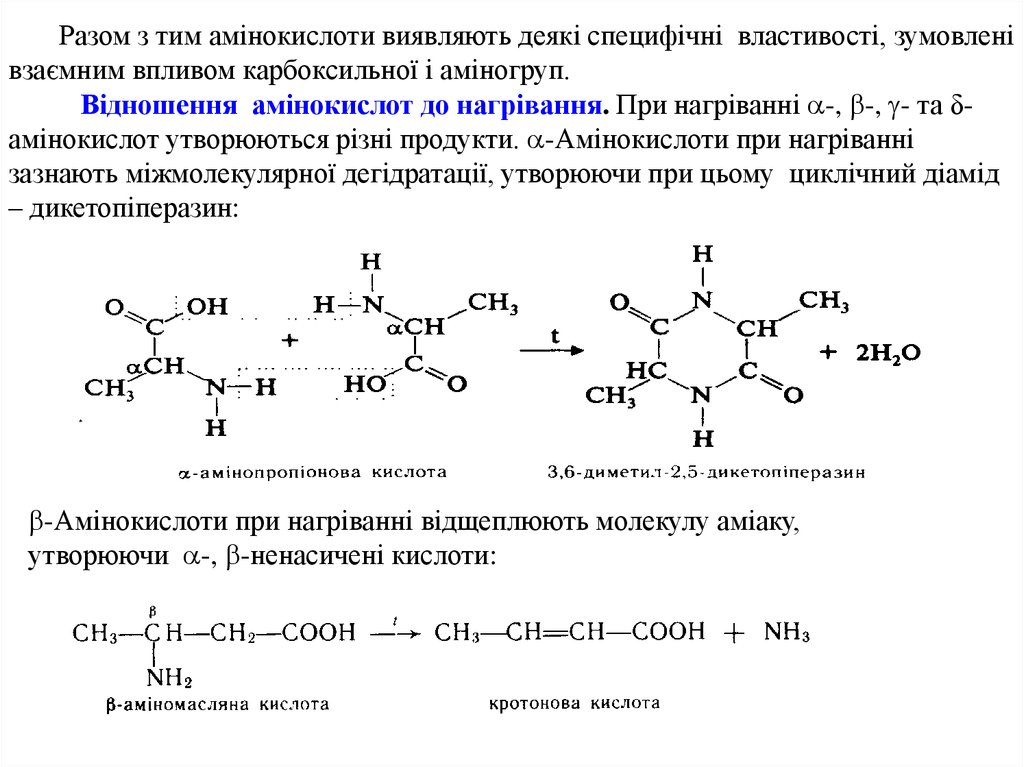
Разом з тим амінокислоти виявляють деякі специфічні властивості, зумовленівзаємним впливом карбоксильної і аміногруп.
Відношення амінокислот до нагрівання. При нагріванні -, -, - та δамінокислот утворюються різні продукти. -Амінокислоти при нагріванні
зазнають міжмолекулярної дегідратації, утворюючи при цьому циклічний діамід
– дикетопіперазин:
-Амінокислоти при нагріванні відщеплюють молекулу аміаку,
утворюючи -, -ненасичені кислоти:
21.
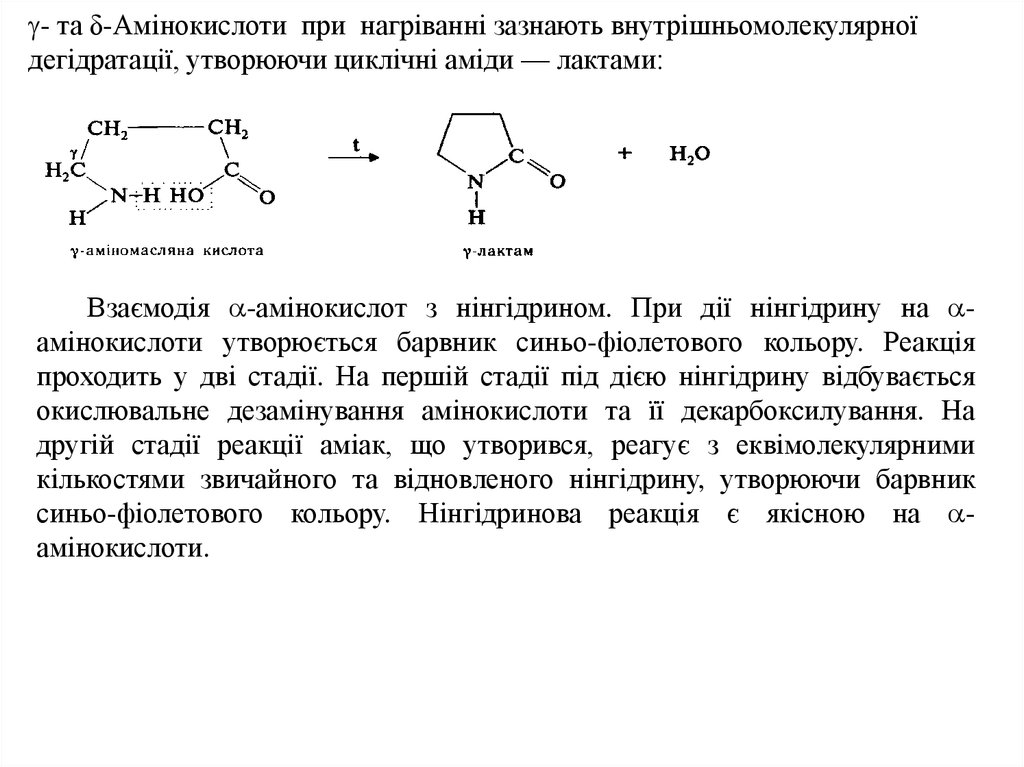
- та δ-Амінокислоти при нагріванні зазнають внутрішньомолекулярноїдегідратації, утворюючи циклічні аміди — лактами:
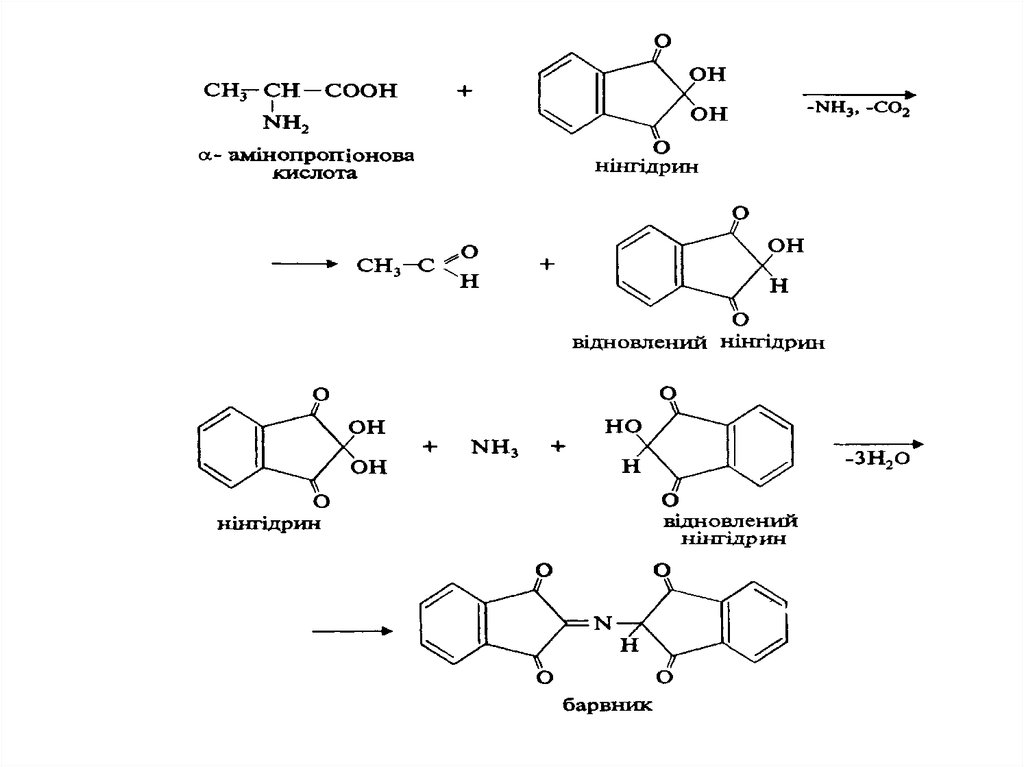
Взаємодія -амінокислот з нінгідрином. При дії нінгідрину на амінокислоти утворюється барвник синьо-фіолетового кольору. Реакція
проходить у дві стадії. На першій стадії під дією нінгідрину відбувається
окислювальне дезамінування амінокислоти та її декарбоксилування. На
другій стадії реакції аміак, що утворився, реагує з еквімолекулярними
кількостями звичайного та відновленого нінгідрину, утворюючи барвник
синьо-фіолетового кольору. Нінгідринова реакція є якісною на амінокислоти.





 Химия
Химия








