Похожие презентации:
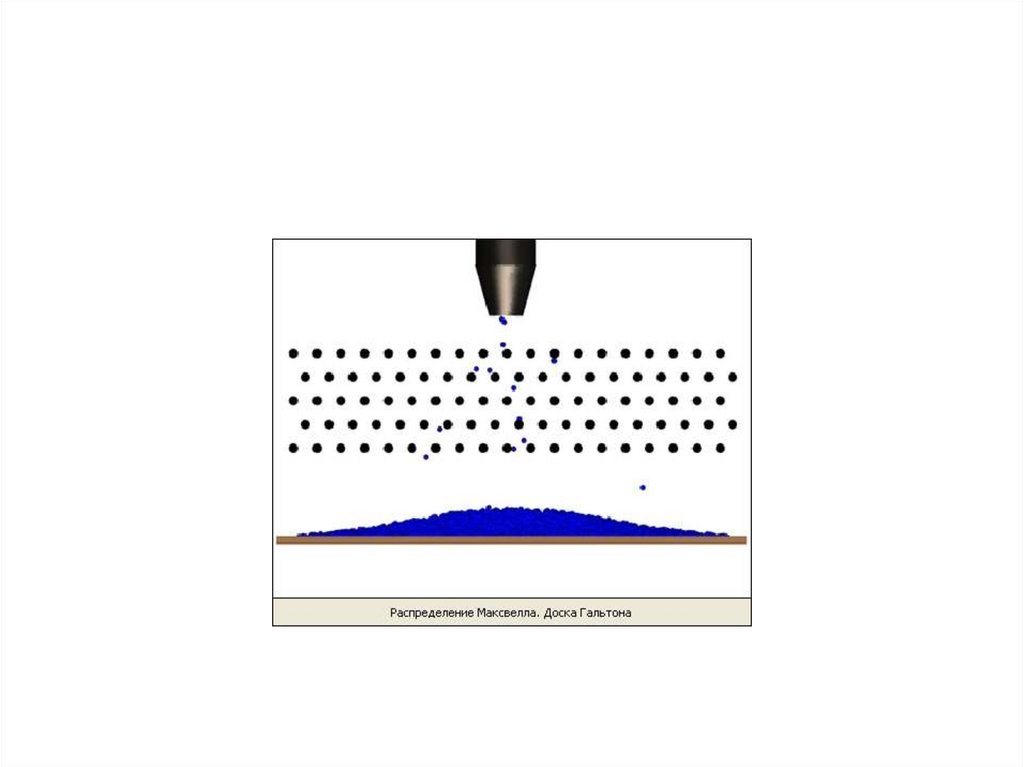
Распределение газовых молекул по скоростям и энергиям
1.
Лекция 17. РАСПРЕДЕЛЕНИЕГАЗОВЫХ МОЛЕКУЛ ПО
СКОРОСТЯМ И ЭНЕРГИЯМ
1. Скорость газовых молекул. Опыт Штерна.
2. Вероятность события. Понятие о распределении
молекул газа по скоростям.
3. Функция распределения Максвелла.
4. Барометрическая формула.
5. Распределение Больцмана.
6. Закон распределения Максвелла-Больцмана.
7. Распределение Бозе-Эйнштейна, Ферми-Дирака.
2.
1. Скорости газовых молекул. ОпытШтерна.
Поставьте себя на место исследователей 60-х
годов позапрошлого столетия. Сформулирована
молекулярно-кинетическая теория, но нет никаких
доказательств существования самих молекул! А вся
теория базируется на предположении о движении
молекул. С какой они движутся скоростью? И как эту
скорость измерить, если молекулы невидимы.
Теоретики первыми нашли выход. Из уравнения
молекулярно-кинетической теории газов известно, что
m υ2 3
kТ
(17.1)
2
2
3.
3kТυ
.
(17.2)
m
Получена хорошая формула, но масса молекулы
неизвестна! Тогда можно записать:
3kNAТ
3RT
υ
.
mN A
ρ
А мы знаем, что p RT
, тогда
μ
υ
3p
,
(17.3)
(17.4)
где р – давление; ρ плотность. Они уже измеряемые
величины.
4.
Например: плотность азота (N2) равна 1,25 кг/м3при Т=0 С и р=1 атм, N2=500 м/c. Для водорода:
H2=2000 м/c.
При этом, интересно отметить, что скорости
молекул в газе близки к скорости звука в этом газе. Это
объясняется тем, что звуковые волны переносятся
молекулами газа. И неудивительно поэтому, что
зв.
p
5.
Экспериментально впервые скорости молекулбыли измерены в 1920 г. Штерном. За этот опыт и за
большой вклад в развитие молекулярной физики в
1943 г. он был удостоен Нобелевской премии.
В этом опыте были не только измерены
скорости газовых молекул, но и показано, что они
имеют большой разброс по скоростям. Причина, в
хаотичности теплового движения молекул. Ещё в XIX
веке Максвелл утверждал, что молекулы беспорядочно сталкиваясь друг с другом как-то «распределяются» по скоростям, причём вполне определённым образом.
Cодержание
6.
2. Вероятность события. Понятие ораспределении молекул газа по скоростям
Математическое
определение вероятности:
вероятность какого-либо события – это предел, к
которому стремится отношение числа случаев,
приводящих к осуществлению события, к общему
числу случаев, при бесконечном увеличении
последних. Или
n
P lim ,
n n
(17.5)
где n число опытов, когда событие произошло, а n
общее число опытов.
7.
Отсюда следует, что Р может быть от нуля доединицы (Р=0 1). Или по определению Лапласа:
вероятность – отношение числа благоприятных случаев
к числу возможных случаев.
Определить распределение молекул по скоростям
вовсе не значит, что нужно определить число молекул,
обладающих той, или иной заданной скоростью. Ибо
число молекул, приходящихся на долю каждого
значения скорости равно нулю (постарайтесь это
понять). Вопрос должен быть поставлен так: «Сколько
молекул обладает скоростями, лежащими в этом
интервале, включающем заданную скорость?» Так
всегда ставятся статистические задачи.
8.
Например: на переписи населения, когдауказывается возраст (20 лет) – это не значит, что 20 лет,
0 часов, 0 минут, а эта цифра свидетельствует, что
возраст лежит в интервале от 20 лет до 21 года.
Итак, молекулы хаотически движутся. Среди них
есть и очень быстрые и очень медленные. Благодаря
беспорядочному движению и случайному характеру их
взаимных столкновений, молекулы определённым
образом распределяются по скоростям.
Это распределение оказывается однозначным и
единственно возможным, и не только не противоречит
хаотическому движению, но именно им и обусловлено.
9.
Мы будем искать число частиц (∆n), скоростикоторых лежат в определённом интервале значения
скорости ∆υ (от υ до υ+∆υ). То есть ∆n – число
благоприятных молекул.
Очевидно, что в единице объёма число таких
благоприятных молекул тем больше, чем больше ∆υ.
Ясно так же, что ∆n должно быть пропорционально
концентрации молекул (n).
∆n зависит и от самой скорости, так как в
одинаковых по величине интервалах, но при разных
абсолютных значениях скорости, число молекул будет
различным (сложная фраза с простым смыслом:
неодинаково, например, число людей в возрасте от 20 лет
до 21 года и от 90 лет до 91 года).
10.
Итак:∆n=nf(υ)∆υ
или перейдя к пределу
(17.6)
dn=nf(υ)dυ,
(17.7)
где f(υ) – функция распределения.
Трудность вычисления (17.7) – в нахождении именно f(υ).
Физический смысл f(υ): при dυ=1.
Физический смысл f(υ) в том, что это отношение числа молекул,
скорости которых лежат в определенном интервале скоростей, к
общему числу молекул в единичном интервале скоростей:
dn
f ( υ)
n
Таким образом, f(υ) – имеет смысл вероятности, То есть
f(υ) показывает, какова вероятность любой молекулы газа в
единице объёма иметь скорость, заключённую в
единичном интервале, включающем заданную скорость υ.
ВCодержание
этом случае f(υ) называют плотностью вероятности.
11.
3. Функция распределения МаксвеллаРаспределение молекул идеального газа по
скоростям было получено Максвеллом в 1860 году с
помощью методов теории вероятностей. Вывод
формулы функции распределения есть:
САМОСТОЯТЕЛЬНО!
учебник Ю.И Тюрина. и др.(ч. 1), И.В.
Савельев. Курс общей физики. Т.1.- М.: Наука, 1982,
с.311-319.
Мы воспользуемся результатами этого вывода.
Скорость – векторная величина. Для x-ой
1
составляющей скорости dnx=nf(υ
mυx x, тогдаmυx
x)dυ
dnx
1 m 2 2 kT
2 kT
f (υx )
e
A
e
,
1
ndυx
π 2kT
(17.8)
12.
Пусть имеется n тождественных молекул,находящихся в состоянии беспорядочного
теплового движения при определенной
температуре. После каждого акта
столкновения между молекулами, их
скорости меняются случайным образом. В
результате невообразимо большого числа
столкновений устанавливается
стационарное равновесное состояние, когда
число молекул в заданном интервале
скоростей сохраняется постоянным.
13. В результате каждого столкновения проекции скорости молекулы испытывают случайное изменение на υx, υy, υz, причем изменения
В результате каждого столкновенияпроекции скорости молекулы
испытывают случайное изменение на
υx, υy, υz, причем изменения каждой
проекции скорости независимы друг от
друга.
Будем предполагать, что силовые
поля на частицы не действуют.
Найдем в этих условиях, каково
число частиц dn из общего числа n имеет
υ
d
υ
скорость в интервале от υ до
14. При этом, мы не можем ничего определенного сказать о точном значении скорости той или иной частицы υi, поскольку за
столкновениями и движениями каждой из молекулневозможно проследить ни в опыте, ни в теории.
Такая детальная информация вряд ли имела бы
практическую
ценность.
15. Если скорость частицы попадает в интервал от υ до , то такая частица изобразится точкой между сферическими поверхностями
Если скорость частицы попадает винтервал от υ до
, то такая частица
изобразится
υ dυ точкой между сферическими
поверхностями радиусом υ и
.
dυ частиц dn, из
Тогда число υ
атомных
общего числа n, имеющих скорость в
интервале пространства скоростей,
равно плотности изображающих точек
ρ(υ) [1/(м/с)3] между сферическими
поверхностями с радиусами υυи dυ ,
умноженной на объем области между
этими сферами
dV 4πυ 2dυ
(рисунок 2.2)
16.
Мы воспользуемся результатами этого вывода. Скорость –векторная величина. Для x-ой составляющей скорости dnx =
nf(υx)dυx, тогда
1
2
dnx
1 m
f (υx )
e
ndυx
π 2kT
mυx
2 kT
A1e
mυx
2 kT
,
(17.8)
17.
А1 – постоянная равная1
2
1 m
.
π 2kT
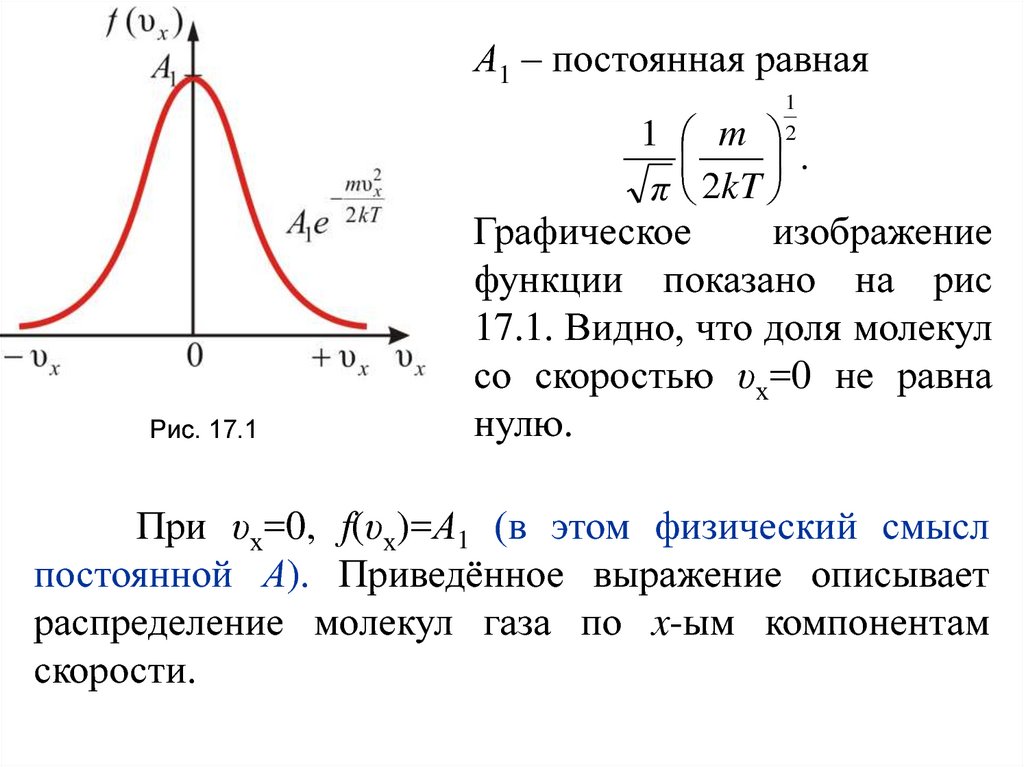
Рис. 17.1
Графическое
изображение
функции показано на рис
17.1. Видно, что доля молекул
со скоростью υх=0 не равна
нулю.
При υх=0, f(υх)=А1 (в этом физический смысл
постоянной А). Приведённое выражение описывает
распределение молекул газа по x-ым компонентам
скорости.
18.
Очевидно, что иdn y
ndυ y
A1e
mυ 2y
2 kT
dn z
и
A1e
ndυz
mυz2
2 kT
.
Вероятность того, что скорость молекулы
одновременно удовлетворяет трём условиям: x –
компонента скорости лежит в интервале от υх до
υх+dυх; y – компонента, в интервале от υy до υy+dυy; z –
компонента, в интервале от υz до υz+dυz будет равна
произведению вероятностей каждого из условий
(событий) в отдельности!
19.
То естьdnxyz
n
mυ2
3
2 kT
1
Ae
dυx dυ y dυz ,
(17.9)
Этой формуле можно дать геометрическое
истолкование: dnxyz – это число молекул в параллелепипеде со сторонами dυx, dυy, dυz, то есть в объёме
dV=dυxdυydυz, находящемся на расстоянии v от начала
координат в пространстве скоростей. Эта величина
(dnxyz) не может зависеть от направления вектора
скорости. Поэтому надо получить функцию распределения молекул по скоростям независимо от их
направления, то есть по абсолютному значению
скорости.
20.
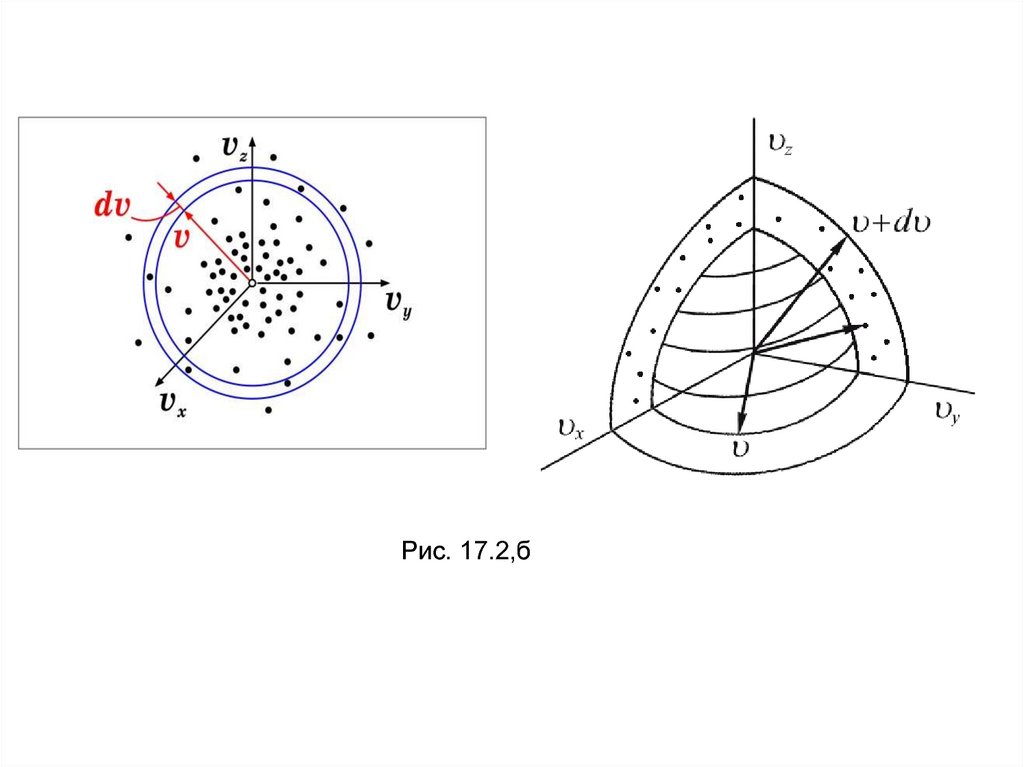
Если собратьвместе все молекулы в единице
объёма,
скорости
которых заключены
в интервале от υ до
υ+dυ (рис. 17.2) по
всем направлениям,
Рис. 17.2
и выпустить их,
то они окажутся через одну секунду в шаровом слое
толщиной dυ и радиусом υ. Этот шаровой слой
складывается из тех параллелепипедов, о которых
говориться выше.
21.
Рис. 17.2,а22.
Рис. 17.2,б23.
Объём этого шарового слояd =4 2d ,
тогда общее число молекул в слое
n m
dn 3 / 2
π 2kT
(17.10)
3/ 2
e
mυ2
2 kT
dΩ.
(17.11)
Отсюда следует закон Максвелла – распределение молекул по абсолютным значениям скоростей!
dn
n
dn
4
n
π
m
2kT
3/ 2
e
mυ2
2 kT
2
υ dυ
(17.`5)
– доля всех молекул единицы объёма, скорости
которых лежат на интервале от υ до υ+dυ.
24.
При dυ=1 получаем плотность вероятности, илифункцию распределения молекул по скоростям:
3
2
dn
4 m
f (υ)
e
ndυ
π 2kT
mυ2
2 kT
υ2 .
(17.14)
Эта функция обозначает долю молекул единицы
объёма газа, абсолютные скорости которых заключены в
единичном интервале скоростей, равном единице
включающем данную скорость.
3
Обозначим через
4 m 2
A
тогда
mυ2
2 kT
,
2кT
f (υ) Ae υ .
График этой функции показан на рис. 17.3.
2
(17.15)
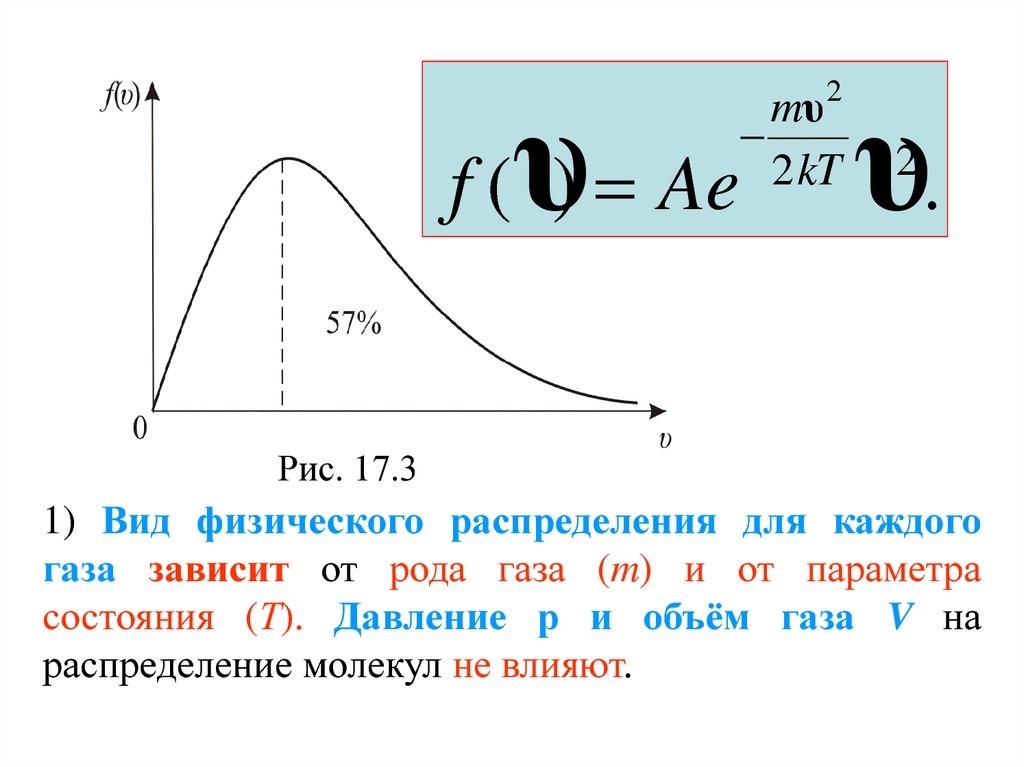
25.
f (υ) Aemυ 2
2 kT
υ.
2
Рис. 17.3
1) Вид физического распределения для каждого
газа зависит от рода газа (m) и от параметра
состояния (Т). Давление р и объём газа V на
распределение молекул не влияют.
26.
2) В показателе степени стоит отношениекинетической энергии, соответствующей данной
скорости υ к (kТ) – средней кинетической энергии
молекул при данной температуре.
Значит распределение Максвелла характеризует
распределение молекул по значениям кинетической
энергии (т. е. показывает, какова вероятность при
данной температуре иметь именно такое значение
кинетической энергии).
27.
28. Рассмотрим пределы применимости классического описания распределения частиц по скоростям. Для этого воспользуемся соотношением
неопределенностейГейзенберга. Согласно этому
соотношению координаты и импульс
частицы не могут одновременно иметь
определенное значение. Классическое
описание возможно, если выполнены
условия:
ΔxΔPx h, ΔyΔPy h, ΔzΔPz h.
29. Здесь – фундаментальная константа (постоянная Планка), определяющая масштаб квантовых (микроскопических процессов). Таким
Здесь–
34
h 6,62 10
Дж с (постоянная
фундаментальная
константа
Планка), определяющая масштаб
квантовых (микроскопических
процессов).
Таким образом, если частица
3
3
yΔz h
находитсяΔвxΔ
объеме
, /P
то
в этом случае возможно описание ее
движения на основе законов
классической механики.
30.
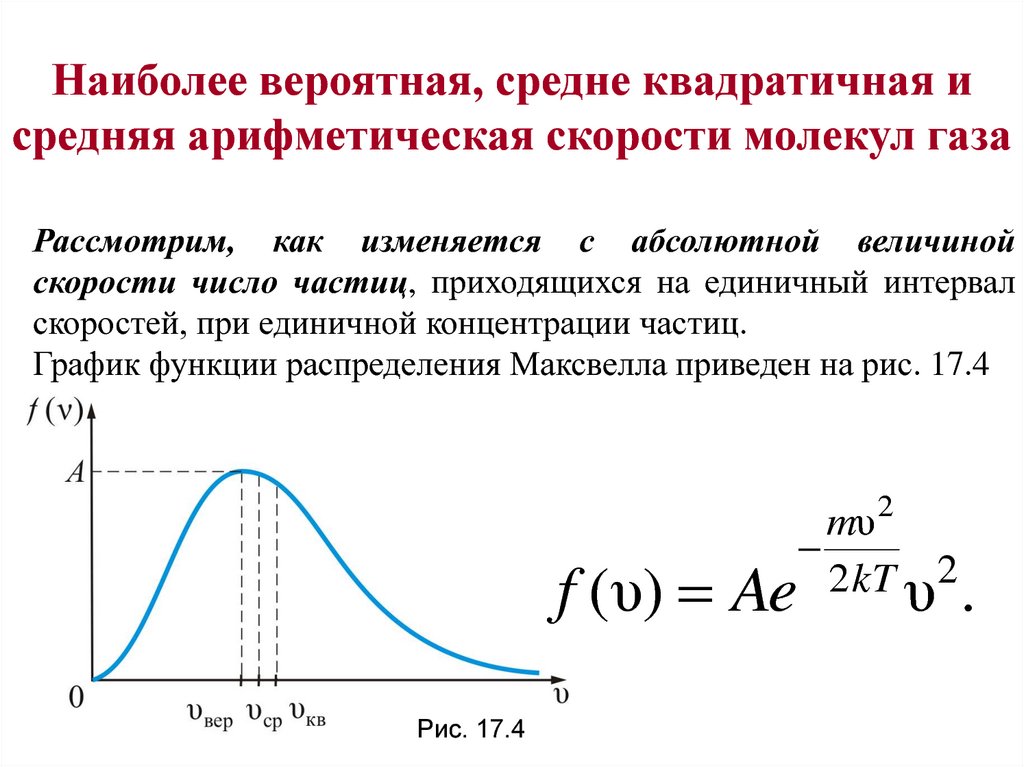
Наиболее вероятная, средне квадратичная исредняя арифметическая скорости молекул газа
Рассмотрим, как изменяется с абсолютной величиной
скорости число частиц, приходящихся на единичный интервал
скоростей, при единичной концентрации частиц.
График функции распределения Максвелла приведен на рис. 17.4
f ( υ)
Рис. 17.4
mυ 2
2
2
kT
Ae
υ.
31.
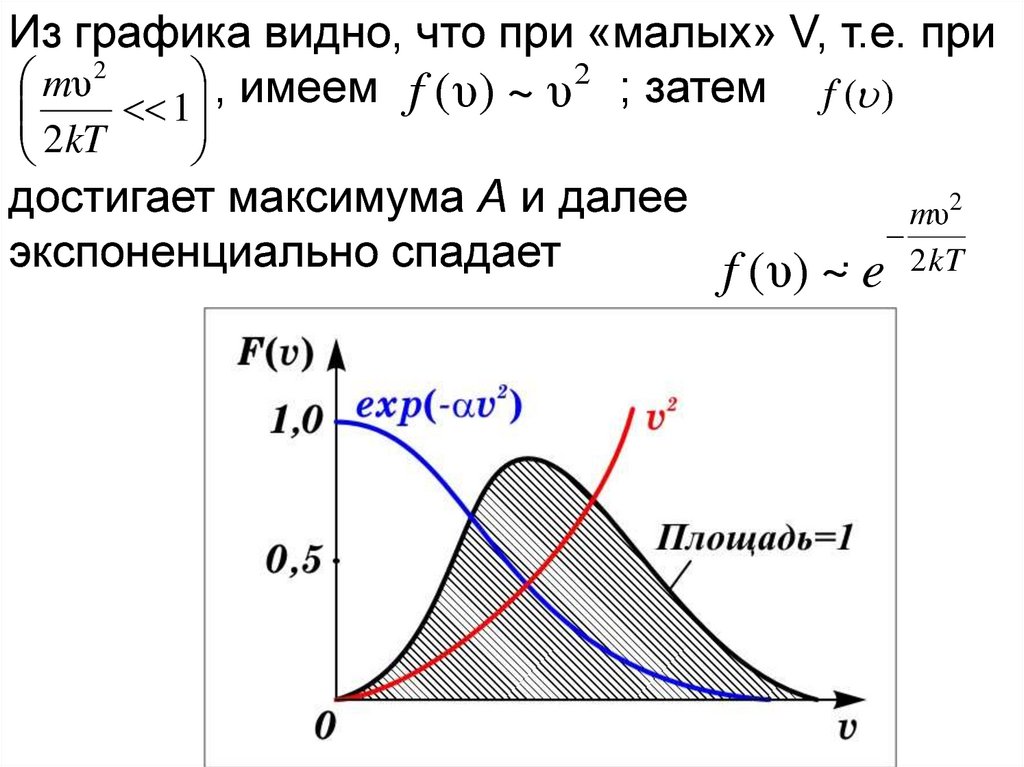
Из графика видно, что при «малых» V, т.е. приmυ 2
, имеем f ( υ) ~ υ 2 ; затем f ( )
1
2kT
достигает максимума А и далее
mυ2
экспоненциально спадает
f ( υ) ~. e 2 kT
32.
Величина скорости, на которую приходится максимум зависимостиназывают наиболее вероятной скоростью.
Величину этой
скорости найдем из условия равенства нулю производной
df ( υ)
0
dυ
2kТ
υв
m
– для одной молекулы.
2kNAT
2 RT
υв
mNA
μ
– для одного моля газа.
(17.17)
(17.17)
33.
Среднююквадратичную
используя соотношение
скорость
найдем
m υ2 3
kТ ,
2
2
Тогда
3kТ
υ
m
3RT
υ
– для одной молекулы.
(17.18)
– для одного моля газа.
(17.19)
34.
Средняя арифметическая скорость υср1
υср υnf (υ)dυ
n0
(17.20)
где nf( )d =dn – число молекул со скоростью от υ до
υ+dυ. Если подставить сюда f(υ) и вычислить, то:
8kТ
2,25kT
υср
;
πm
m
8 RТ
υкв
πμ
Полезно знать, что υср
υв
1,13;
2,25 RT
.
μ
υкв
1,22.
υв
(17.21)
(17.22)
35.
Формула Максвелла для относительныхскоростей
Для решения многих задач удобно использовать
формулу Максвелла, где скорость выражена в
относительных единицах. Относительную
υ
(17.23)
U
υв
dn
4 U 2 2
2kТ
e U
где υв
. Тогда
(17.24)
ndU
π
m
Формула Максвелла для относительных
скоростей. Это уравнение универсальное. В таком виде
функция распределения не зависит ни от рода газа ни от
Cодержание температуры.
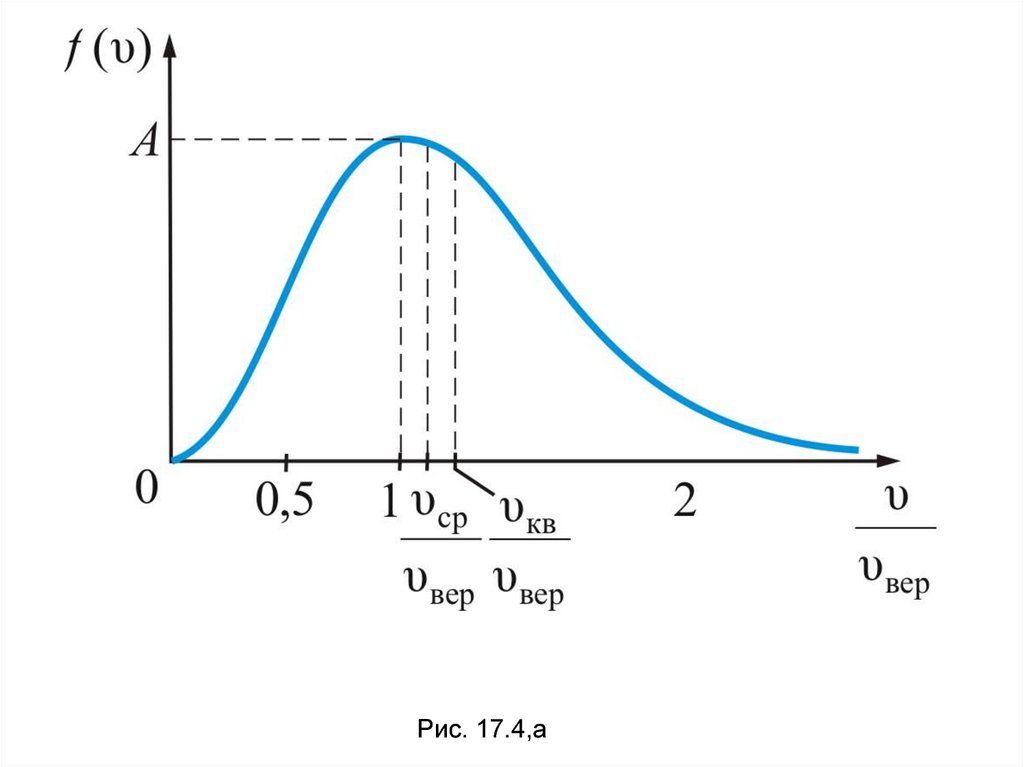
36.
Рис. 17.4,а37. На рисунке 17.4,а показано максвелловское распределение частиц f(υ) имеющих скорости от υ до За единицу скорости здесь взята
На рисунке 17.4,а показаномаксвелловское распределение частиц
f(υ) имеющих скорости
За
υ dυ. от υ до
единицу скорости здесь взята наиболее
вероятная скорость. Все три скорости
незначительно отличаются друг от друга
множителем
причем
υкв порядка
υср υверединицы,
.
38.
Зависимость функции распределенияМаксвелла от массы и температуры газа
Если у нас смесь газов, то в пределах каждого
сорта газа будет своё распределение со своим m
m
T
f (υв )
, кроме того, υв
.
T
m
Можно проследить за изменением f(υ) при
изменении m и T: m1>m2>m3 (T=const) или T1>T2>T3
(m=const) (рис. 17.5). Площадь под кривой f(υ)=const=1
поэтому важно знать как будет изменяться положение
максимума кривой.
39.
Рис. 17.5Максвелловский закон распределения по
скоростям и все вытекающие следствия справедливы
только для газа в равновесной системе. Закон
статически выполняется тем лучше, чем больше число
молекул.

































 Физика
Физика