Похожие презентации:
Органическая химия. Этапы развития органической химии
1. Органическая химия
Куликов Михаил Александровичканд. хим. наук, доцент
Зав. кафедрой ХТ и Э
2. Рекомендуемая литература
1.Березин, Б.Д. Органическая химия: учеб. пособие для бакалавров М.: Издательство Юрайт, 2012. - 768 с.
2.
Грандберг, И.И. Органическая химия: учебник для бакалавров М.: Издательство Юрайт, 2013. - 608 с.
3.
Грандберг, И.И. Практические работы и семинарские занятия по
органической химии: учеб. пособие для бакалавров. - М.:
Издательство Юрайт, 2012. - 349 с.
4.
Разин В.В. Задачи и упражнения по органической химии. - СанктПетербург: Химиздат, 2009. - 336 с.
3. Органическая химия – наука, изучающая соединения углерода.
Этапы развития органической химии1. С древнейших времён до XVIII века.
2. XVIII – XIX век:
Вёлер – синтез щавелевой кислоты и мочевины;
А.М. Бутлеров – теория строения органических соединений;
Н.Н. Зинин – получение анилина и других аминов.
3. XX век – промышленный органический синтез. Новые методы
исследования органических соединений.
4. XXI век – биополимеры, органические полупроводники,
оптические материалы
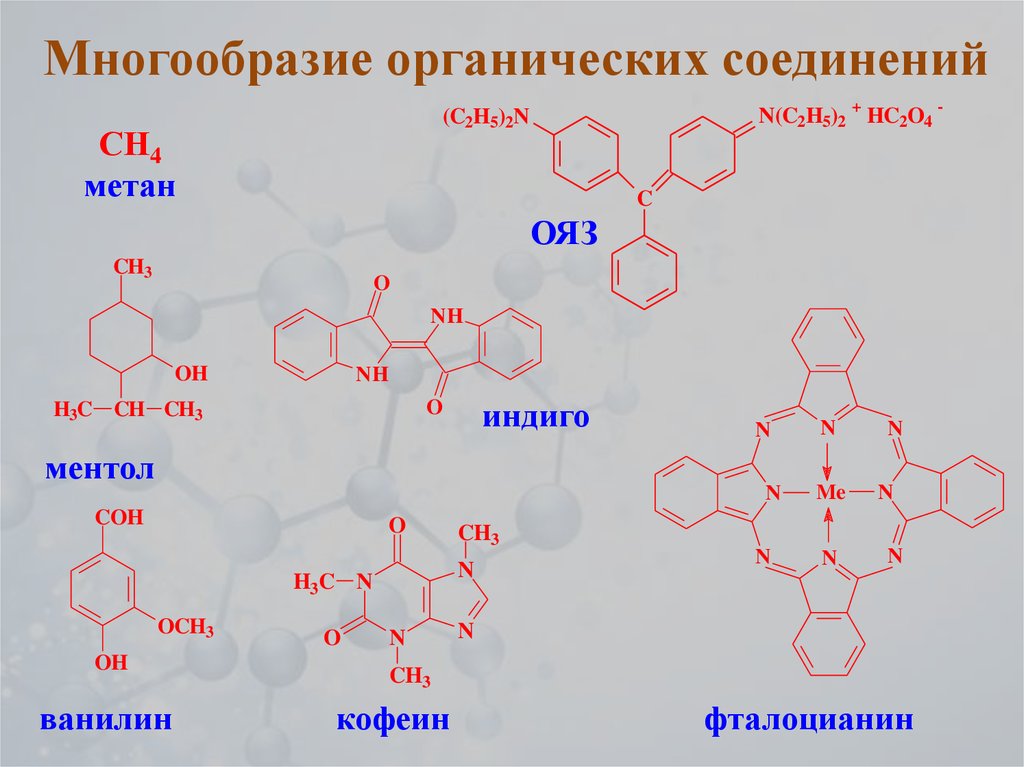
4. Многообразие органических соединений
+N(C2H5)2 HC2O4
(C2H5)2N
СН4
метан
C
ОЯЗ
CH3
O
NH
OH
NH
индиго
O
H3C CH CH3
ментол
N
N
COH
O
OCH3
OH
ванилин
O
N
Me
CH3
N
H3C N
N
N
N
N
N
N
N
CH3
кофеин
фталоцианин
-
5.
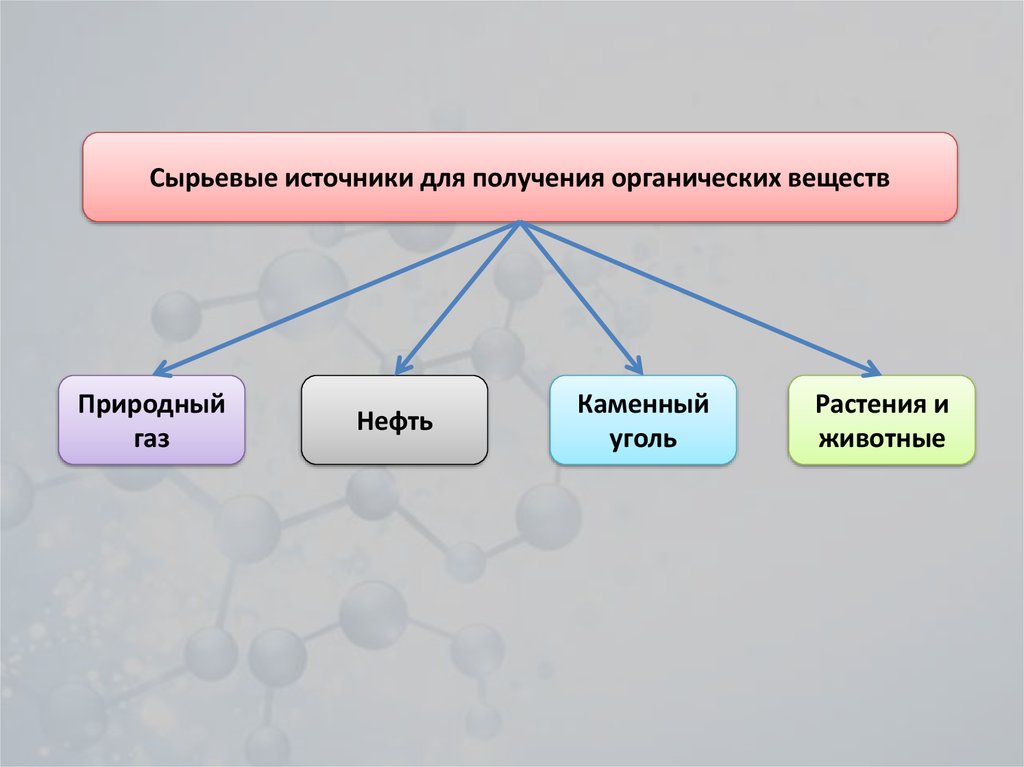
Сырьевые источники для получения органических веществПриродный
газ
Нефть
Каменный
уголь
Растения и
животные
6. Теории химического строения органических соединений
7. Теория радикалов
Первая четверть XIX в.1.
2.
3.
4.
Органические вещества состоят из радикалов – постоянных и
неизменных частиц.
Радикалы могут существовать в свободном состоянии.
Радикалы обладают положительными или отрицательными
зарядами.
Образование молекул происходит в результате притяжения разно
заряженных радикалов.
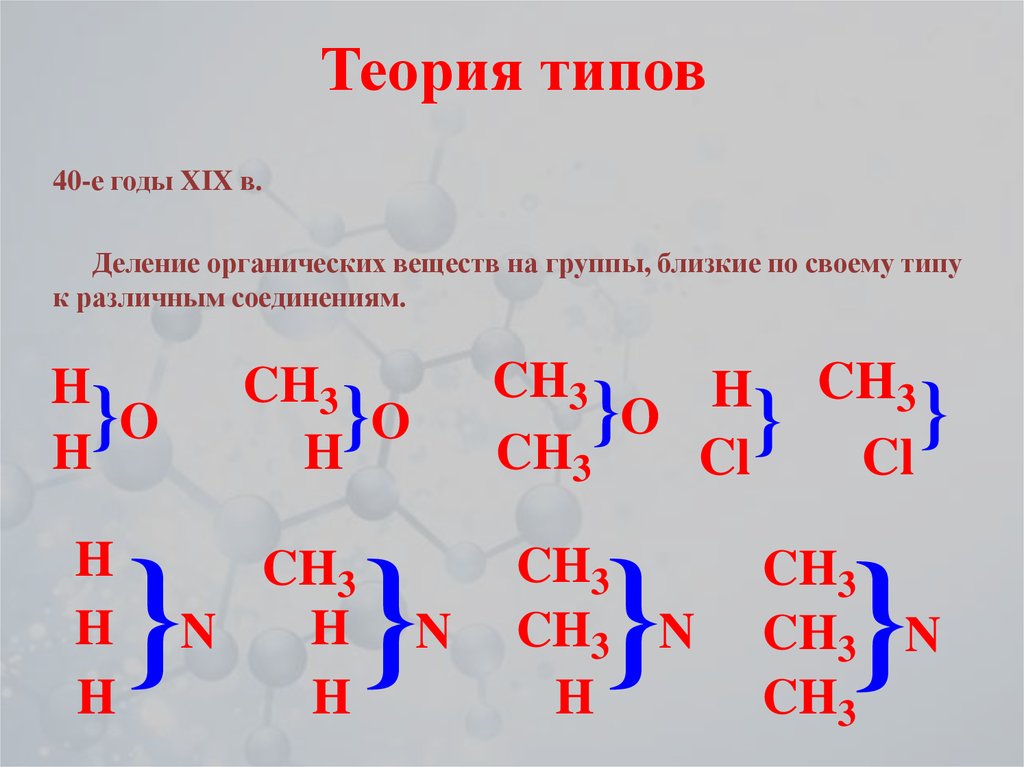
8. Теория типов
40-е годы XIX в.Деление органических веществ на группы, близкие по своему типу
к различным соединениям.
H
H
H
CH3
H CH3
O
}
}
}
CH3
Cl
Cl
CH3
O
}
H
H
O
}
H
CH3
H
N
H
}
}
N
CH3
CH3 N
H
}
CH3
CH3 N
CH3
}
9. Основные положения
Атомы в молекулах соединены друг с другом согласно их валентности,порядок распределения связей в молекуле называется химическим
строением.
Изменение этой последовательности приводит к образованию нового
вещества с новыми свойствами.
Свойства веществ зависят не только от их состава, но и от
«химического строения», то есть от порядка соединения атомов в
молекулах и характера их взаимного влияния. Наиболее сильно
влияют друг на друга атомы, непосредственно связанные между собой.
Атомы в молекулах оказывают влияние друг на друга и это влияние
приводит к химическим изменениям поведения атома.
Определить состав и строение химического вещества можно по
продуктам химических превращений.
10. Классификация органических реакций
11. Направление реакции
реакции присоединения (А)R – CH = CH2 + Br2 R – CHBr – CH2Br
реакции элиминирования (отщепления, Е)
R – CHBr – CH2 – R + KOH R – CH = CH – R + KBr + H2O
реакции замещения (S)
R – H + Cl2 R – Cl + HCl
реакции перегруппировки
H3C C CH COOR
OCH2CH CH2
H3C CO CH COOR
CH2CH CH2
12. Характер реагентов (тип разрыва связей)
радикальные реакции (R) – гомолитический разрыв связейCl : Cl 2Cl
R : H + Cl R + HCl
R + Cl : Cl RCl + Cl
полярные реакции – гетеролитический разрыв связей
Нуклеофильные реакции
R : Cl + :OH– R : OH + :Cl–
Электрофильные реакции
R – H + E+ R – E + H+
13. Молекулярность реакции
мономолекулярные и бимолекулярныесимволы типов реакций
AR – реакции радикального присоединения
Е2 – реакции бимолекулярного элиминирования
SN1 – реакции мономолекулярного нуклеофильного замещения
SE2 – реакции бимолекулярного электрофильного замещения










 Химия
Химия