Похожие презентации:
Требования к лекарственному обеспечению в свете интеграционных процессов и развития регуляторных функций государства
1. Требования к лекарственному обеспечению в свете интеграционных процессов и развития регуляторных функций государства
Муратова Н.П.Кафедра управления и
экономики фармации УГМУ
2. Тенденции развития фармацевтического рынка Российской Федерации
Рост объемов1500
коммерческий
сектор ЛП
1000
млрд. руб.
500
0
975
468 537
609
183
130 149 169
226 234 267 294
2011 2012 2013 2014
коммерческая
парафармацевтика
государственный
сектор
Адаптация НПБ к
общемировой
Корректировка законодательной
и НПБ по обращению ЛС
Интеграция
Создание единого рынка
ЛС в рамках ЕАЭС
(ближе к ЕС, интеграция
интеграций)
3.
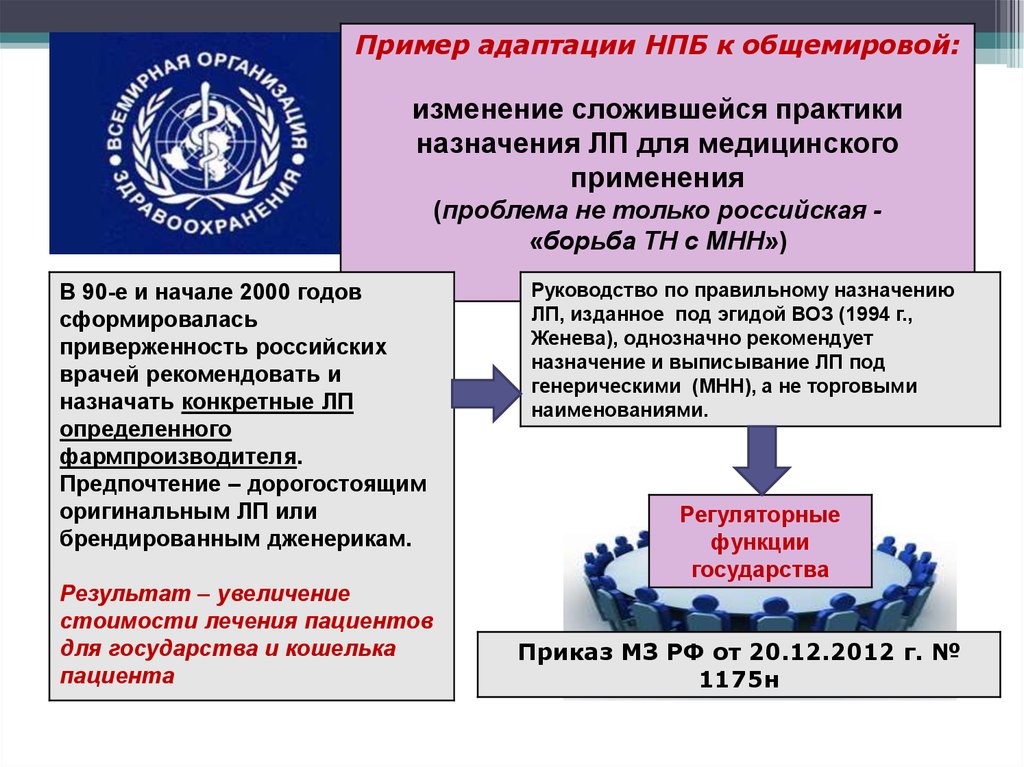
Пример адаптации НПБ к общемировой:изменение сложившейся практики
назначения ЛП для медицинского
применения
(проблема не только российская «борьба ТН с МНН»)
В 90-е и начале 2000 годов
сформировалась
приверженность российских
врачей рекомендовать и
назначать конкретные ЛП
определенного
фармпроизводителя.
Предпочтение – дорогостоящим
оригинальным ЛП или
брендированным дженерикам.
Результат – увеличение
стоимости лечения пациентов
для государства и кошелька
пациента
Руководство по правильному назначению
ЛП, изданное под эгидой ВОЗ (1994 г.,
Женева), однозначно рекомендует
назначение и выписывание ЛП под
генерическими (МНН), а не торговыми
наименованиями.
Регуляторные
функции
государства
Приказ МЗ РФ от 20.12.2012 г. №
1175н
4. Интеграция (восполнение, восстановление) с экономической точки зрения – процесс взаимного приспособления, расширения
экономическогои
производственного
сотрудничества,
объединения национальных хозяйств 2-х и более государств,
форма интернационализации хозяйственной жизни.
ЕАЭС создан на базе
Таможенного союза ЕврАзЭС
(договор от 29.05.2014 г.,
вступил в силу с 1 января
2015 г.).
ТС ЕврАзЭС заработал в 2010 г.
Товары ТС должны соответствовать
единым техническим регламентам ТС
Задача ЕАЭС – дальнейшее углубление интеграции, обеспечение
свободы перемещения товаров, услуг, капитала и рабочей силы
Управление в ЕАЭС:
Высший наднациональный орган ЕАЭС – Высший Евразийский
экономический совет;
Постоянный регулирующий орган ЕАЭС – Евразийская экономическая
комиссия (ЕЭК)
5. История создания ЕАЭС (международного интеграционного экономического объединения – союза)
1994 г.создание зоны
свободной
торговли (ЗСТ)
2000 г.
Евразийское
экономическое
сообщество
(ЕврАзЭС)
2010 г.
Таможенный
союз (ТС)
2014 г.
Евразийский
экономический
союз (ЕАЭС)
2012 г.
Евразийское
экономическое
пространство
6. Параметры ЕАЭС
Население – 182 млн. чел.Площадь - более 20 млн. кв.
км или 14% мировой суши
Объем взаимной торговли ЛС
и МИ – более 350 млн.
долларов в год
Необходимо расширение
преференций на ЛС
происхождения государств –
членов ЕАЭС
7. Базис для преференций:
I: Государства – члены ЕАЭС договорились, что регулированиеобращения ЛС в рамках ЕАЭС осуществляется в соответствии с …
Соглашением, другими международными договорами, входящими
в право ЕАЭС, решениями ЕЭК и законодательством государствчленов ЕАЭС. Решения ЕЭК, регулирующие обращение ЛС,
разрабатываются на основе международных норм.
II:
Возможности Таможенного союза
•Единая таможенная территория стран ЕАЭС
•Беспошлинная торговля товарами ТС на единой таможенной
территории
•Единое таможенное регулирование для торговли с третьими
странами
8. Создание единого рынка ЛС (с 1.01.2016 г.) - одна из важнейших целей ЕАЭС
Реализация :2014 г.: Принятие
документа первого
уровня
23.12.2014 г. государствами – членами
ЕАЭС заключено «Соглашение о единых
принципах и правилах обращения ЛС в
рамках ЕАЭС», вступает в силу с 1 января
2016 г.
2015 г.: Принятие и
ратификация
документов второго
уровня (25 для ЛС, 15
для МИ)
• Подготовка НПД распределена между
государствами – членами ЕАЭС,
рассмотрение – на уровне ЕЭК (рабочая
группа при Коллегии ЕЭК).
• Единый рынок ЛС в рамках ЕАЭС будет
регулироваться Соглашением и НПД ЕЭК.
Национальные НПД должны быть
откорректированы и соответствовать ЕАЭС.
9. Соглашение о единых принципах и правилах обращения ЛС в рамках ЕАЭС охватывает направления:
1. Гармонизация и унификация законодательства государств – членов ЕАЭСв сфере обращения ЛС (Концепция гармонизации ГФ государств – членов
ЕАЭС)
2. Принятие единых правил и требований регулирования обращения ЛС
3. Обеспечение единства обязательных требований к безопасности,
эффективности и качеству ЛС и их соблюдения
4. Обеспечение единых подходов к созданию системы обеспечения качества
ЛС
5. Гармонизация законодательства в области контроля (надзора) в сфере
обращения ЛС (формирование фармацевтических инспекторатов, реестра
фармацевтических инспекторов ЕАЭС)
Государства – члены ЕАЭС определяют органы государственной
власти, уполномоченные на осуществление и (или) координацию
деятельности в сфере обращения ЛС в рамках ЕАЭС
10. Национальному законодательству остается:
1. Регулирование получения лицензий на производство ЛС2. Государственный контроль (надзор) за обращением ЛС
3. Деятельность аптек – Правила надлежащей аптечной практики
(розничная торговля ЛС -задача гармонизации обращения ЛС на
перспективу)
4. Реклама ЛС
5. Формирование перечней и регулирование цен на ЛП из Перечня
ЖНВЛП (задача гармонизации обращения ЛС на перспективу)
11. Документы второго уровня для функционирования единого рынка ЛС в рамках ЕАЭС
Гармонизация государственных фармакопей, образование фармакопеи
ЕАЭС (Концепция гармонизации ГФ государств – членов ЕАЭС, Положение о ФК
ЕАЭС приняты Коллегией ЕЭК 22.09.2015 г.)
Правила надлежащей лабораторной практики (GLP)
Правила надлежащей клинической практики (GCP)
Правила надлежащей производственной практики (GMP)
Правила надлежащей практики фармаконадзора (GVP)
Правила надлежащей дистрибьютерской практики (GDP)
Единые правила регистрации и экспертизы ЛС
Единые требования к проведению исследований (испытаний) ЛС
Единые требования к маркировке ЛС, к инструкции по медицинскому
применению (национальные языки стран ЕАЭС для ЛС ЕА)
Единый порядок аттестации уполномоченных лиц производителей ЛС
Форма инспекционного отчета
Порядок взаимодействия уполномоченных органов по выявлению ФЛС и
(или) контрафактных ЛС
Правила создания и функционирования информационной системы ЕАЭС
в сфере обращения ЛС
12. Переходный период (ключевые даты)
Задача – формированиеединого реестра
зарегистрированных ЛС
ЕАЭС (ЛС ЕА)
01.01.2016 г. вместе с началом функционирования рынка ЛС
вступят в силу новые правила их регистрации
31.12.2025 г. регистрационное досье ЛП, зарегистрированных
до 1 января 2016 г. по законодательству государств – членов
ЕАЭС, должно быть приведено в соответствие с едиными
требованиями, установленными в Правилах регистрации и
экспертизы ЛС ЕАЭС (два типа ЛП)
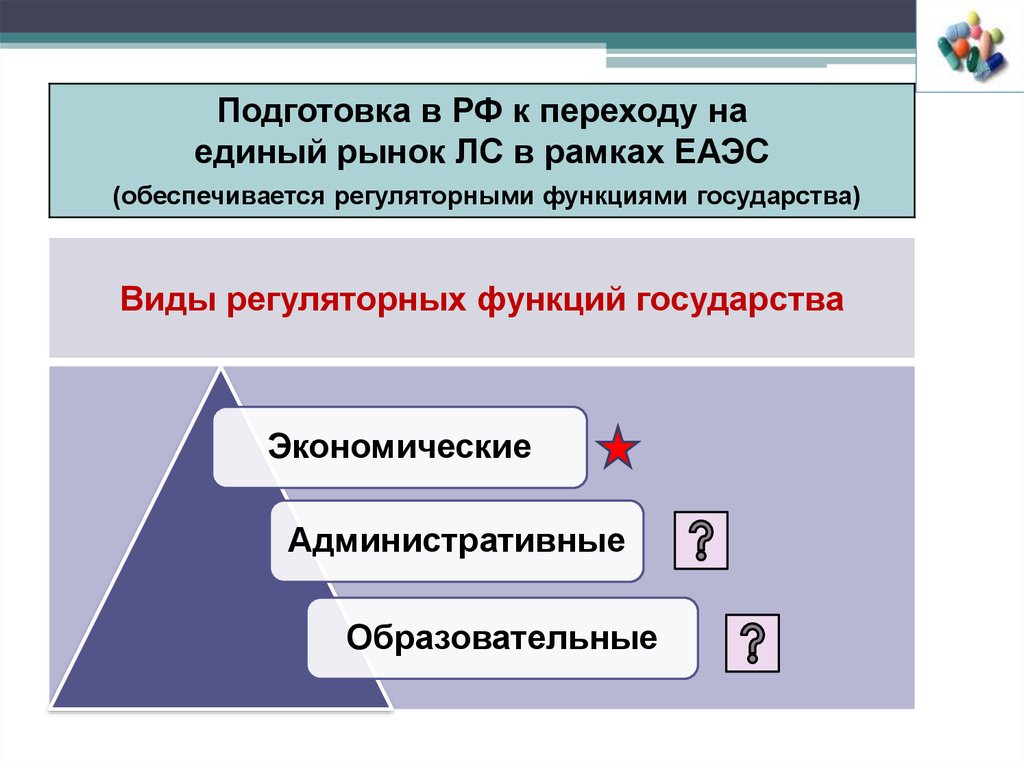
13. Виды регуляторных функций государства
Подготовка в РФ к переходу наединый рынок ЛС в рамках ЕАЭС
(обеспечивается регуляторными функциями государства)
Виды регуляторных функций государства
Экономические
Административные
Образовательные
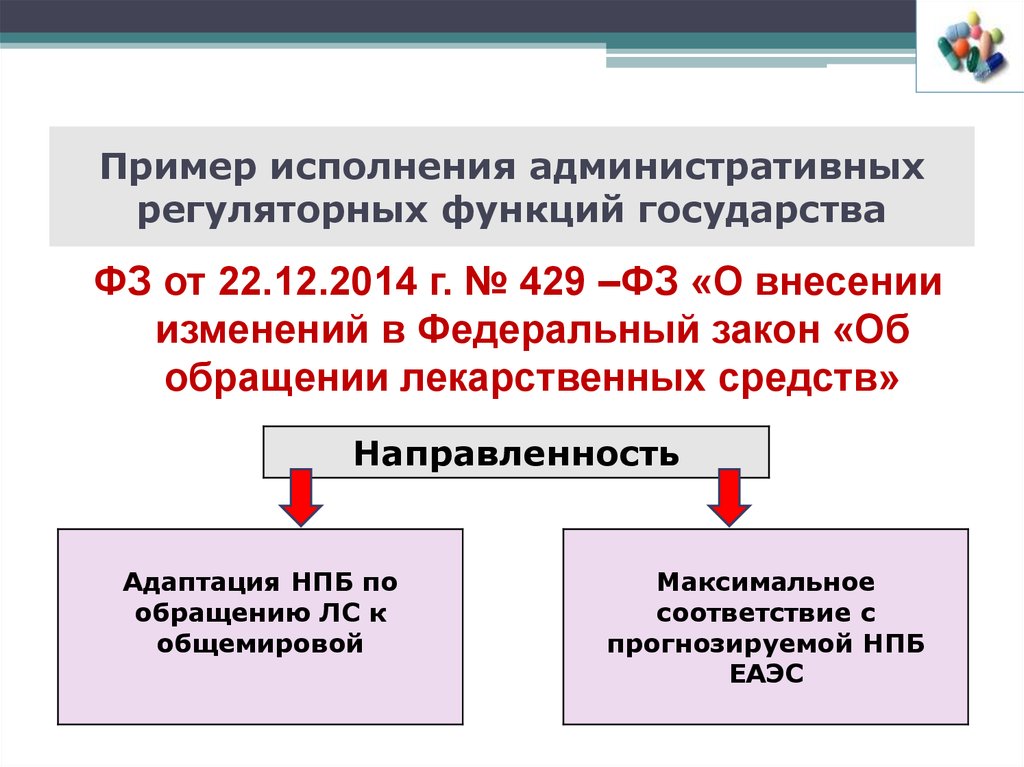
14. Пример исполнения административных регуляторных функций государства
ФЗ от 22.12.2014 г. № 429 –ФЗ «О внесенииизменений в Федеральный закон «Об
обращении лекарственных средств»
Направленность
Адаптация НПБ по
обращению ЛС к
общемировой
Максимальное
соответствие с
прогнозируемой НПБ
ЕАЭС
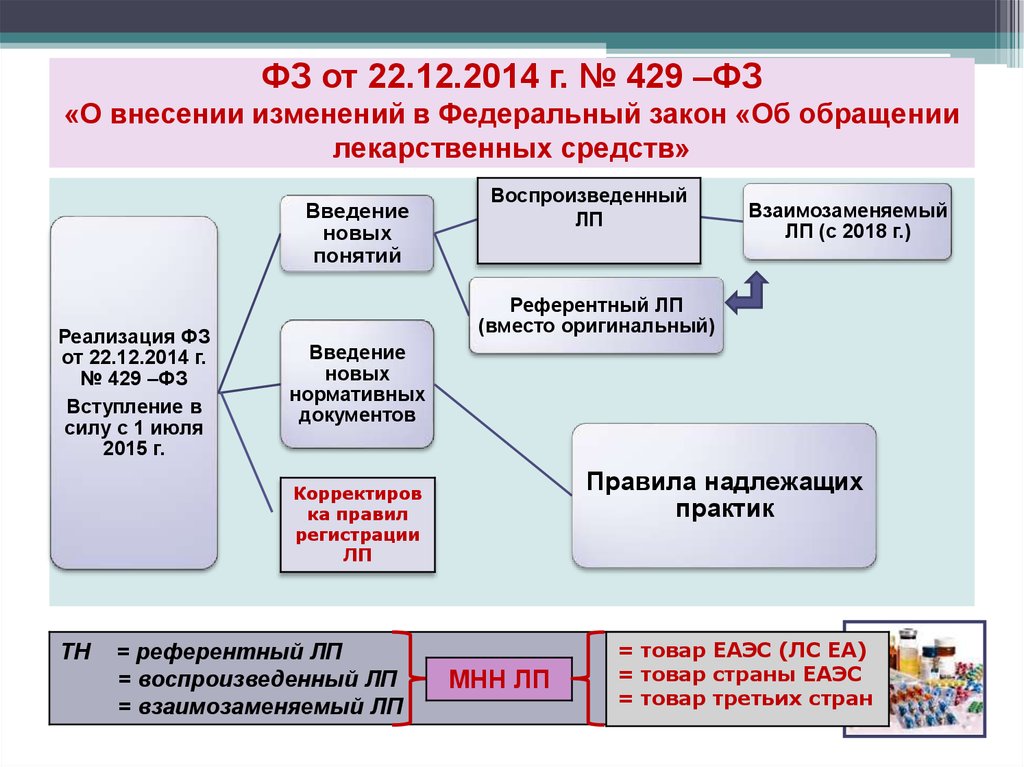
15. ФЗ от 22.12.2014 г. № 429 –ФЗ «О внесении изменений в Федеральный закон «Об обращении лекарственных средств»
Введениеновых
понятий
Реализация ФЗ
от 22.12.2014 г.
№ 429 –ФЗ
Вступление в
силу с 1 июля
2015 г.
Воспроизведенный
ЛП
Референтный ЛП
(вместо оригинальный)
Введение
новых
нормативных
документов
Правила надлежащих
практик
Корректиров
ка правил
регистрации
ЛП
ТН
Взаимозаменяемый
ЛП (с 2018 г.)
= референтный ЛП
= воспроизведенный ЛП
= взаимозаменяемый ЛП
МНН ЛП
= товар ЕАЭС (ЛС ЕА)
= товар страны ЕАЭС
= товар третьих стран
16. Значение ФЗ-429, ситуация
Несмотря на то, что ФЗ-429 направлен на максимальное соответствие с
прогнозируемой НПБ ЕАЭС, специалисты отмечают ряд его расхождений
с новыми документами ЕАЭС (нет ссылок на ЕАЭС, порядок ввоза
(вывоза).
Отсутствуют многие подзаконные акты (надлежащие практики).
Потребуется дальнейшая корректировка ФЗ-61 (первое полугодие 2016
г.).
По причине верховенства международных договоров и
близости 1 января 2016 г. специалисты, занятые в
разработке, регистрации, производстве, дистрибьюции ЛП и
МИ в РФ, ставят вопросы к административному регулятору:
Когда будут приняты новые изменения в ФЗ-61 на основе НПБ ЕАЭС?
Когда будут приняты национальные НПД по обращению ЛС на основе
НПБ ЕАЭС?
Будет ли начата регистрация ЛП по новым правилам ЕАЭС с 1 января
2016 г.?
Не ждет ли фармацевтическую отрасль регуляторный коллапс с
01.01.2016 г.?
17. п. 2. ст. 20 Соглашения о единых принципах и правилах обращения ЛС в рамках ЕАЭС (23.12.2014 г.):
«До вступления в силу решенийКомиссии (ЕЭК), регулирующих
обращение ЛС, применяются
соответствующие нормативные
правовые акты государств – членов
ЕАЭС»
18. Образовательные функции государства – подготовка кадров
Настройка системы высшего и среднегоспециального медицинского и
фармацевтического образования на:
• Изучение нормативной базы по обращению ЛС и МИ в рамках
ЕАЭС для использования ее в учебном процессе
(корректировка образовательных стандартов, подготовка
методические материалов, учебных пособий, образовательных
программ);
• Подготовка специалистов, готовых работать в условиях
функционирования единого рынка ЛС в рамках ЕАЭС, т.е.
выполнять требования к лекарственному обеспечению в
свете интеграционных процессов и развития регуляторных
функций государства в новых условиях
19. Выводы:
• Впереди большое «переформатирование»фармацевтической отрасли, и оно назрело;
• Масштабы реформирования велики, затрагивают
все виды обращения ЛС;
• Задача системы образования научить будущих
специалистов и действующих практиков работать с
учетом требований единого рынка ЛС ЕАЭС;
• В дальнейшем ожидаема унификация правил
потребления ЛС (стандарты МП), госзакупок.
















 Медицина
Медицина Право
Право








