Похожие презентации:
Ароматические кислоты фенолокислоты
1. Ароматические кислоты фенолокислоты
2. Производные ароматических углеводородов в молекуле которой один или несколько атомов Н+ замещены одной или несколько
СООНБензойная кислота
Бензолкарбоновая
3. Номенклатура
Родоначальник- бензойная кислотаСООН
NО2
2-нитробензойная кислота
о-нитробензойная кислота
4. Способы получения: 1. Из 3-х галогенопроизводных
ClС Cl + 3НОН
Cl
-3HCl
он
с он
он -H2O
O
C
OH
2. Окисление боковой цепи
СН3
КMnO 4
+ 3О
C
ОН
ОН
-Н2О
С О
ОН
5. Химические свойства
Карбоксильнаягруппа. Диссоциация
(взаимодействие с щелочами, со спиртами,
РСl3 ,РСl5) Ароматические более сильнее
кислоты, чем алифатические по степени
диссоциации, что объясняет
электроноакцепторный характеристикой
бензольного кольца.
Замещение в бензольном ядре.
Реакция гидрирования бензольного ядра с
образованием гексагидробензойной кислоты.
6. Отдельные представители
Бензойная кислота обнаружена в составесмол, по физическим свойствам твёрдое
кристаллическое вещество, хорошо
растворяется в горячей воде. Легко
возгоняется, на холоде не имеет запаха,
пары обладают характерным запахом,
раздражает слизистые оболочки, вызывает
кашель. В медицине, применяется как
антисептическое средство(мази), при
консервирование продуктов, в
производстве красителей.
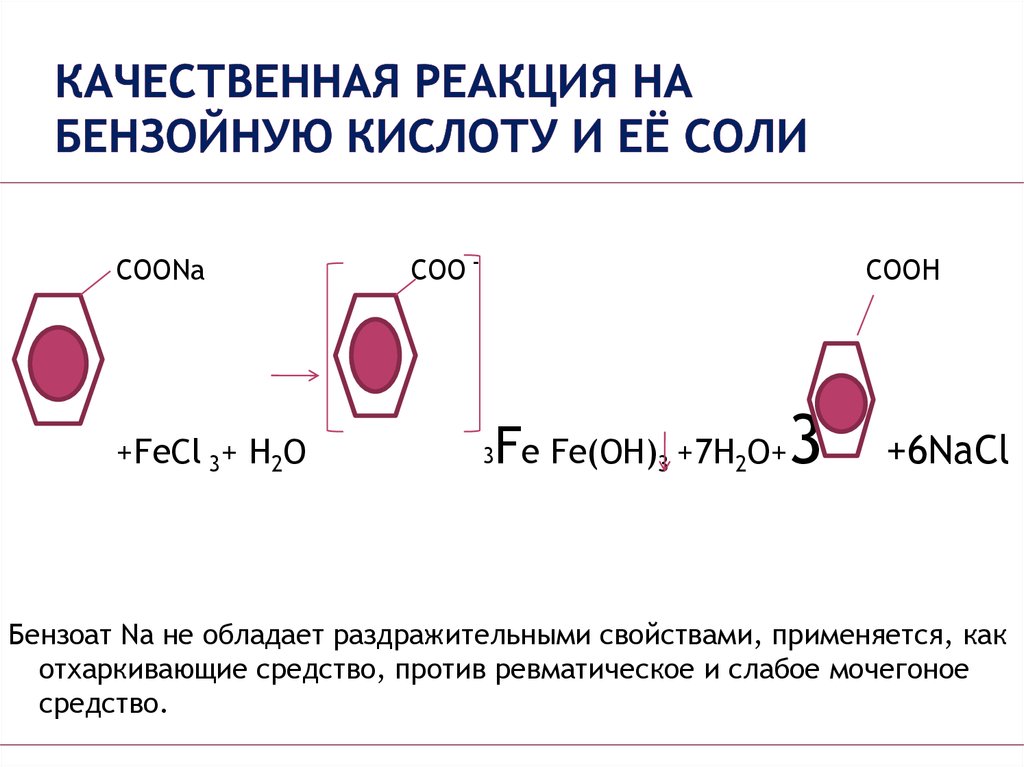
7. Качественная реакция на бензойную кислоту и её соли
COONa+FeCl 3+ H2O
COO -
COOH
3
Fe Fe(OH)3 +7H2O+3
+6NaCl
Бензоат Na не обладает раздражительными свойствами, применяется, как
отхаркивающие средство, против ревматическое и слабое мочегоное
средство.
8. Фенолокислоты
Фенолокислоты- это ароматическиегидроксикислоты, у которых ОН- группы
непосредственно связаны с бензольным
кольцом.
9. Изомерия
Родоначальник- бензойная кислота, наличиеОН
группы отражается префиксом «гидрокси».
Для многих сохраняется тривиальное названия.
10. Получение
1. Карбоксинирование фенолов(получается из фенолятаNa)
ONa
ONa
ОН
Н + СО2 125
С О
С О
ОН
ОН
СООН +NaCl
О Na
11. 2.Из ароматических кислот
СООНCOOH
+ НОSO3H -н2о
СООК
+KOH
-K2SO3
2кон
SO3H 2н2о
COOH
+HCl
OH
+ KCl
OH
COOH
SO3K
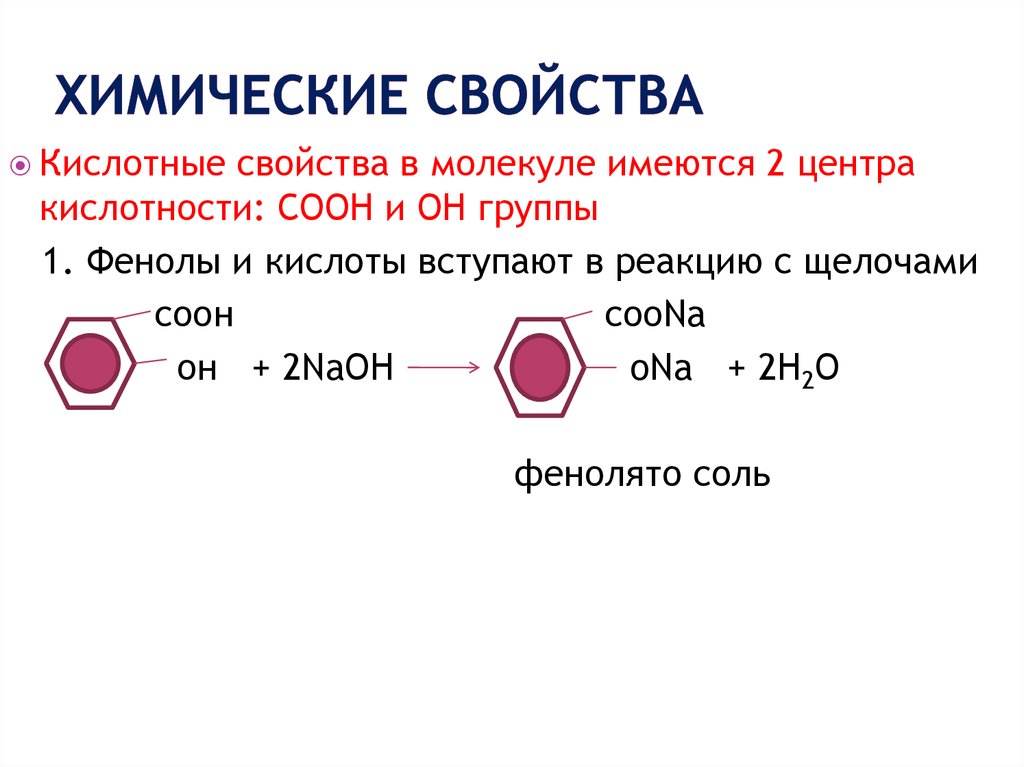
12. Химические свойства
Кислотныесвойства в молекуле имеются 2 центра
кислотности: СООН и ОН группы
1. Фенолы и кислоты вступают в реакцию с щелочами
соон
сооNa
он + 2NaОН
oNa + 2Н2О
фенолято соль
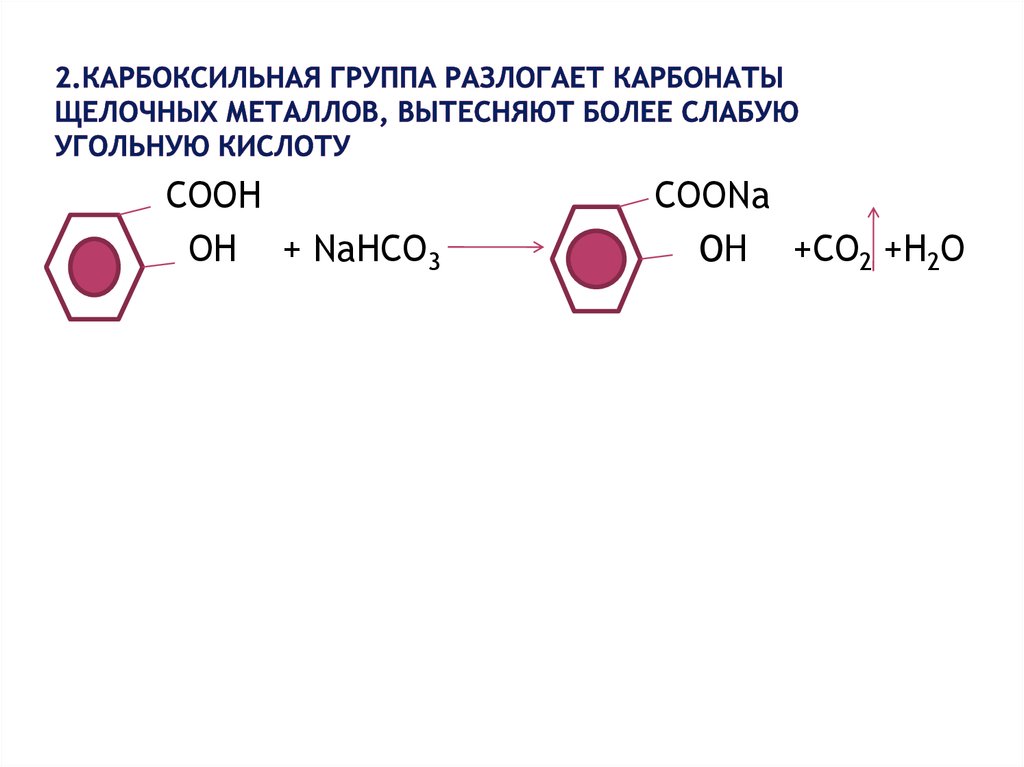
13. 2.Карбоксильная группа разлогает карбонаты щелочных металлов, вытесняют более слабую угольную кислоту
СООНОН + NaНСО3
СООNa
OH +СО2 +Н2О
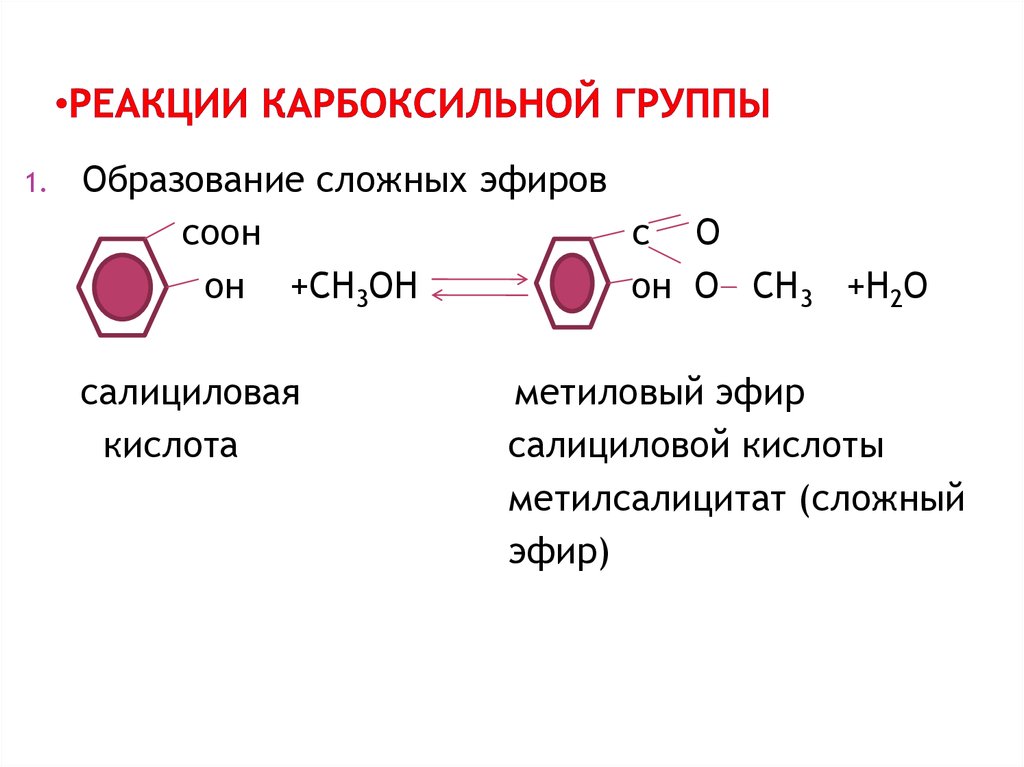
14. Реакции Карбоксильной группы
1.Образование сложных эфиров
соон
с О
он +СН3ОН
он О СН3 +Н2О
салициловая
кислота
метиловый эфир
салициловой кислоты
метилсалицитат (сложный
эфир)
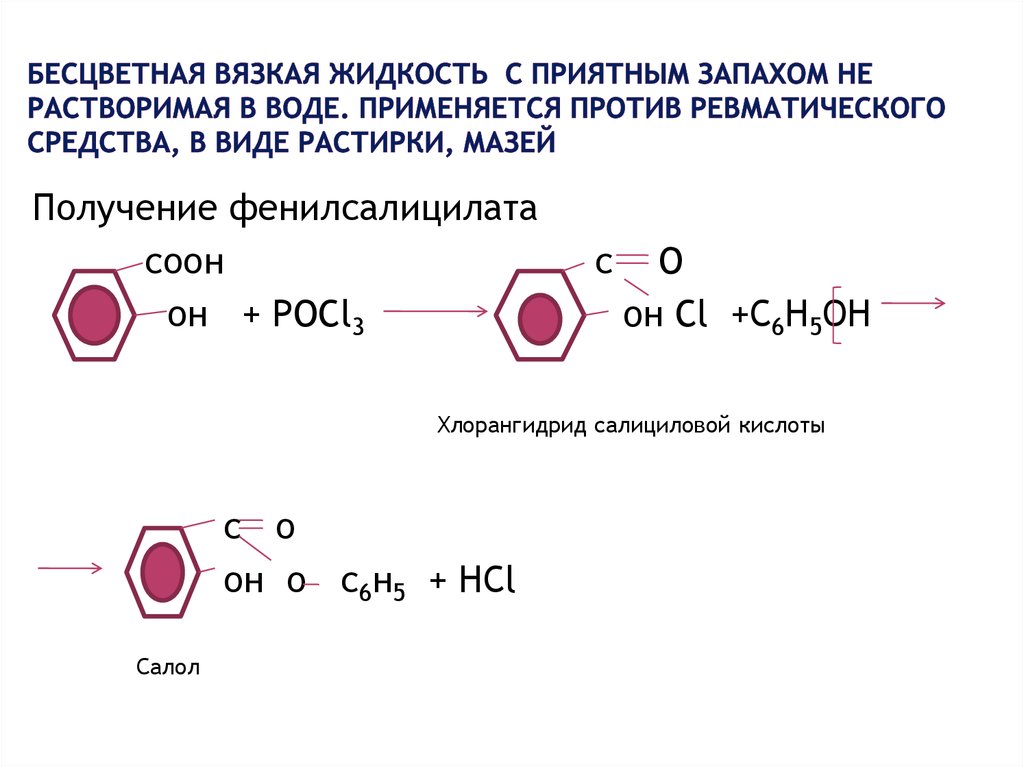
15. Бесцветная вязкая жидкость с приятным запахом не растворимая в воде. Применяется против ревматического средства, в виде
Получение фенилсалицилатасоон
он + POCl3
с
O
oн Cl +С6Н5ОН
Хлорангидрид салициловой кислоты
с о
он о с6н5 + НСl
Салол
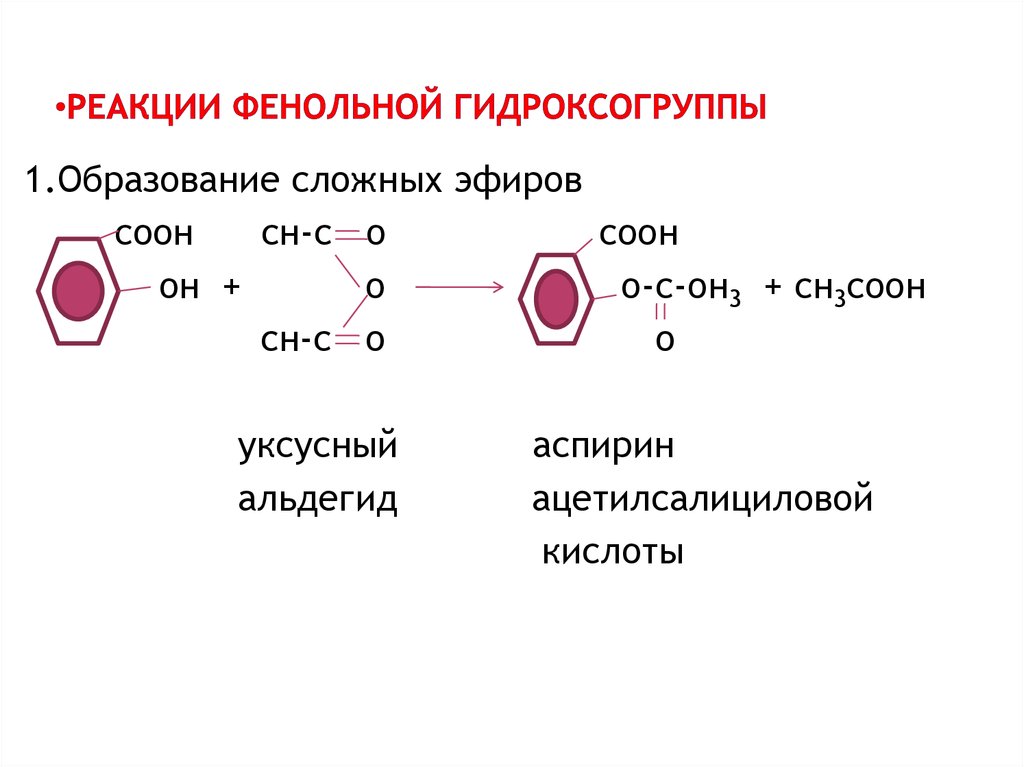
16. Реакции фенольной гидроксогруппы
1.Образование сложных эфировсоон
сн-с о
соон
он +
о
о-с-он3 + сн3соон
сн-с о
о
уксусный
альдегид
аспирин
ацетилсалициловой
кислоты
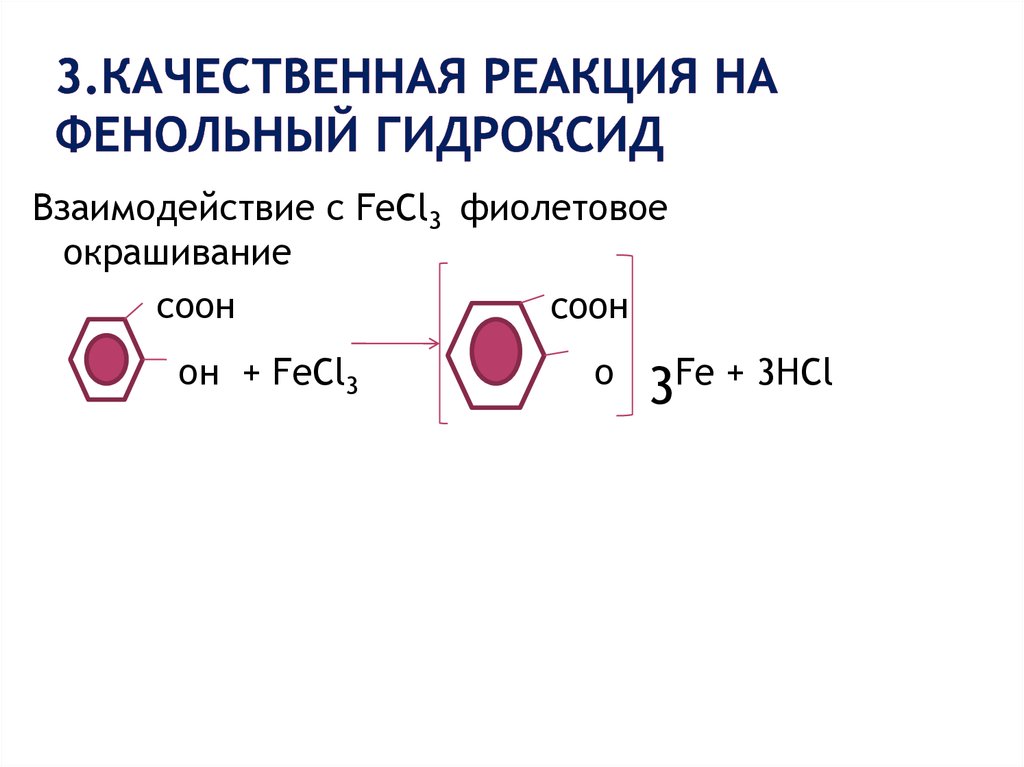
17. 3.Качественная реакция на фенольный гидроксид
Взаимодействие с FeCl3 фиолетовоеокрашивание
соон
cooн
он + FeCl3
о
Fe + 3HCl
3
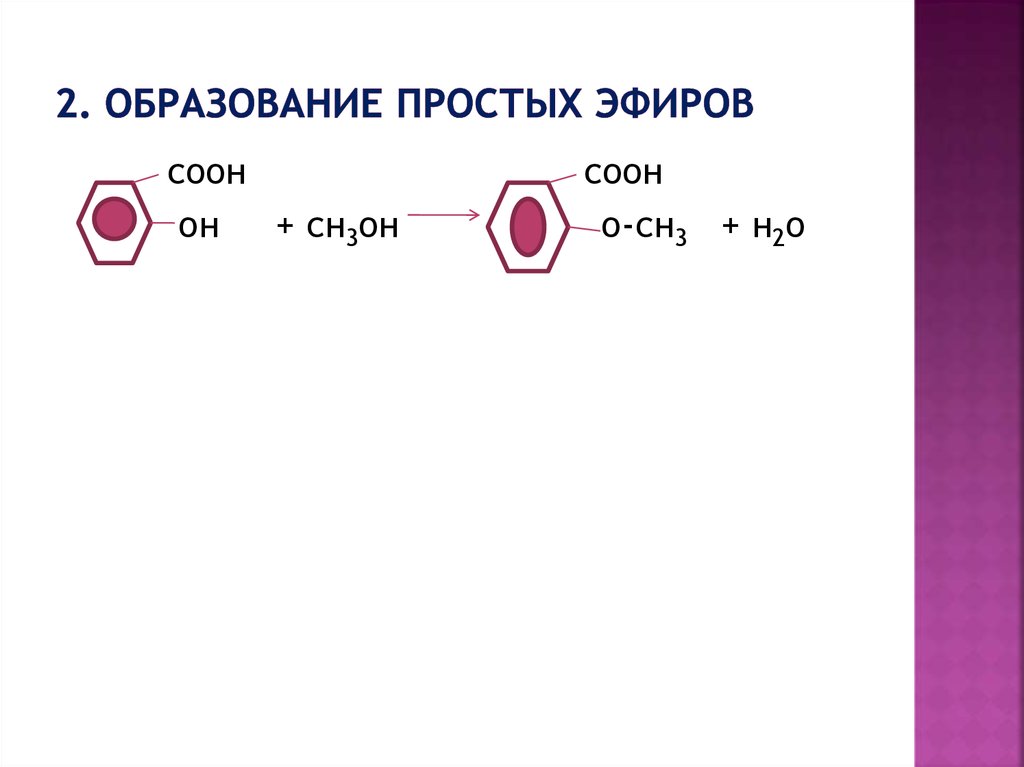
18. 2. Образование простых эфиров
соонон
+ сн3он
соон
о-сн3 + н2о
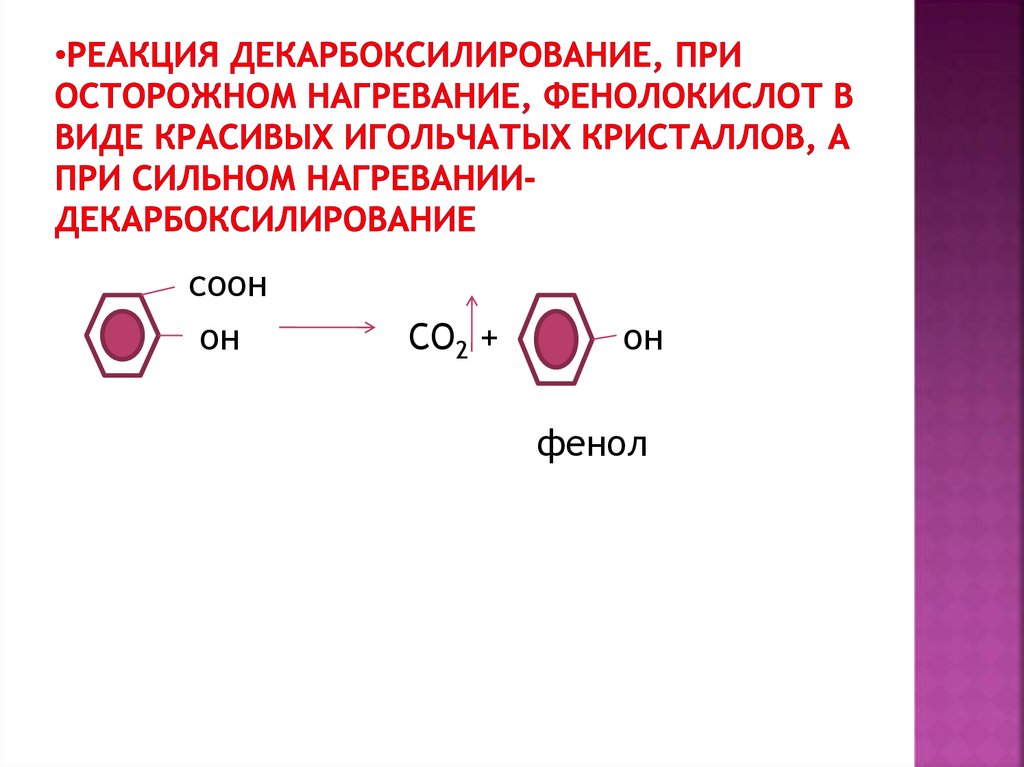
19. Реакция декарбоксилирование, при осторожном нагревание, фенолокислот в виде красивых игольчатых кристаллов, а при сильном
соонон
СО2 +
он
фенол
20. Фенолы представители
Салициловаякислота- кристаллическое
вещество трудно растворяется в воде,
возгоняется при нагревании.
Противоревматическое, жаропонижающие,
но раздражающие слизистые оболочки
21.
Аспирин-сложные эфир легко
гидролизуется, как в кислой, так и в
щелочных средах, что следует
учитывать при его хранение,
исключается контакт с водой, для
определения доброкачественности
аспирина используется реакция с FeCl3.
Аспирин не даёт фиолетовое
окрашивание, так как он не содержит
фенольный гидроксил, если и даёт,
значит испорчен, в медицине
используется как жаропонижающие и
анальгетическое средство.
22.
Салол(фенилсалицетат) -кристаллический
порошок, плохо растворимрим в воде, с FeCl 3
не даёт фиолетовое окрашивание,
гидролизуется медленно, дезинфицирующее
средство при заболевание кишечника.













 Химия
Химия








