Похожие презентации:
Сложные эфиры. Жиры. Мыло
1. Сложные эфиры. Жиры. Мыла.
2. Сложными эфирами называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён на углеводородный
радикал. Ихсостав соответствует общей
формуле:
3. Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами. Реакция называется реакцией этерификации
(от лат. аether – эфир).Катализаторами являются
минеральные кислоты.
Н+
4. Пример реакции этерификации
CH3COOH + НОС2Н5⇄ CH3COOС2Н5 + H2Oуксусная кислота
этиловый спирт
этиловый эфир
уксусной кислоты
(этилацетат)
Эта реакция обратима. Продукты реакции могут
взаимодействовать друг с другом с
образованием исходных веществ – спирта и
кислоты. Таким образом, реакция сложных
эфиров с водой – гидролиз сложного эфира –
обратна реакции этерификации.
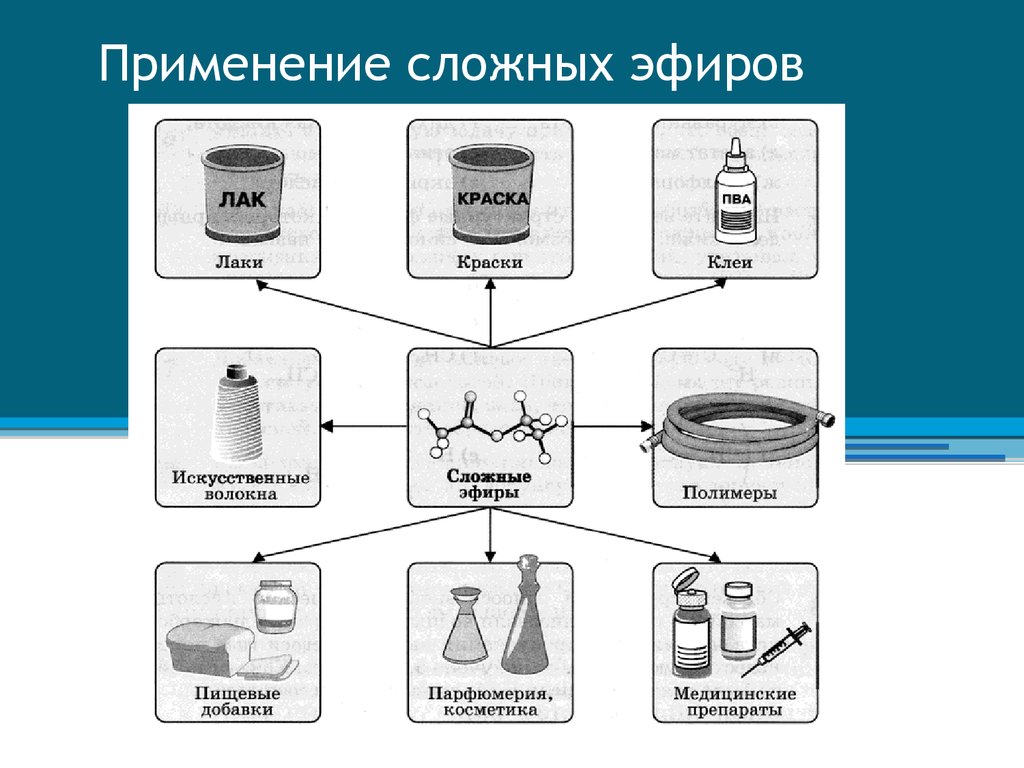
5. Применение сложных эфиров
6.
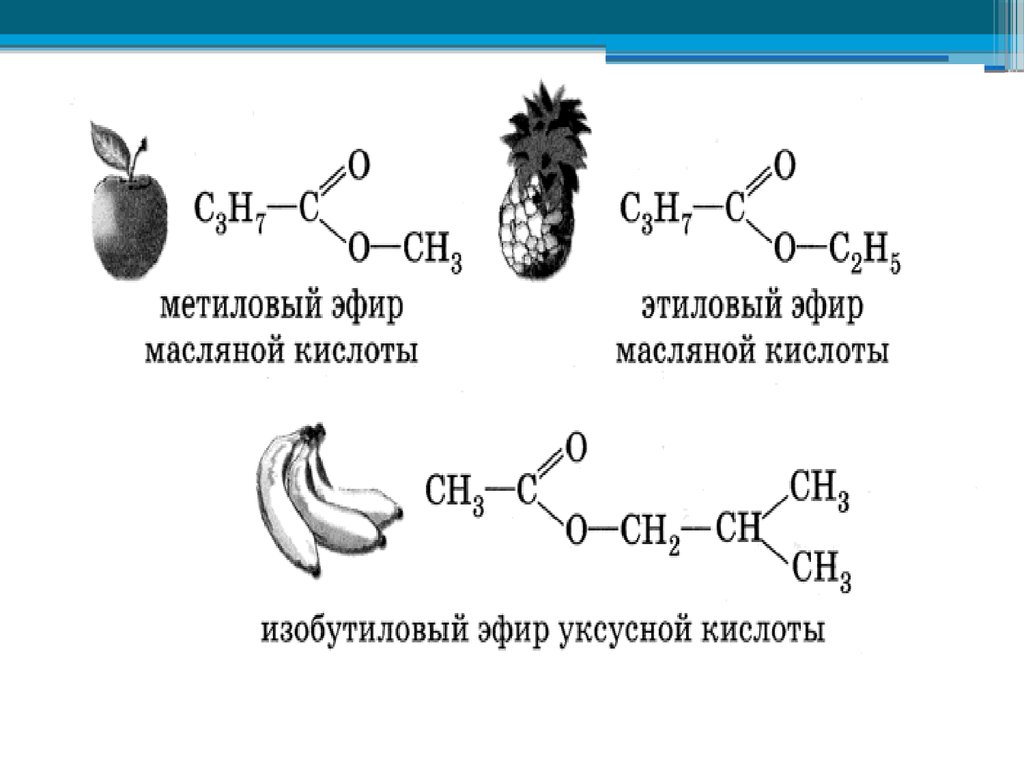
Сложные эфиры – жидкости,обладающие приятными
фруктовыми запахами. В воде
они растворяются очень мало,
но хорошо растворимы в
спиртах. Сложные эфиры
очень распространены в
природе. Их наличием
обусловлены приятные
запахи цветов и фруктов.
7.
ЖАСМИНОВЫЙ ЗАПАХС 2 Н 5 СОО СН 2 С 6 Н 5
Бензилацетат
8.
ГРУШЕВЫЙ ЗАПАХСН 3 СОО С2 Н 5
этилацетат
9.
10.
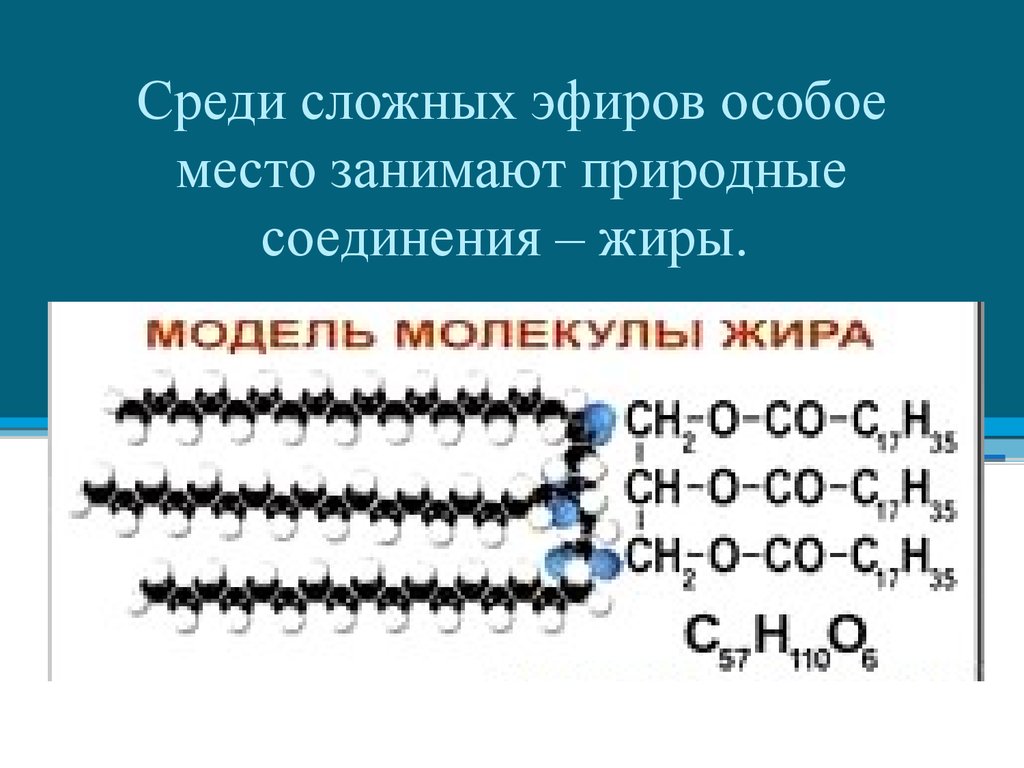
Среди сложных эфиров особоеместо занимают природные
соединения – жиры.
11.
Жиры – природные соединения,которые представляют собой
сложные эфиры глицерина и
высших карбоновых кислот
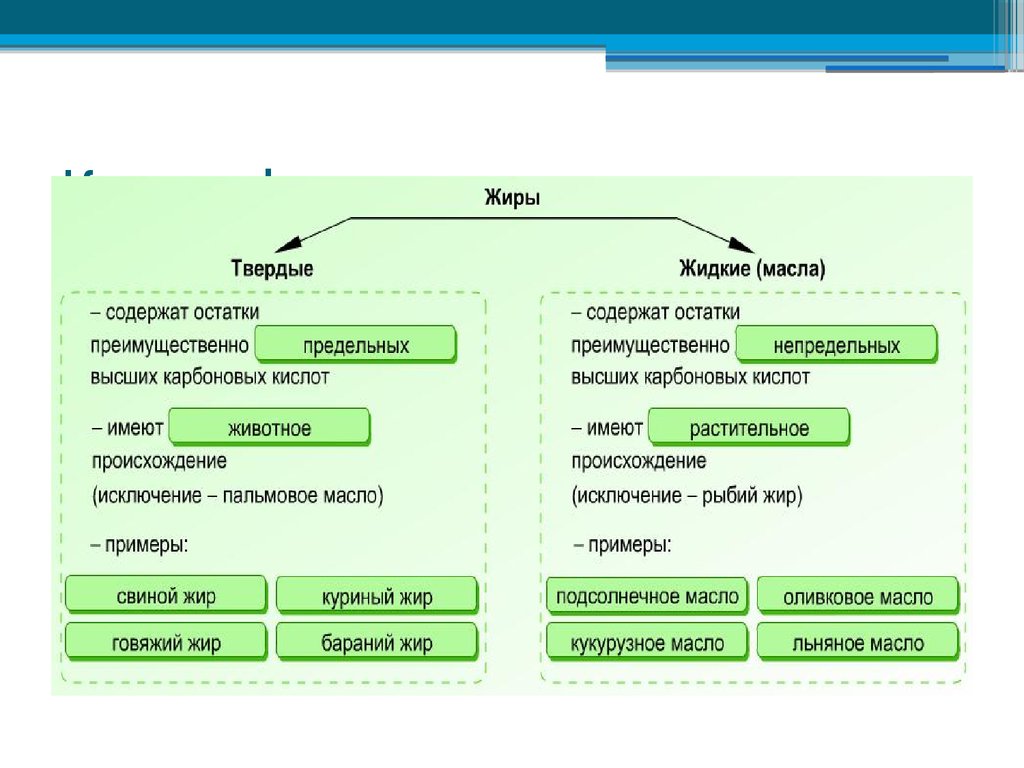
12. Классификация жиров
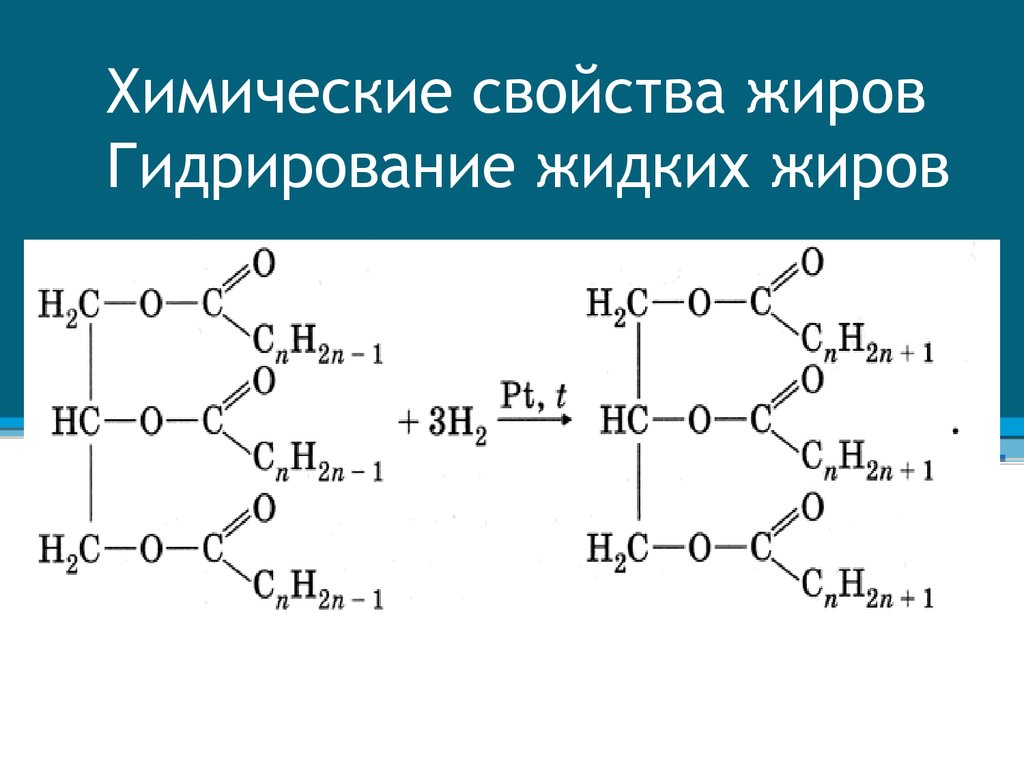
13. Химические свойства жиров Гидрирование жидких жиров
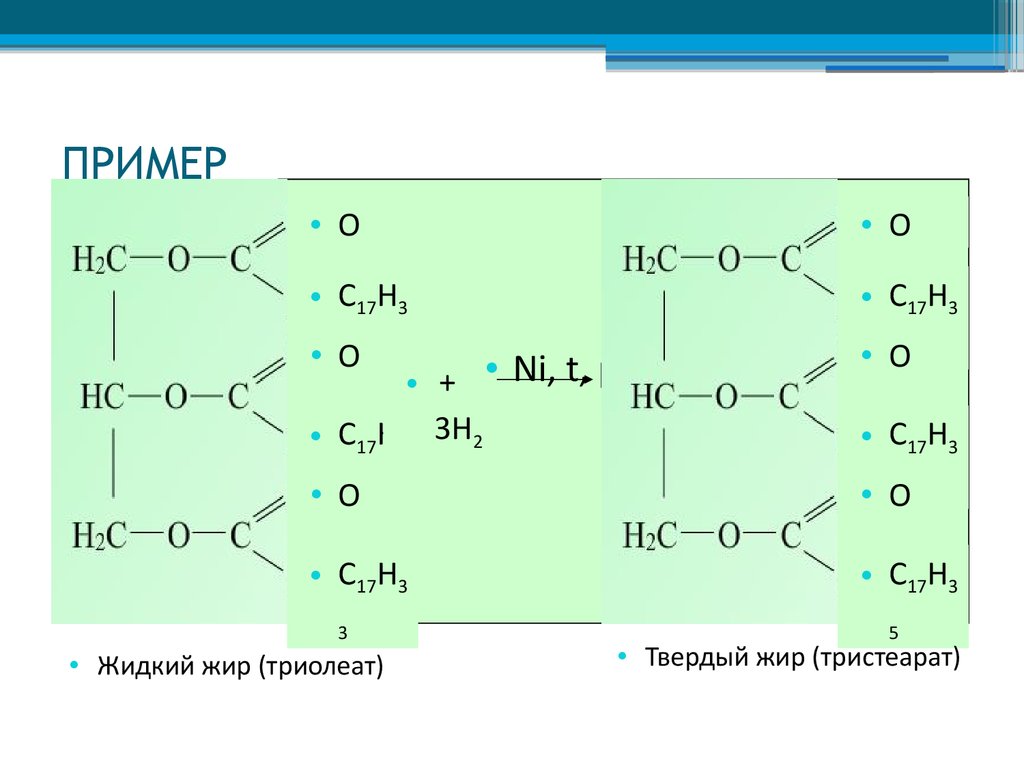
14. ПРИМЕР Гидрирования жидких жиров
ПРИМЕРГидрирования
• О жидких жиров
• О
• С17Н3
• С17Н3
• 3О
• 5О
• + • Ni, t, p
• С17Н3 3H2
• С17Н3
• 3О
• 5О
• С17Н3
• С17Н3
3
• Жидкий жир (триолеат)
5
• Твердый жир (тристеарат)
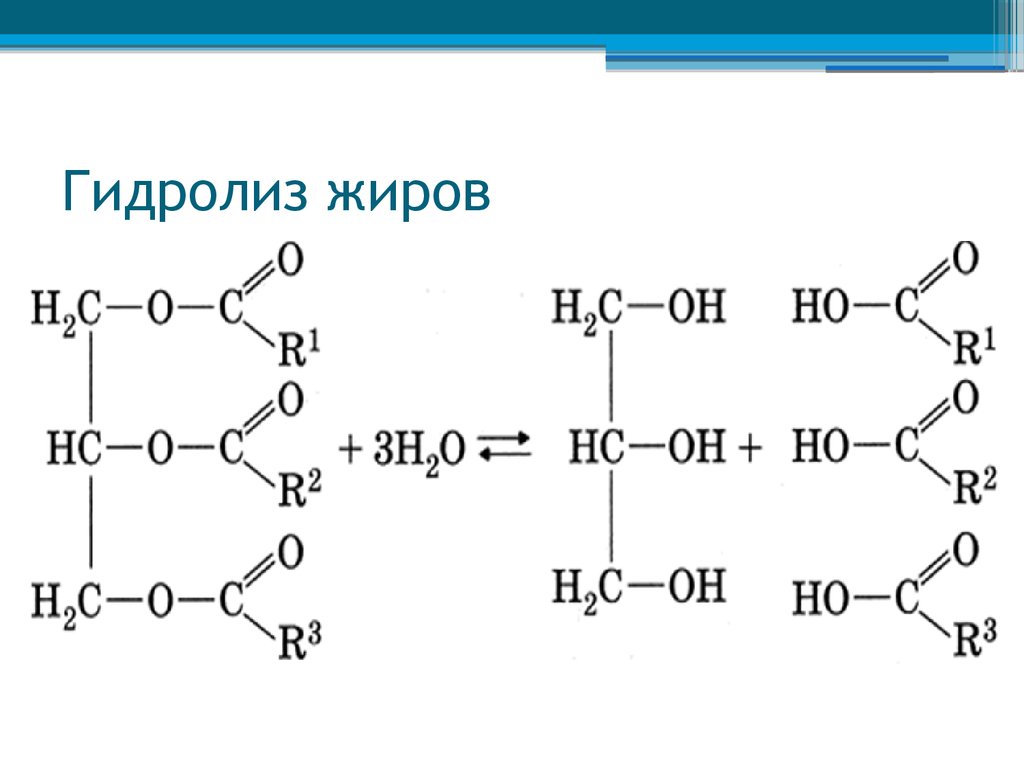
15. Гидролиз жиров
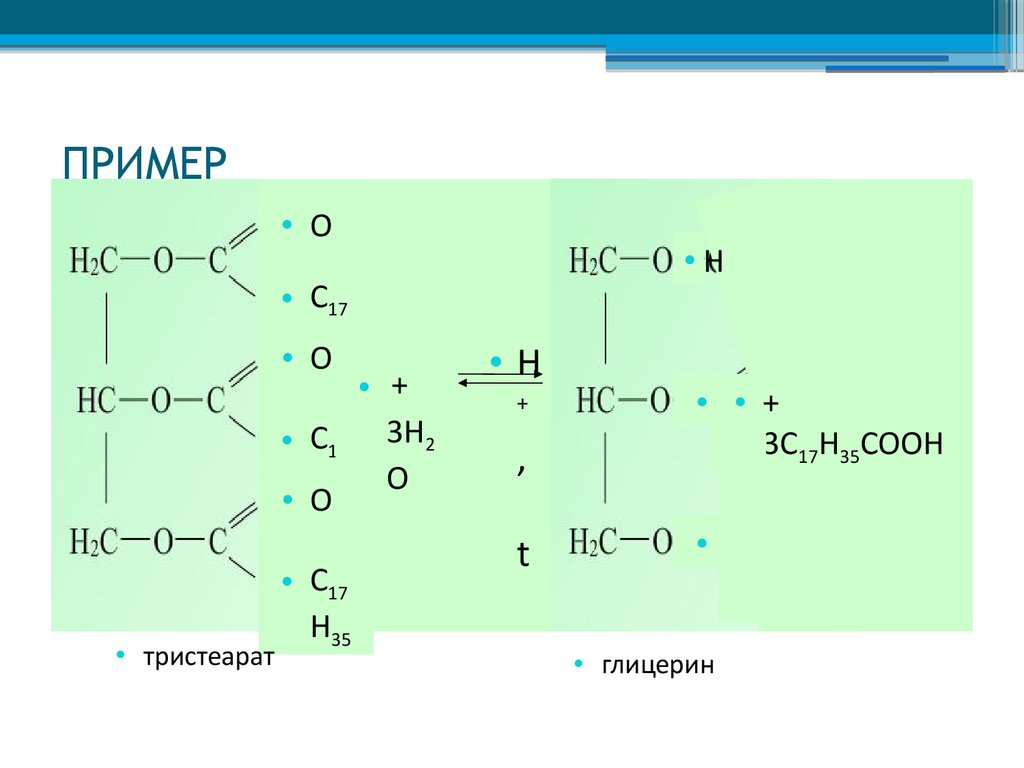
16. ПРИМЕР Гидролиза жиров
ПРИМЕРГидролиза•жиров
О
• С17
• Н
О35
• +
• С17 3H2
O
Н
35
• О
• тристеарат
• С17
Н35
•H
•H
,
• H• +
3C17H35COOH
t
• H
+
• глицерин
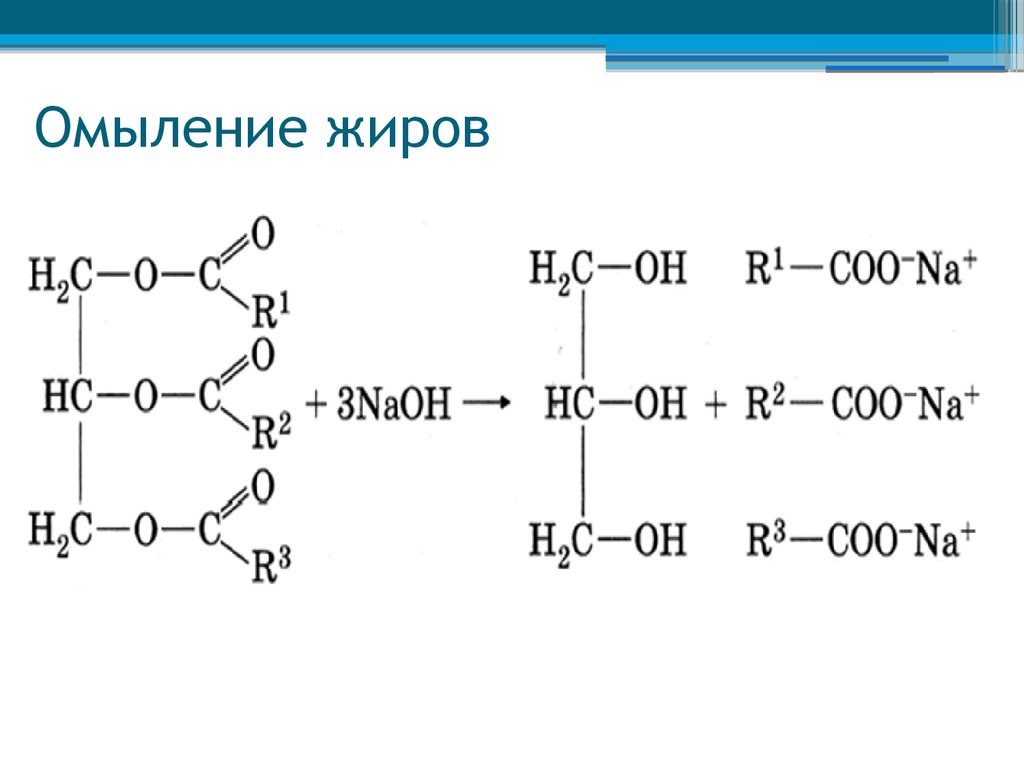
17. Омыление жиров
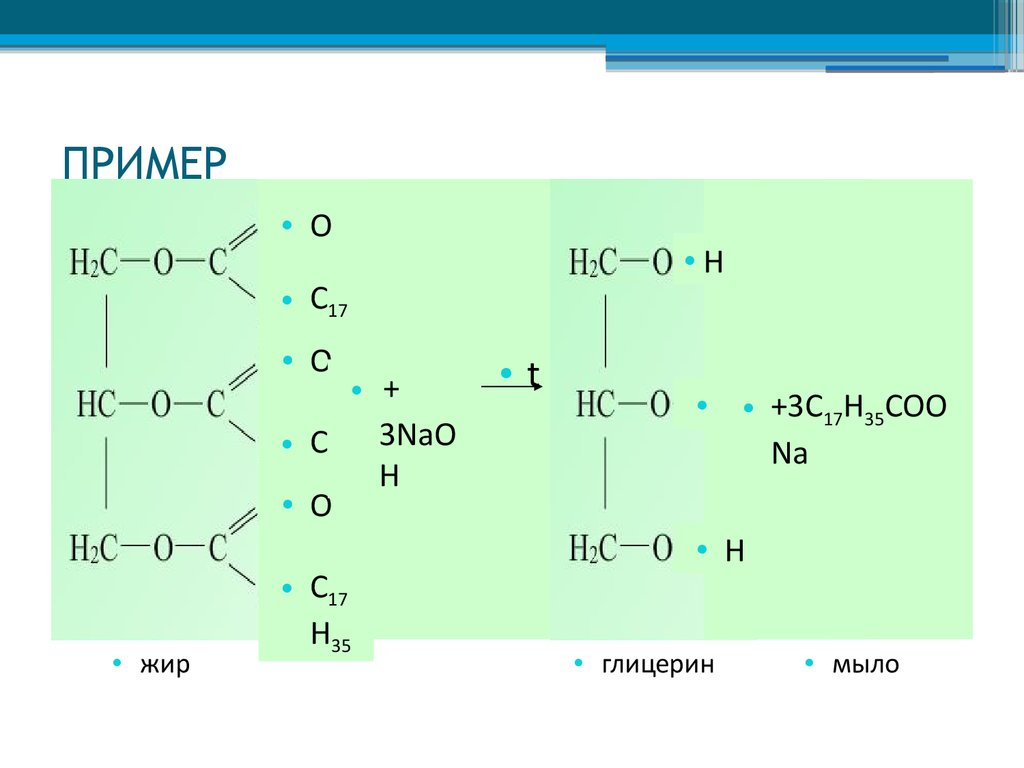
18. ПРИМЕР Омыления жиров
ПРИМЕРОмыления •жиров
О
• С17
• Н
О35
• +
• С17 3NaO
H
Н
• О35
• жир
• С17
Н35
•H
•t
• H• +3C17H35COO
Na
• H
• глицерин
• мыло
19.
Мыла – это соли карбоновыхкислот. Натриевые соли
карбоновых кислот – это
твердое мыло, а калиевые – это
жидкое мыло.
20. Применение жиров:
- Пищевые продукты- Сырье в производстве маргарина
- В медицине
- Производстве мыла
- В косметике
- В технике
- В лаках и красках.
21. Функции жиров
• Энергетическая (при полном расщеплении 1гжира до СО2 и Н 2О освобождается 38,9 кДж
энергии);
• Структурная (жиры – важный компонент
каждой клетки);
• Защитная (жиры накапливаются в
подкожных тканях и тканях, окружающих
внутренние органы).












 Химия
Химия








