Похожие презентации:
Титриметрический метод анализа
1. Титриметрический метод анализа
12. Титрование смесей протолитов
1. До начала титрования:2. До ТЭ:
рН рК HА1 lg
СA
1
С НA1
2
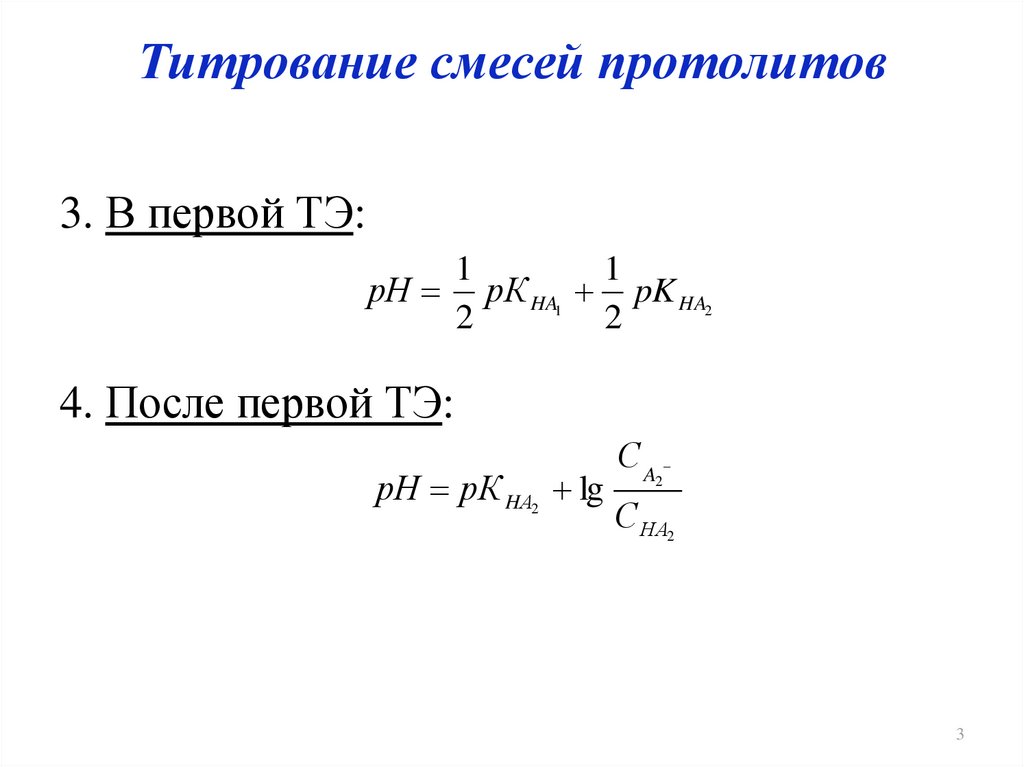
3. Титрование смесей протолитов
3. В первой ТЭ:1
1
рН рК HA1 pK HA2
2
2
4. После первой ТЭ:
рН рК HА2 lg
СA
2
С НA2
3
4. Титрование смесей протолитов
3. Во второй ТЭ:1
рН 7 рК HА2 lg C A
2
2
4. После второй ТЭ:
рН = 14 – рОН.
4
5. Ионная теория
HInd ↔+
H
+
Ind
5
6. Протолитическая теория
HInd + Н2О↔ H3О+ + Ind-6
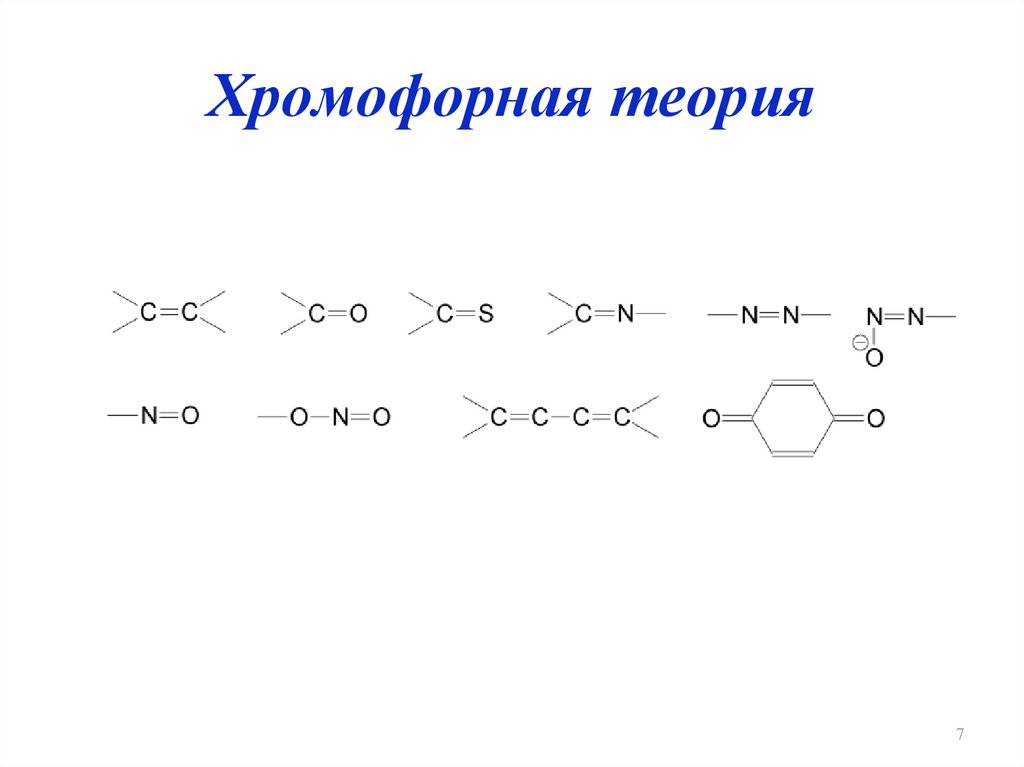
7. Хромофорная теория
78.
ХромофорыТаутомеры
Ауксохромы:
Hal-, –CH3, –OH, –OCH3, –NH2,
–NHCH3, –N(CH3)2
8
9. Требования к индикаторам
I. Индикатор должен обладать высоким светопоглощением,чтобы окраска даже его небольшого количества (СInd = 10-5 –
10-4 моль/л) была заметна для человеческого глаза. Большие
концентрации индикатора могут привести к заметному
расходу на него титранта.
II. Переход окраски должен быть контрастным.
III. Область перехода окраски должна быть как можно ýже.
IV. Изменение цвета индикатора должно происходить резко.
Количество протолита, необходимое для изменения цвета
индикатора должно быть настолько мало, чтобы не искажать
результаты титрования.
V. Изменение цвета индикатора должно быть обратимым.
9
10. Метиловый оранжевый
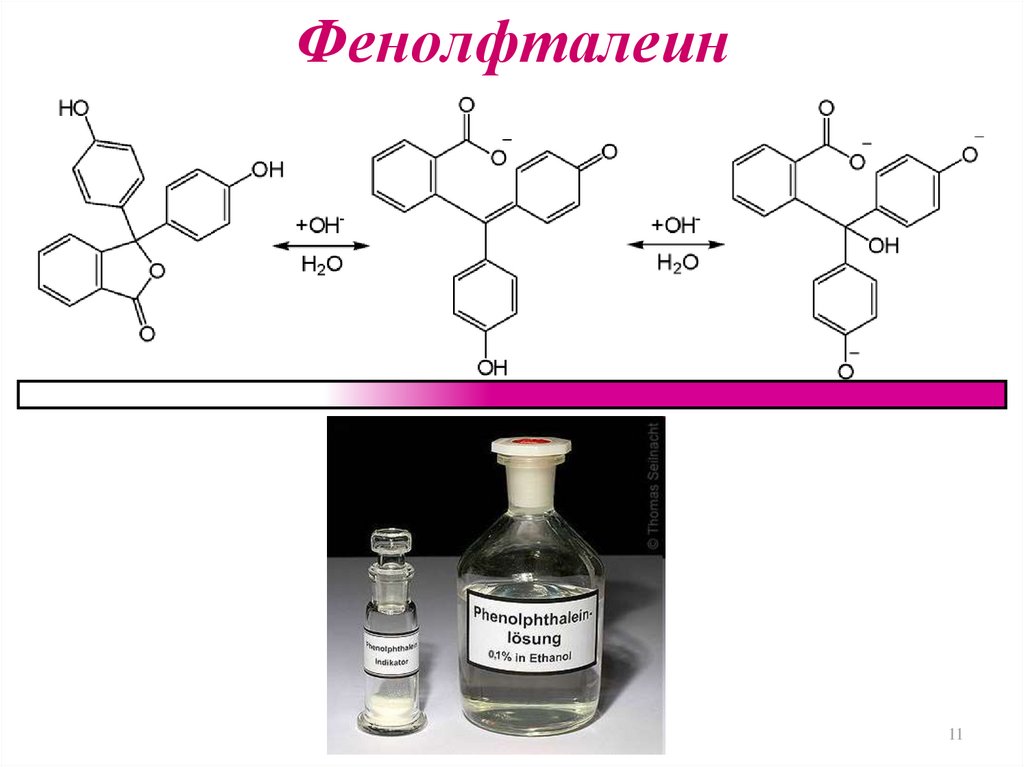
1011. Фенолфталеин
1112. Равновесие в растворе индикатора
HInd + H2O ↔ Ind- + H3O+12
13.
1314. Для одноцветного индикатора
1415. Показатель титрования
рТ – показатель титрованиярН = рКа
15
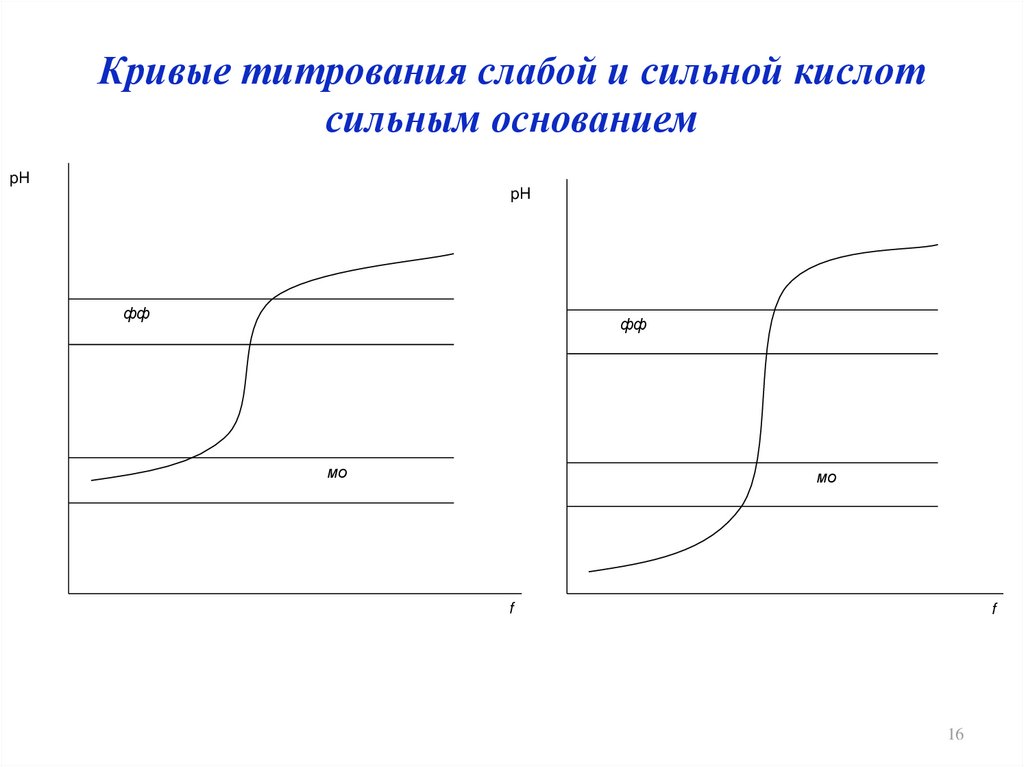
16. Кривые титрования слабой и сильной кислот сильным основанием
pHpH
фф
фф
мо
мо
f
f
16
17. Индикаторные погрешности
Оценка индикаторной погрешности:❖Графический вариант;
❖Расчетный способ.
Избыток титранта – ошибка положительная
Избыток титруемого вещества – ошибка
отрицательная
17
18. Водородная (гидроксониевая) ошибка
1. Если сильная кислота титруется сильнымоснованием и рТ < рНТЭ
2. Если сильное основание титруется
сильной кислотой и рТ > рНТЭ
3. Если слабое основание титруется
сильной кислотой и рТ > рНТЭ
18
19. Водородная (гидроксониевая) ошибка
1920. Гидроксильная ошибка
1. Если сильная кислота титруется сильнымоснованием и рТ > рНТЭ
2. Если сильное основание титруется
сильной кислотой и рТ < рНТЭ
3. Если слабая кислота титруется сильным
основанием и рТ > рНТЭ
20
21. Гидроксильная ошибка
2122. Кислотная или НА-ошибка
Если слабая кислота титруется сильнымоснованием и рТ < рНТЭ
22
23. Кислотная или НА-ошибка
2324. Основная или В-ошибка
Если слабое основание титруется сильнойкислотой и рТ > рНТЭ
24





















 Химия
Химия








