Похожие презентации:
Модификация моноцитов периферической крови аденозином с целью повышения их регенеративного потенциала при аутотрансплантации
1. модификация моноцитов периферической крови аденозином с целью повышения их регенеративного потенциала при аутотрансплантации
Государственное Бюджетное Образовательное УчреждениеВысшего Профессионального Образования
Сибирский Государственный Медицинский Университет
Центральная Научно-Исследовательская Лаборатория
НОЦ «Клинической и лабораторной иммуногенетики»
МОДИФИКАЦИЯ
МОНОЦИТОВ
ПЕРИФЕРИЧЕСКОЙ КРОВИ
АДЕНОЗИНОМ С ЦЕЛЬЮ
ПОВЫШЕНИЯ ИХ
РЕГЕНЕРАТИВНОГО
ПОТЕНЦИАЛА ПРИ
АУТОТРАНСПЛАНТАЦИИ
Студент 4 курса МБФ Мосунов Иван
2. Актуальность
Клеточная терапия является альтернативой трансплантации донорских
органов[Abdel-Latif A Adult bone marrow-derived cells for cardiac repair: a
systematic review and meta-analysis / Abdel-Latif A, Bolli R, Tleyjeh IM,
Montori VM, Perin EC, Hornung CA, Zuba-Surma EK, Al-Mallah M, Dawn B.//
Arch Intern Med. – 2007 - 167(10) - 989-97].
Доказано, что клеточная терапия стволовыми клетками способствует
восстановлению структуры ткани [Lipinski et al; 2007; Impact of intracoronary
cell therapy on left ventricular function in the setting of acute myocardial
infarction: a collaborative systematic review and meta-analysis of controlled
clinical trials. // J Am Coll Cardiol. doi:10.1016/j.jacc.2007.07.041]..
Паракринные факторы, обеспечивающие эффект терапии, не являются
уникальными для стволовых клеток и вырабатываются, хотя и в меньшей
степени, также клетками периферической крови.
3. Актуальность
Среди клеток периферической крови широким спектром секретируемых
цитокинов обладают моноциты. Эти клетки легко выделить из крови
человека в количестве, достаточном для культивирования и последующей
аутологической трансплантации [Abdel-Latif A Adult bone marrow-derived
cells for cardiac repair: a systematic review and meta-analysis / Abdel-Latif A,
Bolli R, Tleyjeh IM, Montori VM, Perin EC, Hornung CA, Zuba-Surma EK, AlMallah M, Dawn B.// Arch Intern Med. 59 – 2007 - 167(10) - 989-97; Burchfield
et al; 2008; Role of paracrine factors in stem and progenitor cell mediated cardiac
repair and tissue fibrosis // Fibrogenesis Tissue Repair. doi:10.1186/1755-1536-14].
Аденозин (эндогенный нуклеозид), образующийся в повышенных
количествах при повреждении ткани, в условиях воспаления и гипоксии,
влияет на выработку паракринных факторов различными клетками, в том
числе моноцитами [Novitskiy et al.; 2008; Adenosine receptors in regulation of
dendritic cell differentiation and function. / Novitskiy SV, Ryzhov SV / Blood;
(ISI) Impact factor – 10.555 doi: 10.1182/blood-2008-02-136325].
4. Цель
Изучение
влияния
модифицированных
аденозином
моноцитов
периферической крови кроликов на процесс заживления термической
травмы кожных покровов.
Задачи
Провести модификацию моноцитов периферической крови кроликов
аденозином при 72-часовой стимуляции;
Осуществить экспериментальную оценку регенеративного потенциала
модифицированных аденозином клеток в модели in vivo.
5. Материалы и методы
забор крови у 30 лабораторных животных (кроликов);
выделение мононуклеарных клеток (МНК) из периферической крови
методом центрифугирования на градиенте Фиколла;
выделение моноцитов из МНК методом центрифугирования в градиенте
Перколла;
культивирование моноцитов в полной питательной среде с ростовыми
факторами и цитокинами;
стимуляция моноцитов с использованием негидролизируемого аналога
аденозина NECA (5’-N-этилкарбоксамидоаденозин), добавлением DMSO –
растворителя NECA – в качестве контроля.
моделирование термического ожога на освобожденном от шерсти участке
кожи под наркозом с помощью металлического стержня;
аутологическая трансплантация стимулированных (2-я группа) и не
стимулированных клеток (3-я группа), а также введение физиологического
раствора (контрольная группа) в место ожога;
6. Материалы и методы
вывод кроликов на 5 и 14 сутки с помощью CO2-асфиксии;
биопсия пограничного участка здоровой кожи с ожогом;
фиксация кусочков в 10% нейтральном забуференном формалине;
обезвоживание в изопропиловом спирте;
заливка в парафин по методике Ю.А.Криволапова;
приготовление срезов на микротоме;
окраска препаратов гематоксилином и эозином, по методу Ван Гизона;
морфометрия препаратов кожи.
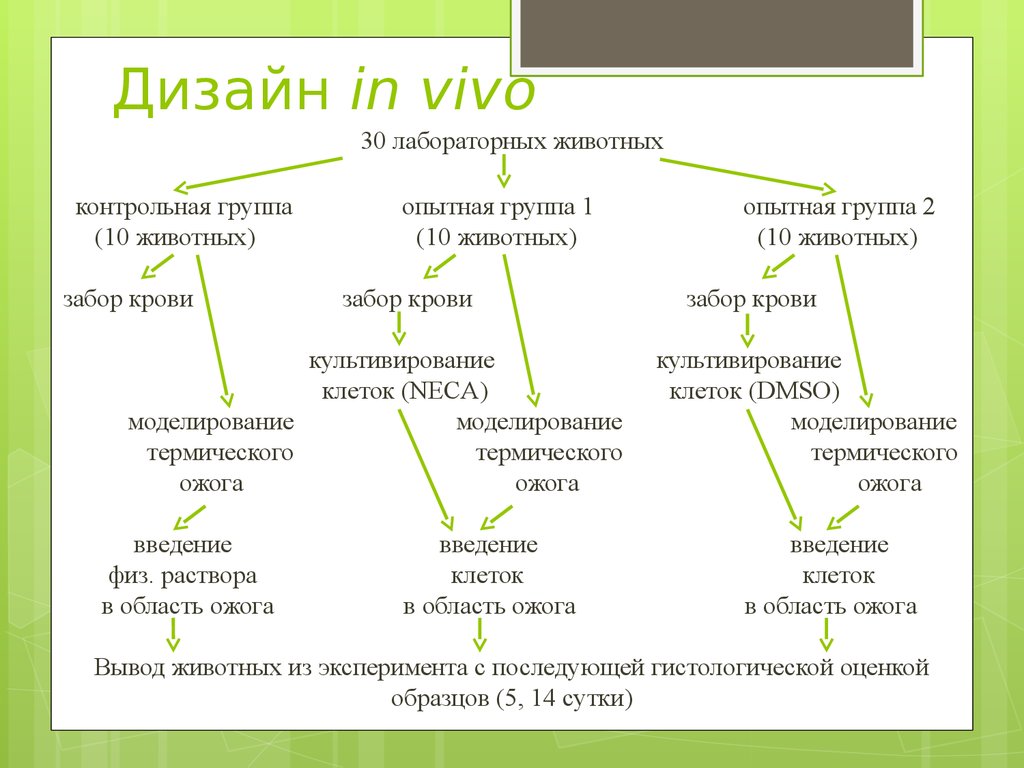
7. Дизайн in vivo
30 лабораторных животныхконтрольная группа
(10 животных)
забор крови
опытная группа 1
(10 животных)
забор крови
культивирование
клеток (NECA)
моделирование
моделирование
термического
термического
ожога
ожога
введение
физ. раствора
в область ожога
введение
клеток
в область ожога
опытная группа 2
(10 животных)
забор крови
культивирование
клеток (DMSO)
моделирование
термического
ожога
введение
клеток
в область ожога
Вывод животных из эксперимента с последующей гистологической оценкой
образцов (5, 14 сутки)
8. Ожидаемые результаты
Ожидается, что терапия моноцитами, модифицированными аналогомаденозина (NECA), будет активно способствовать регенерации
поврежденных тканей, имея при этом минимальное количество побочных
эффектов.
9. модификация моноцитов периферической крови аденозином с целью повышения их регенеративного потенциала при аутотрансплантации
МОДИФИКАЦИЯМОНОЦИТОВ
ПЕРИФЕРИЧЕСКОЙ КРОВИ
АДЕНОЗИНОМ С ЦЕЛЬЮ
ПОВЫШЕНИЯ ИХ
РЕГЕНЕРАТИВНОГО
ПОТЕНЦИАЛА ПРИ
АУТОТРАНСПЛАНТАЦИИ
Студент 4 курса МБФ Мосунов Иван








 Медицина
Медицина Биология
Биология