Похожие презентации:
Растворы. Виды выражения концентрации
1.
РастворыРаствор – термодинамически устойчивая, гомогенная
на молекулярном уровне система, состоящая из двух
и более компонентов
Растворы классифицируют на растворы электролитов
и растворы неэлектроитов
Также по применяемой модели различают растворы
идеальные, предельно разбавленные и реальные
1
2.
РастворыМежду растворителем и растворённым веществом с
термодинамической точки зрения нет разницы
Растворителем принято называть тот компонент:
А. Который в том же агрегатном состоянии, что и
раствор
Б. Содержание которого больше
В. Который будет кристаллизоваться из жидкого
раствора первым
Растворитель
индексом «1»
принято
обозначать
подстрочным
2
3.
Виды выражения концентрации3
4.
Парциальные молярные величины4
5.
Парциальные молярные величины5
6.
Парциальные молярные величины6
7.
Парциальные молярные величиныПервый закон Гиббса-Дюгема
7
8.
Второй закон Гиббса-Дюгема8
9.
Относительные молярные парциальные величины9
10.
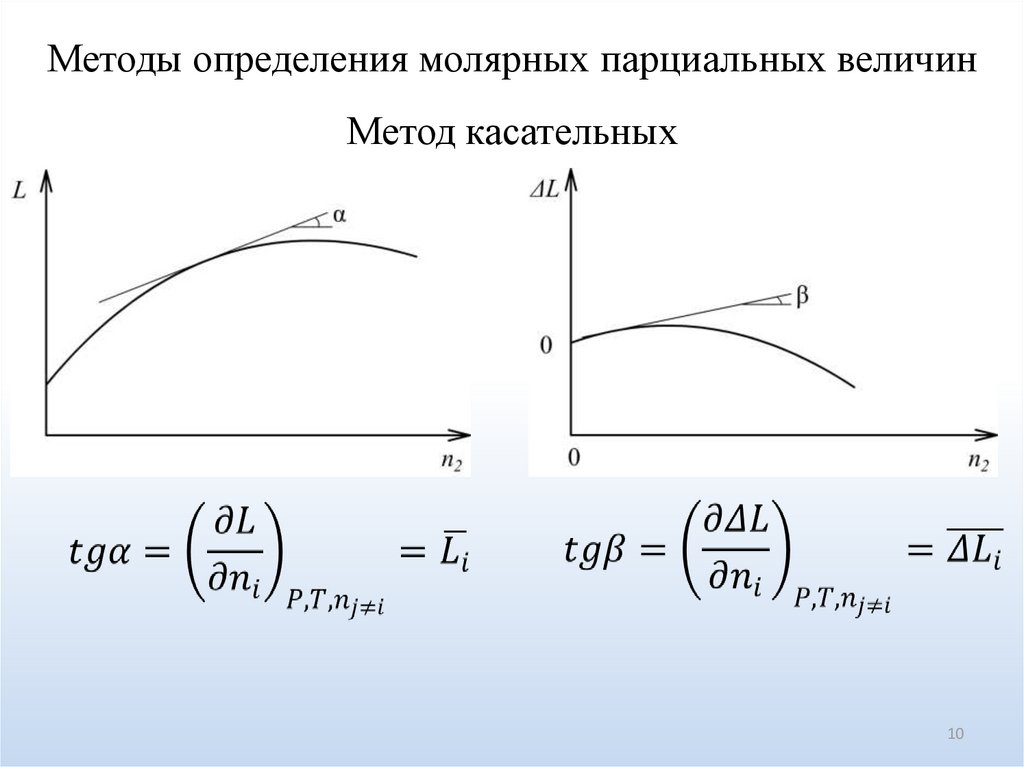
Методы определения молярных парциальных величинМетод касательных
10
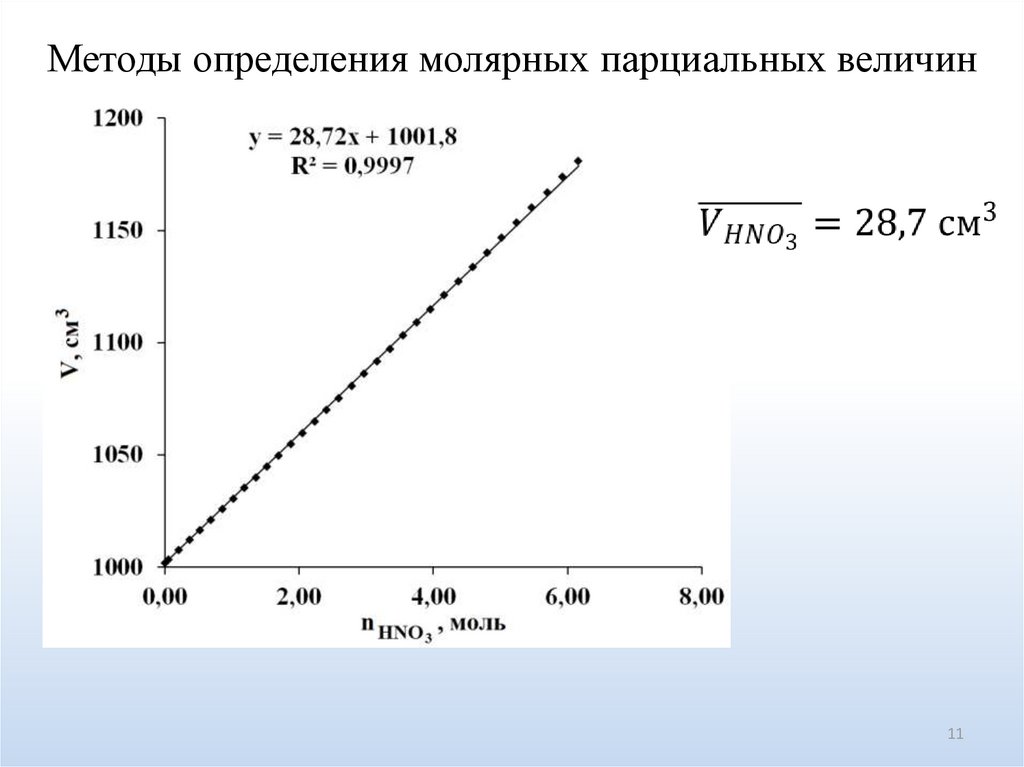
11.
Методы определения молярных парциальных величин11
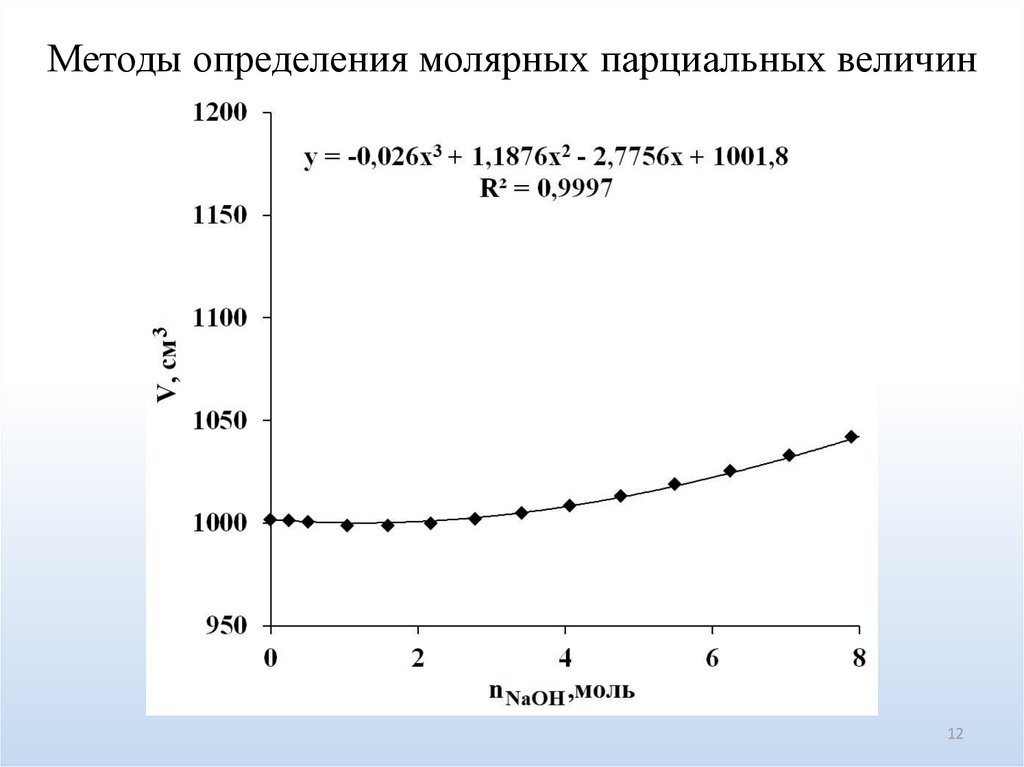
12.
Методы определения молярных парциальных величин12
13.
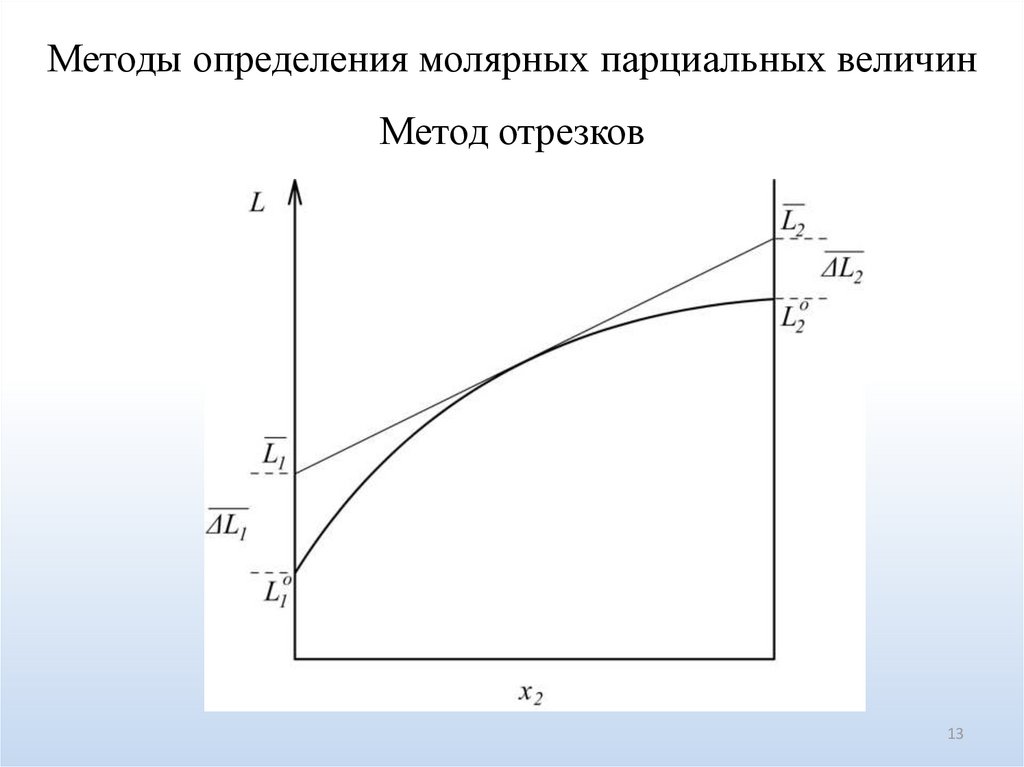
Методы определения молярных парциальных величинМетод отрезков
13
14.
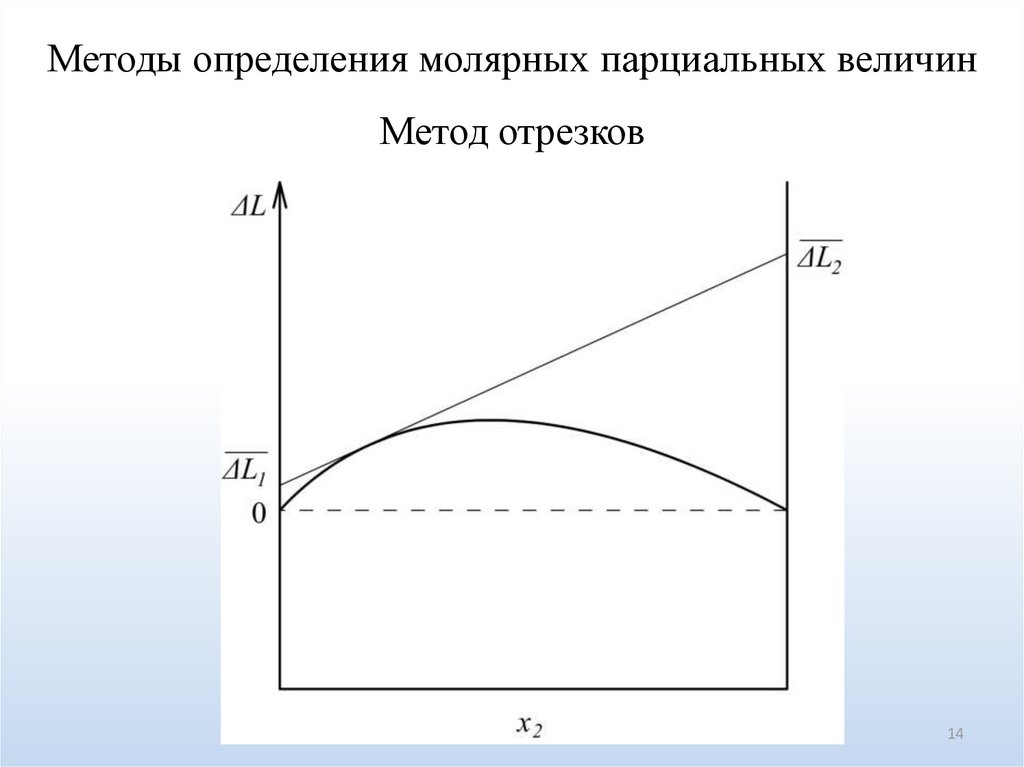
Методы определения молярных парциальных величинМетод отрезков
14
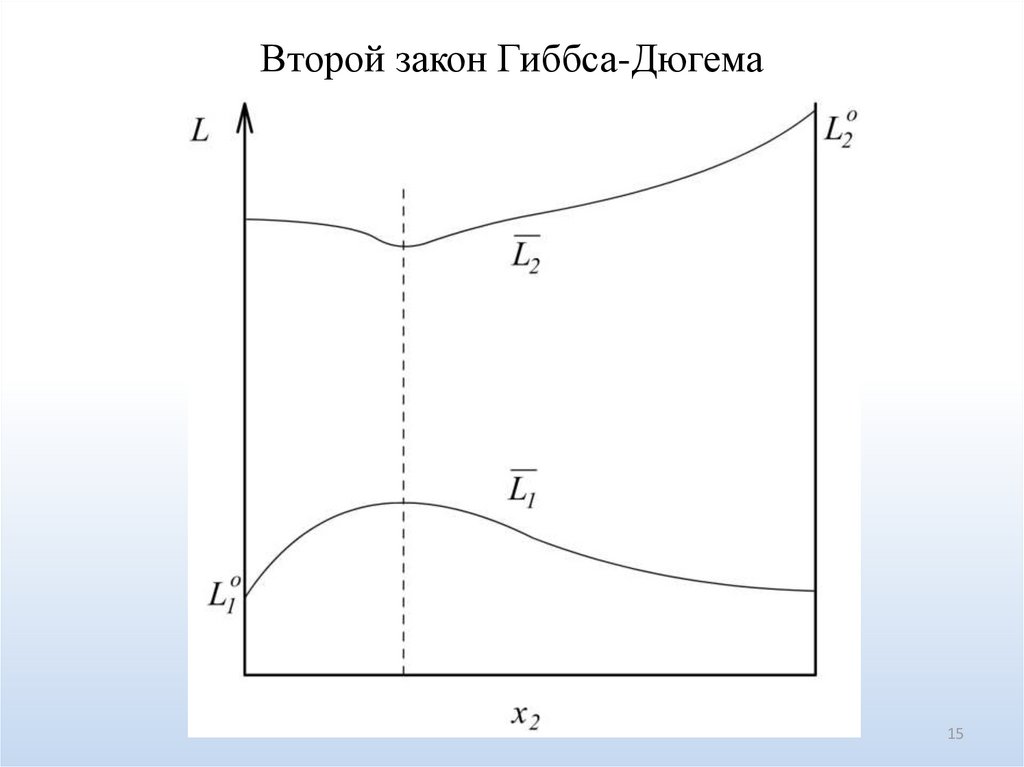
15.
Второй закон Гиббса-Дюгема15
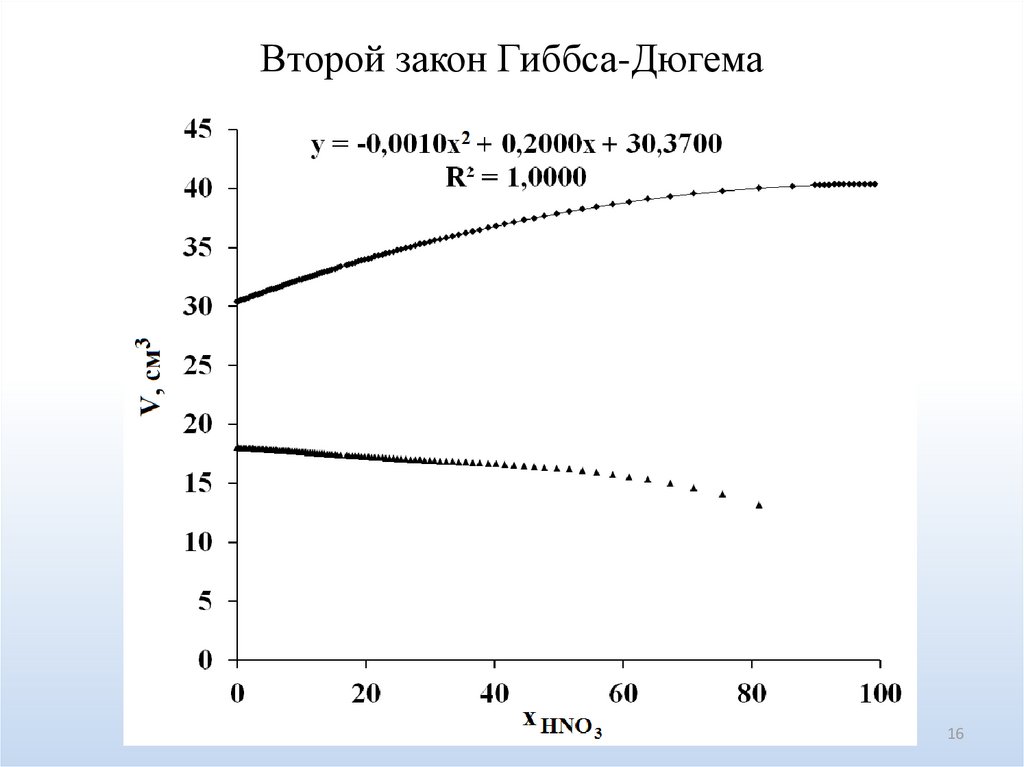
16.
Второй закон Гиббса-Дюгема16
17.
Идеальные растворы17
18.
Реальные растворы18
19.
Предельно разбавленные растворы19












 Химия
Химия








