Похожие презентации:
Органическая химия. Классификация и номенклатура органических соединений (ОС). Пространственное строение ОС
1.
ФГБОУ ВО ОрГМУ Минздрава РоссииКАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ ХИМИИ
Введение в предмет.
Классификация и номенклатура
органических соединений (ОС).
Пространственное строение ОС.
Д.М.Н., ДОЦЕНТ ИВАНОВА Е.В.
г. ОРЕНБУРГ, 2019
2.
Органическая химияэто химия соединений углерода.
Соединения, в состав которых входит углерод,
называются органическими (углеводороды). Кроме углерода,
они почти всегда содержат водород, довольно часто – кислород,
азот и галогены, реже – фосфор, серу и другие элементы.
Огромное количество органических соединений (свыше 20 млн.;
ОС — самый обширный класс химических соединений) и их
специфика объясняются строением атома С, природой химических
связей между этими атомами, а также связей с другими атомами.
ОРГАНИЗМ – ОРГАНИЧЕСКОЕ
3.
Й.Я. Берцелиус(1808) –
предложил термин
«органическая
химия» для
обозначения
химии веществ,
образующихся
только в живых
организмах с
участием особой
жизненной силы
(виталистические
воззрения)
http://crystal.geology.spbu.ru
4.
http://crystal.geology.spbu.ru5.
Краткая история развития органической химии•Синтез мочевины (1828 г.).
•Синтез уксусной (1845г.),
салициловой (1860г.),
муравьиной кислоты (1861 г.).
•Получение жиров (1854 г.).
•Создание теории типов (1853 г.).
• Открытие четыре валентности атома
углерода (1857г.).
• Открытие способности атома
углерода образовывать длинные цепи
(1858 г.).
•Создание первой теории в ОХ – теории радикалов (первая половина XIX в.)
Фридрих Велер Адольф Колбе
(1800-1882)
(1818-1884)
Пьер Бертло
(1827-1907)
Шарль Жерар Фридрих Кекуле
(1816-1856)
(1829-1896)
6.
Теория строения А.М. БутлероваАлександр Михайлович Бутлеров
(1828 - 1886)
6
Русский химик-органик.
Академик Петербургской АН.
Создал и обосновал теорию химического
строения органических соединений.
Объяснил явление изомерии.
Открыл реакцию полимеризации.
Синтезировал многие ОС.
Написал в 1864 г. “Введение к полному изучению органической химии”
- первое в истории науки руководство, основанное на теории
химического строения.
Создал школу химиков. Активно боролся за признание Академией
наук заслуг русских ученых.
Был поборником высшего образования для женщин.
Труды по сельскому хозяйству, пчеловодству, этимологии.
7.
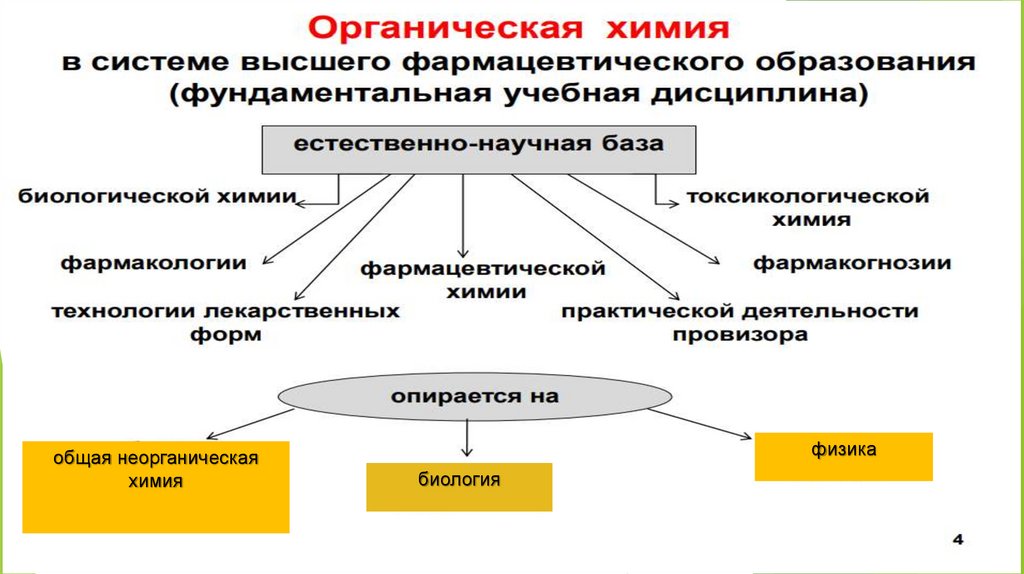
общая неорганическаяхимия
7
физика
биология
8.
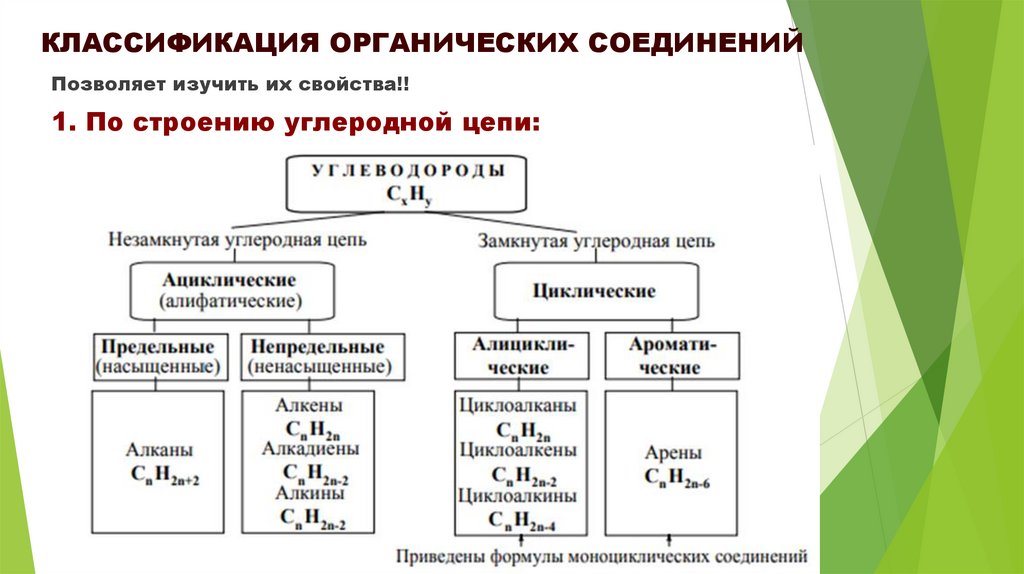
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙПозволяет изучить их свойства!!
1. По строению углеродной цепи:
9.
2. По природефункциональных групп
органические соединения
делят на классы.
Функциональные группы – это
заместители неуглеводородной
природы, определяющие
принадлежность к классу ОС и
типичные химические свойства
соединений.
Функциональные группы
связаны с углеродным
скелетом и химические
превращения идут за счет
этих групп без изменения
углеродного скелета!
10.
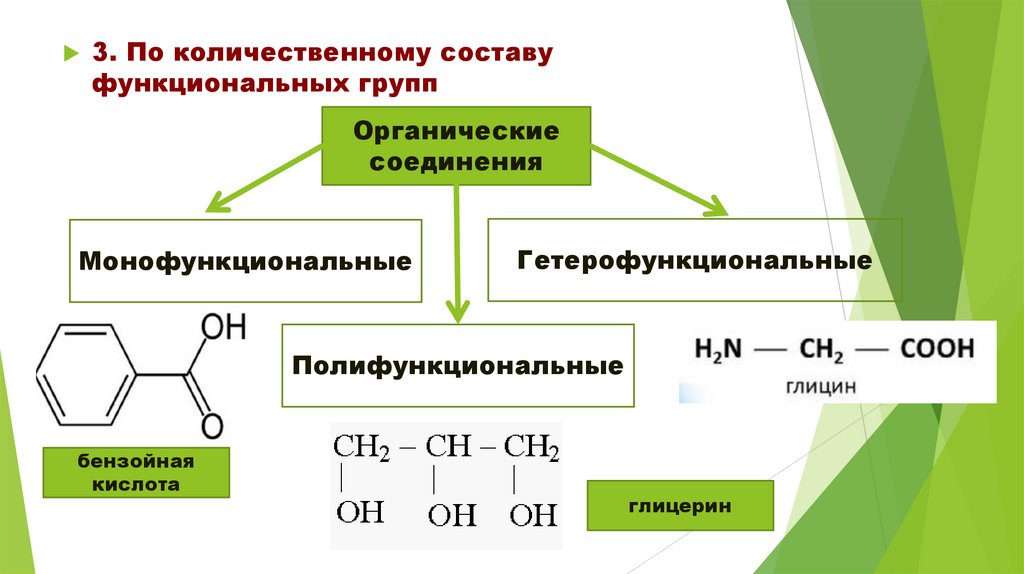
3. По количественному составуфункциональных групп
Органические
соединения
Монофункциональные
Гетерофункциональные
Полифункциональные
бензойная
кислота
глицерин
11.
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙНоменклатура – это система правил, с помощью которых называют
индивидуальные соединения!!!
В настоящее время в органической химии общепринятой
является систематическая номенклатура, разработанная
Международным союзом чистой и прикладной химии
(IUPAC). Наряду с ней сохранились и используются
тривиальная и радикально-функциональная
(рациональная) номенклатуры.
Тривиальная номенклатура состоит из исторически сложившихся названий,
которые не отражают состава и строения вещества. Они являются случайными и
отражают природный источник вещества (молочная кислота, мочевина, кофеин),
характерные свойства (глицерин, гремучая кислота), способ получения
(пировиноградная кислота, серный эфир), имя первооткрывателя (кетон
Михлера, углеводород Чичибабина), область применения (аскорбиновая
кислота). Преимуществом тривиальных названий является их лаконичность,
поэтому употребление некоторых из них разрешено правилами IUPAC, но они не
могут быть объединены в систему. Тривиальные названия широко используются
в классах углеводы, аминокислоты, стероиды, алкалойды и др.
12.
Рациональная (радикально-функциональная) номенклатураиспользуется для названий простых моно- и бифункциональных
соединений и некоторых классов природных соединений. Название
простых соединения складывается из 2-х элементов – названия
углеводородного радикала и названия характеристической
(функциональной) группы или соответствующего класса соединений.
В качестве локантов, как правило, используются греческие буквы.
Например:
метилэтилкетон
этиловый спирт,
масляный альдегид
Если функциональных групп несколько, выбирают родоначальную
структуру, выбор довольно произволен. Заместители называют в
приставках (α-,β-, γ- и т.д. или орто-, мета-, пара-положение).
13.
Систематическая (заместительная) номенклатураСоединение называют в следующем порядке:
является научной и отражает
состав, химическое и пространственное строение соединения. Название соединения отражает определенные
элементы строения молекулы вещества. В её основе лежит выбор родоначальной структуры (самая длинная
углеродная цепь или цикл, лежащий в основе соединения).
1. Выбирают старшую функциональную группу (если она есть) по таблице старшинства.
Её название дает окончание.
1. Определяют родоначальную структуру – углеводород, лежащий в основе соединения и
нумерую атомы С так, чтобы старшая группа или заместитель получили наименьший
порядковый номер. Родоначальная структура составляет корень слова.
2. В названии указывают степень насыщенности родоначальной структуры
(суффикс – ан, -ен, -ин, -диен).
1. Младшие функциональные группы, неуглеродные группы и радикалы называют в
приставке в алфавитном порядке.
Заместителем называют любую функциональную группу или радикал, связанный с
родоначальной структурой (атом, или группа атомов, замещающая атом Н в род.структуре)
4
2
3
1
14.
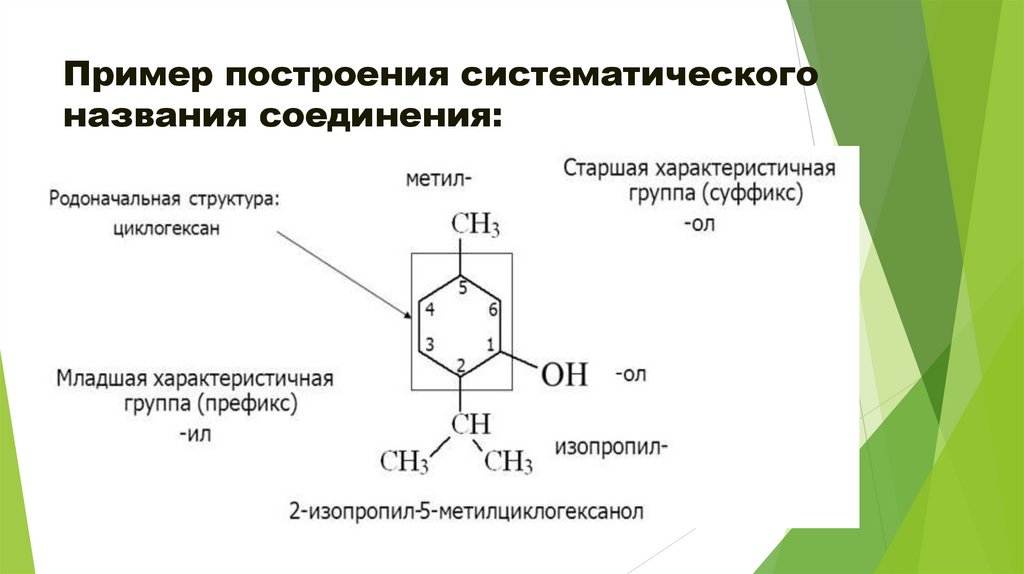
Пример построения систематическогоназвания соединения:
15.
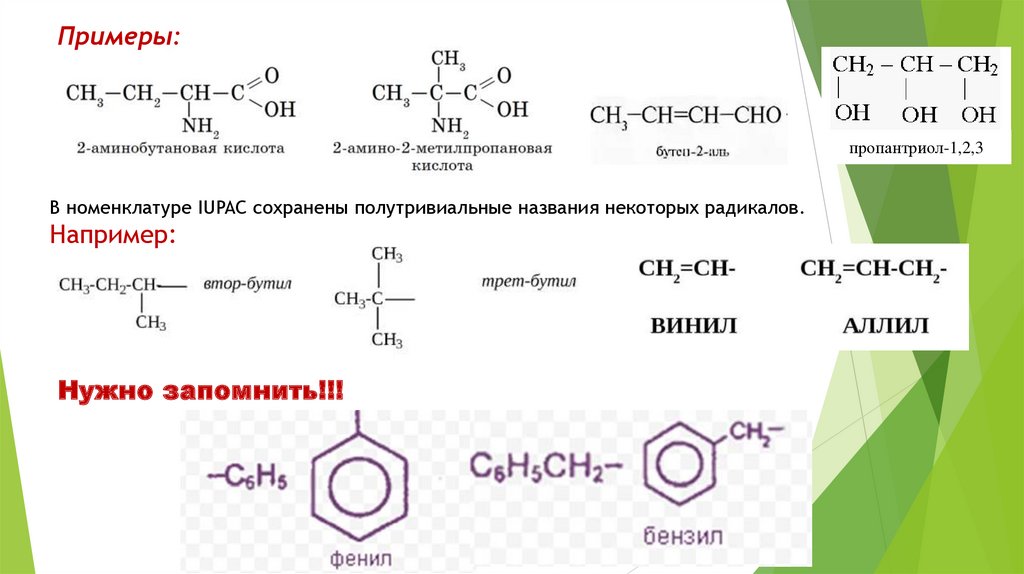
Примеры:пропантриол-1,2,3
В номенклатуре IUPAC сохранены полутривиальные названия некоторых радикалов.
Например:
Нужно запомнить!!!
16.
Пространственное строение ОС Стереохимия.Строение органического соединения – это
последовательность связей атомов в
молекуле, с учетом природы связей.
Важнейшая характеристика молекулы –
это её состав.
Но в ОХ одному составу может
соответствовать несколько соединений.
17.
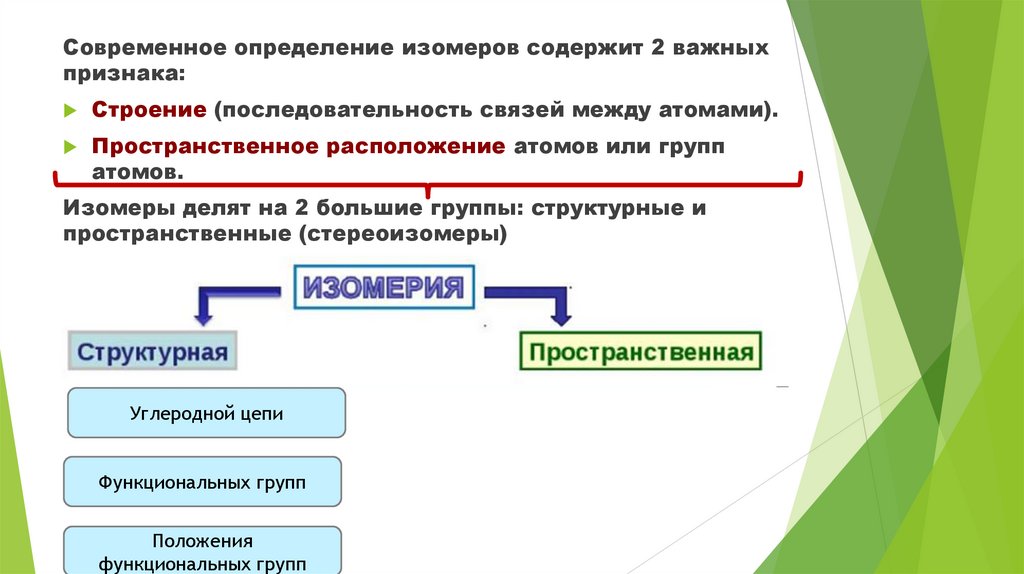
Современное определение изомеров содержит 2 важныхпризнака:
Строение (последовательность связей между атомами).
Пространственное расположение атомов или групп
атомов.
Изомеры делят на 2 большие группы: структурные и
пространственные (стереоизомеры)
Углеродной цепи
Функциональных групп
Положения
функциональных групп
18.
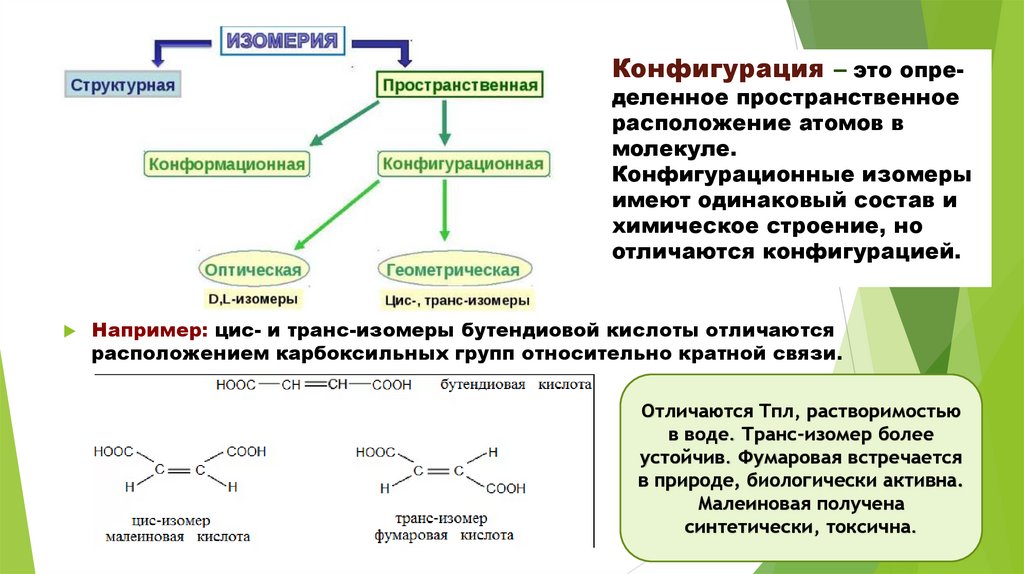
Конфигурация – это опре-деленное пространственное
расположение атомов в
молекуле.
Конфигурационные изомеры
имеют одинаковый состав и
химическое строение, но
отличаются конфигурацией.
Например: цис- и транс-изомеры бутендиовой кислоты отличаются
расположением карбоксильных групп относительно кратной связи.
Отличаются Tпл, растворимостью
в воде. Транс-изомер более
устойчив. Фумаровая встречается
в природе, биологически активна.
Малеиновая получена
синтетически, токсична.
19.
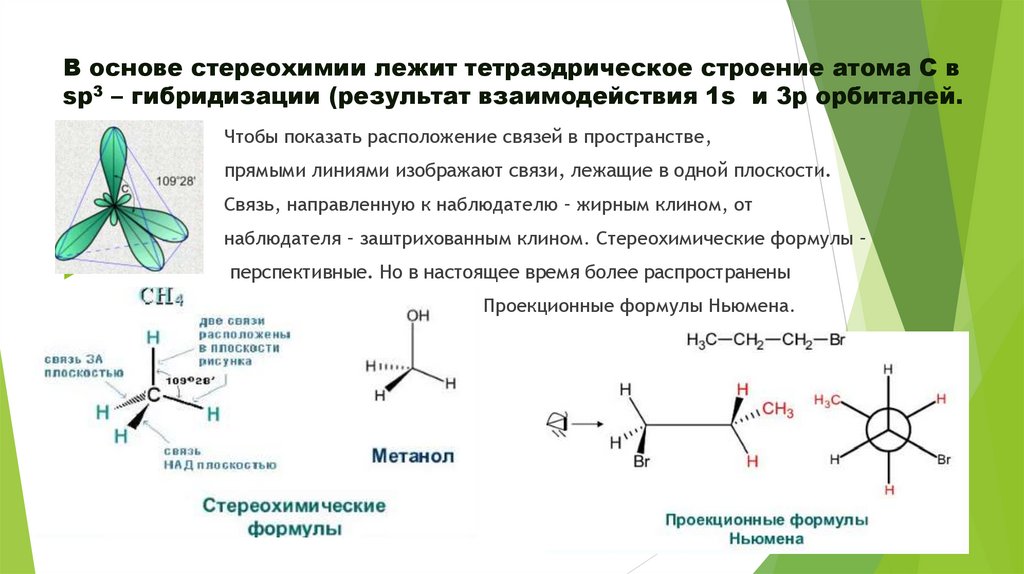
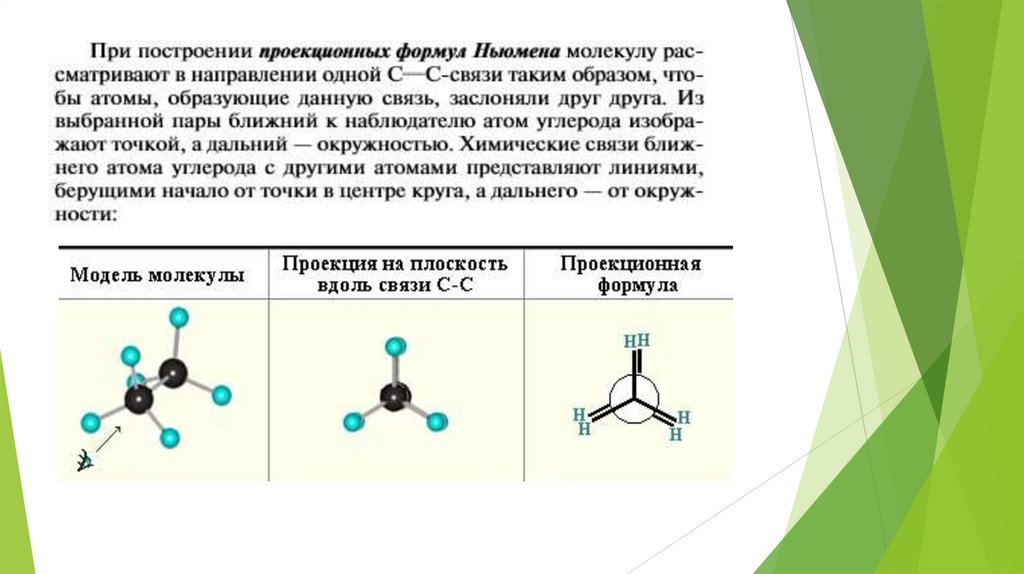
В основе стереохимии лежит тетраэдрическое строение атома С вsp3 – гибридизации (результат взаимодействия 1s и 3р орбиталей.
Чтобы показать расположение связей в пространстве,
прямыми линиями изображают связи, лежащие в одной плоскости.
Связь, направленную к наблюдателю – жирным клином, от
наблюдателя – заштрихованным клином. Стереохимические формулы –
перспективные. Но в настоящее время более распространены
Проекционные формулы Ньюмена.
20.
21.
Многие органические молекулы обладают плоскостьюсимметрии, у некоторых она отсутствует и такие молекулы не
совместимы со своим зеркальным изображением. Их
называют хиральными. Примером может служить правая и
левая рука, перчатки, ботинки и т.д.
Центром хиральности служит sp3-гибридный атом
углерода, соединенный с 4-мя разными заместителями.
Такой атом называют асимметрическим.
В некоторых случаях
наличие такого атома
не является причиной
возникновения хиральности
(винная кислота) и наоборот.
Стереоизомеры делят на
энантио- и диастереомеры.
Зеркало Венеры, 1898, Edward Jones.
Все объекты на этой картине имеют
зеркальные отображения.
22.
a14
2
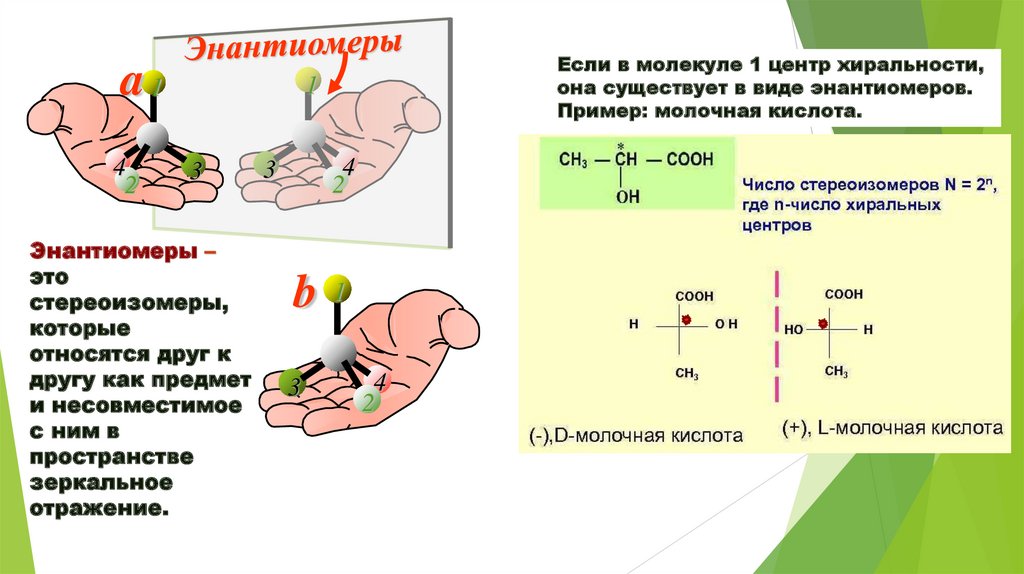
Если в молекуле 1 центр хиральности,
она существует в виде энантиомеров.
Пример: молочная кислота.
1
3
Энантиомеры –
это
стереоизомеры,
которые
относятся друг к
другу как предмет
и несовместимое
с ним в
пространстве
зеркальное
отражение.
4
2
3
b
3
1
4
2
23.
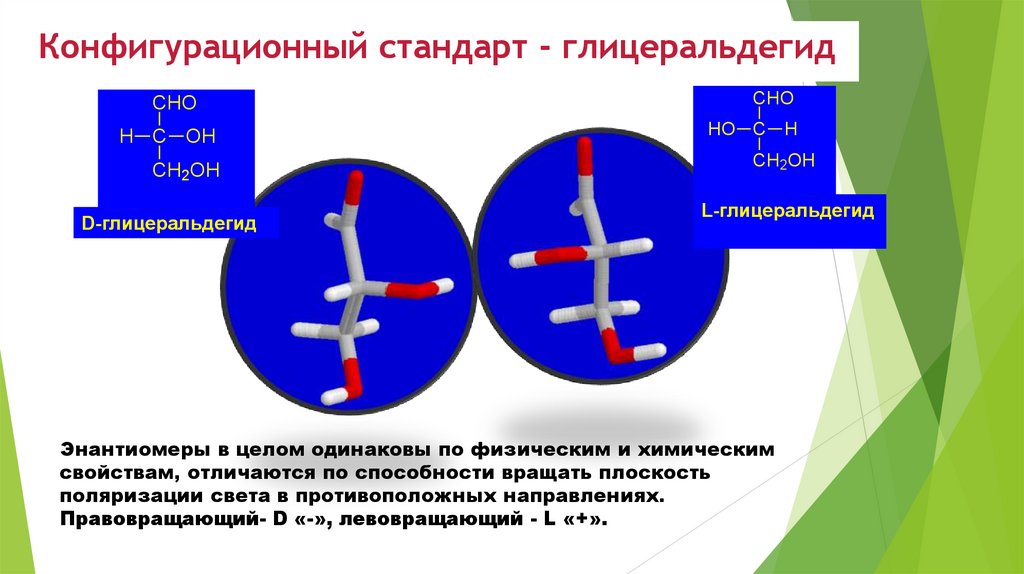
Конфигурационный стандарт - глицеральдегидCHO
H C OH
CH2OH
D-Gliceraldehido
D-глицеральдегид
CHO
HO C H
CH2OH
L-Gliceraldehido
L-глицеральдегид
Энантиомеры в целом одинаковы по физическим и химическим
свойствам, отличаются по способности вращать плоскость
поляризации света в противоположных направлениях.
Правовращающий- D «-», левовращающий - L «+».
24.
• Смесь равных количеств энантиомеров называют рацемат,оптически не активный. Энантиомеры отличаются
некоторыми химическими свойствами при взаимодействии с
хиральными молекулами, в основном с ферментами.
• Специфичность биологического действия
определяется пространственным соответсвием ферменту (ключ и замок), его
активному центру (Фишер).
Поэтому в живых организмах присутствует в
основном одна стереоизомерная форма.
Около 40% фарм.препаратов – хиральные соединения,
в основном в виде рацемата, т.е. биологически активна лишь
половина препарата. Более физиологически активный
энантиомер- называют эвтомер, другой – дистомер. У них
может быть и различное физиологическое действие.
Энантиомеры обладают одинаковыми физическими и
химическими свойствами, но являются оптическими
антиподами и имеют различную физиологическую активность.
25.
σ - ДиастереомерияЭНАНТИОМЕРЫ
ДИАСТЕРЕОМЕРЫ
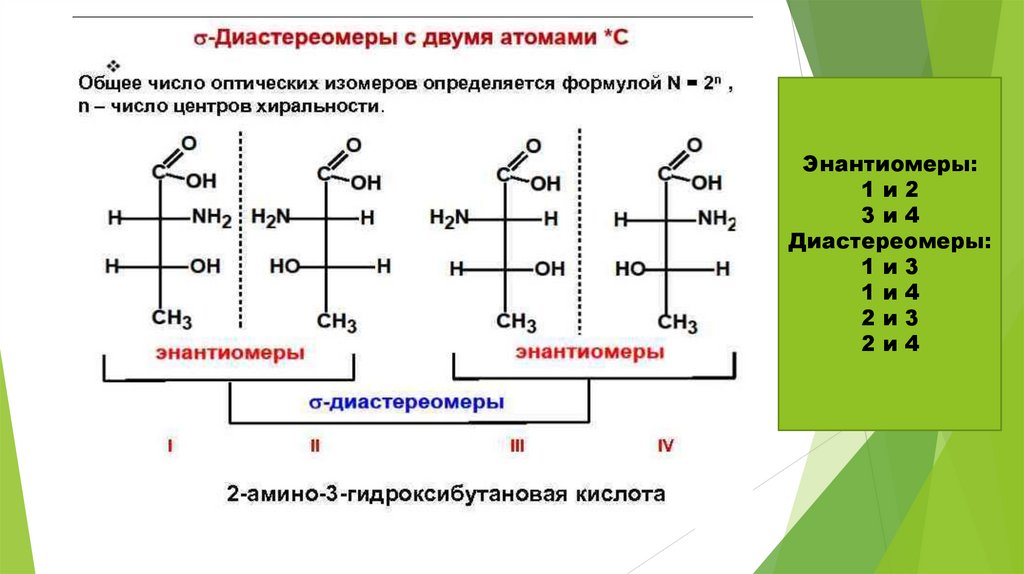
σ-Диастереомерия возникает в молекулах с 2 и более
центрами хиральности.
σ- Диастереомеры – оптические изомеры, не
являющиеся зеркальным изображением друг друга.
Число стереоизомеров рассчитывают по формуле Фишера: Z =2n ,
где n-число центров хиральности.
σ– Диастереомеры имеют разные физические и химически
свойства и физиологическое действие.
26.
Энантиомеры:1и2
3и4
Диастереомеры:
1и3
1и4
2и3
2и4
27.
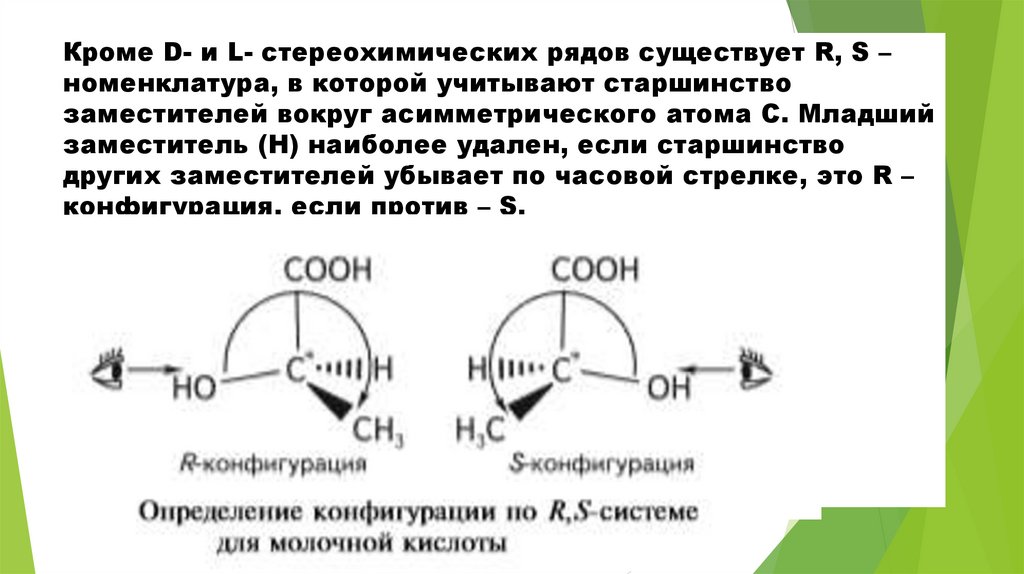
Кроме D- и L- стереохимических рядов существует R, S –номенклатура, в которой учитывают старшинство
заместителей вокруг асимметрического атома С. Младший
заместитель (Н) наиболее удален, если старшинство
других заместителей убывает по часовой стрелке, это R –
конфигурация, если против – S.
28.
Также выделяют π-диастереомеры, которые содержат πсвязь, например в алкенах. Заместители могутрасполагаться либо по одному, либо по разные стороны
относительно плоскости π-связи. Их также называют цис-,
транс-изомеры, они образуются из-за невозможности
вращения вокруг π-связи.
Используют E, Z – классификации,
по которой в Z-изомере старшие
заместители по одну сторону
от плоскости двойной связи,
в Е-изомере – по разные стороны.
29.
Конформация – пространственное расположениеатомов в молекуле определенной конфигурации,
обусловленное поворотом вокруг одинарных δ-связей.
Начиная с этана в алканах появляется возможность
вращения вокруг одинарной С-С δ-связи без
нарушения химического строения, меняется
расположение заместителей у атома С, молекула
принимает разные геометрические формы, или
конформации. Угол поворота называют торсионным.
Конформации соединений с открытой цепью
Минимальный угол поворота (торсионный) принят за
600, при полном обороте на 3600 возникают 6
различных конформаций.
30.
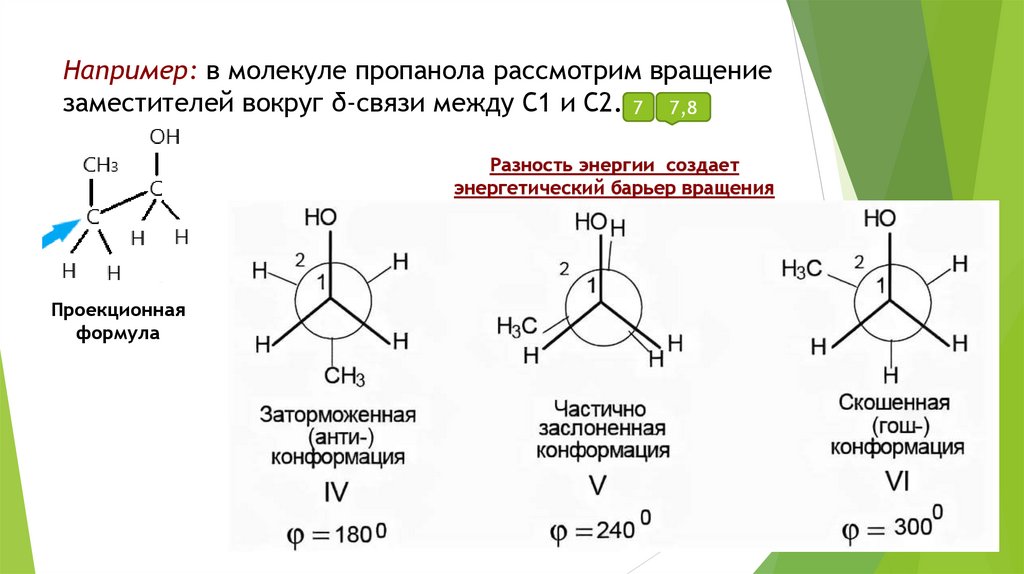
Например: в молекуле пропанола рассмотрим вращениезаместителей вокруг δ-связи между С1 и С2. 7 7,8
Разность энергии создает
энергетический барьер вращения
Проекционная
формула
31.
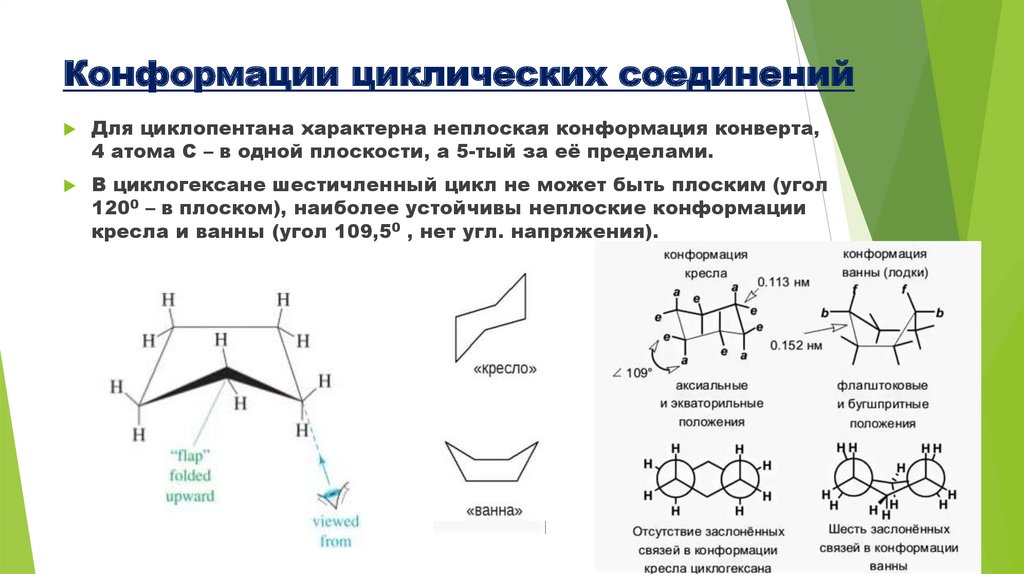
Конформации циклических соединенийДля циклопентана характерна неплоская конформация конверта,
4 атома С – в одной плоскости, а 5-тый за её пределами.
В циклогексане шестичленный цикл не может быть плоским (угол
1200 – в плоском), наиболее устойчивы неплоские конформации
кресла и ванны (угол 109,50 , нет угл. напряжения).
32.
Конфигурационные изомеры отличаютсярасположением атомов или групп атомов
без учета конформаций.
Конформационный изомеры различаются
за счет поворота атомов или групп атомов
вокруг одинарных связей.
33.
Благодарим за внимание!34.
Атомы углерода могут соединяться друг с другом:а) разными видами связей:
одинарной
двойной
тройной
СН3
СН2
СН
СН3
СН2
СН
ЭТАН
ЭТИЛЕН
АЦЕТИЛЕН
б) в цепочки разного вида:
ПРЯМЫЕ
С
С
С
РАЗВЕТВЛЕННЫЕ
С
ЗАМКНУТЫЕ
34
С
С
С
С
35.
Свойства органических соединений зависят: а) от качественного иколичественного состава молекулы,
Реакционная способность отдельных атомов в
молекуле меняется в зависимости от
того, с какими атомами других
элементов они соединены, от взаимного влияния
атомов в молекуле.
б) от химического строения, т.е. порядка связей в молекуле с
учетом взаимного влияния атомов.
Строение вещества
можно отразить
структурной формулой,
которая для него
будет единственной.
35




















 Химия
Химия








