Похожие презентации:
Химическая связь в органических соединениях
1. Органическая химия
2. Теория строения А. М. Бутлерова
• 1. Химические вещества определеннымобразом построены, т.е. имеют строгий
порядок в чередовании атомов в молекуле,
определенную закономерность во влиянии
атомов друг на друга;
• 2. Химическое строение веществ определяет
их химические и физические свойства;
• 3. Химическое строение веществ может быть
определено на основании их свойств.
3. Химическая связь в органических соединениях
4. Классические представления о химической связи
Теория Льюиса и Косселя:1. Связь между атомами осуществляется
парой валентных электронов.
2. Атомы, входящие в молекулы,
стремятся достроить свою внешнюю
оболочку до наиболее устойчивой
электронной конфигурации - октета (8
электронов) или дублета (2
электрона).
5. Электронный октет (или дублет) может образоваться двумя способами:
1. Перенос электронов.2. Обобществление электронов.
6.
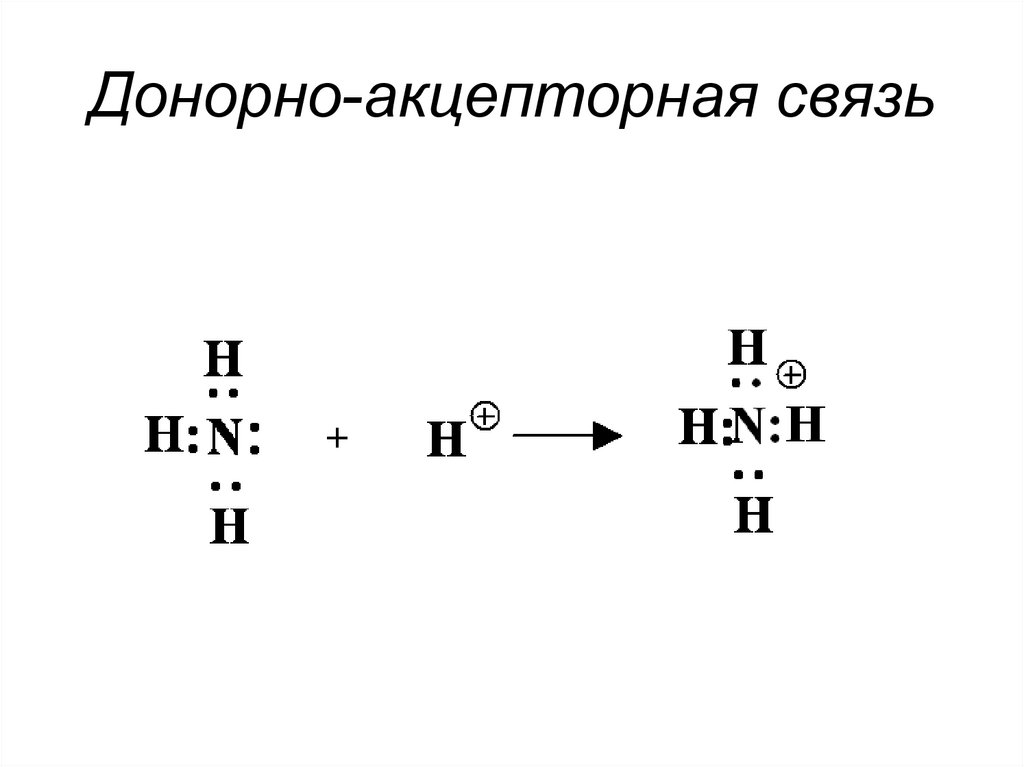
7. Донорно-акцепторная связь
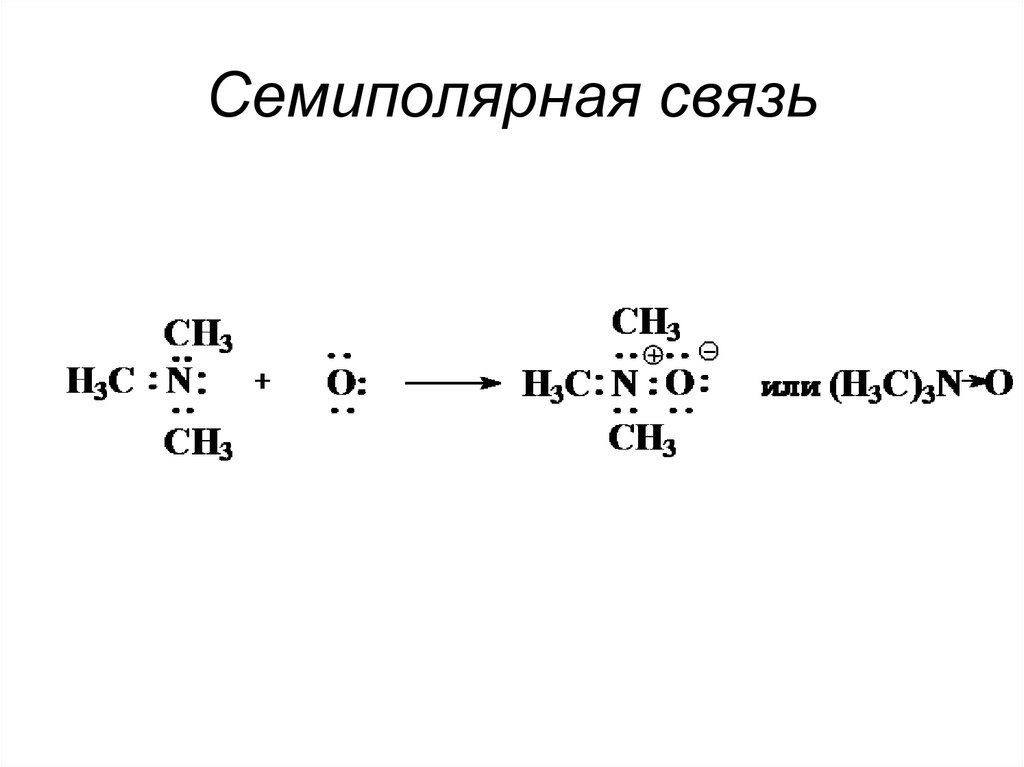
8. Семиполярная связь
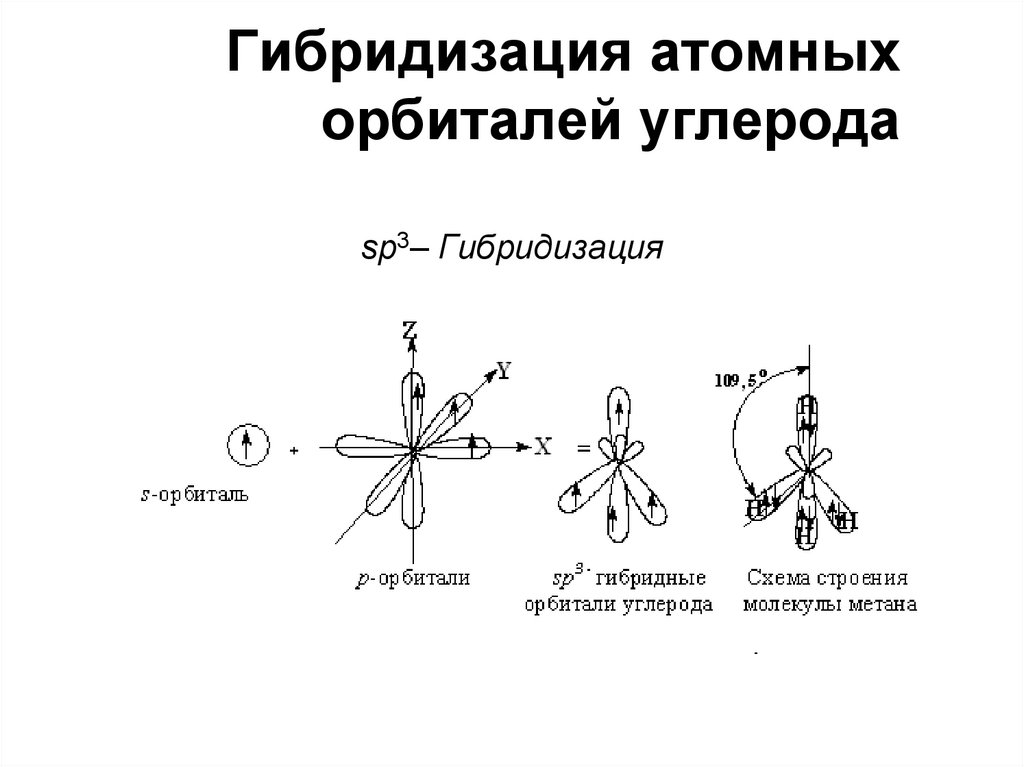
9. Гибридизация атомных орбиталей углерода
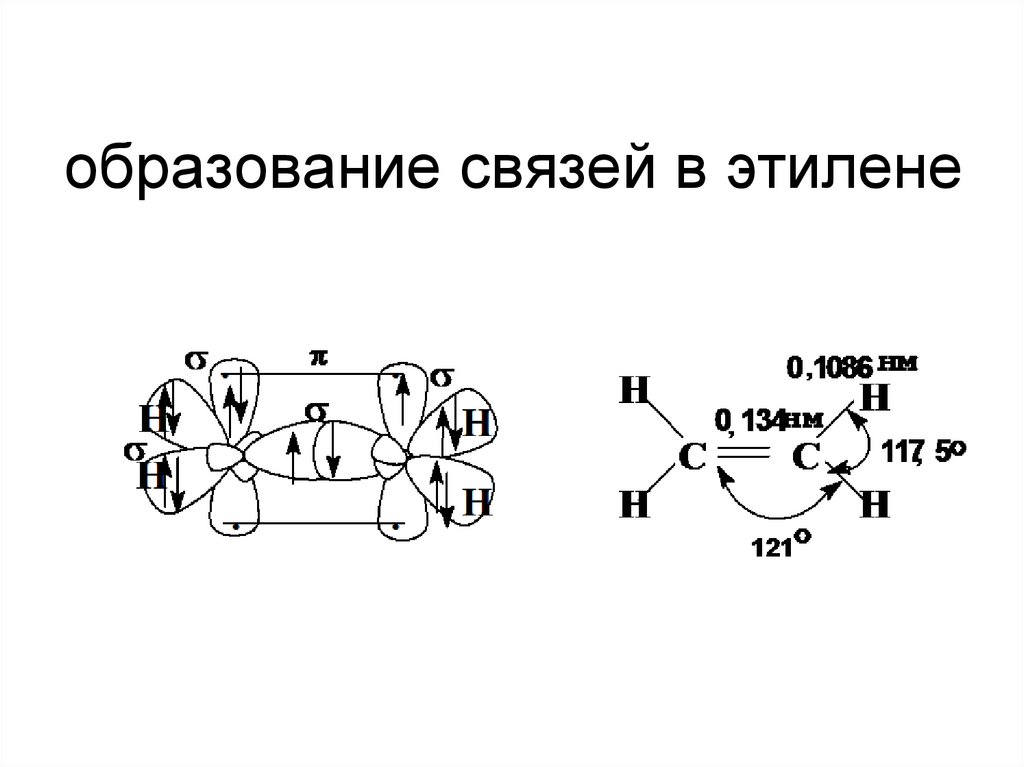
sр3– Гибридизация10. образование связей в этилене
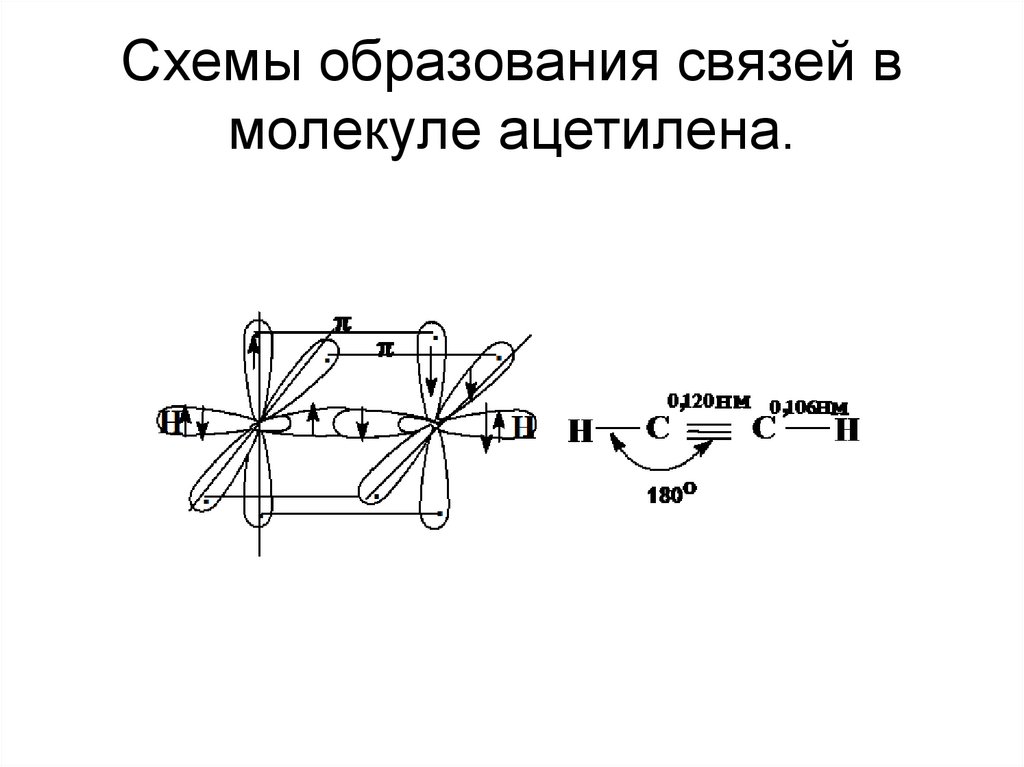
11. Схемы образования связей в молекуле ацетилена.
12.
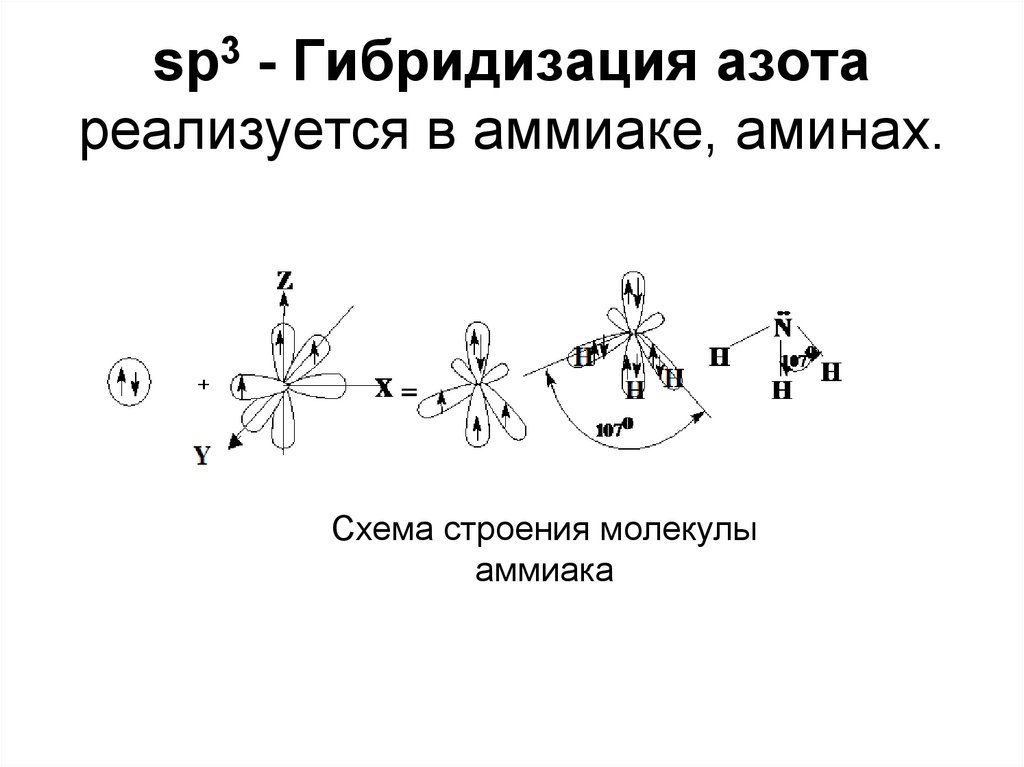
Гибридизация атомных орбиталей кислорода и азота13. sp3 - Гибридизация азота реализуется в аммиаке, аминах.
Схема строения молекулыаммиака
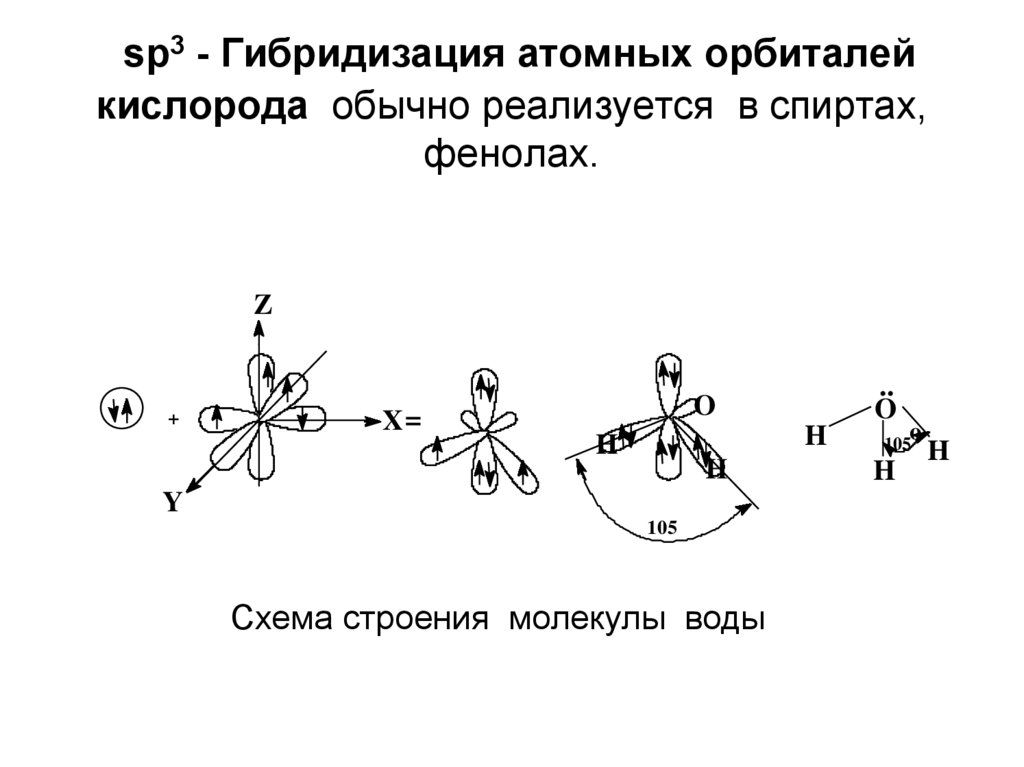
14. sp3 - Гибридизация атомных орбиталей кислорода обычно реализуется в спиртах, фенолах.
Z+
X=
..
O
O
H
H
H
Y
105
Схема строения молекулы воды
o
105
H
H
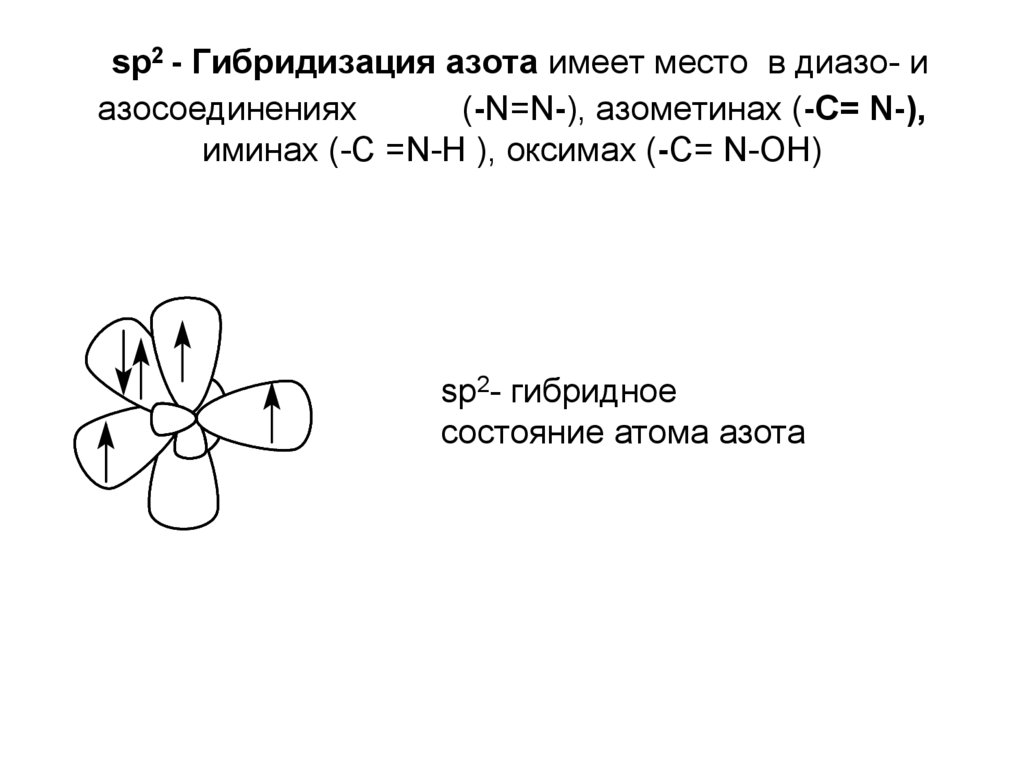
15. sp2 - Гибридизация азота имеет место в диазо- и азосоединениях (-N=N-), азометинах (-С= N-), иминах (-С =N-Н ), оксимах (-С=
N-ОН)sp2- гибридное
состояние атома азота
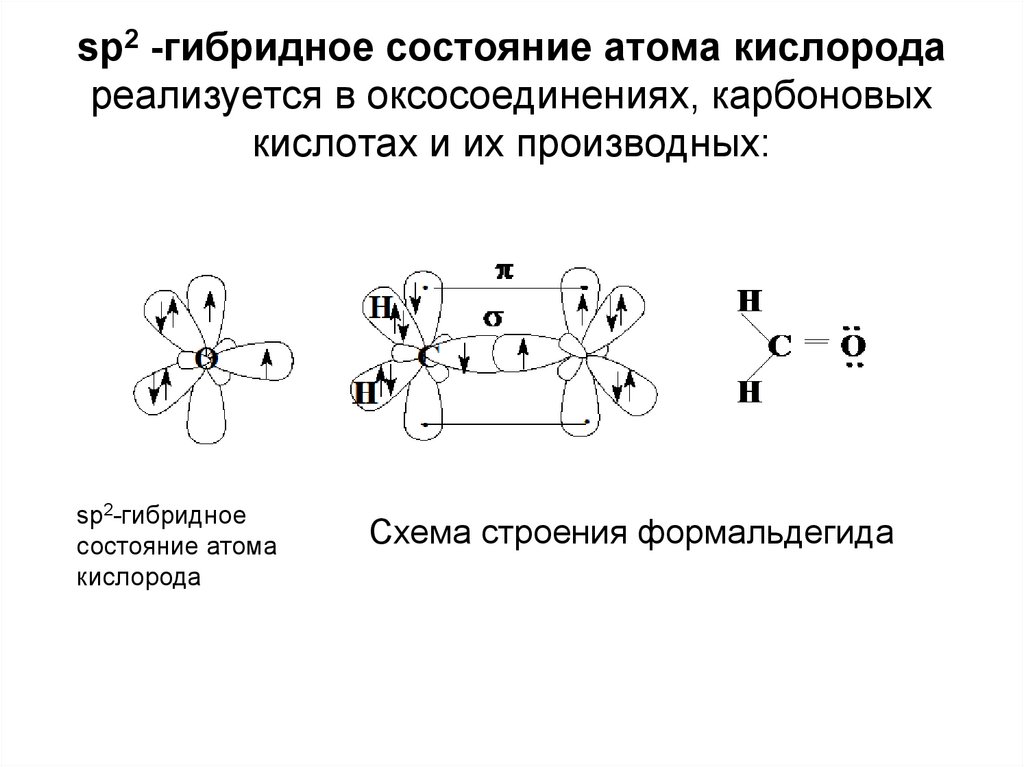
16. sp2 -гибридное состояние атома кислорода реализуется в оксосоединениях, карбоновых кислотах и их производных:
sp2-гибридноесостояние атома
кислорода
Cхема строения формальдегида
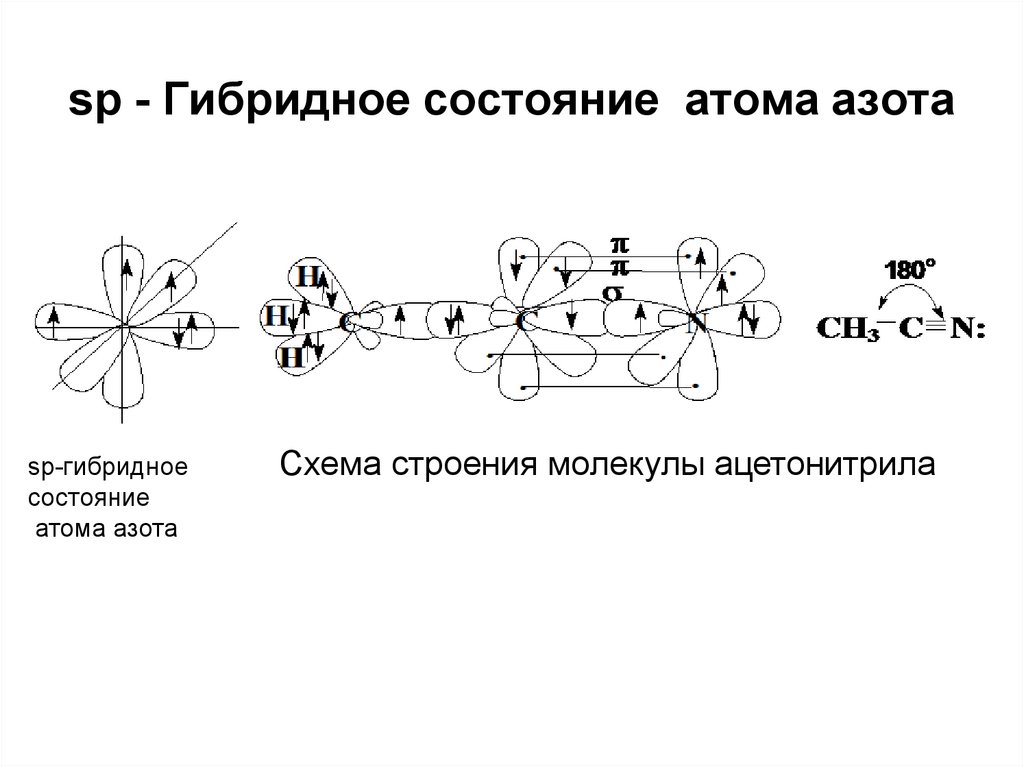
17. sp - Гибридное состояние атома азота
sp-гибридноесостояние
атома азота
Схема строения молекулы ацетонитрила
18.
Механизмы распределения электронной плотностив молекулах органических соединений
19. Индукционный эффект
20. Электроноакцепторные (-I-эффект) заместители
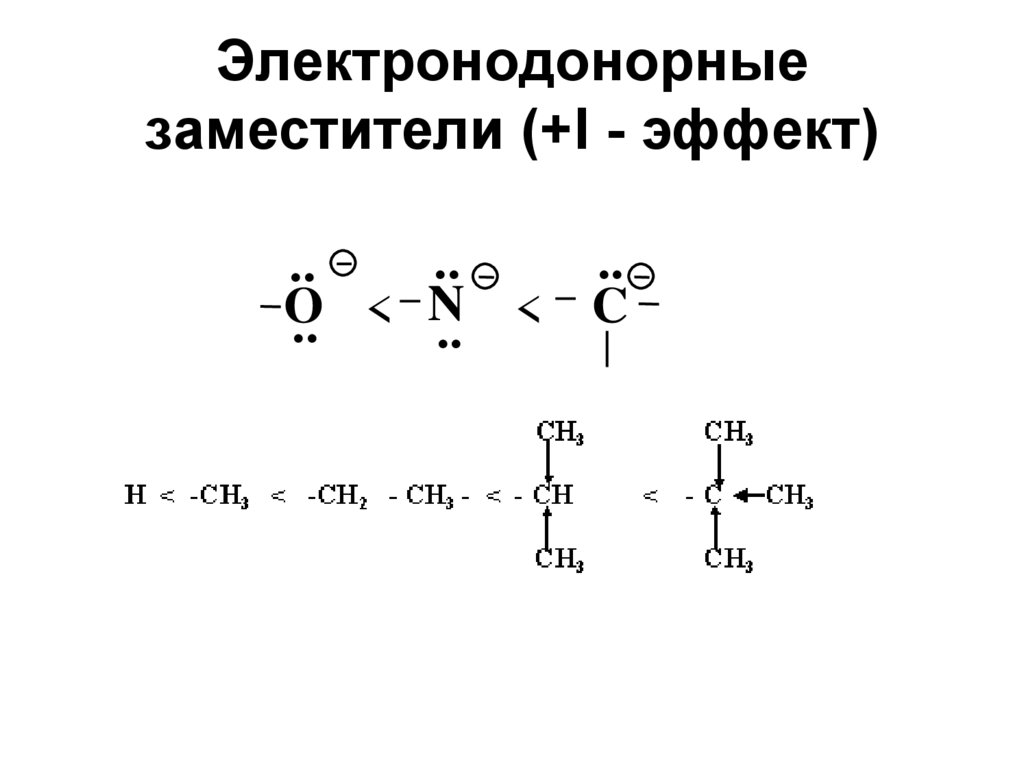
Электроноакцепторные (-Iэффект) заместители21. Электронодонорные заместители (+I - эффект)
....
..
N
O
C
<
<
..
..
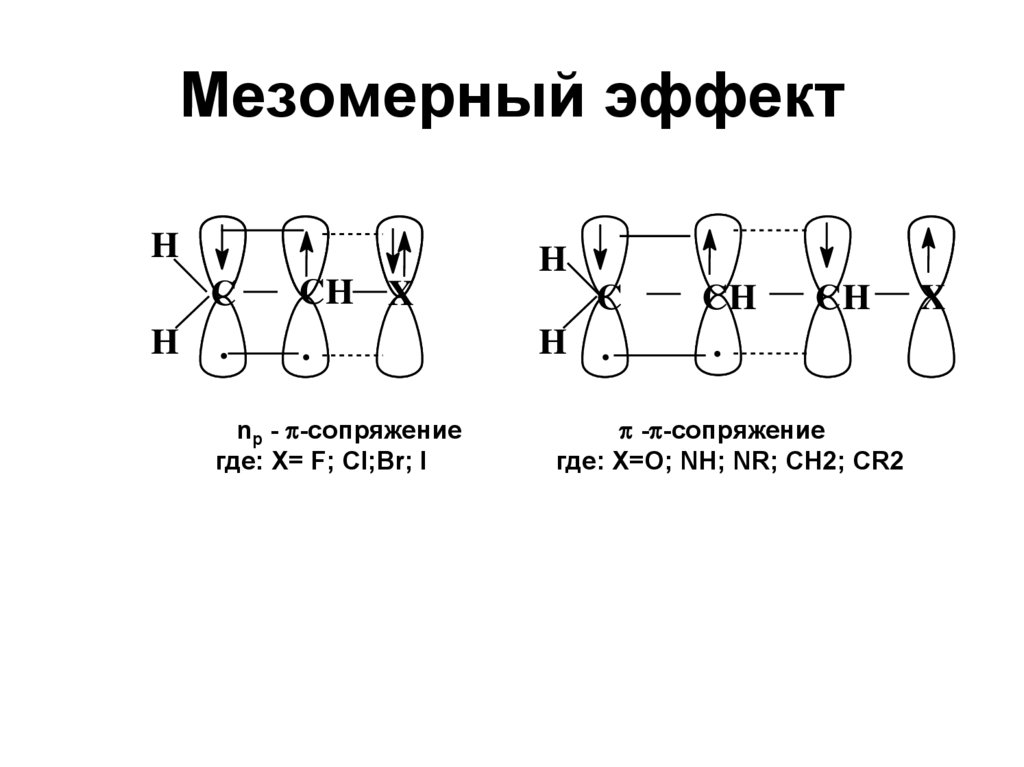
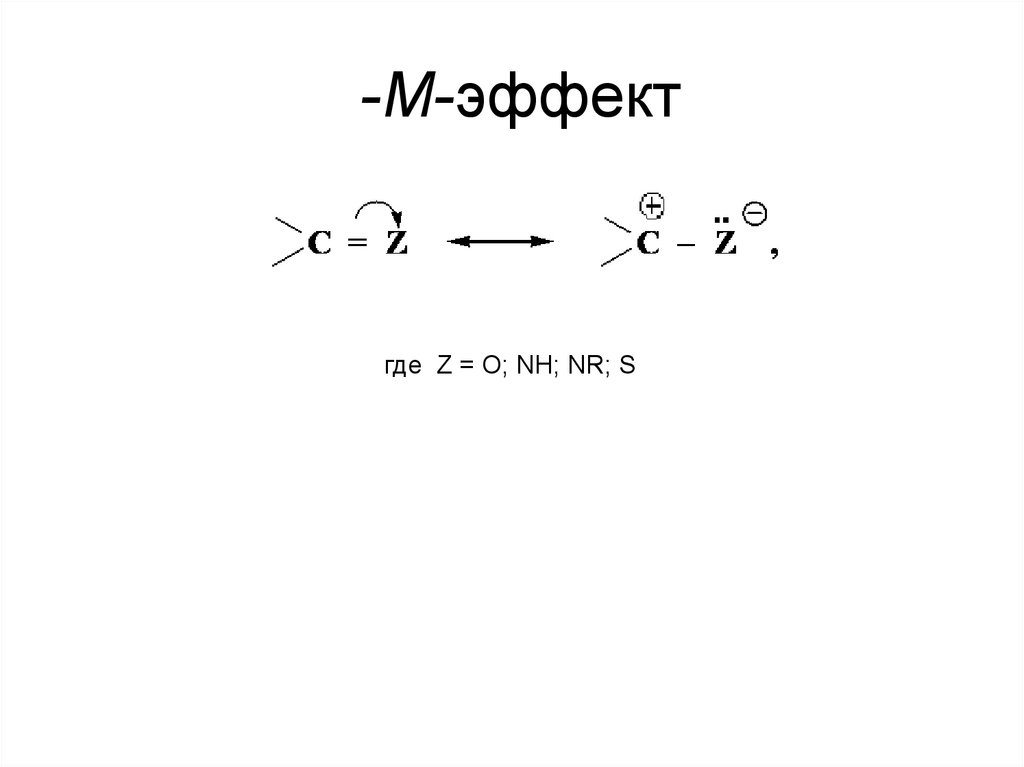
22. Мезомерный эффект
HH
C
H .
CH X
.
nр - -сопряжение
где: X= F; Cl;Br; I
C
H .
CH
.
CH
- -сопряжение
где: X=O; NH; NR; CH2; CR2
X
23.
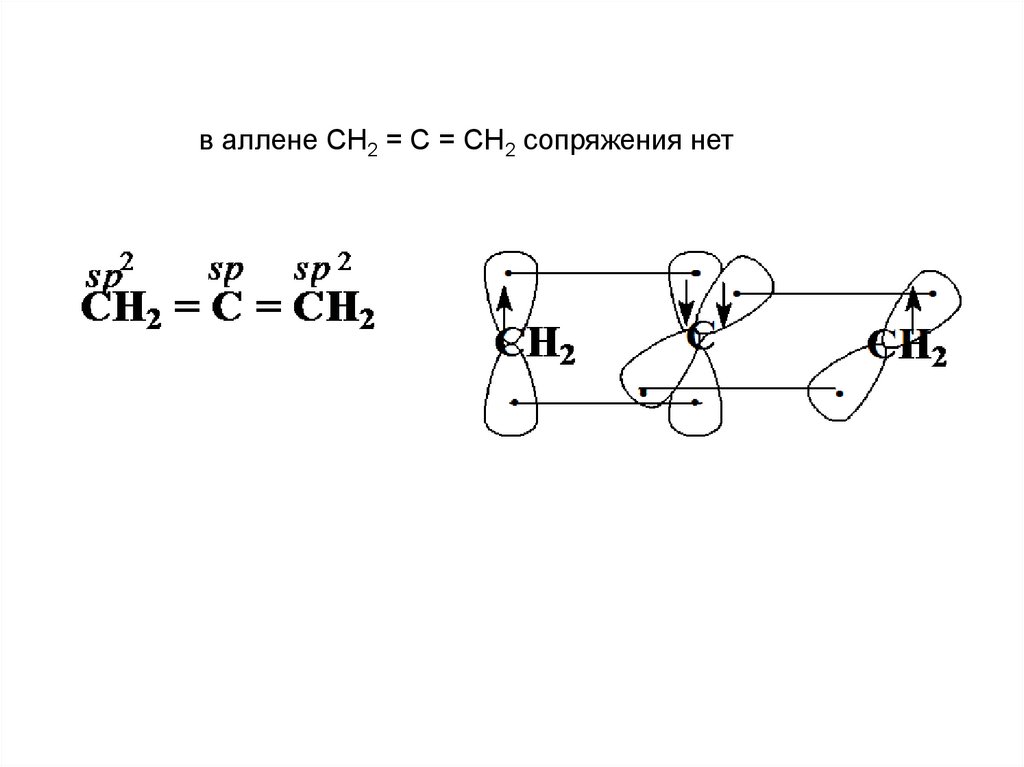
в аллене СН2 = С = СН2 сопряжения нет24.
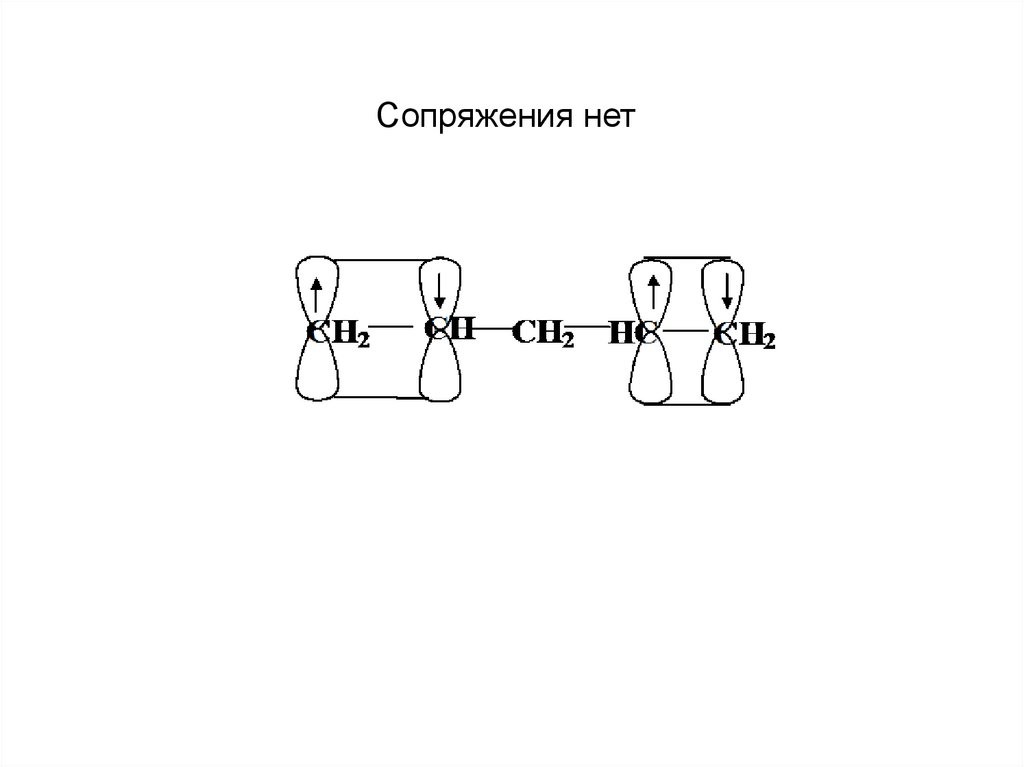
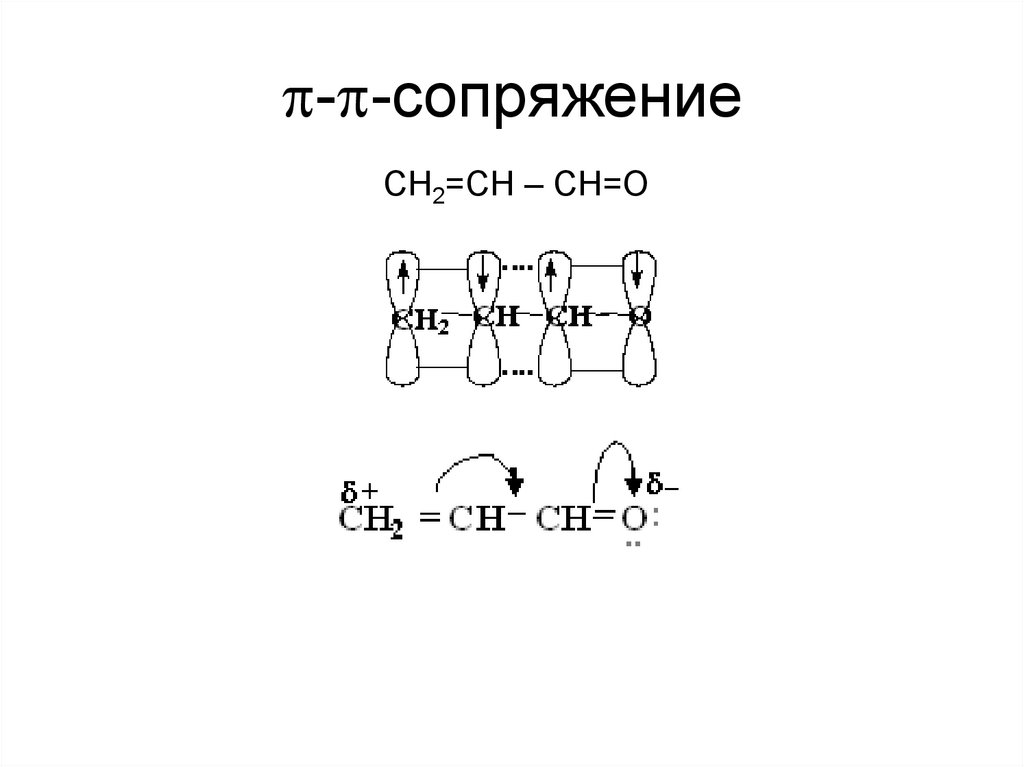
Сопряжения нет25. --сопряжение
- -сопряжениеСН2=СН – СН=О
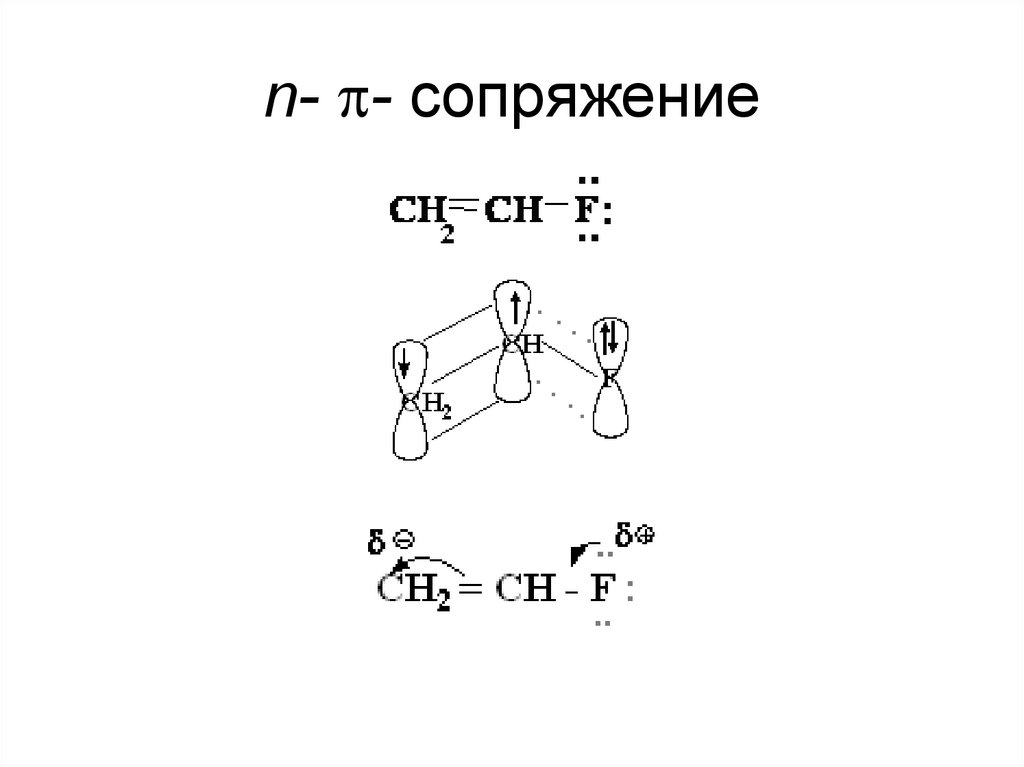
26. n- - сопряжение
n- - сопряжение27. +М-эффект
..> :Cl
..
:F
..
..
:O
..
..
> :Br
..
>>> H
..
> :I..
..
O
..










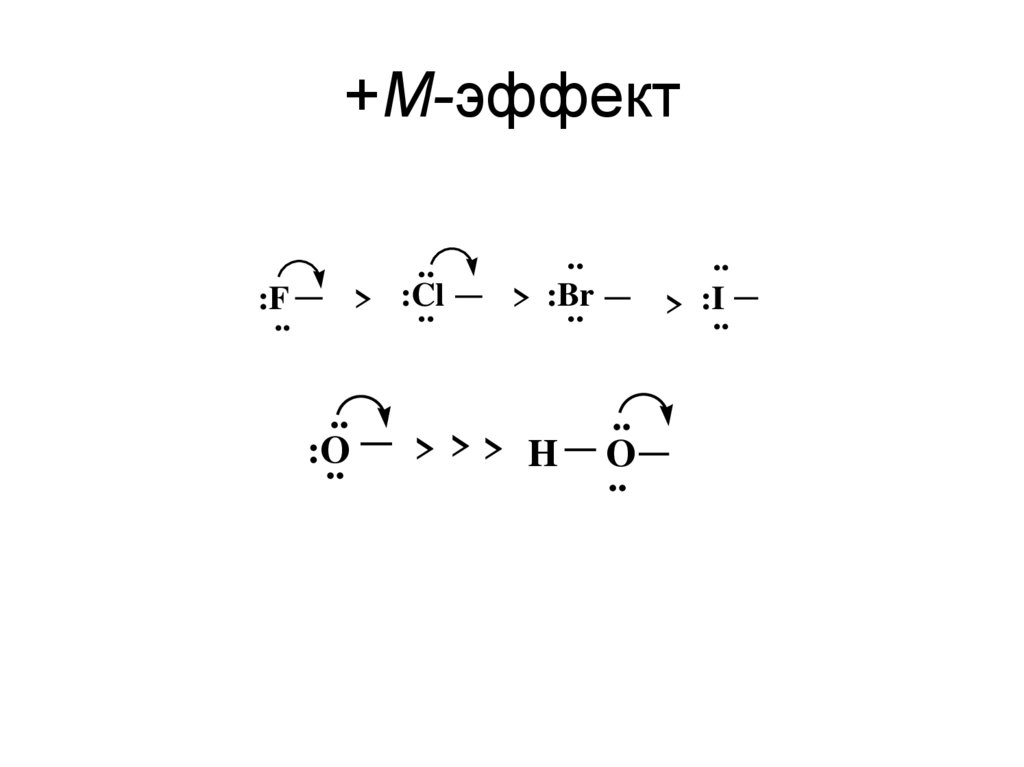
 Химия
Химия








