Похожие презентации:
Химическая кинетика. (Лекция 4)
1.
КАФЕДРА ФИЗИЧЕСКОЙ ХИМИИ СПБГЭТУЭЛЕМЕНТЫ
ХИМИЧЕСКОЙ КИНЕТИКИ
ВЕСЕННИЙ СЕМЕСТР 2015-2016 УЧ.ГОД.
2.
ХИМИЧЕСКАЯ КИНЕТИКАХимическая кинетика – раздел физической химии,
в котором химические превращения веществ
изучаются как процессы, протекающие во времени,
исследуются закономерности, определяющие скорости
этих превращений, а также их механизмы
Формальная (феноменологическая) или макрокинетика –
описание химического превращения проводится на основании
экспериментальных данных о текущих концентрациях
(парциальных давлениях) реагентов
Молекулярная или микрокинетика – описание процессов
производится на микроуровне с учетом свойств реагирующих частиц
2
3.
ХИМИЧЕСКАЯ КИНЕТИКАПрямая задача – определение скоростей химических
реакций и концентраций участников этих реакций
в любой момент времени
начальные условия
(начальные концентрации участников реакции)
вид кинетического уравнения
(определяется механизмом химической реакции)
Обратная задача – определение вида кинетического
уравнения, описывающего реакцию
кинетические данные
(зависимости концентраций
участников реакции от времени Ci = f(t))
механизм реакции
• константа скорости химической реакции
• порядок химической реакции
3
4.
ХИМИЧЕСКАЯ КИНЕТИКАХимическая реакция – процесс,
при котором происходит разрыв
существующих связей и образование новых
Необходимо:
• столкновение реагирующих частиц
• наличие у этих частиц
достаточного запаса энергии
• оптимальное расположение частиц
друг относительно друга в пространстве
4
5.
ХИМИЧЕСКАЯ КИНЕТИКАХимическая реакция – процесс,
при котором происходит разрыв
существующих связей и образование новых
Необходимо:
• столкновение реагирующих частиц
• наличие у этих частиц
достаточного запаса энергии
• оптимальное расположение частиц
друг относительно друга в пространстве
Молекулярность, определяется числом частиц
(молекул, атомов, ионов), принимающих участие
в элементарном акте химической реакции
Мономолекулярные реакции
• реакции разложения, перегруппировка,
полиморфные превращения в твердых телах
Бимолекулярные (тримолекулярные)
• реакции присоединения, замещения, обмена
5
6.
ХИМИЧЕСКАЯ КИНЕТИКА• столкновение реагирующих частиц
• наличие у этих частиц достаточного запаса энергии
• оптимальное расположение частиц друг
относительно друга в пространстве
Скорость химической реакции
определяется числом соударений (элементарных актов
химической реакции), приводящих к химическому
превращению в единице объема в единицу времени
1 dni
dCi
vi
V d
d
моль
л с
На практике скорость гомогенных реакций определяется
изменением концентрации реагирующих веществ в единицу времени
1 dni
vi
Скорость гетерогенной реакции
S d
определяется числом молей веществ, вступивших в
или образующихся в результате реакции в единицу
времени на единице поверхности
моль
2
м с
6
7.
ХИМИЧЕСКАЯ КИНЕТИКА2 H2O2 = 2 H2O + O2
C(H O ),
моль/л
C C2 C1
2
С2
С1
2
C
v
Средняя
скорость
dC
v
d
А
C
Кинетическое уравнение
Мгновенная
скорость
v tg
α
1
2
2 1
τ, с
dCO
dCH O
2
2 2
v
2
7
8.
ХИМИЧЕСКАЯ КИНЕТИКАСкорость химической реакции зависит от
Природы реагирующих веществ
Концентрации реагирующих веществ
Температуры
Наличия катализатора
Величины поверхности раздела (для гетерогенных реакций)
Прочих энергетических воздействий (светового, радиационного и др.)
8
9.
ХИМИЧЕСКАЯ КИНЕТИКАСкорость химической реакции зависит от
Природы реагирующих веществ
Концентрации реагирующих веществ
Температуры
Наличия катализатора
Величины поверхности раздела (для гетерогенных реакций)
Прочих энергетических воздействий (светового, радиационного и др.)
Закон действующих масс
скорость химической реакции при постоянной температуре
прямо пропорциональна произведению мольных концентраций
реагирующих веществ, возведенных в определенные степени
mАВ nС A BC
m
CC
(К. Гульдберг, П.Вааге, 1867 г. Норвегия)
n
CAB
CC ,CAB- молярные концентрации, моль/л
v k
- порядок реакции
m
n
константа
скорости
реакции
k
(скорость химической реакции при концентрации
реагирующих веществ, равных 1 моль/л)
9
10.
ХИМИЧЕСКАЯ КИНЕТИКАmАВ nС A BC
CC ,CAB- молярные концентрации, моль/л
m n - порядок реакции
n
v k CCm CAB
k - константа скорости реакции
(скорость химической реакции при концентрации
реагирующих веществ, равных 1 моль/л)
Константа скорости химической реакции НЕ ЗАВИСИТ от
концентраций (парциальных давлений) участников реакции
и ЗАВИСИТ от:
• температуры
• давления (для газофазных реакций, для жидкофазных
выражено слабо, т.к. сжимаемость жидкостей очень мала)
• наличия катализатора (или ингибитора)
• ряда других факторов (например, природы растворителя
– для реакций, протекающих в растворах)…
10
11.
ХИМИЧЕСКОЕИ
ФАЗОВОЕ
РАВНОВЕСИЕ
Обратимые реакции - химические реакции, протекающие
одновременно в двух противоположных направлениях
Химическое равновесие - состояние системы, в котором скорость
прямой реакции (v1) равна скорости обратной реакции (v2)
v1
t
k1
K
k2
v1
aА bB
dD
v2
v2
dD
aА bB
При химическом равновесии концентрации веществ
остаются неизменными
Химическое равновесие имеет динамический характер:
прямая и обратная реакции при равновесии не
прекращаются
Состояние химического равновесия количественно
C
характеризуется константой равновесия,
представляющей собой отношение констант
C aA C bB
прямой (k1) и обратной (k2) реакций
d
D
Константа равновесия зависит от температуры и природы
реагирующих веществ и не зависит от присутствия катализаторов
11
12.
ХИМИЧЕСКАЯ КИНЕТИКАmАВ nС A BC
CC ,CAB- молярные концентрации, моль/л
m n - порядок реакции
n
v k CCm CAB
k - константа скорости реакции
(скорость химической реакции при концентрации
реагирующих веществ, равных 1 моль/л)
Молекулярность определяется по числу молекул
одновременное соударение которых
приводит к химическому взаимодействию
Порядок реакции равен сумме показателей степеней
у концентрации в уравнении, выражающем зависимость
скорости реакции от концентрации
реагирующих веществ
12
13.
ХИМИЧЕСКАЯ КИНЕТИКАПорядок реакции устанавливается экспериментально
при обработке данных кинетических исследований и
основан на решении кинетического уравнения
А→В
dC
v
d
v k C
n
dC
n
kC
d
13
14. Необратимые реакции 0-ого порядка
ХИМИЧЕСКАЯ КИНЕТИКАА→В
n=0
Необратимые реакции 0-ого порядка
где k - константа скорости
dC
kC 0 dC
d
k
необратимой реакции 0-го порядка
d
• концентрация реагента автоматически поддерживается постоянной
(например, в насыщенном растворе вещества, контактирующем с
избытком этого не растворившегося вещества);
• скорость реакции определяется не концентрацией реагирующего
вещества, которая очень велика и практически не изменяется (или
изменяется незначительно) в ходе реакции, а иными факторами –
концентрацией катализатора (при гомогенном катализе) или
фермента (при ферментативном катализе), количеством
поглощенного света (для фотохимических реакций) и др.
14
15. Необратимые реакции 0-ого порядка
ХИМИЧЕСКАЯ КИНЕТИКАНеобратимые реакции 0-ого порядка
Графическое определение константы скорости
необратимой реакции 0-го порядка
А→В
dC
kC 0
d
dC
d
k
k
1
k C0, A CA
CA C0, A k
τ, c
15
16. Необратимые реакции 0-ого порядка
ХИМИЧЕСКАЯ КИНЕТИКАНеобратимые реакции 0-ого порядка
А→В
Время (период) полупревращения
(полураспада) - время, в течение которого
dC
исходного вещества
kC 0 концентрация
уменьшается в два раза
d
CA C0, A k
С0,А
т.е. если 1
то СА
2
2
Время полупревращения
1
2
С0,А
2k
16
17. Необратимые реакции 1-ого порядка
ХИМИЧЕСКАЯ КИНЕТИКАn=1
А→В
Необратимые реакции 1-ого порядка
dC
kC n
d
dC
1
kC
d
интегрируем
ln CA ln C0, A k
C0, A
ln
k
CA
k
1
τ, c
2
ln 2 0.693
k
k
17
18.
ХИМИЧЕСКАЯ КИНЕТИКАПорядок реакции устанавливается экспериментально
при обработке данных кинетических исследований и
основан на решении кинетического уравнения dC
Порядок
реакции
0
1
2
n
Кинетическое уравнение
dC
k
d
dC
kС
d
dC
kС 2
d
dC
kС n
d
d
kC n
Координаты, в которых
график зависимости С(τ)
линеен
C
ln C
1
n 1
C
1
C
18
19.
ХИМИЧЕСКАЯ КИНЕТИКАСкорость химической реакции зависит от
Природы реагирующих веществ
Концентрации реагирующих веществ
Температуры
Наличия катализатора
Величины поверхности раздела (для гетерогенных реакций)
Прочих энергетических воздействий (светового, радиационного и др.)
правило Вант-Гоффа
T2 T1
vT
2
10
vT
γ - температурный
коэффициент скорости реакции
1
При повышении температуры
на каждые 10 градусов
константа скорости гомогенной элементарной
реакции увеличивается в два – четыре раза
Якоб Хендрик
Вант-Гофф
19
20.
ХИМИЧЕСКАЯ КИНЕТИКАЗависимость скорости химической реакции от
H
ln K
температуры
ln K
B
ln k
T
C
Допущения Аррениуса
T p
RT
U
T
V RT 2
2
Изобара
химической реакции
Изохора
химической реакции
- реагировать могут не все молекулы, а лишь находящиеся
в особой таутомерной форме или активной модификации
- образование активной модификации рассматривается
как обратимая реакция, а концентрация этой модификации
всегда соответствует термодинамическому равновесию
и в принципе ее можно выразить через константу
равновесия
- концентрация активной модификации всегда мала и ее
образование практически не влияет на концентрацию
исходных молекул
- образовавшаяся активная модификация
превращается в продукт со скоростью,
независящей от температуры
k
Сванте Август
Аррениус
Ea
Аe RT
20
21.
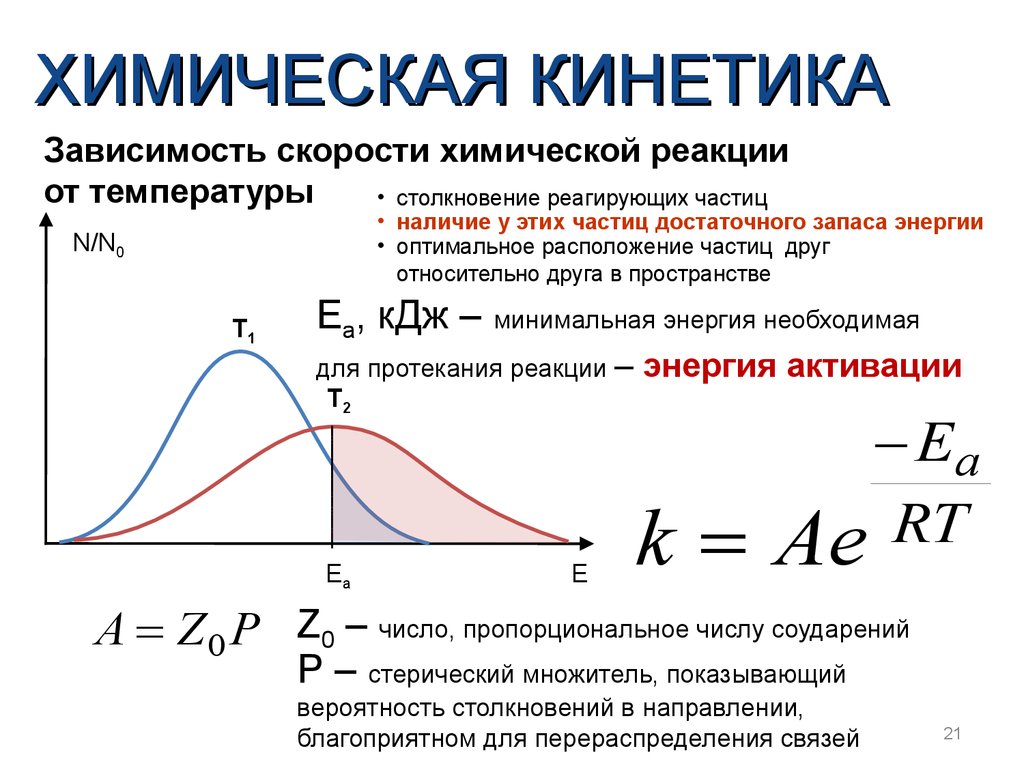
ХИМИЧЕСКАЯ КИНЕТИКАЗависимость скорости химической реакции
от температуры
• столкновение реагирующих частиц
• наличие у этих частиц достаточного запаса энергии
• оптимальное расположение частиц друг
относительно друга в пространстве
N/N0
T1
Eа, кДж – минимальная энергия необходимая
для протекания реакции –
T2
Ea
E
энергия активации
k
Ea
RT
Аe
А Z 0 P Z0 – число, пропорциональное числу соударений
P – стерический множитель, показывающий
вероятность столкновений в направлении,
благоприятном для перераспределения связей
21
22.
ХИМИЧЕСКАЯ КИНЕТИКАОпределение энергии активации
Аналитический метод
T1 и T2
Ea 1
ln k ln A
RT
Ea 1
ln k1 ln A
R T1
Ea 1 1
ln k2 ln kили
1
R T1 T2
Ea 1
ln k2 ln A
R T2
k 2 Ea 1 1
ln
k1 R T1 T2
ln k2 ln k1 RT1T2
k2
Ea R
ln
T2 T1 k1
1
1
T1 T2
22
23.
ХИМИЧЕСКАЯ КИНЕТИКАОпределение энергии активации
Графический метод
Ea 1
ln k ln A
RT
1
ln k f
T
Ea
tg tg b
R
Ea
tg b
R
Ea Rtg b Rtg
23
24.
ХИМИЧЕСКАЯ КИНЕТИКАСкорость химической реакции зависит от
Природы реагирующих веществ
Концентрации реагирующих веществ
Температуры
Наличия катализатора
Величины поверхности раздела (для гетерогенных реакций)
Прочих энергетических воздействий (светового, радиационного и др.)
Катализатор – вещество, увеличивающее скорость химической
реакции и не расходующееся в процессе взаимодействия
Ингибитор – вещество, уменьшающее скорость химической
реакции
Гомогенный катализ – реагенты и катализатор находятся в
одном агрегатном состоянии и между ними нет поверхности раздела
Гетерогенный катализ – реакция проходит на поверхности
раздела двух фаз, одна из которых является катализатором
24
25.
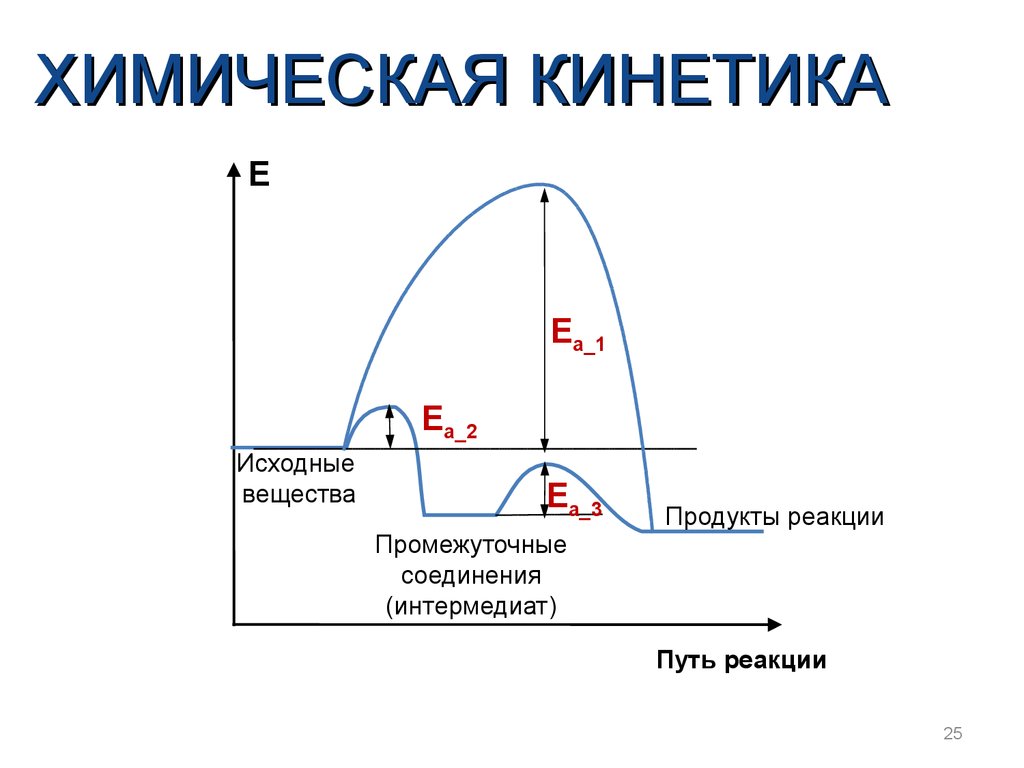
ХИМИЧЕСКАЯ КИНЕТИКАE
Ea_1
Ea_2
Исходные
вещества
Ea_3
Продукты реакции
Промежуточные
соединения
(интермедиат)
Путь реакции
25
26.
ХИМИЧЕСКАЯ КИНЕТИКАСложные реакции
- химические реакции, протекающие более чем в одну стадию
Общая скорость таких реакций определяется скоростью
более медленной стадии, называемой
скоростьопределяющей или лимитирующей
Сделать вывод о том, является реакция элементарной или
сложной, можно на основании результатов изучения её кинетики
Реакция является сложной, если
экспериментально определенные частные порядки
реакции не совпадают с коэффициентами
при исходных веществах
в стехиометрическом уравнении реакции
(частные порядки сложной реакции могут быть дробными
либо отрицательными, в кинетическое уравнение сложной
реакции могут входить концентрации не только исходных
26
веществ, но и продуктов реакции)
27.
ХИМИЧЕСКАЯ КИНЕТИКАКлассификация сложных реакций
Последовательные реакции
сложные реакции, протекающие таким образом, что вещества,
образующиеся в результате одной стадии (т.е. продукты этой
стадии), являются исходными веществами для другой стадии
Параллельные реакции
химические реакции, в которых одни и те же исходные
вещества одновременно могут образовывать различные
продукты реакции
Сопряжённые реакции
сложные реакции, протекающие следующим образом:
1) А + В ––> С
2) А + D ––> Е,
причём одна из реакций может протекать самостоятельно,
а вторая возможна только при наличии первой
27
28.
ХИМИЧЕСКАЯ КИНЕТИКАКлассификация сложных реакций
Цепные реакции
реакции, состоящие из ряда взаимосвязанных
стадий, когда частицы, образующиеся в результате
каждой стадии, генерируют последующие
Как правило, цепные реакции протекают с участием
свободных радикалов. Для всех цепных реакций
характерны три типичные стадии:
Николай Николаевич
Семёнов
1. Зарождение цепи (инициация): Сl2 + hν ––> 2 Сl
2. Развитие цепи:
Н2 + Сl• ––> НСl + Н
Н• + Сl2 ––> НСl + Сl
3. Обрыв цепи (рекомбинация):
Стадия развития цепи
характеризуется длиной цепи,
т.е. числом молекул продукта
реакции, приходящихся на одну
активную частицу
Н• + Н• ––> Н2
Сl• + Сl• ––> Сl2
28
29. Автоколебательные химические реакции
ХИМИЧЕСКАЯ КИНЕТИКАКлассификация сложных реакций
Автоколебательные химические реакции
Этого не может быть, потому что этого не может быть никогда!
1951
1958
1964
1969
Б.П. Белоусов
С.Э. Шноль
А.М. Жаботинский
Йодные часы
Бриггса-Раушера
1973
29
30.
ХИМИЧЕСКАЯ КИНЕТИКАКинетика твердофазных реакций
Механизм разрыва связи
Связь между двумя атомами может разрываться по
Гомолитическому механизму, т.е. с образованием радикалов
для разрыва связи требуется энергия активации близкая к энергии
этой связи. Чаще реализуется при реакциях в газовой фазе
Гетеролитическому механизму, т.е. с образованием ионов
для разрыва связи требуется значительно большая энергия.
Чаще реализуется при реакциях в растворах
Цепные реакции – последовательные реакции в которых появление
промежуточной активной частицы (чаще всего радикала) вызывает цепь
превращений исходных веществ
•зарождение
•продолжение
•обрыв цепи
•Неразветвленные – в каждом акте образуется столько же
радикалов
•Разветвленные – число активных частиц возрастает
30
31.
ХИМИЧЕСКАЯ КИНЕТИКАКинетика твердофазных реакций
Основные особенности:
•Реакция происходит на поверхности раздела фаз
•Доставка реагирующих частиц в зону реакции затруднена
•В процессе реакции происходит образование новой фазы
Лимитирующей стадией твердофазных реакций является диффузия
реагентов через слой продукта
Скорость диффузии (dn/dτ) зависит от площади поверхности раздела (S)
и градиента концентраций диффундирующего вещества в слое (dC/dX)
dn
dC
DS
d
dX
А
В
• температура
• малые размеры
• реагенты с повышенной
реакционной способностью
А АВ В
31





























 Физика
Физика Химия
Химия








