Похожие презентации:
(1)Основные понятия молекулярной физики. Молекулярно-кинетическая теория. Идеальный газ
1. Термодинамические параметры
I. Давление газа:F
p
S
Н
p м2 Па
F - суммарная сила, действующая по нормали к
поверхности
S - площадь поверхности
II. Объём газа:
V
V м3
III. Абсолютная температура:
T
T К
T t 273,15 K
1 C 1K
2.
Эмпирические газовые законы (1)Изопроцессы – процессы, протекающие в системе с
постоянной массой газа при каком-либо фиксированном
термодинамическом параметре.
I. p=const
Закон Гей-Люссака:
V V0 (1 V t C ) , где
V V0 ( t 0 C )
температурный коэффициент объемного расширения:
V
1 V
1
V0 T V
273
3.
Эмпирические газовые законы (2)II. V=const
Закон Шарля:
p p0 (1 p t C) , где
p p0 ( t 0 C )
температурный коэффициент объемного расширения:
p
1 p
1
p0 T V
273
III. T=const
Закон Бойля-Мариотта :
pV const
4.
Закон АвогадроРавные объёмы различных газов при одинаковых давлениях и
температурах содержат одно и то же число молекул.
Количество вещества
N
m
NA
M
N A - число Авогадро
М - молярная масса
моль
1
N A 6,02 10
моль
23
5. Уравнение Менделеева-Клапейрона
mPV
RT
M
P
V
m
M
T
R
уравнение состояния идеального газа
- давление газа
- объём газа
- масса газа
- молярная масса газа
- абсолютная температура газа
- универсальная газовая постоянная
Дж
R kN A
R 8,31
моль К
P, V, T – параметры состояния системы
6. Закон Дальтона
pсмесиp
i
i
Давление смеси газов равно сумме их парциальных
давлений.
pi - парциальное давление – давление, которое
данный газ создавал бы в отсутствие остальных
pi ni kT nсмеси kT pсмеси
i
i
7. Получим связь давления идеального газа с его концентрацией и температурой
m RTNA
p
kT nkT
M V
V
n
n - концентрация газа
k - постоянная Больцмана
8. Количество вещества смеси газов
смесиi
i
- количество вещества газов, входящих в состав
смеси
Молярная масса смеси газов
смеси
m
i
i
i
i
m
i
i
mi
i
i
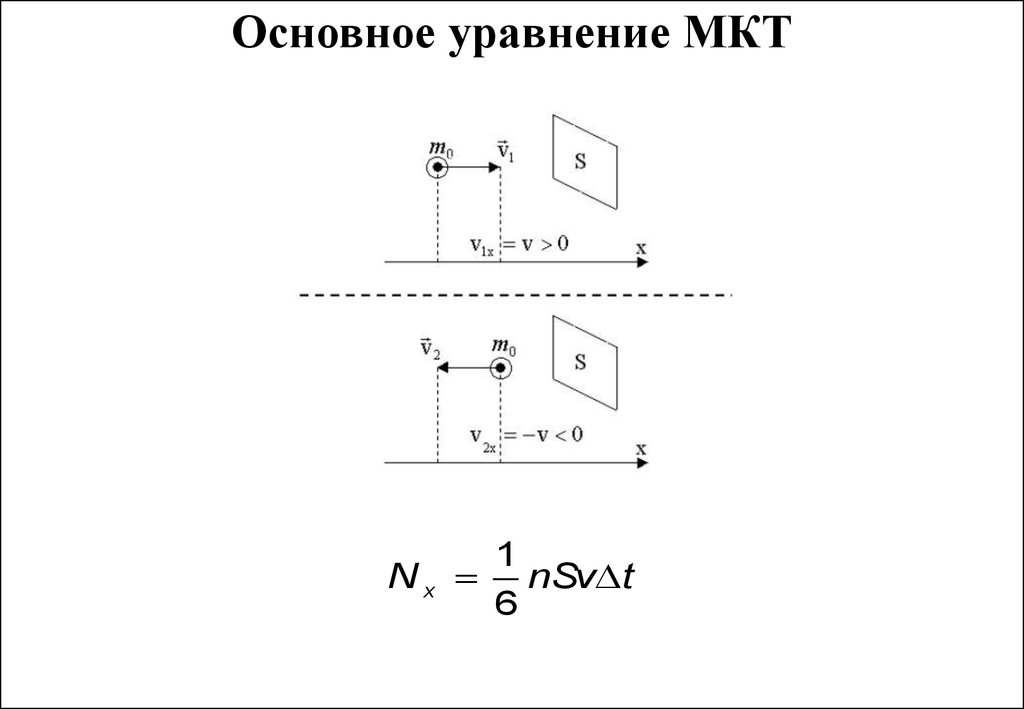
9. Основное уравнение МКТ
Nx1
nSv t
6
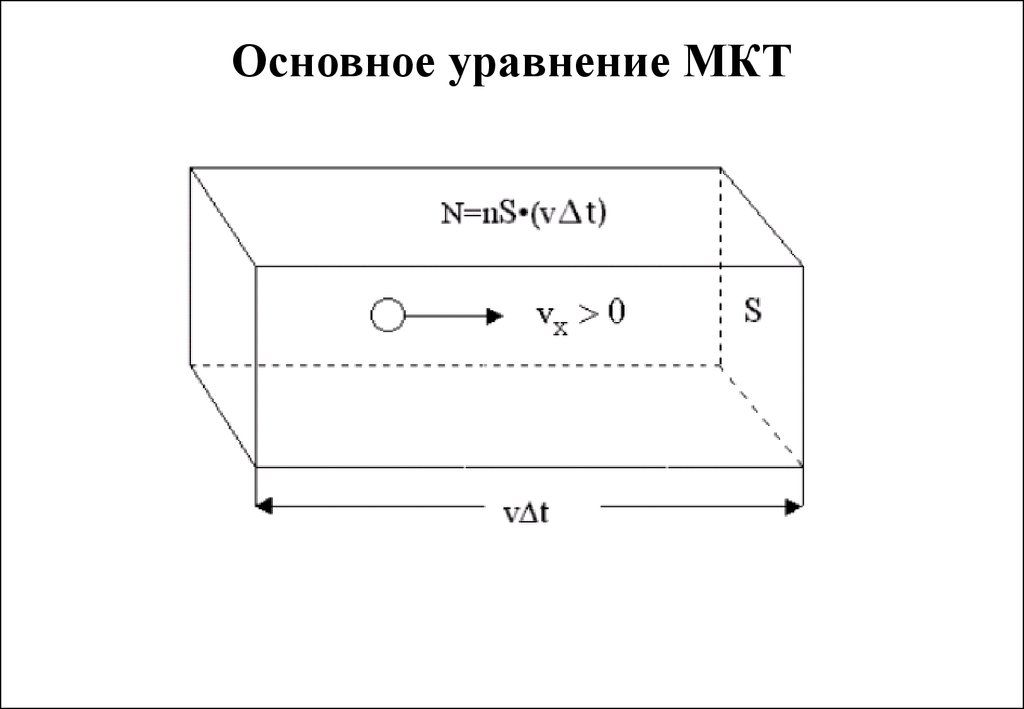
10. Основное уравнение МКТ
11. Основное уравнение МКТ
Средняя сила, действующая на стенку со стороны одноймолекулы:
Fx
vx
2m0v
m0
t
t
Число ударов молекул о стенку за время t:
Nx
Давление газа:
Fx N x
p
S
1
nSv t
6
2
m
v
1
2
0
2
nm0v n
3
3
2
2
n пост
3
пост - средняя кинетическая энергия поступательного движен
одной молекулы
12. Физический смысл температуры T
УравнениеМенделеева-Клапейрона:
pV RT
Основное уравнение
кинетической теории газа:
2
p n
3
1
пост
N
2
RT N
NA
3
1
пост
1
пост
3 R
3
T kT
2 NA
2
k 1, 38 10 23 Дж К










 Физика
Физика








