Похожие презентации:
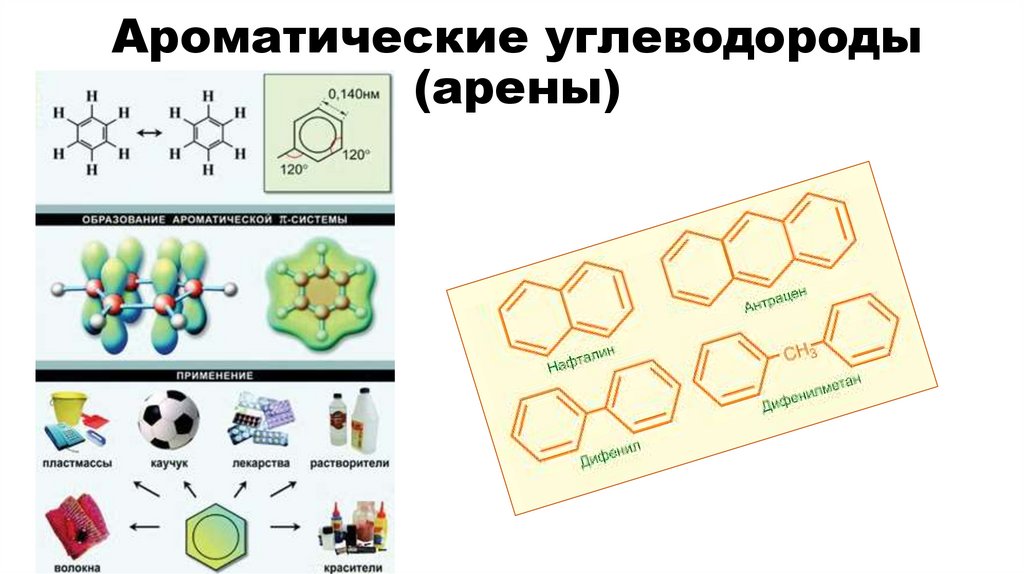
Ароматические углеводороды (арены)
1.
Ароматические углеводороды(арены)
2.
Вопросы лекции:1.
2.
3.
4.
5.
История открытия бензола
Гомологи бензола. Номенклатура и изомерия.
Физические свойства
Химические свойства бензола
Получение бензола
3.
Задания по предыдущим темам1. Напишите структурные формулы веществ:
3-метилпентин-2; 3,6-диэтилоктин-4; 3,4-диметилпентин-1; бутин-1;
пентин-2; 4,4-диметилпентин -2; 2,2,5-триметилгексин-3.
1. Дать определение и написать общую формулу алкадиенов.
2. Дать определение и написать общую формулу алкинов.
1. Назвать вещества по номенклатуре ИЮПАК:
СН2=СН-СН2-СН=СН2
СН2=СН-СН2-СН3
СН =С-СН2-СН3
4.
1. Заполните таблицу по образцуАлкен
Структурная формула
Пентен-1
CH2=CH-CH2-CH2-CH3
Бутен-2
2-метилгексен-2
3-этилдекен-5
2,3,5-триметилнонен-1
Число
атомов
углерода
5
Число атомов
водорода
10
5.
История открытия бензолаВпервые бензол описал немецкий химик Иоганн Глаубер, который
получил это соединение в 1649 году в результате перегонки
каменноугольной смолы. Но названия вещество не получило, и
состав его был неизвестен.
1825 г – Майкл Фарадей установил, что вещество состоит только из
водорода и углерода, назвал его «карбюрированным водородом»
1833 г – Эйльгард Мичерлих определил
эмпирическую формулу С6Н6 нагрел негашеную
известь CaO с бензойной кислотой C6H5COOH
(она содержится во многих ягодах, в частности, в
клюкве и бруснике, и препятствует их гниению) и
получил неизвестную, легкокипящую жидкость с
резким запахом. Вот тогда и вспомнили об
открытии Фарадея. Он назвал его "бензином".
6.
Анализируя различные экспериментальные данные, химики всех стран искали ключ к разгадкестроения бензола. Успеха добился немецкий химик Август Кекуле, и легенда гласит, что идея
пришла к нему во сне. Однажды, размышляя о строении бензола, Кекуле задремал и увидел во
сне змею, которая вцепилась в собственный хвост. Этот сон послужил толчком к гипотезе,
которая впоследствии блестяще подтвердилась, гипотезе о циклическом строении бензола.
В 1865 г. Кекуле предложил для бензола циклическую гексатриеновую структуру, в которой
атомы углерода, замкнутые в шестичленное кольцо, связаны между собой попеременно
простыми и двойными связями, а каждый атом углерода еще соединен с водородом — до
насыщения валентности.
7.
В настоящее время для изображениябензола
принято
использовать
структурные формулы Кекуле или Тиле
8.
Ароматическими углеводородами (аренами) называются вещества, вмолекулах которых содержится одно или несколько бензольных колец —
циклических групп атомов углерода с особым характером связей.
Гомологический ряд бензола отвечает общей формуле С6Н2n-6.
9.
Гомологи бензолаПри замещении одного или более атомов водорода в бензольном
кольце образуются гомологи. Вещества отличаются друг от друга
на один атом углерода. Чем больше атомов углерода, тем
твёрже вещество.
10.
Номенклатура и изомерияСтруктурные именования веществ формируются из названий предельного углеводородного
радикала и окончания «-бензол».
Наряду со структурными используются тривиальные наименованиями, оканчивающиеся на
«-ол». Например, метилбензол – это толуол с формулой С6Н5-СН3.
Если в ароматическом кольце несколько
заместителей, то атомы углерода бензольного
кольца нумеруются: в направлении, где
больше заместителей, от самого главного
заместителя (чем больше атомов углерода в
радикале, тем он старше).
1,2-диметилбензол
11.
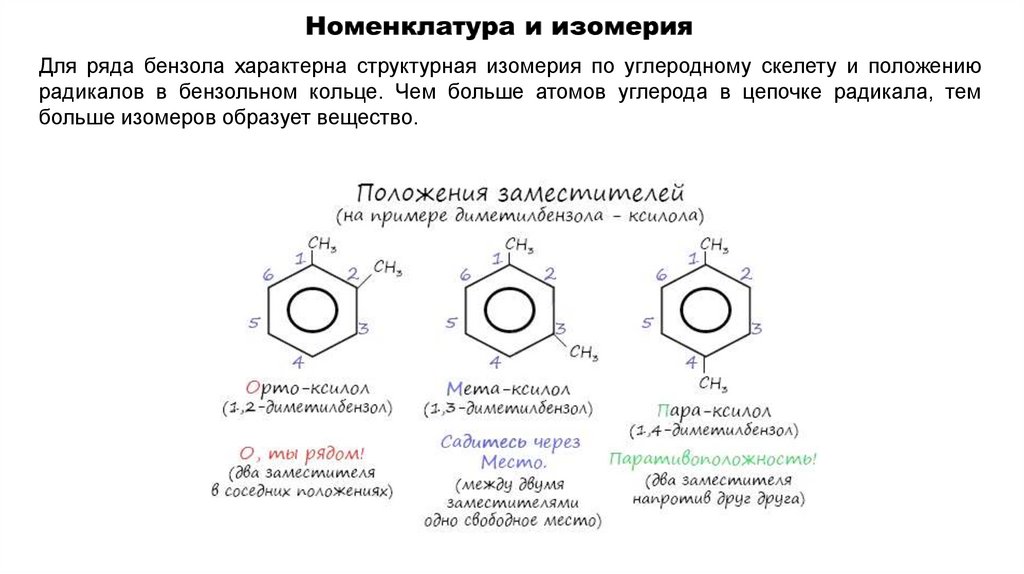
Номенклатура и изомерияЕсли в молекуле бензола присутствуют два заместителя, то также используют систему
специальных приставок:
орто — (о-) если заместители расположены у соседних атомов углерода в бензольном
кольце (1,2-положения);
мета — (м-) заместители расположены через один атом углерода (1,3-положения);
пара — (п-) заместители расположены на противоположных сторонах кольца (1,4положения).
1,2-Диметилбензол
1,3-Диметилбензол
орто-Диметилбензол
мета-Диметилбензол
1,4-Диметилбензол
пара-Диметилбензол
12.
Для ряда бензола характерна структурная изомерия по углеродному скелету и положениюрадикалов в бензольном кольце. Чем больше атомов углерода в цепочке радикала, тем
больше изомеров образует вещество.
13.
Изомерия углеродного скелетаНапишите молекулярные формулы веществ
14.
Физические свойстваБензол – бесцветная, летучая, огнеопасная жидкость со своеобразным
запахом. В воде практически не растворим. Горит сильно коптящим
пламенем. Пары бензола с воздухом образуют взрывчатую смесь.
Жидкий бензол и пары бензола ядовиты! Поражает почки, печень,
костный мозг, кровь. Изменяет формулу крови (при длительном
воздействии), может нарушать структуру хромосом.
Первые члены гомологического ряда бензола –
бесцветные жидкости со специфическим запахом.
Ароматические углеводороды легче воды и в ней не
растворяются,
однако
легко
растворяются
в
органических растворителях – спирте, эфире, ацетоне.
Бензол и его гомологи сами являются хорошими
растворителями для многих органических веществ. Все
арены горят коптящим пламенем ввиду высокого
содержания углерода в их молекулах.
Большинство
ароматических
углеводородов опасны для жизни,
токсичны.
15.
Химические свойства бензолаРеакции замещения в бензольном кольце проходят в присутствии катализаторов: солей
Al(3+) или Fe(3+).
Реакция галогенирования бензола (взаимодействие с бромом — качественная реакция на
бензол):
C6H6 + Br2 = C6H5Br + HBr
16.
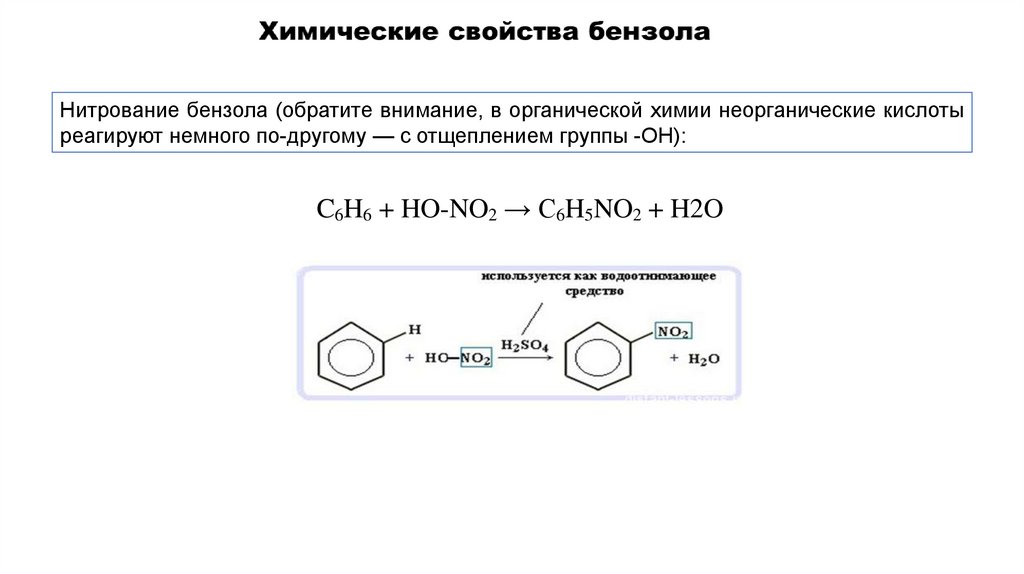
Нитрование бензола (обратите внимание, в органической химии неорганические кислотыреагируют немного по-другому — с отщеплением группы -OH):
C6H6 + HO-NO2 → C6H5NO2 + H2O
17.
АлкилированиеПолучение гомологов бензола, алкилбензолов (катализаторы реакции — галогениды
алюминия: AlCl3, AlBr3 и т.д.):
С6H6 + С2H5Cl → C6H5C2H5 + HCl
18.
Галогенирование алкилбензолов:С6H5-CH3 + Br2 (на свету) = С6H5-CH2Br + HBr
Бром идет в боковую цепь, а не в
кольцо.
Чтобы бром пошел в кольцо, надо использовать катализатор — соли Al(3+)
19.
Нитрование алкилбензоловС6H5-CH3 + 3HNO3 → C6H2CH3(NO2)3
тринитротолуол, он же тротил
20.
ОкислениеРеакция, характерная для алкилбензолов и не характерная для самого бензола
С6H5CH3 + [O] → C6H5COOH — бензойная кислота
21.
Гидрирование бензола и алкилбензоловПри гидрировании всех аренов (температура, давление, катализатор — бензольное кольцо
разорвать не так уж и просто) получаются циклоалканы, а точнее, циклогексан или
циклогексан с радикалами:
С6H5CH3 + 3 H2 → C6H11-CH3 — метилциклогексан
22.
Получение бензолаВ настоящее время основными источниками ароматических соединений, в том числе и
бензола, являются продукты коксования каменного угля (коксовый газ и
каменноугольная смола) и продукты переработки нефти.



















 Химия
Химия








