Похожие презентации:
Арены - ароматические соединения
1.
2.
Ароматические соединения, или арены,— большая группа соединений
карбоциклического ряда, молекулы
которых содержат устойчивую
циклическую группировку из шести
атомов углерода (бензольное кольцо),
обладающую особыми физическими и
химическими свойствами.
СnН2n-6
3. Фридрих Август Кекуле 7.09. 1829 г.–13.07. 1896 г. Первую наиболее удачную структурную формулу строения бензола предложил
1896 г.Фридрих Август Кекуле
7.09. 1829 г.–13.07.
Первую наиболее удачную структурную
формулу строения бензола предложил
немецкий химик Ф.А.Кекуле в 1865 г.
4.
5. Атомы углерода в бензоле замкнуты в цикл, в котором соблюдается валентность углерода (IV) и двойные связи чередуются с
одинарными.По современным представлениям молекула бензола
является правильным шестиугольником.
Эта формула отражает равноценность 6 атомов
углерода.
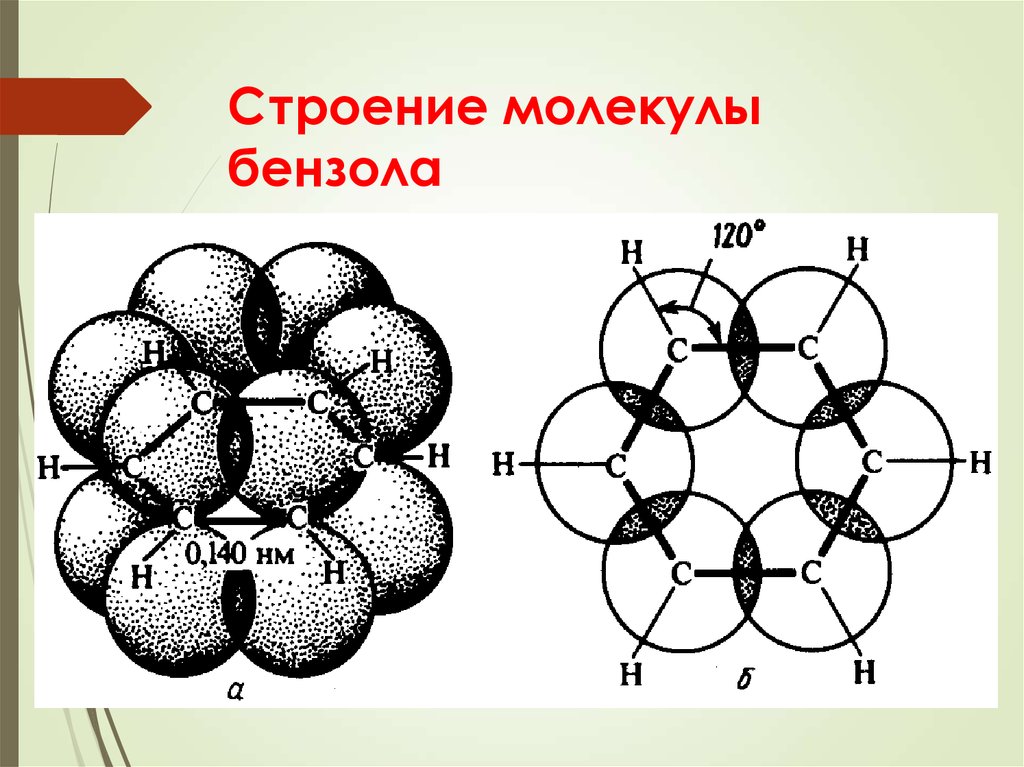
Атомы углерода находятся в SP2 – гибридизации.
Валентные углы между σ – связями равны 120 0,
длина связи С-С равна 0,14 нм. Лежащие в одной
плоскости 6 атомов углерода образуют σ –скелет
молекулы. При взаимном перекрывании образуется
единое π – электронное облако, т е. происходит
декализация электронов. Все связи между атомами
углерода выравнены.
6. Строение молекулы бензола
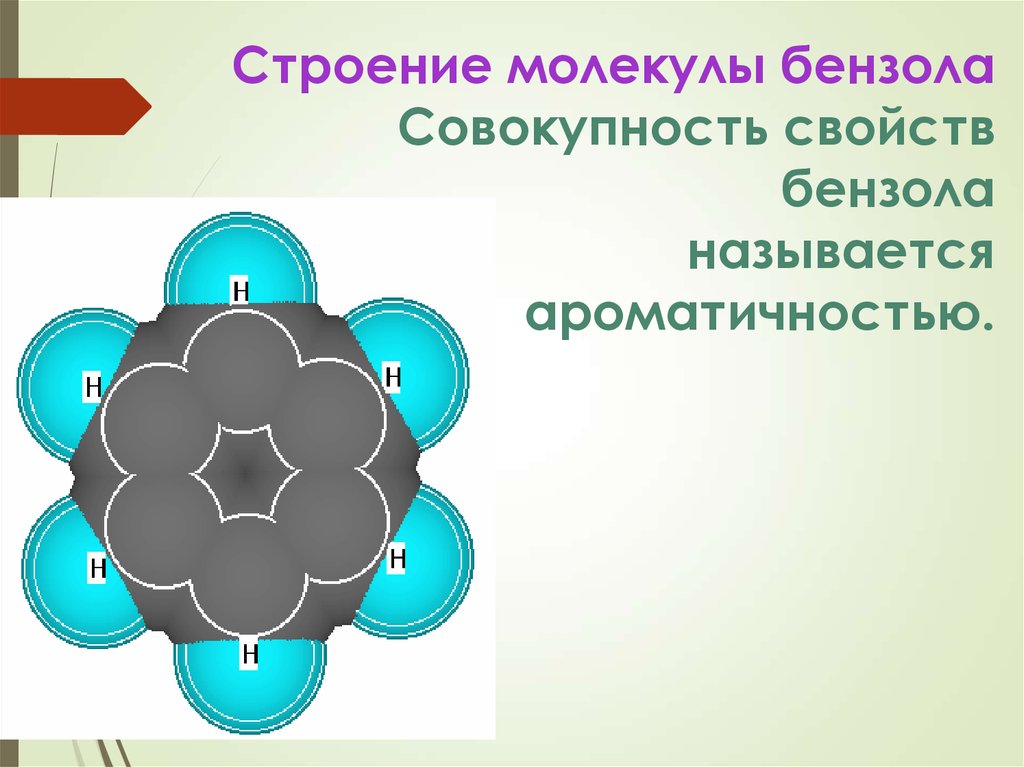
7. Строение молекулы бензола Совокупность свойств бензола называется ароматичностью.
8.
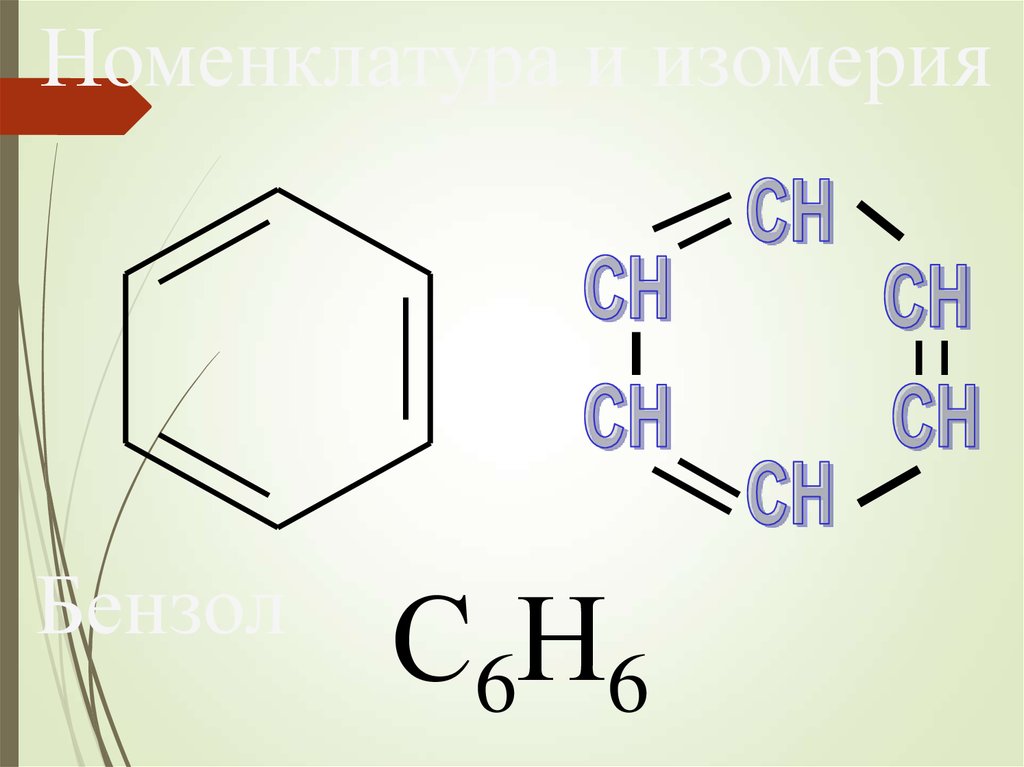
Номенклатура и изомерияБензол
С6Н6
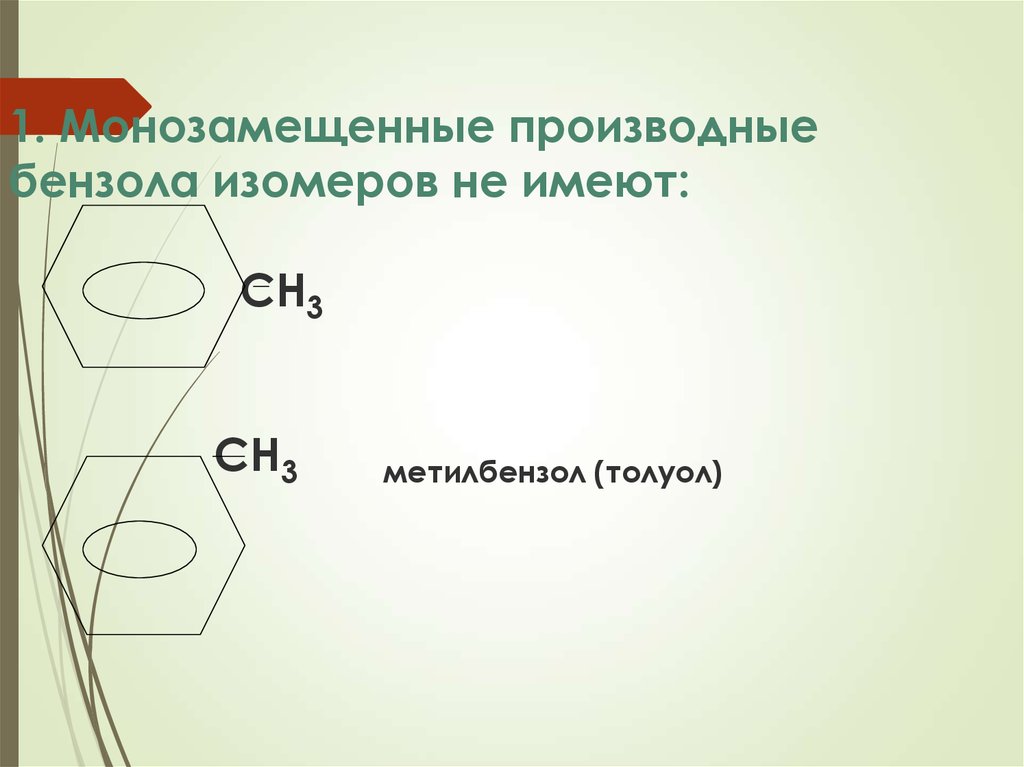
9. 1. Монозамещенные производные бензола изомеров не имеют: СН3 СН3 метилбензол (толуол)
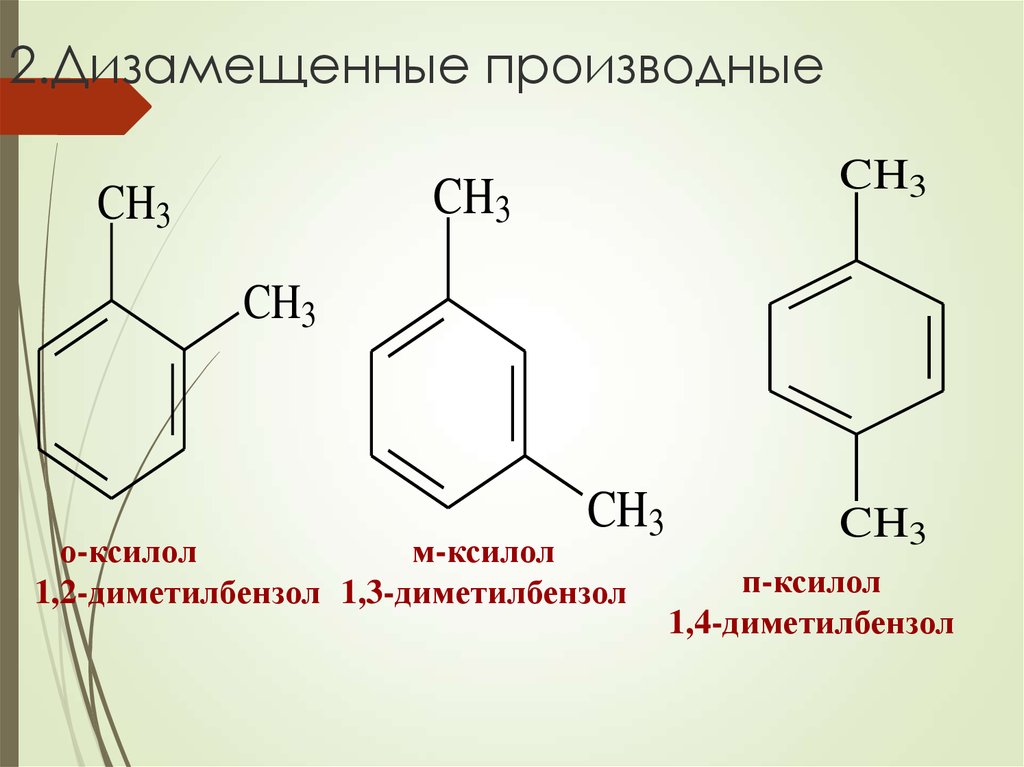
10. 2.Дизамещенные производные
CH3CH3
CH3
CH3
CH3
о-ксилол
м-ксилол
1,2-диметилбензол 1,3-диметилбензол
CH3
п-ксилол
1,4-диметилбензол
11.
1) . Бензол образуется из циклогексана2) . Бензол образуется из гексана
3) .Бензол образуется из ацетилена
(реакция Зелинского)
4). Лабораторный способ получения бензола
12.
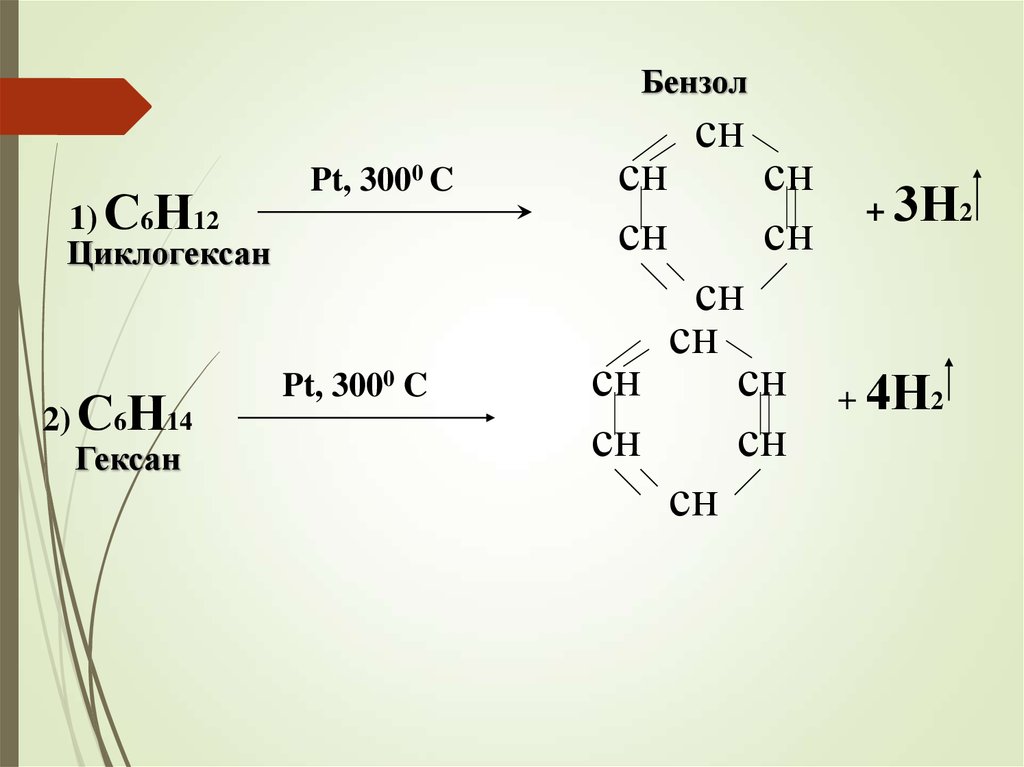
Бензол1) С6Н12
Циклогексан
2) С6Н14
Гексан
Pt, 3000 C
Pt, 3000 C
сн
сн
сн
сн
сн
сн
сн
сн
сн
сн
сн
сн
+ 3Н2
+ 4Н2
13.
3).3С2Н2C, 6000 C
Ацетилен
4). С6Н5СООNа +NаОН → Nа2СО3 + С6Н6
сплав
14.
Агрегатноесостояние
ЖИДКОСТЬ
Температура 5,50С (ПОВЫШАЕТСЯ С УВЕЛИЧЕНИЕМ
плавления
относительных молекулярных МАСС)
Температура
кипения
80,10С (ПОВЫШАЕТСЯ С УВЕЛИЧЕНИЕМ
ОТНОСИТЕЛЬНЫХ
МОЛЕКУЛЯРНЫХ МАСС)
15.
1. РЕАКЦИИ ЭЛЕКТРОФИЛЬНОГО ЗАМЕЩЕНИЯ(замещение атомов Н в бензольном кольце)
а) Реакция галогенирования
СН
СН
СН
СН
СН
СН
БЕНЗОЛ
+ Br2
FeCl3 ,t
БРОМБЕНЗОЛ
C6H5Br + HBr
16.
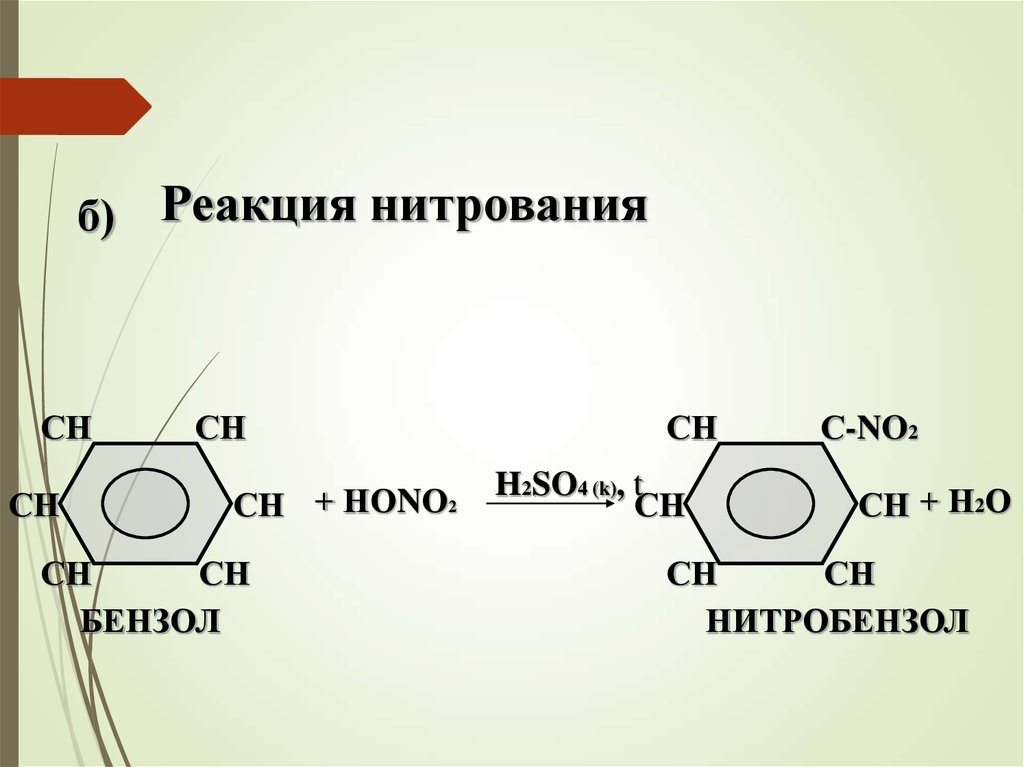
б) Реакция нитрованияСН
СН
СН
СН + НОNО2
СН
СН
БЕНЗОЛ
СН
H2SO4 (k), t
СН
С-NO2
СН + Н2О
СН
СН
НИТРОБЕНЗОЛ
17. в)Реакция сульфирования +НОSО3Н С6Н6 С6Н5SО3Н - Н2О сульфобензол
18.
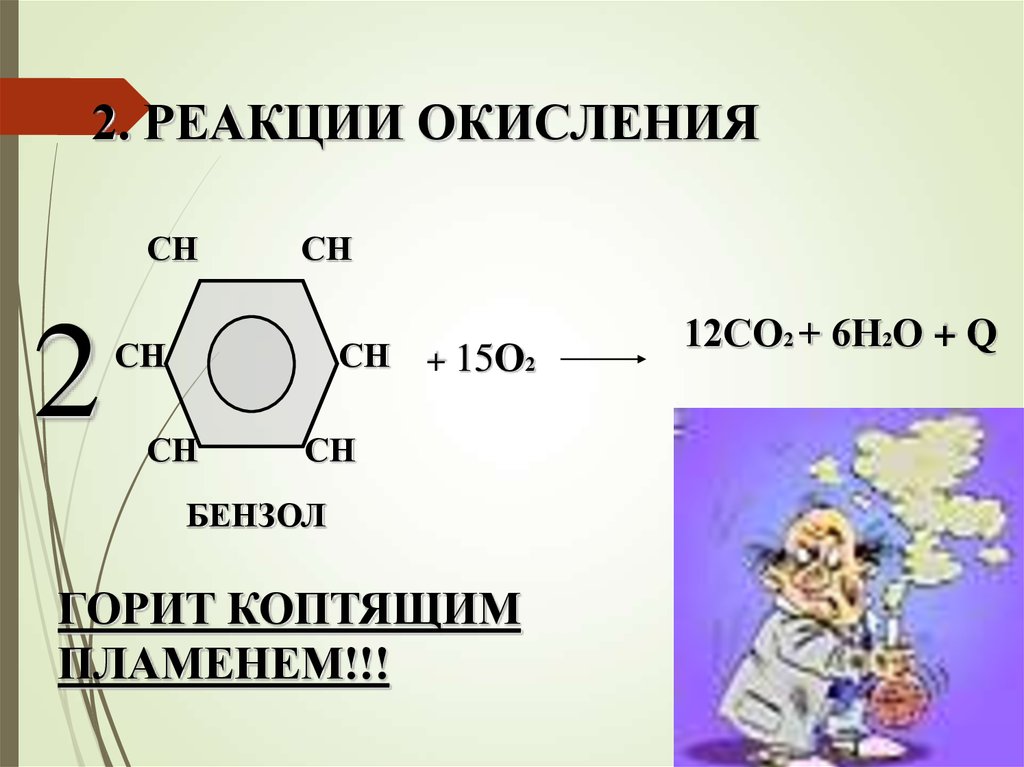
2. РЕАКЦИИ ОКИСЛЕНИЯСН
2
СН
СН
СН
СН
+ 15О2
СН
БЕНЗОЛ
ГОРИТ КОПТЯЩИМ
ПЛАМЕНЕМ!!!
12СО2 + 6Н2О + Q
19.
Реакция окисления гомологов бензолаСН3
Толуол
[О]
СООН
Бензойная кислота
[О]= КМnО4 + Н2SО4
20.
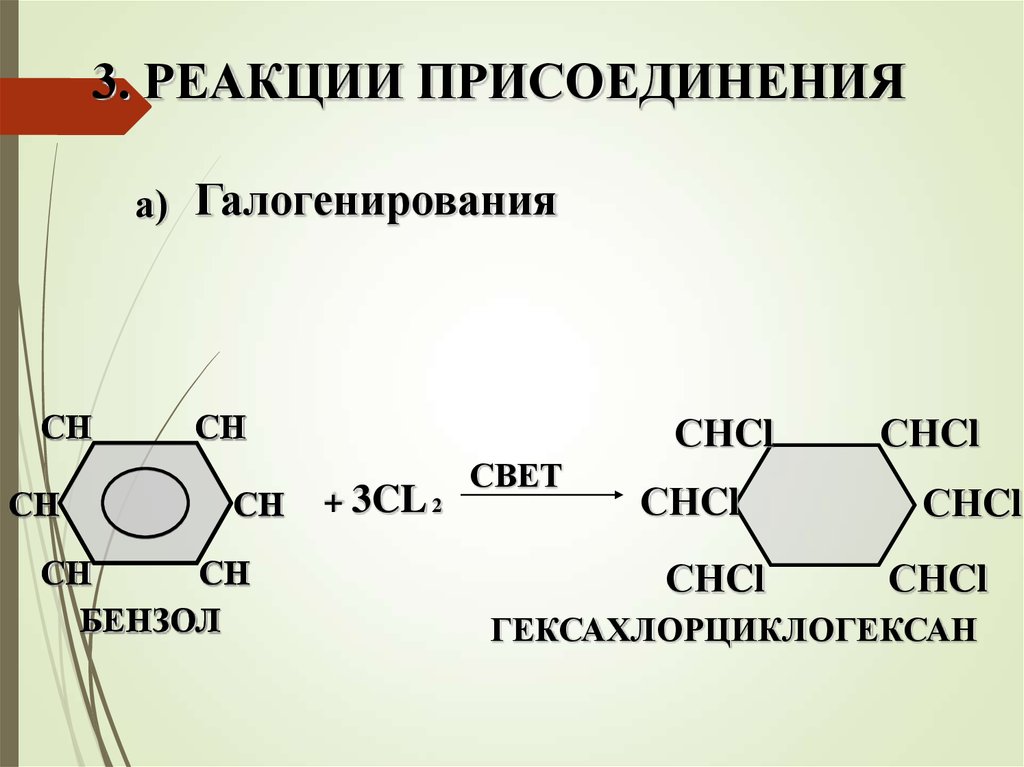
3. РЕАКЦИИ ПРИСОЕДИНЕНИЯа) Галогенирования
СН
СН
СН
СН
СН
СН
БЕНЗОЛ
СНCl
+ 3CL 2
СВЕТ
СНCl
СНCl
СНCl
СНCl
СНCl
ГЕКСАХЛОРЦИКЛОГЕКСАН
21.
б)СН
СН
Гидрирование
СН
СН + 3Н2
СН
СН
БЕНЗОЛ
СН2
КТ, t
СН2
СН2
СН2
СН2
СН2
ЦИКЛОГЕКСАН
22.
Реакции электрофильногозамещения для гомологов бензола
Эффекты заместителей при электрофильном
замещении
1. Заместители (ориентанты) первого рода: —ОН, —
OR, —OCOR, —SH, —NH2, —NHR, (Hal). Эти
заместители смещают электронную плотность в
сторону бензольного кольца, т.е. обладают
электронодонорными свойствами. Они активируют
бензольное кольцо (за исключением галогенов).
Облегчая вхождение электрофильных реагентов в
бензольное кольцо, они ориентируют новый
заместитель в орто- и пара-положения. Такие
заместители называют орто- и пара-ориентантами.
23.
OH-
-
фенол
-
24.
2. Заместители (ориентанты) второго рода: —CN, —СООН, —SO3H, —СНО, —COR, —COOR, —NO2.
Эти заместители смещают электронную плотность
от бензольного кольца, т.е. они обладают
электроноакцепторными свойствами. Эти
заместители дезактивируют бензольное кольцо,
затрудняя вхождение электрофильных реагентов.
При этом вновь входящий заместитель ориентируют
в мета-положение. Такие заместители называют
мета-ориентантами.
25.
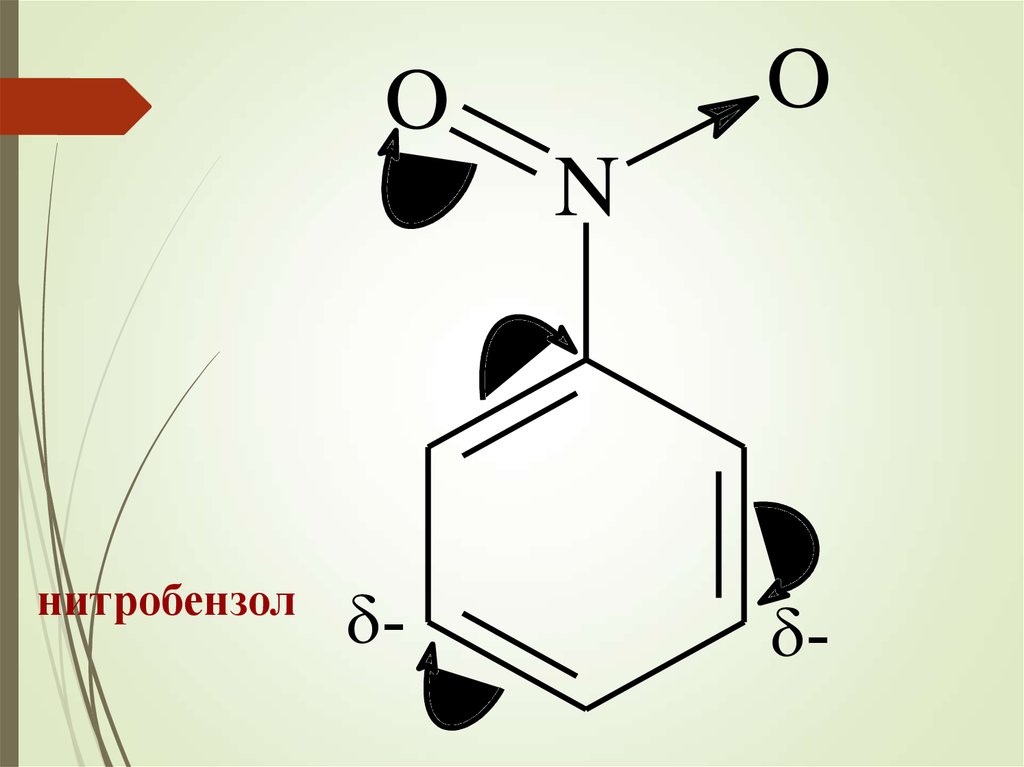
OO
N
нитробензол
-
-
26.
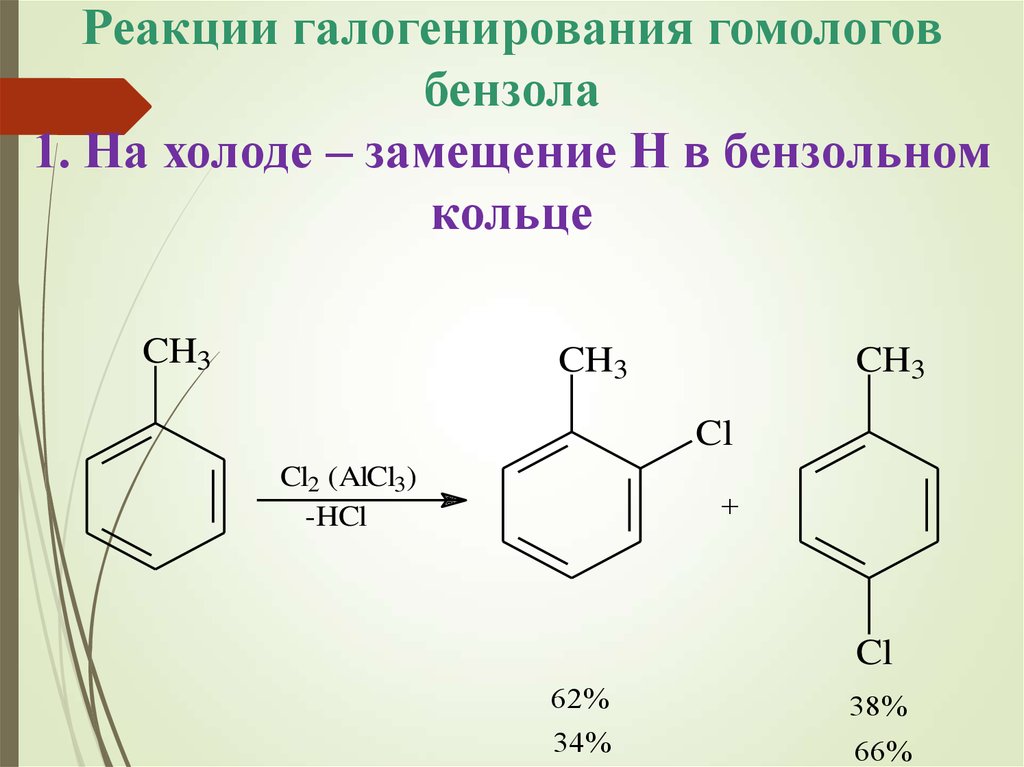
Реакции галогенирования гомологовбензола
1. На холоде – замещение Н в бензольном
кольце
CH3
CH3
CH3
Cl
Cl2 (AlCl3)
-HCl
+
Cl
62%
38%
34%
66%
27.
2). На свету происходит замещение Н вбоковой цепи
+Сl - Сl
СН3
СН2Сl + НСl
хлористый
бензил
28.
Многоядерные ареныНафталин - бесцветное
кр.вещество, tплавл. = 800 С
8
1
7
2
3
6
5
4
29.
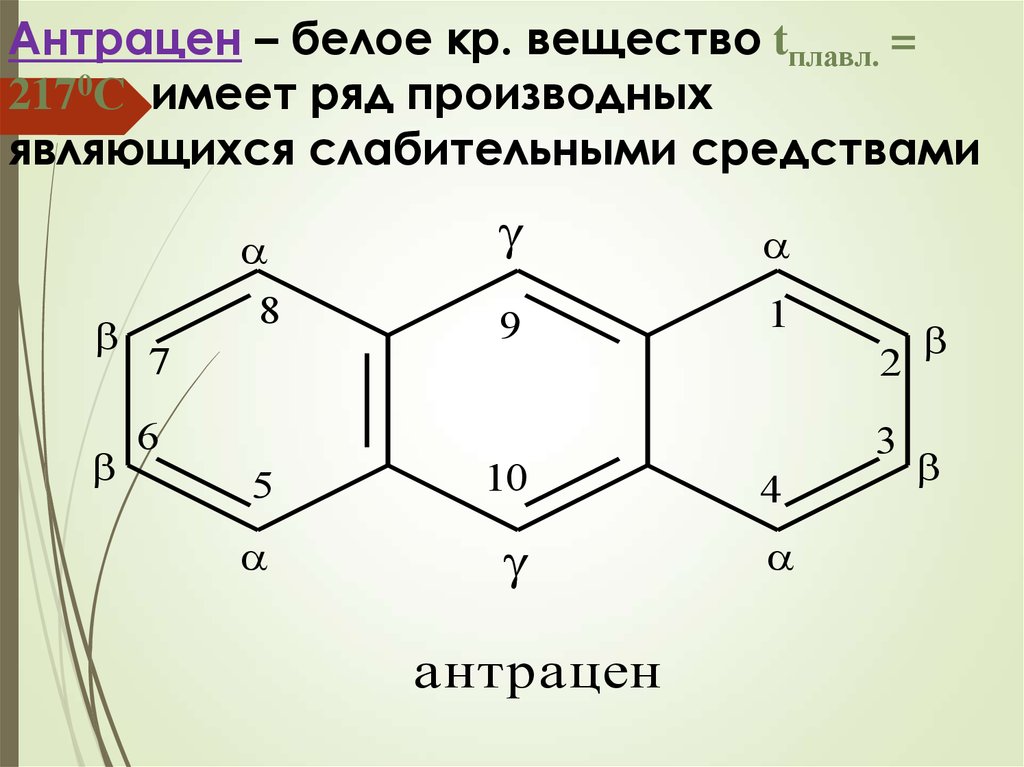
Антрацен – белое кр. вещество tплавл. =2170С имеет ряд производных
являющихся слабительными средствами
8
7
6
9
1
2
3
5
10
4
антрацен
30.
Фенантрен – кр. вещество, tплавл. = 1000С входит в состав ценныхалкалоидов. Фенантрен основа класса орг.веществ – стероидов,
выполняющих в организме роль гормонов – регуляторов
жизненных процессов. Многие из них применяются
как ЛП – гидрокортизон, эстрадиол.
9
10
8
1
2
7
6
5
4
3
31.
Получениепластмасс
красители
КИСЛОТЫ
с6н5-он
Лавсановые
волокна
инсектициды
лекарства
С6Н6
Получение
пластмасс
анилин
с6н5-с2н5
Бутадиенстироль
ный каучук
сахарин
с6н5-сн=сн2
растворители
красители
с6н5 - сн3



















 Химия
Химия








