Похожие презентации:
Бериллий, магний и щелочно-земельные металлы
1.
2.
Щёлочноземельные металлыэлементы IIA группыCa
Щелочноземельными являются не все
элементы IIА группы, а только начиная с
кальция и вниз в подгруппе.
Sr
Оксиды этих элементов («земли» - по
старинной терминологии) взаимодействуют с
водой, образуя щелочи.
Ba
Ra
3.
Ве - металл, которомусоответствуют амфотерный
оксид и гидроксид
Mg – металл,
Сa, Sr,Ba - щёлочноземельные
металлы
Ra –радиоактивный элемент
4.
Общая характеристика элементов главнойподгруппы II группы
5.
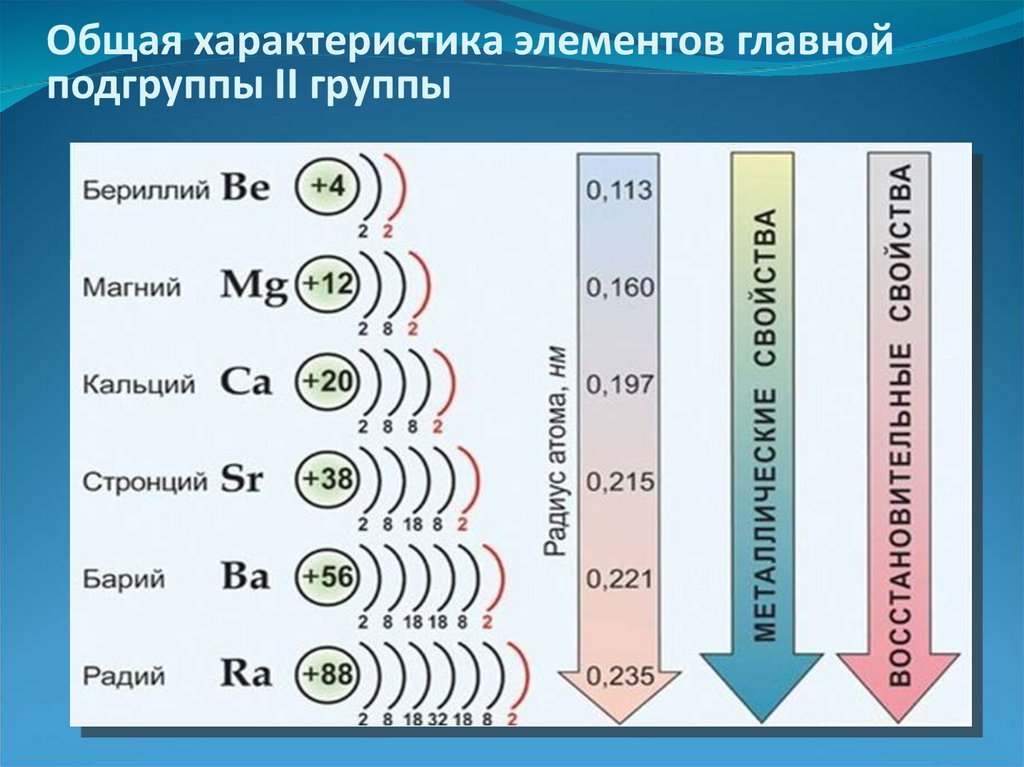
Общая характеристика элементов главнойподгруппы II группы
Одинаковое строение внешнего электронного слоя
Элементы проявляют ст.ок. +2 в сложных вещ-ах
Атомы элементов являются сильными
восстановителями, т.к. содержат 2 электрона на
внешнем энергетическом уровне.
С увеличением № элементов увеличивается атомный
радиус, увеличивается число электронных слоев,
следовательно возрастает легкость отдачи
электронов. Восстановительные свойства
увеличиваются в группе сверху вниз.
6.
Нахождение в природеКак активные металлы, они
встречаются в природе только в виде
соединений
Кальциевые горные породы –
известняк, мрамор, мел.
Магниевая горная порода –
магнезит.
6
7.
БериллийМагний
Барий
Радий
Кальций
Стронций
8.
Физические свойстваКальций - твердый и
пластичный
Магний - относительно
мягкий, пластичный,
25.11.20
ковкий
Щелочные металлы легкие,
мягкие и легкоплавкие,
серебристы, стронций
имеет золотистый оттенок.
Бериллий - светлосерый, твердый,
хрупкий
Стронций ковкий
8
9.
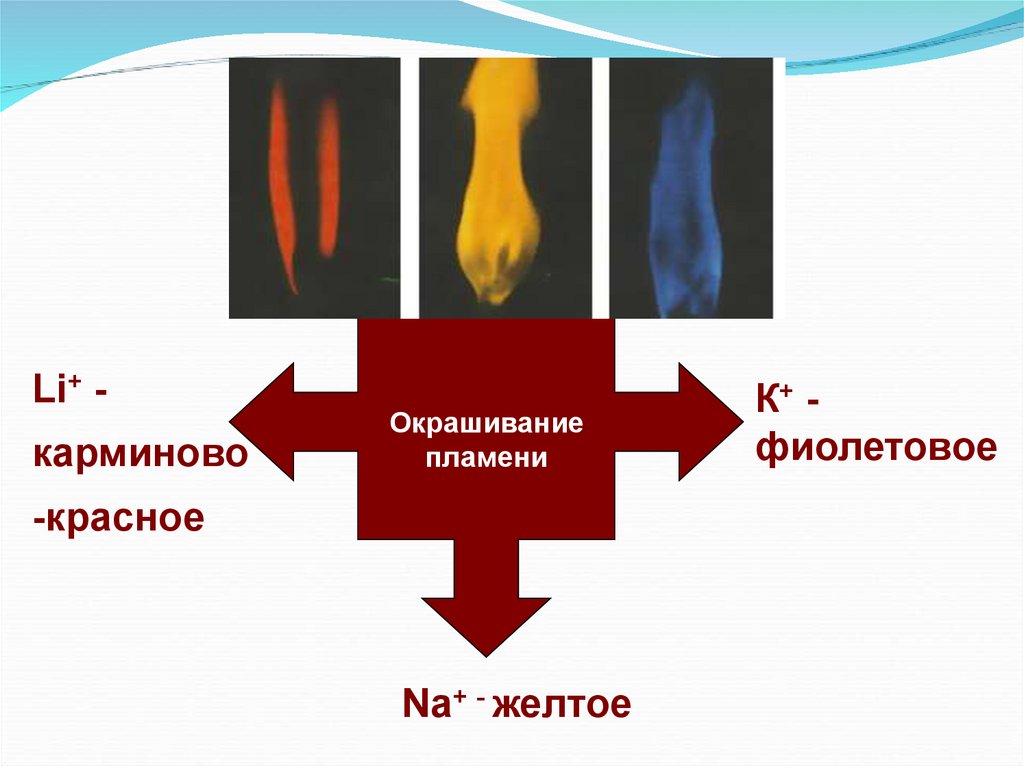
Li+ карминовоОкрашивание
пламени
-красное
Na+ - желтое
К+ фиолетовое
10.
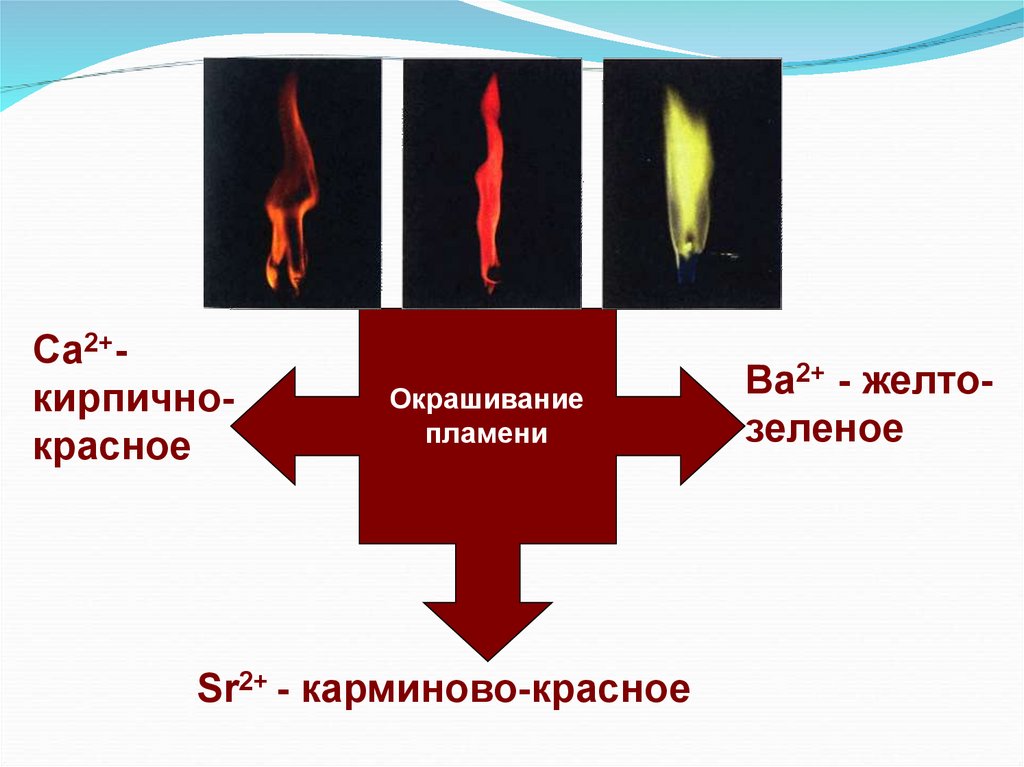
Са2+кирпичнокрасноеОкрашивание
пламени
Sr2+ - карминово-красное
Bа2+ - желтозеленое
11.
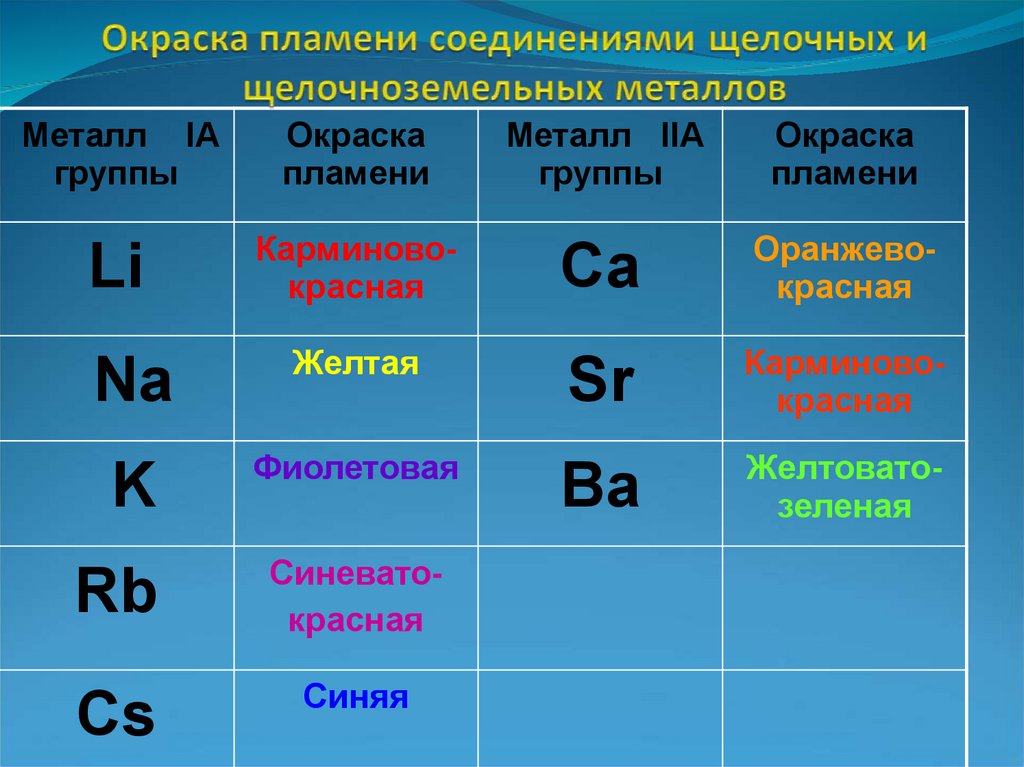
Металл IАгруппы
Окраска
пламени
Li
Карминовокрасная
Na
Желтая
K
Фиолетовая
Rb
Синеватокрасная
Cs
Синяя
Металл IIА
группы
Окраска
пламени
Ca
Оранжевокрасная
Sr
Карминовокрасная
Ba
Желтоватозеленая
12.
РАЗДЕЛ: Соли элементов IIA группы13.
14.
Химические свойства элементовIIА группы
Взаимодействуют с простыми веществами
1.С кислородом
2Mе+O2=2MеO (оксид)
2.С галогенами
Mе+Cl2=MеCl2 (хлорид)
3.С серой
Mе+S=MеS (сульфид)
4.С азотом
3Mе+N2=Mе3N2 (нитрид)
5.С водородом
Mе+H2=MеH2 (гидрид)
6.С водой
Mе+2H2O=Mе(OH)2+H2
15.
Химические свойства1. Металлы взаимодействуют почти со
всеми
неметаллами:
2Ме0 + О20 =2Ме+2О-2 (оксид)
Ме0 + Н20 = Ме+2Н2-1 (гидрид)
Ме0 + Cl20 = Mе+2Cl2-1 (хлорид)
Ме0 + S0 = Mе+2S-2 (сульфид)
3Ме0 + N20 = Mе3+2N2-3 (нитрид)
25.11.20
15
16.
Взаимодействие с кислотамиВсе взаимодействуют с хлороводородной и
разбавленной серной кислотами с выделением
водорода:
Be + 2HCl = BeCl2 + H2
Разбавленную азотную кислоту металлы
восстанавливают главным образом до аммиака
или нитрата аммония:
2Ca + 10HNO3 (разб.) = 4Ca(NO3)2 +
NH4NO3 + 3H2O
В концентрированных азотной и серной кислотах
(без нагревания) бериллий пассивирует,
остальные металлы реагируют с этими
кислотами.
17.
Взаимодействие со щелочамиБериллий взаимодействует с водными
растворами щелочей:
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2
Остальные металлы IIА группы с
щелочами не реагируют.
18.
Как и алюминий, Mg и Са способнывосстанавливать редкие
металлы из их оксидов:
2Mg+TiO2=2MgO + Ti
5Ca + V2O5 = 5CaO + 2V
Такие способы получения называют
магниетермией и кальциетермией
19.
Проверь себя(работа с таблицей Д.И. Менделеева)
Сравните атомы элементов, поставив знаки <, >
или = вместо *:
а) заряд ядра: Be* Ba; Мg * Al; Ca * К;
б) число электронных слоев: Be * Ba; Мg * Al;
Ca * К;
в) число электронов на внешнем уровне:
Be * Ba; Мg * Al; Ca * К;
г) радиус атома: Be * Ba; Мg * Al; Ca * K;
д) восстановительные свойства: Be* Ba; Мg *Al;
Ca * K.
25.11.20
19
20.
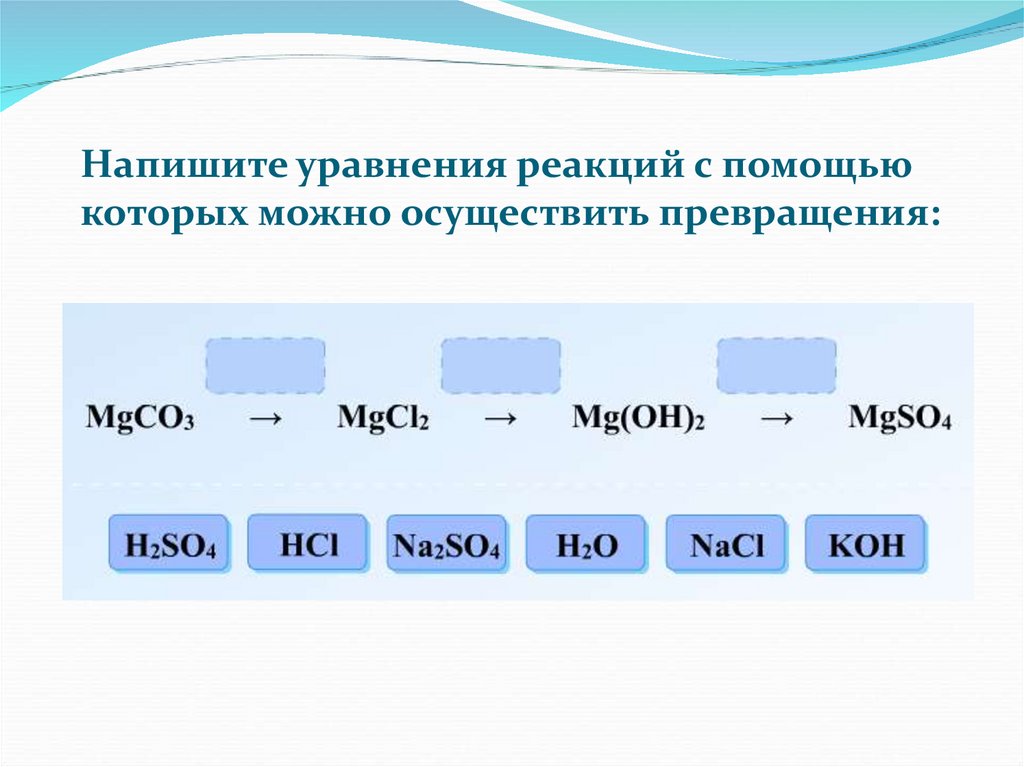
Напишите уравнения реакций с помощьюкоторых можно осуществить превращения:
21.
Домашнее задание:§ 13 (до с. 59 - «Соединения бериллия …»)
Переписать презентацию в тетрадь
Пройти интерактив в электронном приложении к
учебнику















 Химия
Химия








