Похожие презентации:
Карбоновые кислоты
1. Органическая химия
Центр дистанционного обученияОрганическая химия
ФИО преподавателя: Коновалова Надежда Валерьевна
e-mail: nadejda_73@mail.ru
Online-edu.mirea.ru
online.mirea.ru
2. Тема лекции: Карбоновые кислоты
Центр дистанционного обученияТема лекции: Карбоновые кислоты
Карбоновые кислоты - органические вещества, молекулы которых
содержат одну или несколько карбоксильных групп -СООН.
Номенклатура и классификация карбоновых кислот
1. Одноосновные карбоновые кислоты
1.1. Алифатические
а) насыщенные (предельные)
O
H C
O
CH3
OH
муравьиная кислота
(метановая кислота)
C
OH
уксусная кислота
(этановая кислота)
O
CH3
CH2
C
O
CH3
OH
пропионовая кислота
(пропановая кислота)
CH2
CH2
C
OH
масляная кислота
(бутановая кислота)
online.mirea.ru
3.
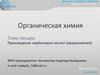
Центр дистанционного обучения1. Одноосновные карбоновые кислоты
1.1. Алифатические
а) насыщенные (предельные)
O
CH3
CH2
CH2
CH2
O
C
CH3
OH
валериановая кислота
(пентановая)
CH2
CH2
CH2
CH2
C
OH
капроновая кислота
(гексановая)
CH2
C
OH
CH 3
изовалериановая кислота
(3-метилбутановая кислота)
O
CH3
CH
O
CH3
CH
CH3
C
OH
изомасляная кислота
(2-метилпропановая)
online.mirea.ru
4.
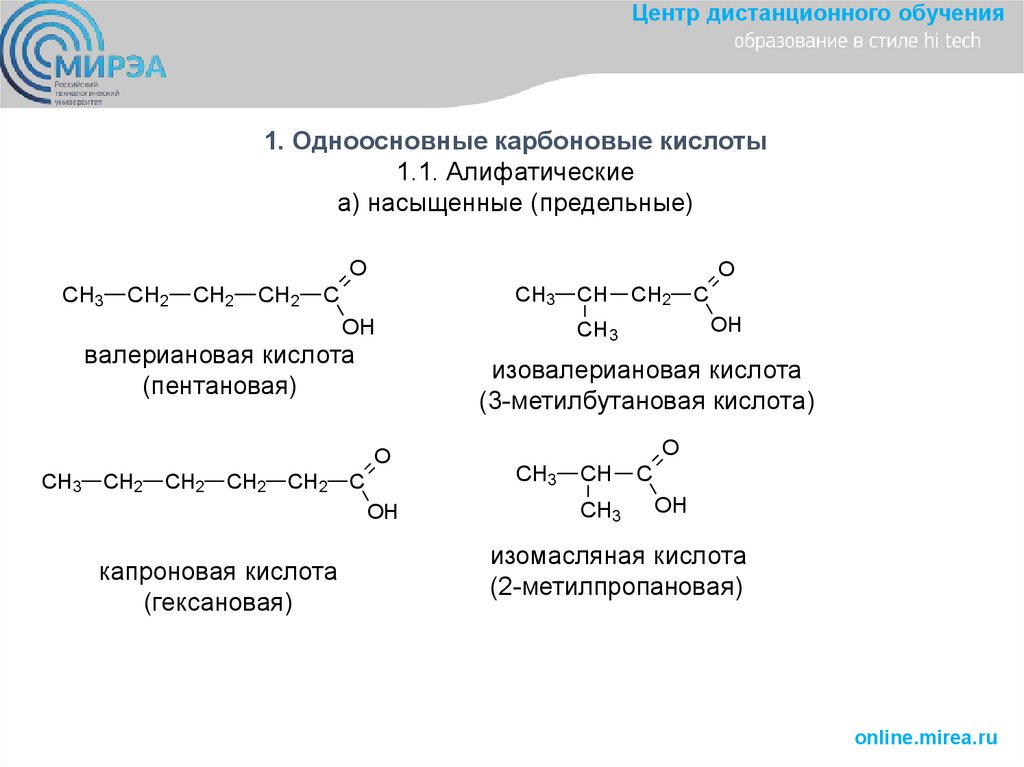
Центр дистанционного обучения• б) ненасыщенные (непредельные)
O
CH 2
CH C
OH
акриловая кислота
(пропеновая кислота)
O
CH3
CH CH C
OH
кротоновая кислота
(2-бутеновая кислота)
• 1.2. Ароматические
C
O
OH
O
C
C
O
OH
OH
бензойная кислота
(бензолкарбоновая)
OH
салициловая кислота
(2-гидроксибензойная)
CH3
пара-толуиловая кислота
(4-метилбензойная)
online.mirea.ru
5.
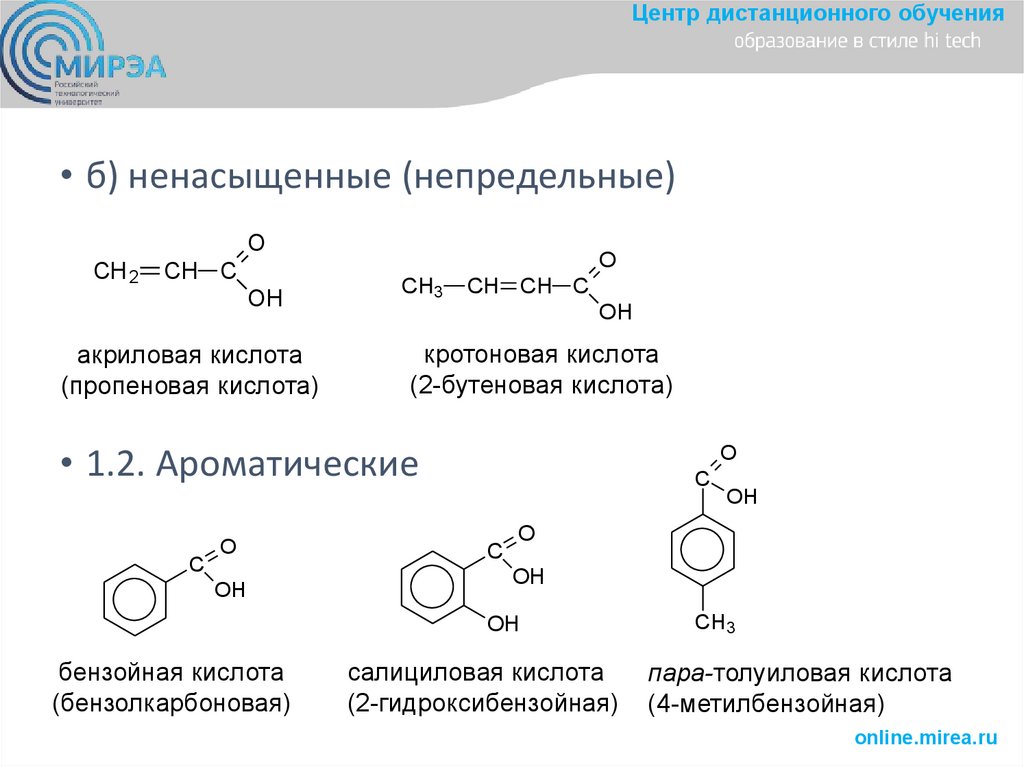
Центр дистанционного обучения• 1.3. Алициклические
O
CH2 CH COOH
CH2
циклопропанкарбоновая
кислота
C
C
O
OH
OH
циклопентанкарбоновая
кислота
циклогексанкарбоновая
кислота
• 1.4. Гетероциклические
C
O
OH
N
никотиновая кислота
(3-пиридинкарбоновая)
O
C
O
OH
пирослизевая кислота
(2-фуранкарбоновая)
online.mirea.ru
6.
Центр дистанционного обучения• 2. Двухосновные карбоновые кислоты
• 2.1. Алифатические
• а) насыщенные (предельные)
HOOC COOH
щавелевая кислота (этандиовая кислота)
COOH
H2C
COOH
CH2
COOH
CH2
COOH
CH2
COOH
CH2
CH2
малоновая кислота (1,3-пропандиовая)
янтарная кислота (1,4-бутандиовая кислота)
глутаровая кислота (1,5-пентандиовая)
COOH
online.mirea.ru
7.
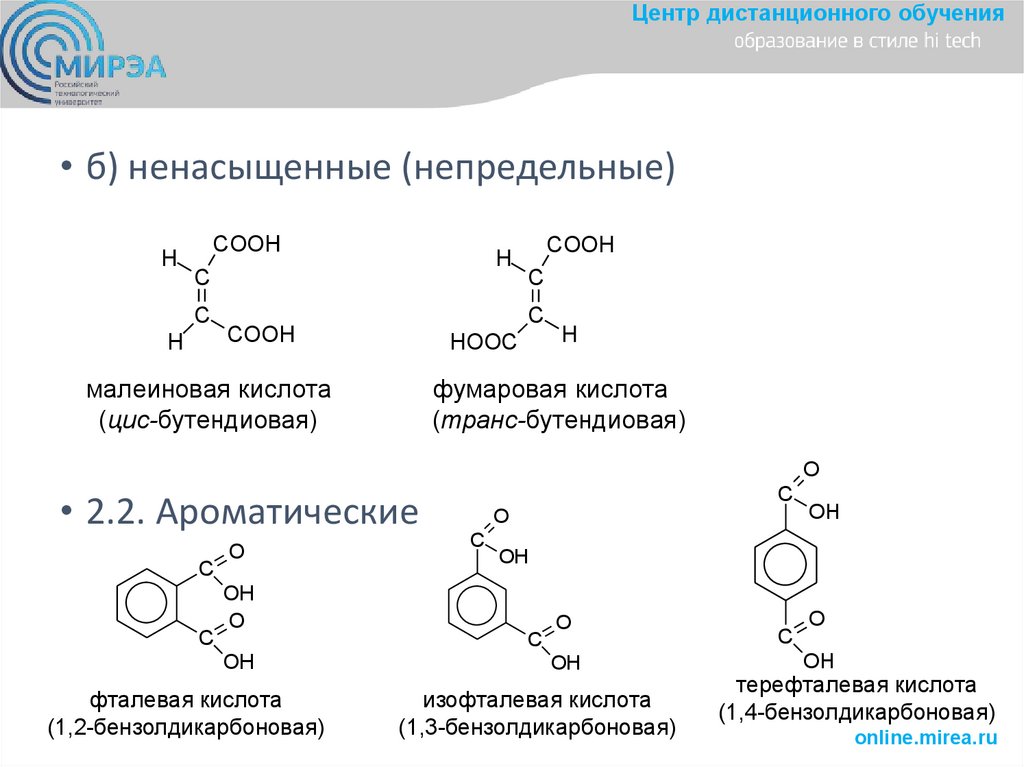
Центр дистанционного обучения• б) ненасыщенные (непредельные)
H
COOH
H
C
C
H
COOH
C
C
COOH
HOOC
малеиновая кислота
(цис-бутендиовая)
H
фумаровая кислота
(транс-бутендиовая)
O
• 2.2. Ароматические
C
C
O
OH
O
OH
фталевая кислота
(1,2-бензолдикарбоновая)
C
O
C
OH
OH
C
O
OH
изофталевая кислота
(1,3-бензолдикарбоновая)
C
O
OH
терефталевая кислота
(1,4-бензолдикарбоновая)
online.mirea.ru
8.
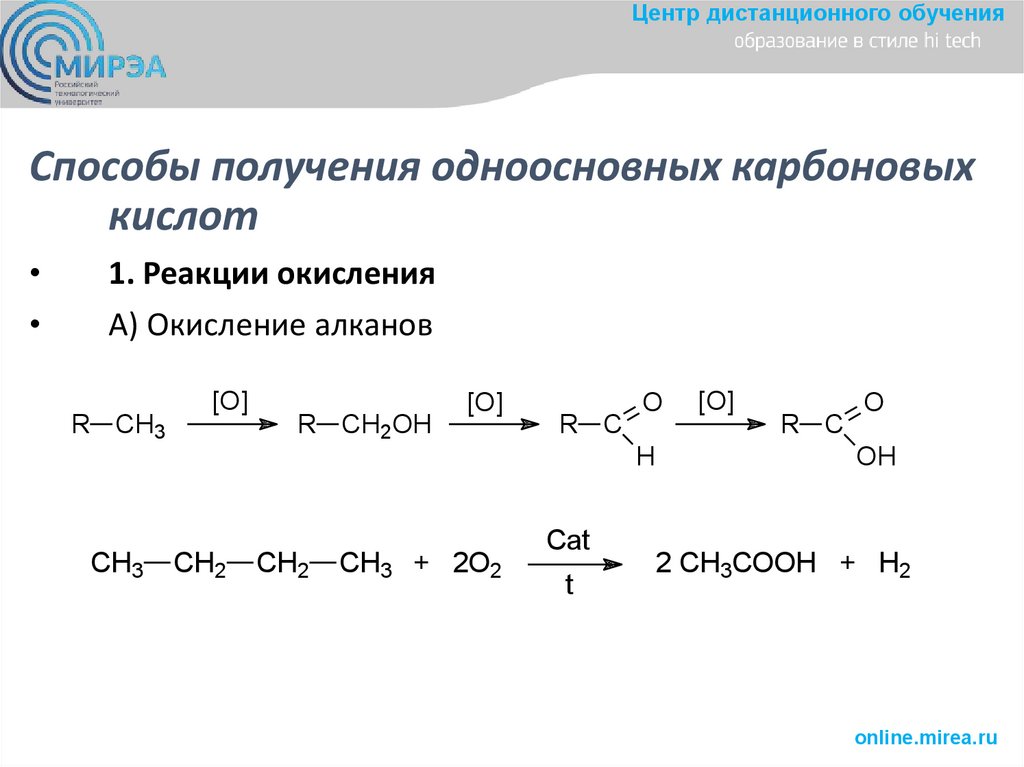
Центр дистанционного обученияСпособы получения одноосновных карбоновых
кислот
1. Реакции окисления
А) Окисление алканов
R CH3
CH3
[O]
CH2
R CH2OH
CH2
[O]
CH3 + 2O2
R C
O
H
Cat
t
[O]
R C
O
OH
2 CH3COOH + H2
online.mirea.ru
9.
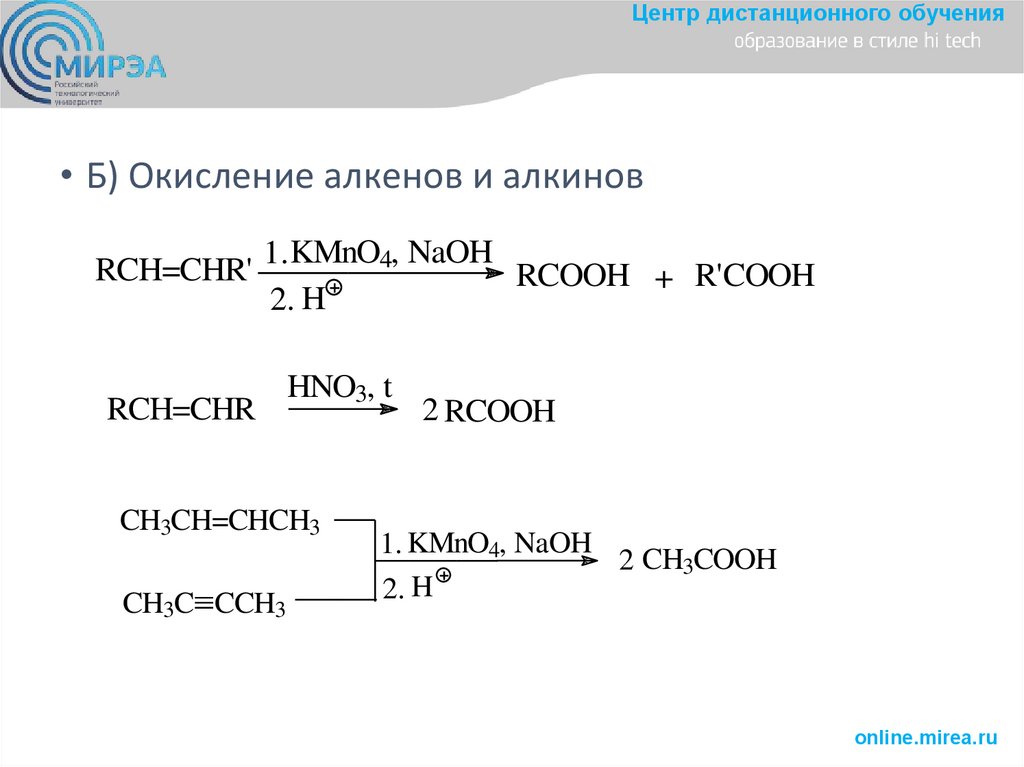
Центр дистанционного обучения• Б) Окисление алкенов и алкинов
RCH=CHR'
1. KMnO4, NaOH
RCOOH + R'COOH
2. H
RCH=CHR
HNO3, t
CH3CH=CHCH3
CH3C CCH3
2 RCOOH
1. KMnO4, NaOH
2 CH3COOH
2. H
online.mirea.ru
10.
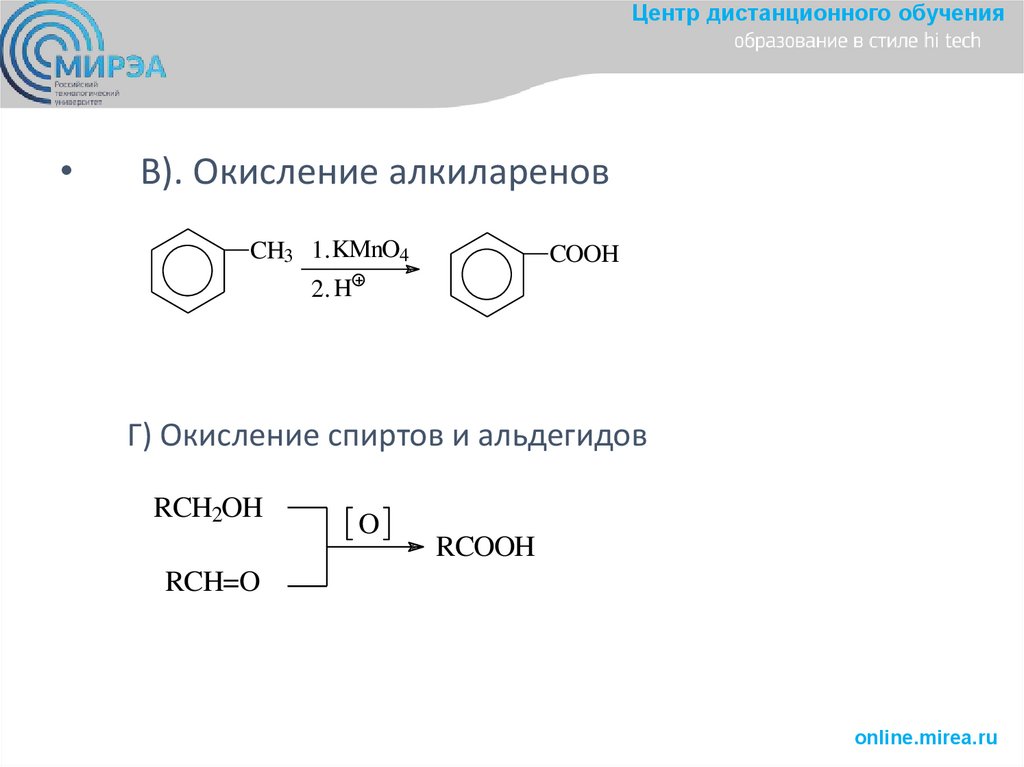
Центр дистанционного обученияВ). Окисление алкиларенов
CH3 1. KMnO4
COOH
2. H
Г) Окисление спиртов и альдегидов
RCH2OH
O
RCOOH
RCH=O
online.mirea.ru
11.
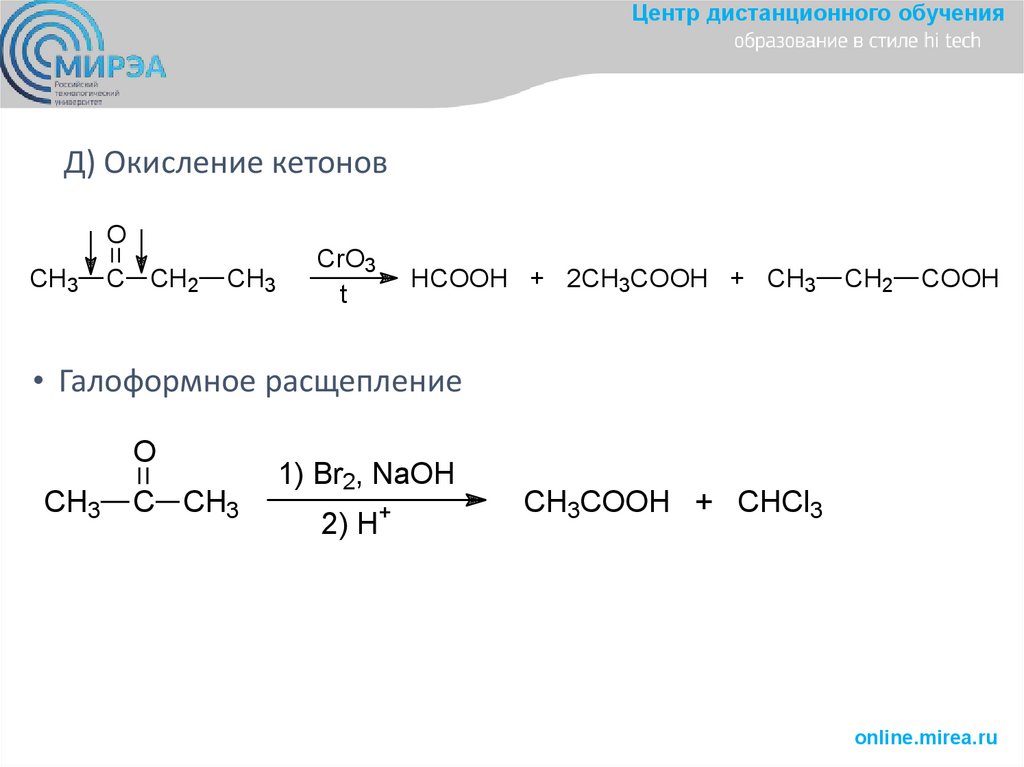
Центр дистанционного обученияД) Окисление кетонов
O
CH3
C CH2
CH3
CrO3
t
HCOOH + 2CH3COOH + CH3
CH2
COOH
• Галоформное расщепление
O
CH3
C CH3
1) Br2, NaOH
2) H+
CH3COOH + CHCl3
online.mirea.ru
12.
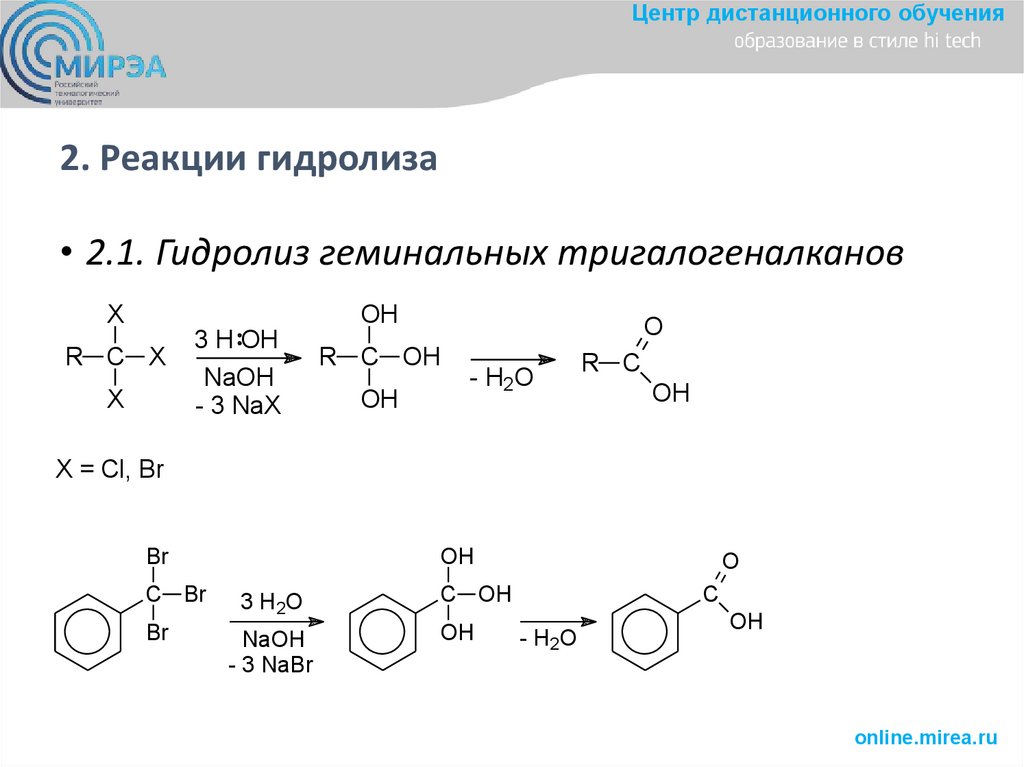
Центр дистанционного обучения2. Реакции гидролиза
• 2.1. Гидролиз геминальных тригалогеналканов
X
R C X
X
3 H OH
NaOH
- 3 NaX
OH
R C OH
OH
O
- H2O
R C
OH
X = Cl, Br
Br
C Br
Br
OH
3 H2O
NaOH
- 3 NaBr
O
C OH
OH
C
- H2O
OH
online.mirea.ru
13.
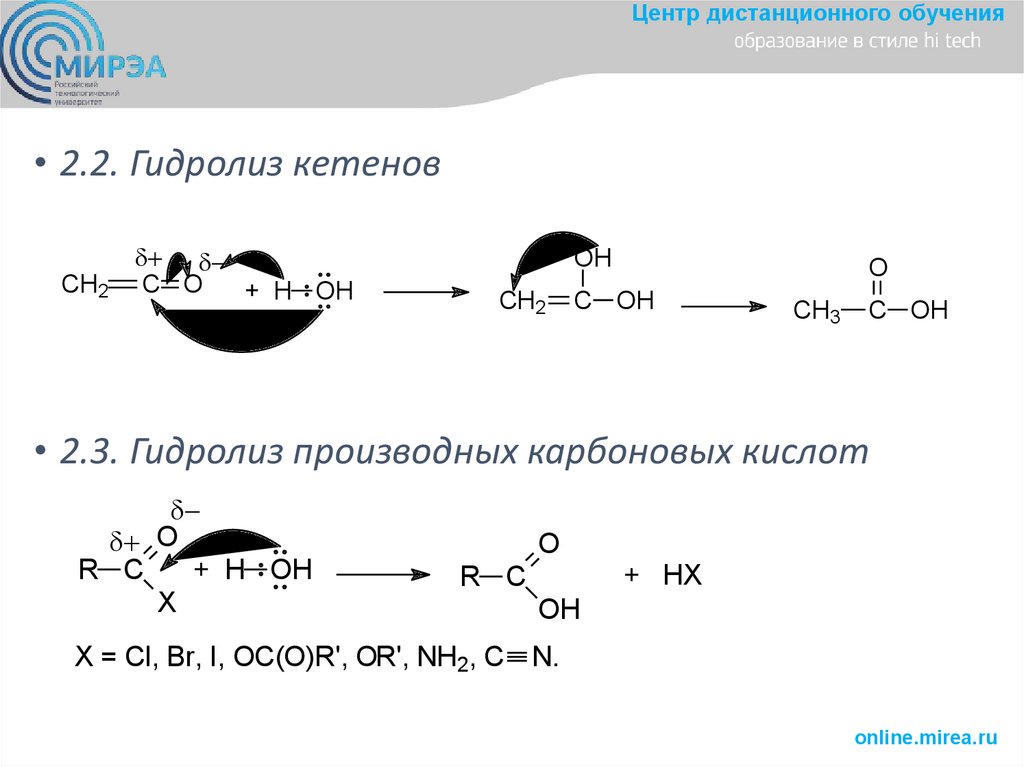
Центр дистанционного обучения• 2.2. Гидролиз кетенов
CH2
C O
+ H OH
OH
CH2
O
C OH
CH3
C OH
• 2.3. Гидролиз производных карбоновых кислот
O
R C
+ H OH
X
O
+ HX
R C
OH
X = Cl, Br, I, OC(O)R', OR', NH2, C N.
online.mirea.ru
14.
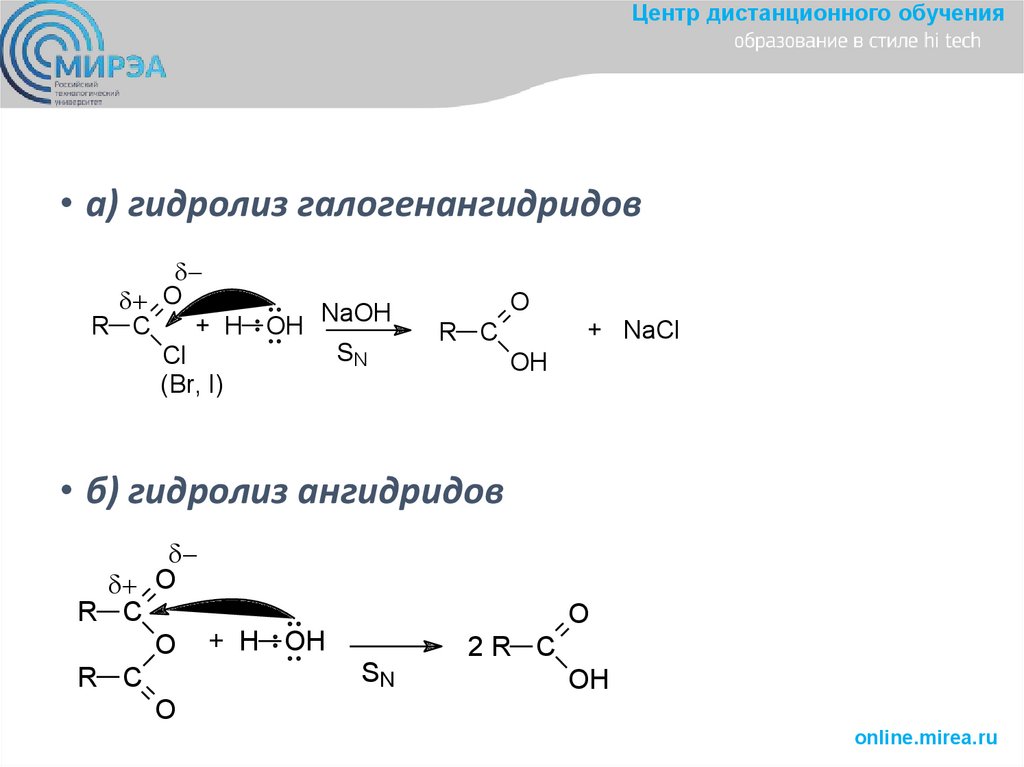
Центр дистанционного обучения• а) гидролиз галогенангидридов
O
NaOH
R C
+ H OH
SN
Cl
(Br, I)
O
+ NaCl
R C
OH
• б) гидролиз ангидридов
O
R C
O + H OH
R C
O
O
SN
2R C
OH
online.mirea.ru
15.
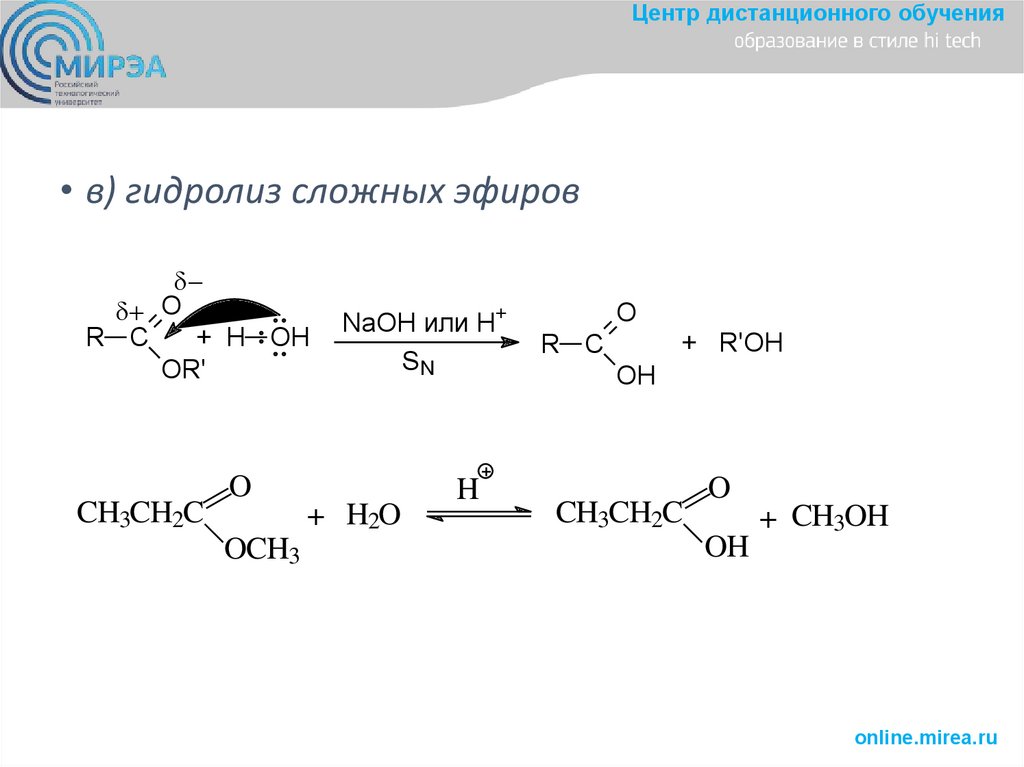
Центр дистанционного обучения• в) гидролиз сложных эфиров
O
R C
+ H OH
OR'
CH3CH2C
NaOH или H+
SN
O
+ H2O
OCH3
H
O
+ R'OH
R C
OH
CH3CH2C
O
+ CH3OH
OH
online.mirea.ru
16.
Центр дистанционного обученияг) гидролиз амидов
O
R C
+ H OH
NH2
CH3C NH
O
NaOH
SN
H2O
NaOH
O
R C
-
+
O Na
+ NH3
CH3C ONa + NH2
O
online.mirea.ru
17.
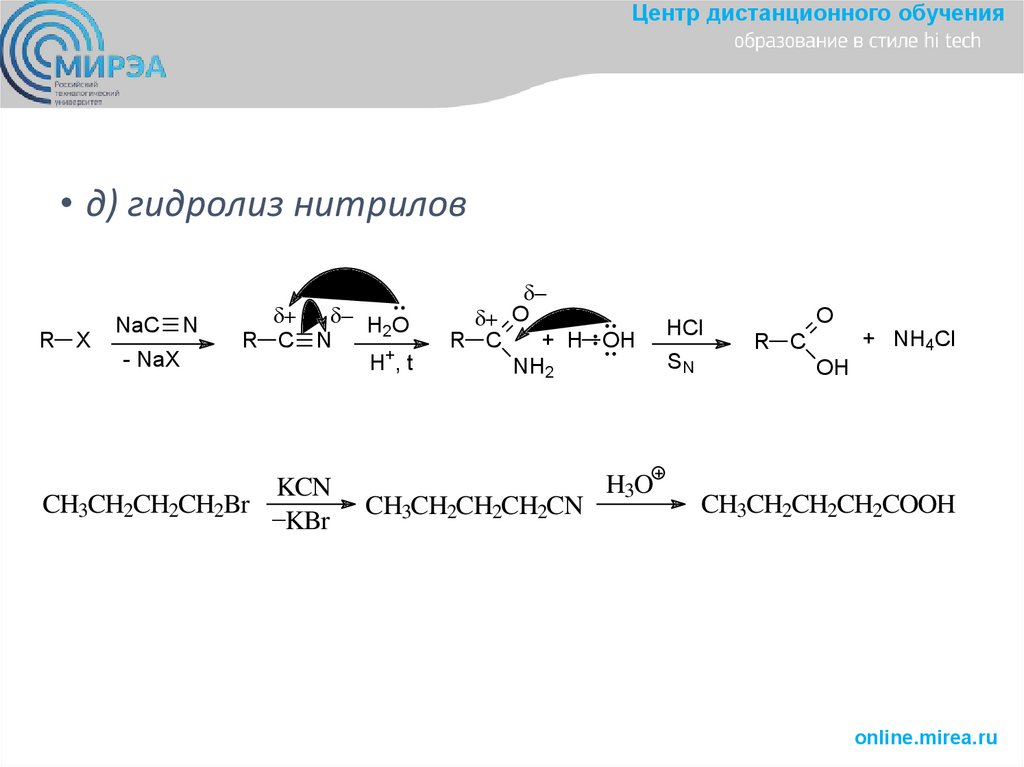
Центр дистанционного обучения• д) гидролиз нитрилов
R X
NaC N
- NaX
H O
2
R C N
H+, t
KCN
CH3CH2CH2CH2Br _
KBr
O
R C
+ H OH
NH2
CH3CH2CH2CH2CN
H3O
HCl
SN
O
R C
+ NH4Cl
OH
CH3CH2CH2CH2COOH
online.mirea.ru
18.
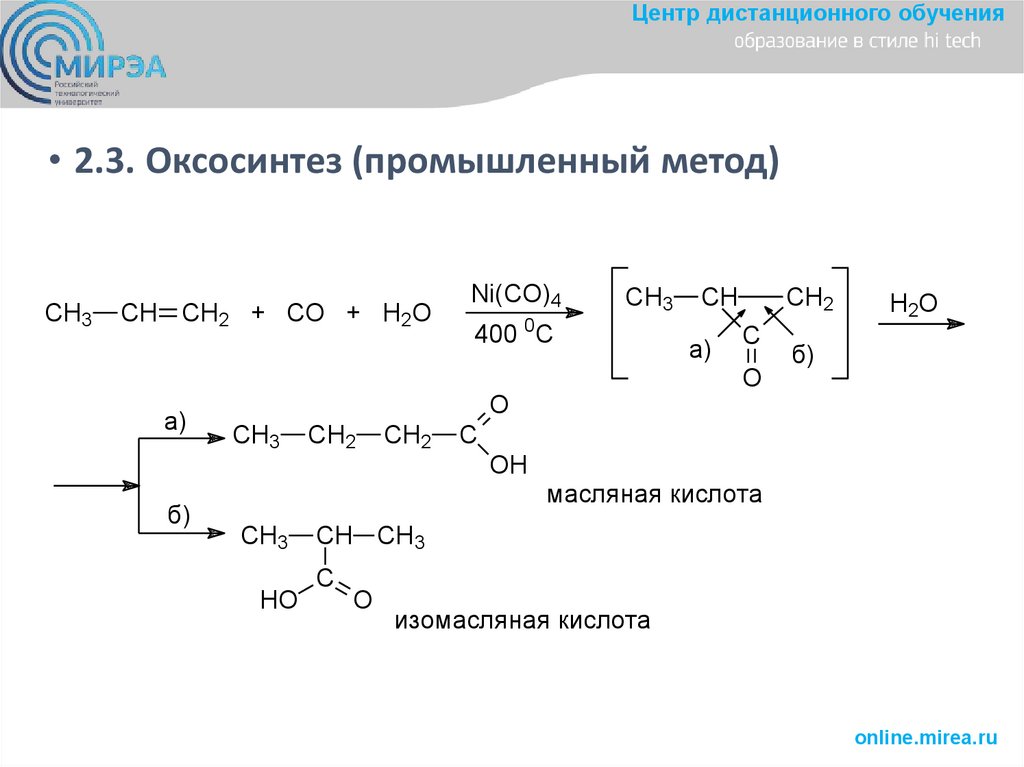
Центр дистанционного обучения• 2.3. Оксосинтез (промышленный метод)
CH3
CH CH2 + CO + H2O
a)
б)
Ni(CO)4
CH3
400 0C
CH2
CH2
a)
CH2
C
O
O
CH3
CH
H 2O
б)
C
OH
масляная кислота
CH3
HO
CH CH3
C
O
изомасляная кислота
online.mirea.ru
19.
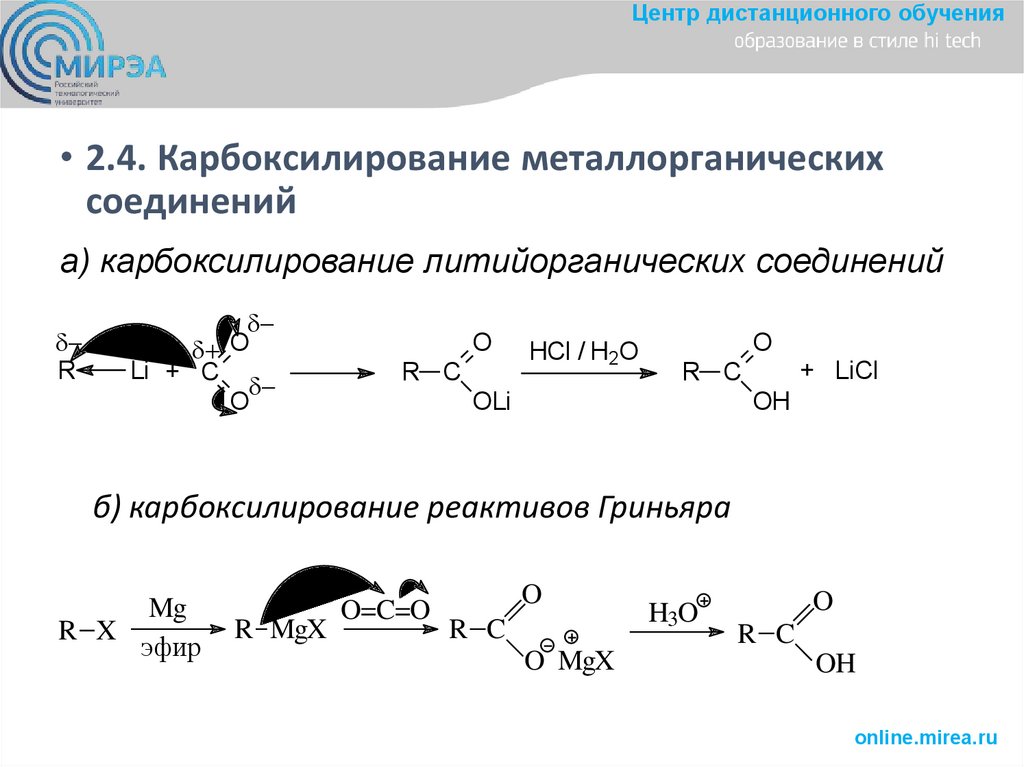
Центр дистанционного обучения• 2.4. Карбоксилирование металлорганических
соединений
а) карбоксилирование литийорганических соединений
R
O
Li + C
O
O
R C
HCl / H2O
O
+ LiCl
R C
OLi
OH
б) карбоксилирование реактивов Гриньяра
Mg
R X
эфир
R MgX
O=C=O
O
R C
O MgX
H3O
O
R C
OH
online.mirea.ru
20.
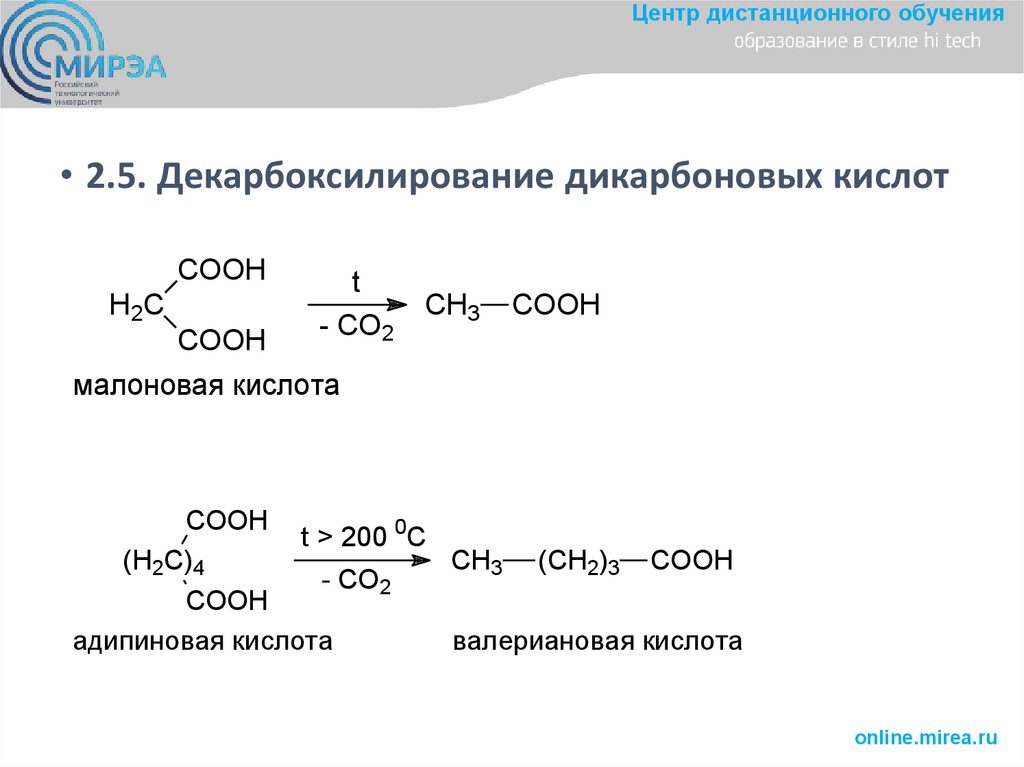
Центр дистанционного обучения• 2.5. Декарбоксилирование дикарбоновых кислот
COOH
H2C
COOH
t
- CO2
CH3
COOH
малоновая кислота
COOH
t > 200 0C
(H2C)4
CH3 (CH2)3 COOH
- CO2
COOH
адипиновая кислота
валериановая кислота
online.mirea.ru
21.
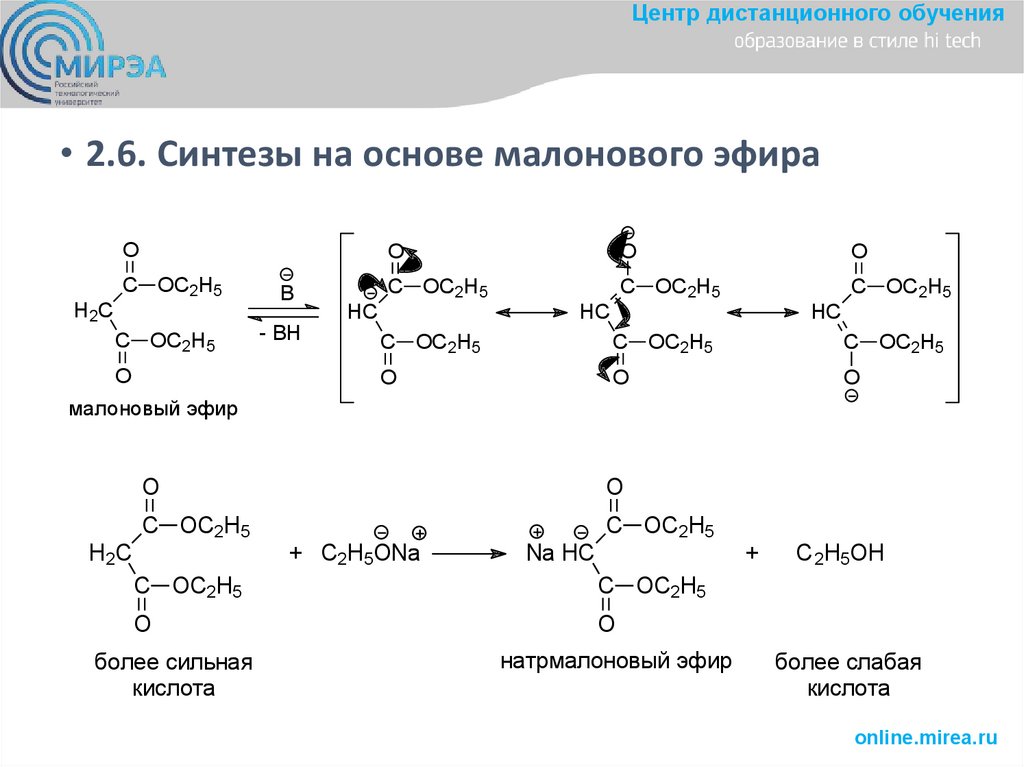
Центр дистанционного обучения• 2.6. Синтезы на основе малонового эфира
O
H2C
C OC2H5
C OC2H5
O
B
- BH
HC
O
O
O
C OC2H5
C OC2H5
C OC2H5
HC
HC
C OC2H5
C OC2H5
C OC2H5
O
O
O
малоновый эфир
H2C
O
O
C OC2H5
C OC2H5
+ C2H5ONa
Na HC
C OC2H5
C OC2H5
O
O
более сильная
кислота
натрмалоновый эфир
+
C 2H5OH
более слабая
кислота
online.mirea.ru
22.
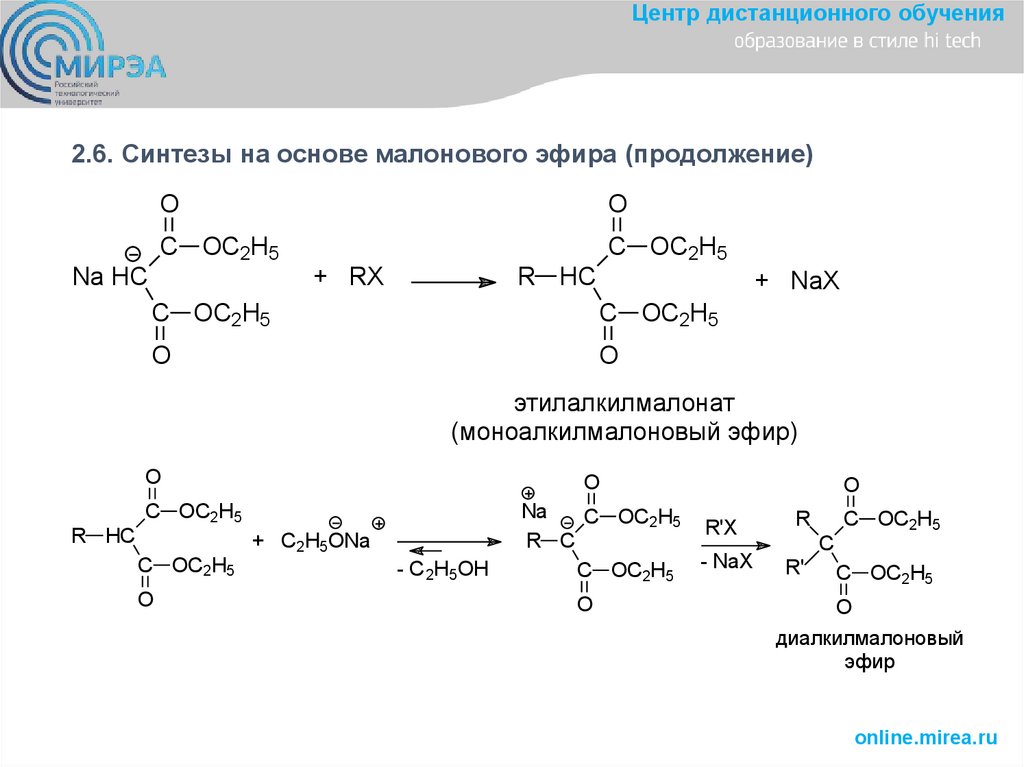
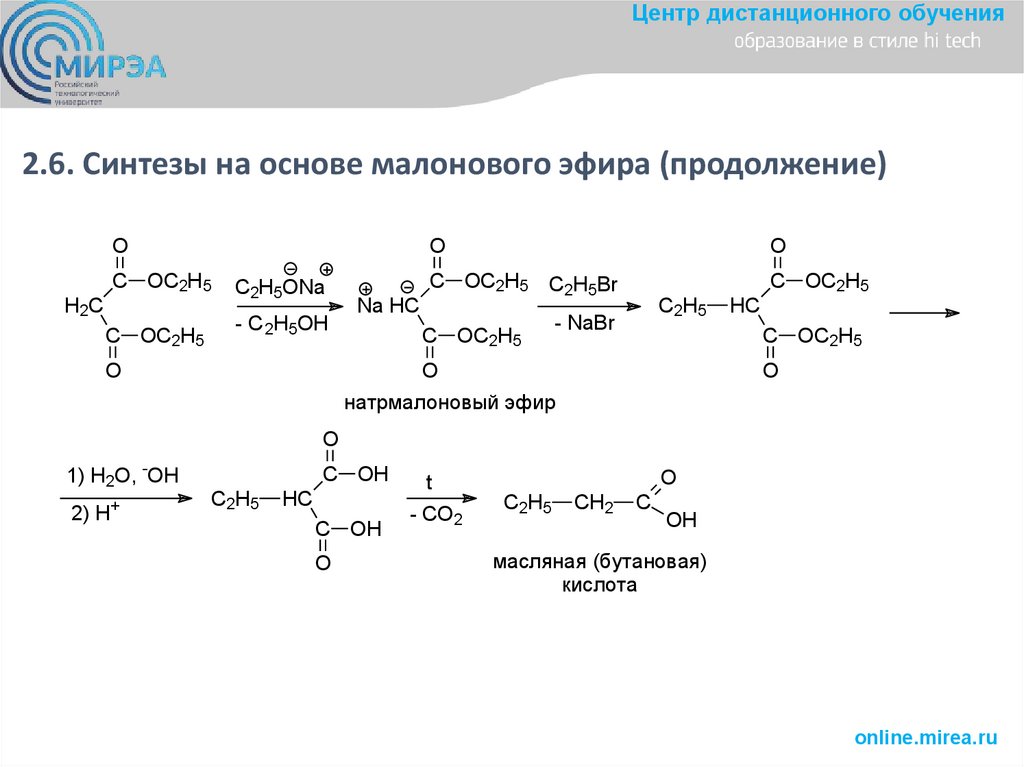
Центр дистанционного обучения2.6. Синтезы на основе малонового эфира (продолжение)
Na HC
O
O
C OC2H5
C OC2H5
+ RX
R HC
+ NaX
C OC2H5
C OC2H5
O
O
этилалкилмалонат
(моноалкилмалоновый эфир)
O
R HC
O
C OC2H5
C OC2H5
O
+ C2H5ONa
- C 2H5OH
Na
C OC2H5
R'X
R C
C OC2H5 - NaX
O
O
R
C
R'
C OC2H5
C OC2H5
O
диалкилмалоновый
эфир
online.mirea.ru
23.
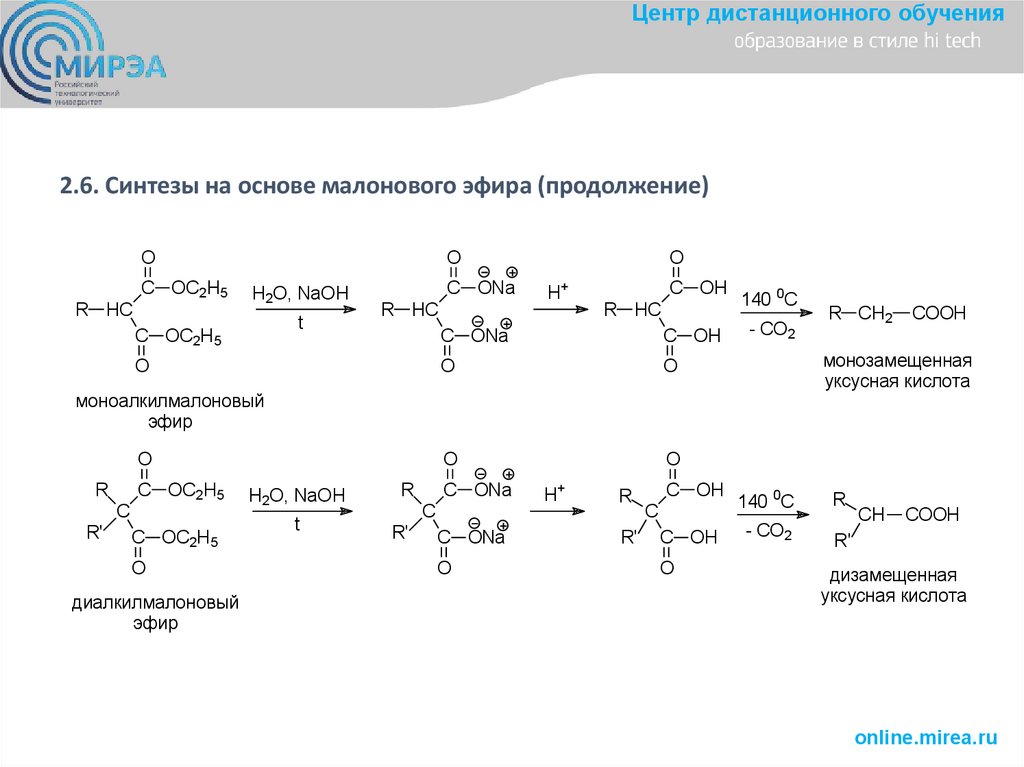
Центр дистанционного обучения2.6. Синтезы на основе малонового эфира (продолжение)
O
R HC
C OC2H5
O
H2O, NaOH
t
C OC2H5
C ONa
R HC
O
O
H+
C OH
R HC
C ONa
C OH
O
O
O
O
140 0C
- CO2
R
C
R'
C OC2H5
C OC2H5
O
диалкилмалоновый
эфир
H2O, NaOH
t
R
C ONa
C
R'
C ONa
O
H+
R
R'
C OH
C
C OH
O
COOH
монозамещенная
уксусная кислота
моноалкилмалоновый
эфир
O
R CH2
140 0C
R
- CO2
R'
CH
COOH
дизамещенная
уксусная кислота
online.mirea.ru
24.
Центр дистанционного обучения2.6. Синтезы на основе малонового эфира (продолжение)
O
H 2C
O
C OC2H5
C OC2H5
C2H5ONa
- C 2H5OH
Na HC
O
C OC2H5
C2H5Br
C OC2H5
O
C 2H 5
- NaBr
HC
C OC2H5
C OC2H5
O
O
натрмалоновый эфир
O
1) H2O, -OH
2) H+
C OH
C 2H 5
HC
C OH
O
t
- CO2
O
C2H5
CH2
C
OH
масляная (бутановая)
кислота
online.mirea.ru
25. Строение и химические свойства
Центр дистанционного обученияСтроение и химические свойства
Уменьшается электрофильность
карбонильного атома углерода из-за
наличия р π-сопряжения (-I и –Mэффекты С=О группы);
Скорость реакций с нуклеофильными
реагентами ниже, чем для альдегидов и
кетонов; реакции AdN не протекают.
Резко возрастает подвижность протона
в OH-группе, что отражается в усилении
кислотных свойств
Карбоксильная группа является
акцептором электронов (-I-эффект) по
отношению к α-углеродному атому и
атомам водорода, связанным с ним.
online.mirea.ru
26.
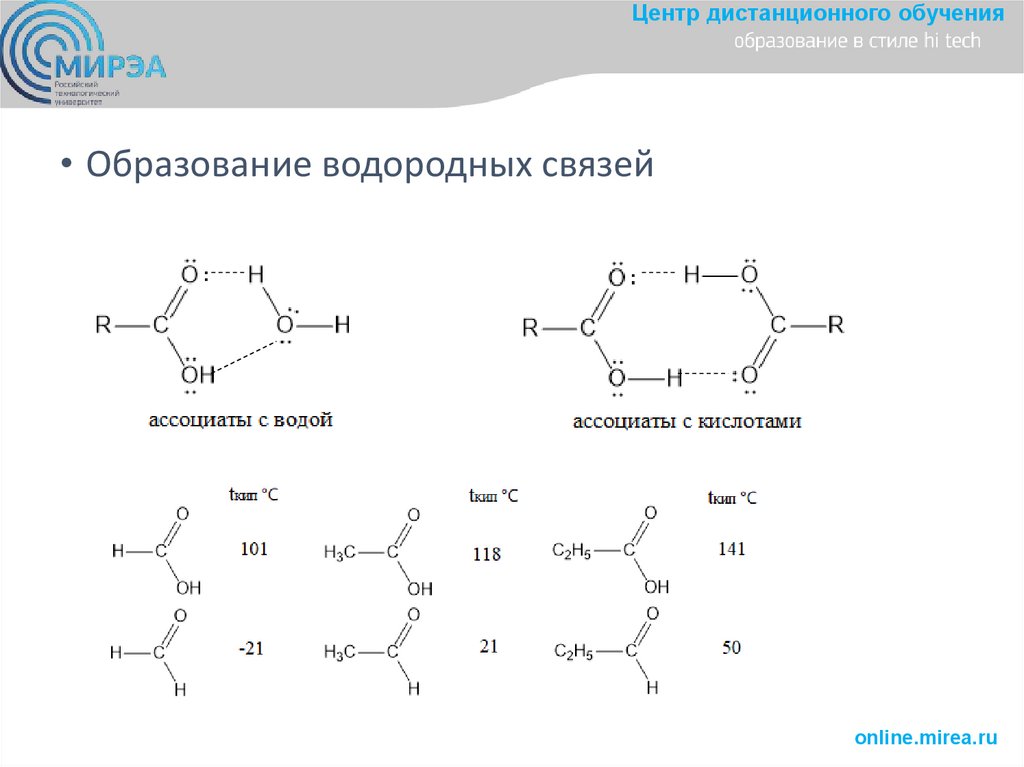
Центр дистанционного обучения• Образование водородных связей
online.mirea.ru
27.
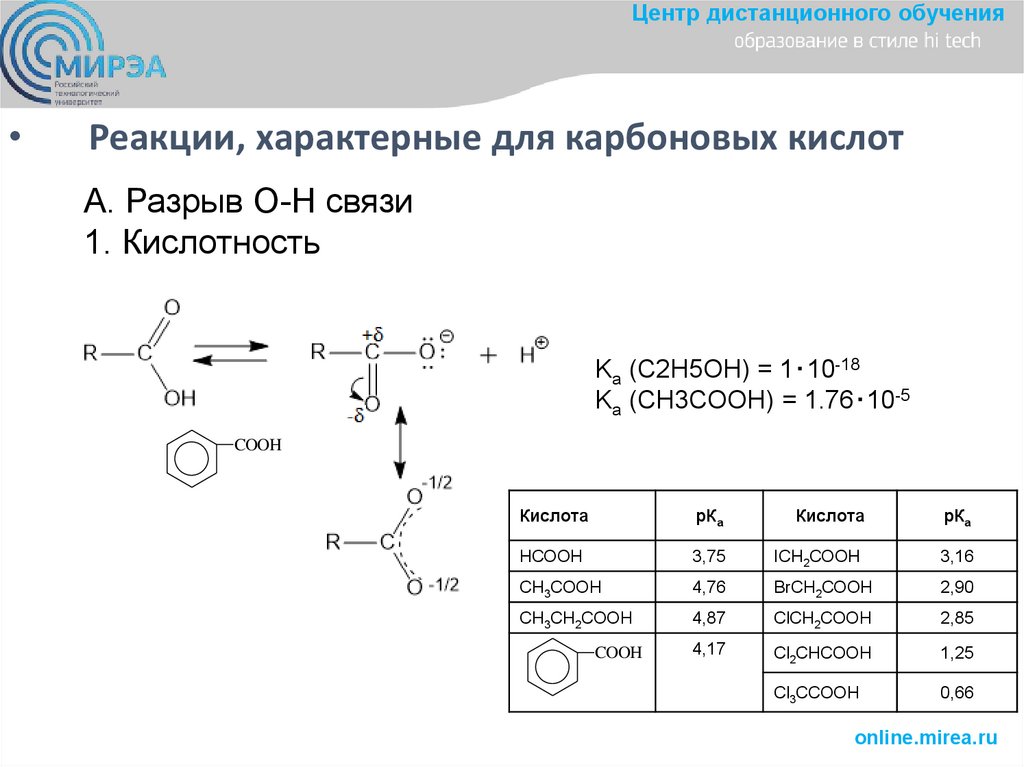
Центр дистанционного обученияРеакции, характерные для карбоновых кислот
А. Разрыв O-H связи
1. Кислотность
Ka (C2H5OH) = 1‧10-18
Ka (CH3COOH) = 1.76‧10-5
COOH
Кислота
рКа
Кислота
рКа
НСООН
3,75
IСН2СООН
3,16
СН3СООН
4,76
BrСН2СООН
2,90
СН3СН2СООН
4,87
ClСН2СООН
2,85
4,17
Cl2СНСООН
1,25
Cl3ССООН
0,66
COOH
online.mirea.ru
28.
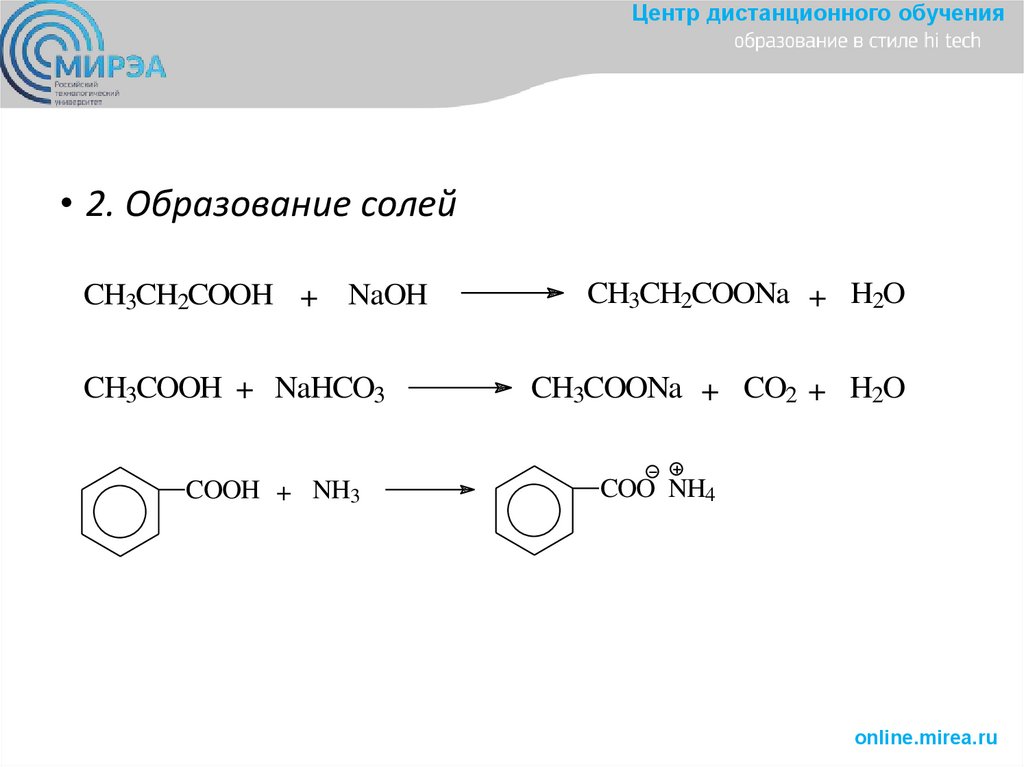
Центр дистанционного обучения• 2. Образование солей
CH3CH2COOH + NaOH
CH3COOH + NaHCO3
COOH + NH3
CH3CH2COONa + H2O
CH3COONa + CO2 + H2O
COO NH4
online.mirea.ru
29.
Центр дистанционного обучения• 2. Образование солей (продолжение)
2 CH3COOH
Ca
_H
2
(CH3COO)2Ca
online.mirea.ru
30.
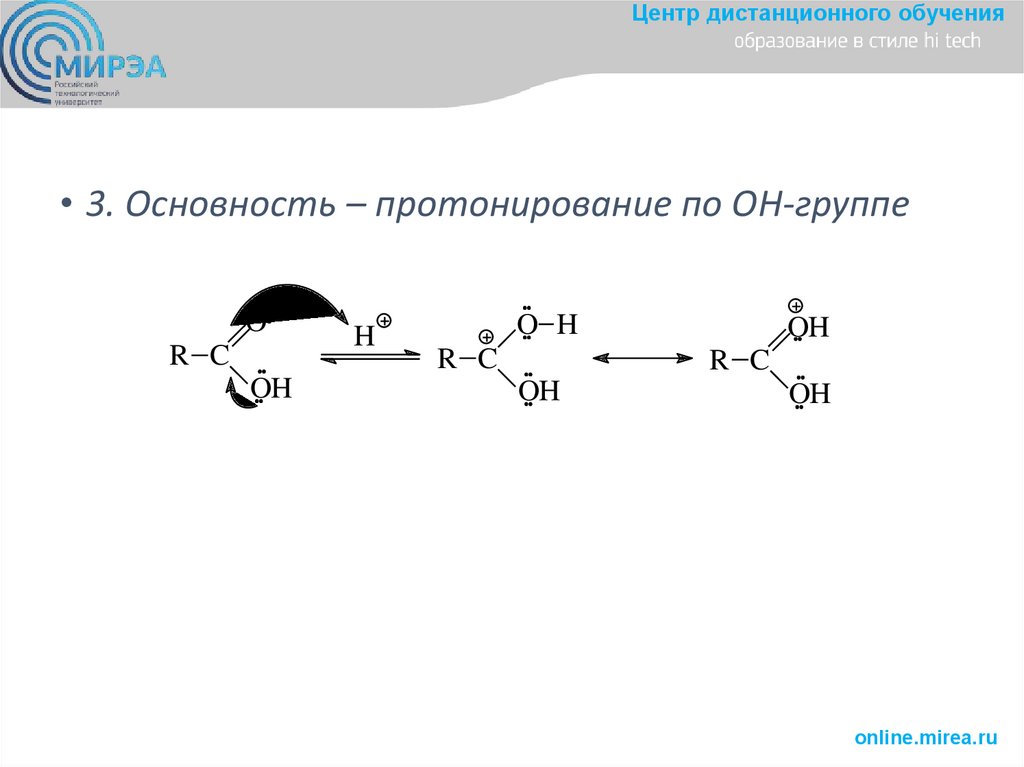
Центр дистанционного обучения• 3. Основность – протонирование по ОН-группе
O
R C
OH
H
O H
R C
OH
R C
OH
OH
online.mirea.ru
31.
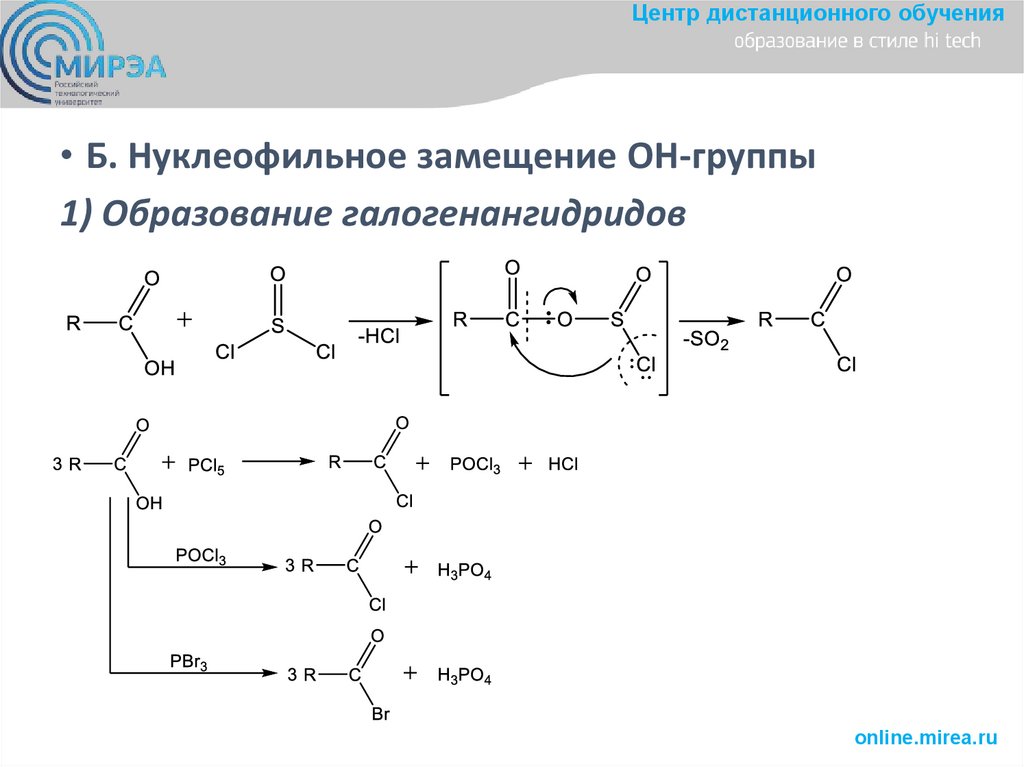
Центр дистанционного обучения• Б. Нуклеофильное замещение OH-группы
1) Образование галогенангидридов
online.mirea.ru
32.
Центр дистанционного обучения2) Образование ангидридов
online.mirea.ru
33.
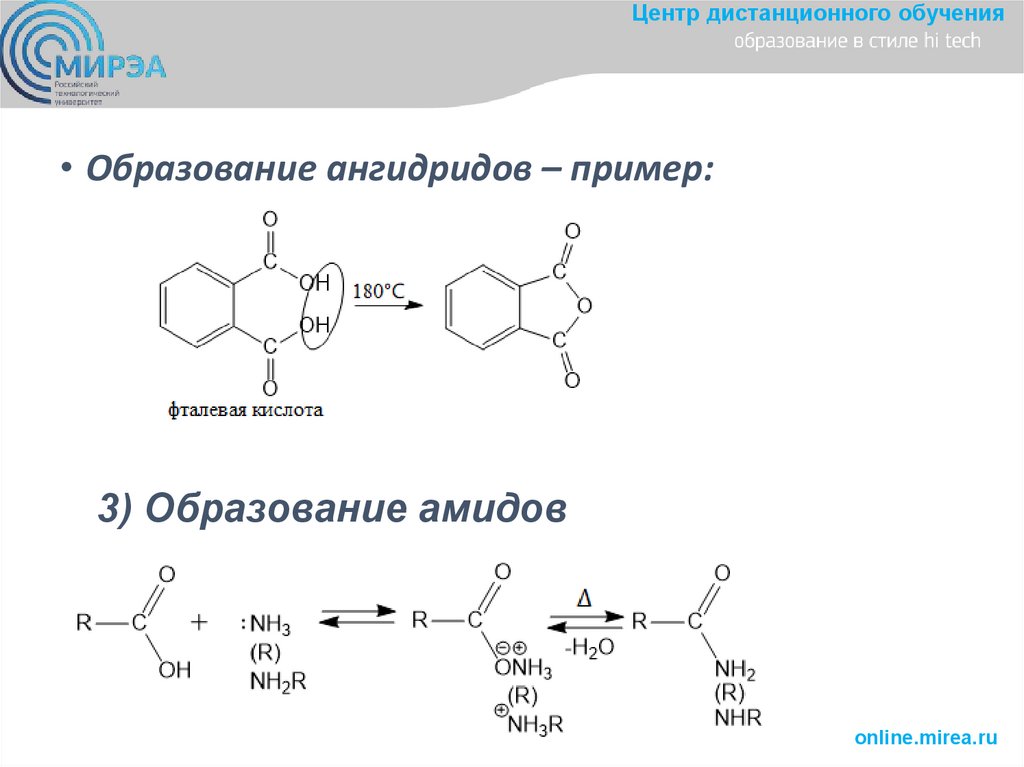
Центр дистанционного обучения• Образование ангидридов – пример:
3) Образование амидов
online.mirea.ru
34.
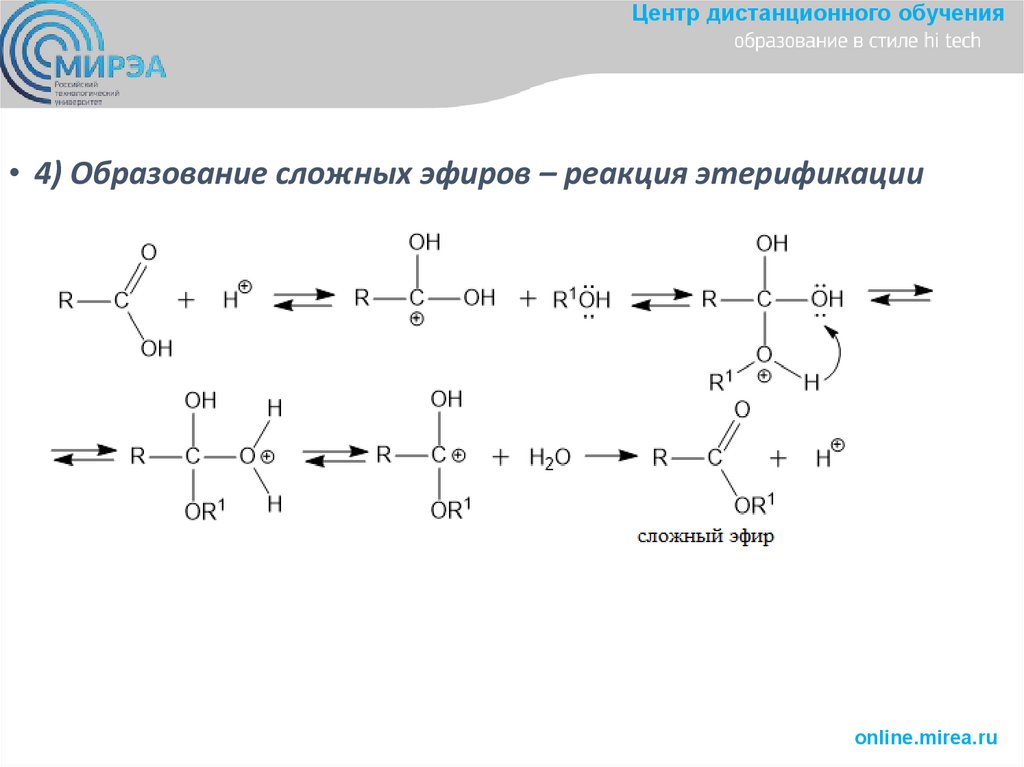
Центр дистанционного обучения• 4) Образование сложных эфиров – реакция этерификации
online.mirea.ru
35.
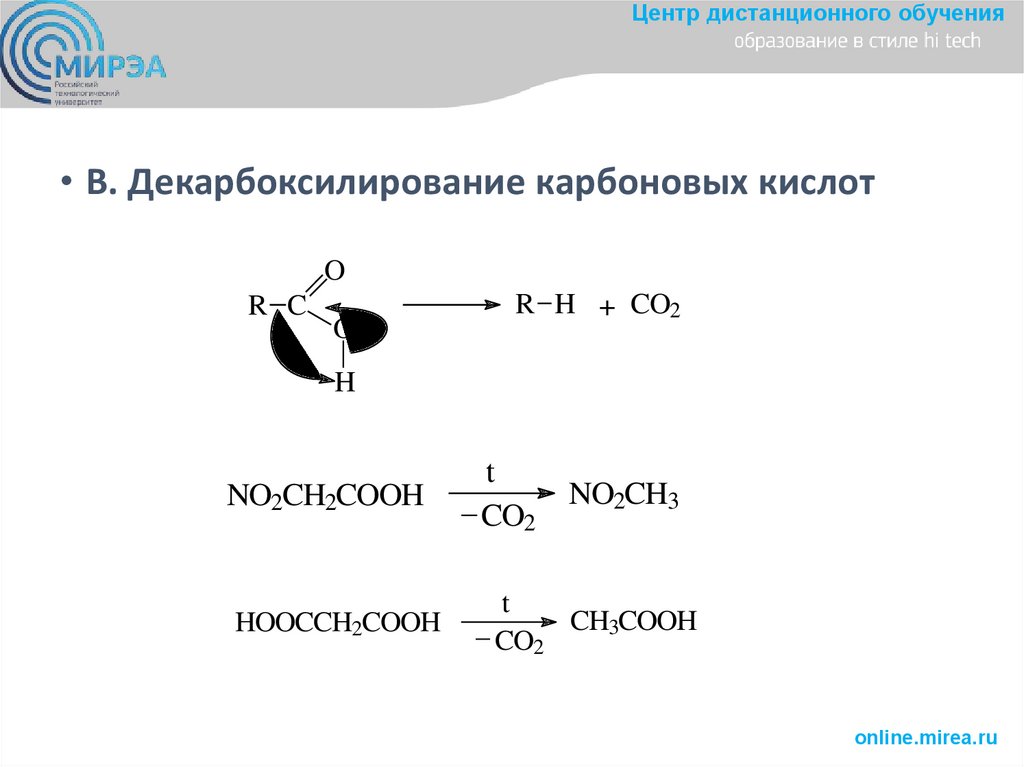
Центр дистанционного обучения• В. Декарбоксилирование карбоновых кислот
O
R C
O
R H + CO2
H
NO2CH2COOH
HOOCCH2COOH
t
_ CO
2
NO2CH3
t
_ CO CH3COOH
2
online.mirea.ru
36. В. Декарбоксилирование карбоновых кислот
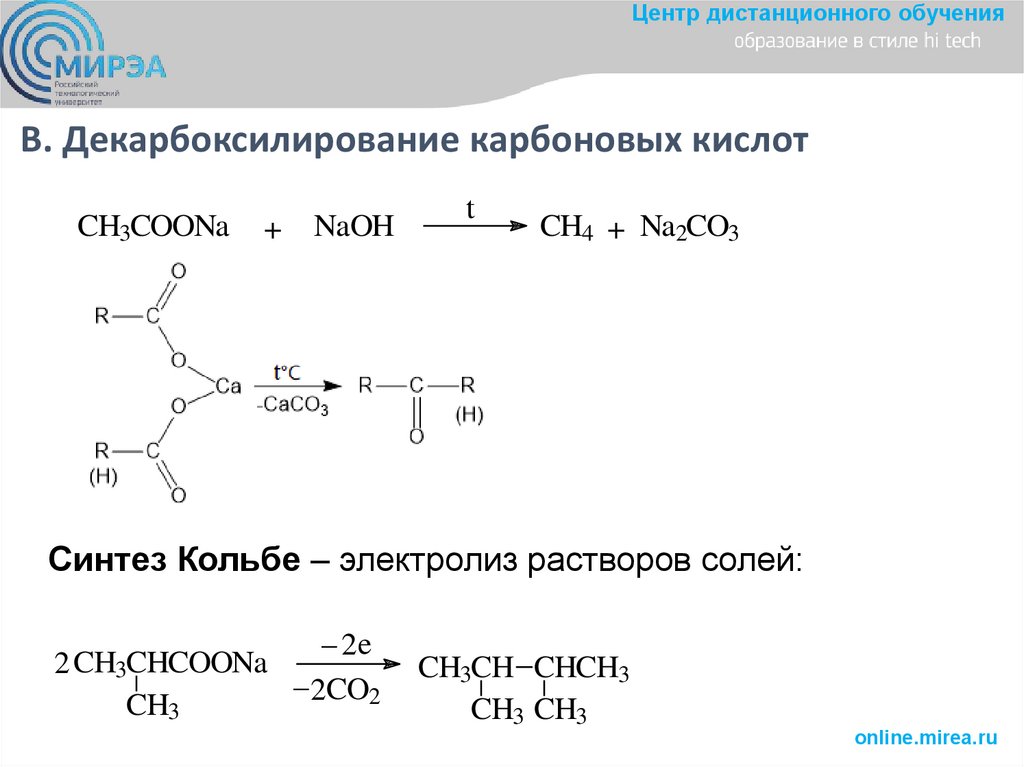
Центр дистанционного обученияВ. Декарбоксилирование карбоновых кислот
CH3COONa
+
NaOH
t
CH4 + Na2CO3
Синтез Кольбе – электролиз растворов солей:
_ 2e
2 CH3CHCOONa _
2CO2
CH3
CH3CH CHCH3
CH3 CH3
online.mirea.ru
37.
Центр дистанционного обучения• Г. Реакции окисления и восстановления
• 1. Реакции восстановления
online.mirea.ru
38.
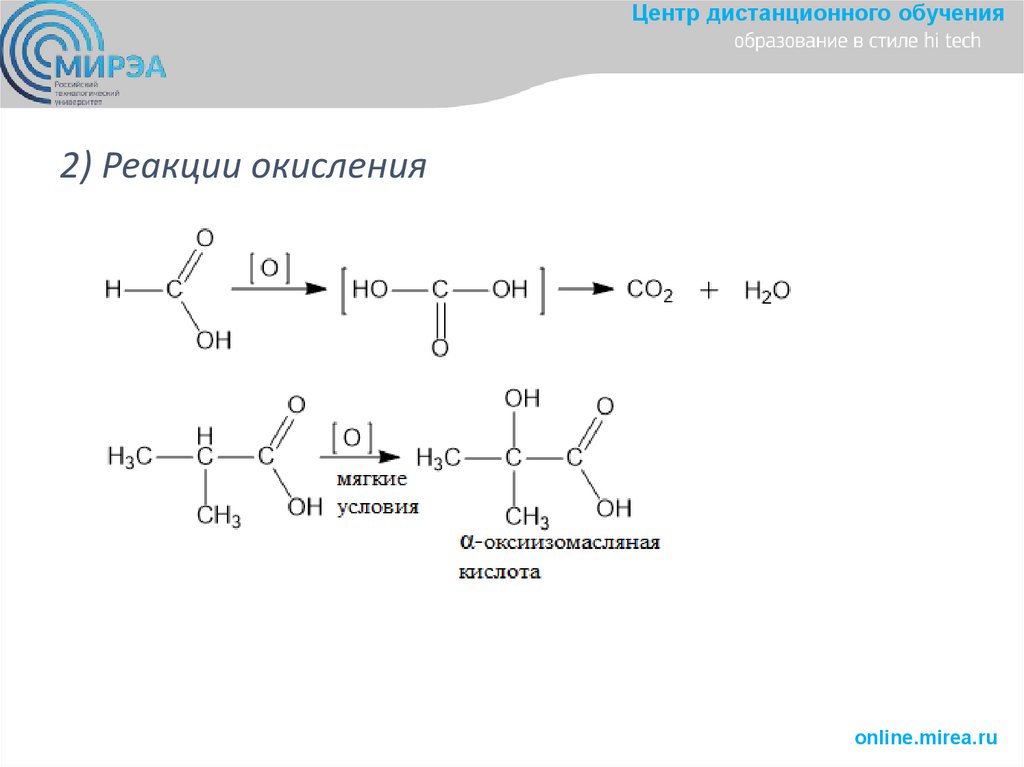
Центр дистанционного обучения2) Реакции окисления
online.mirea.ru
39.
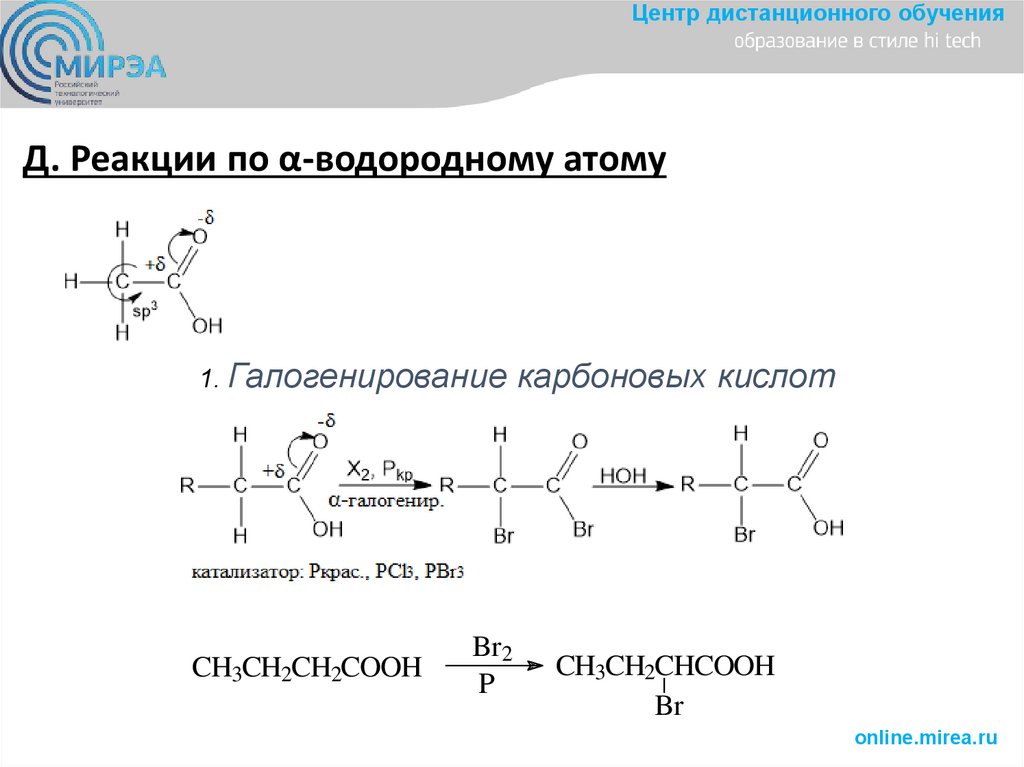
Центр дистанционного обученияД. Реакции по α-водородному атому
1. Галогенирование
CH3CH2CH2COOH
Br2
P
карбоновых кислот
CH3CH2CHCOOH
Br
online.mirea.ru
40.
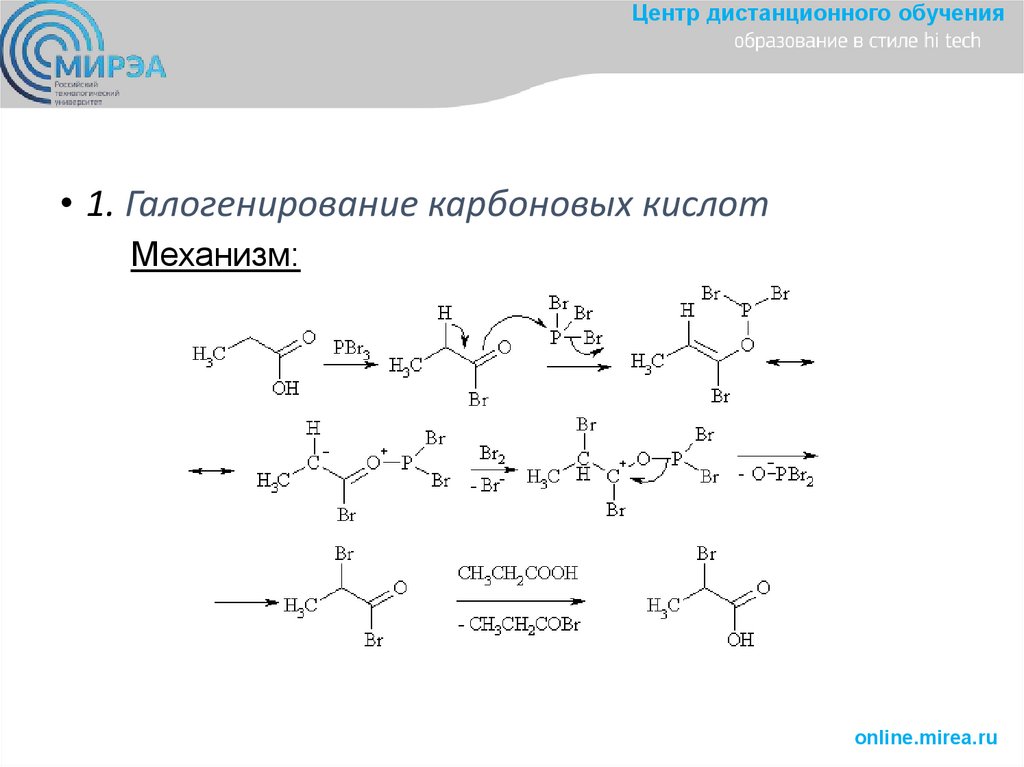
Центр дистанционного обучения• 1. Галогенирование карбоновых кислот
Механизм:
online.mirea.ru
41.
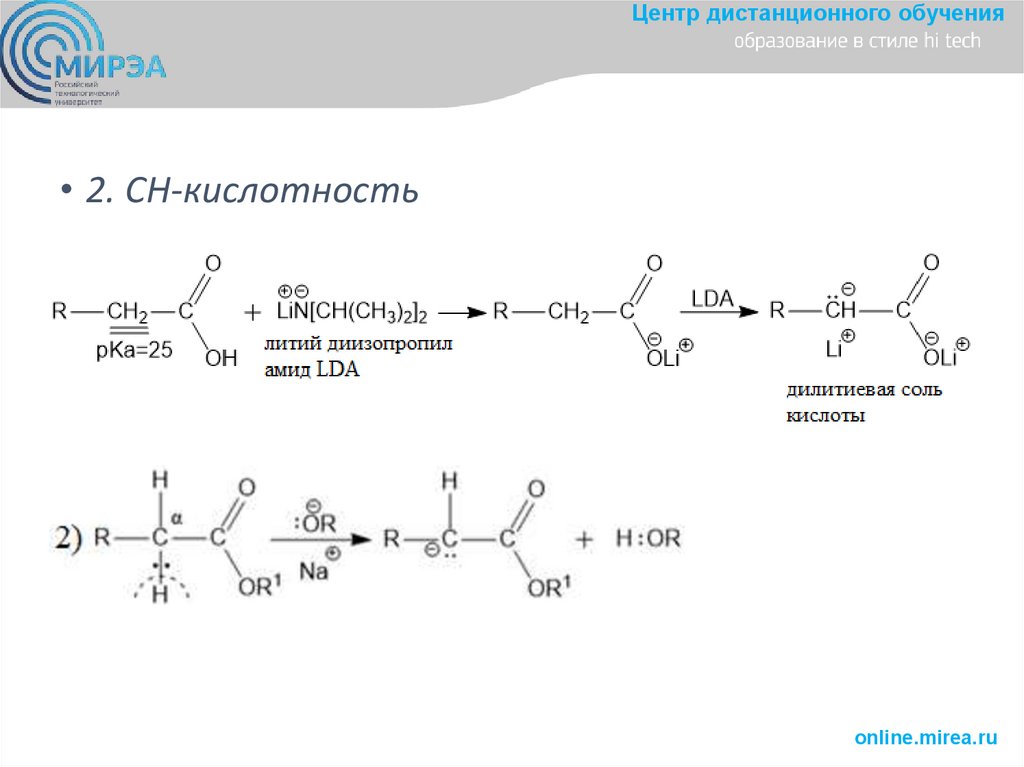
Центр дистанционного обучения• 2. СН-кислотность
online.mirea.ru
42. Список литературы
Центр дистанционного обученияСписок литературы
• Электронный конспект лекции на сайте учебного портала
МИРЭА https://online-edu.mirea.ru/course/view.php?id=1628
• Реутов, О. А. Органическая химия : учебник : в 4 частях / О.
А. Реутов, А. Л. Курц, К. П. Бутин. — 6-е изд. — Москва :
Лаборатория знаний, [б. г.]. — Часть 3 — 2017. — 547 с. —
ISBN 978-5-00101-508-6. — Текст : электронный // Лань :
электронно-библиотечная система. — URL:
https://e.lanbook.com/book/94166 (дата обращения:
07.04.2020). — Режим доступа: для авториз. пользователей.
online.mirea.ru
43. Спасибо за внимание!
Центр дистанционного обученияСпасибо за внимание!
online.mirea.ru










 Химия
Химия