Похожие презентации:
Миома матки. Диагностика и лечение
1. Миома матки. Диагностика и лечение.
2. Определение
Миома матки (ММ) — моноклональныйгормоночувствительный пролиферат,
состоящий из фенотипически изменённых
гладкомышечных клеток миометрия.
3. Происхождение
Растет из одной первичной клетки,которая в результате произошедшей
в ней мутации приобрела
способность нерегулируемого роста.
Множественные узлы клонально не
связаны, что и объясняет различный
темп роста.
4. Эпидемиология
Распространенность ММ составляет30% среди женщин репродуктивного
возраста, по данным аутопсических
исследований – значительно больше,
достигая 80%.
5. Классификация
По локализации:Подбрюшинная
Межмышечная
Подслизистая
6. Классификация
По гистологическим особенностям:Простая
Пролиферирующая
7. Простая ММ
Встречается в 75% случаевСтрома преобладает над паренхимой
Растет медленно
Митотическая активность миоцитов
практически отсутствует
8. Пролиферирующая ММ
Встречается в 25% случаевПреобладают миогенные элементы
Множественная
Растет быстро
Митотическая активность повышена
9. Диагностика
В 50-60% случаев протекаетбессимптомно
Основные симптомы: менометроррагии,
бесплодие, прерывание беременности,
сдавление смежных органов, хр.тазовые
боли, острый болевой синдром при
перекруте ножки, железодефицитная
анемия
10. Диагностика
Анамнез:Отсутствие родов и лактации к 30 годам
Аборты
Неадекватная контрацепция
ВЗОМТ
Ультрафиолетовое облучение
Стрессы
11. Диагностика
Физикальное исследование:бимануальное исследование с
определением размеров матки, при
обнаружение миоматозных узлов – из
количество, размеры, локализация.
12. Лабораторные исследования
ОАК – гипохромная анемияБ/Х анализ крови: уменьшение
концентрации сывороточного железа,
увеличение железосвязывающей
способности сыворотки
Обнаружение в периферической крови мРНК раковотестикулярных генов (обнаруживаются в 86% миом, в
49% случаев выявляются в периферической крови) –
экспериментальный метод
13. Инструментальные методы
14. УЗИ
Используются трансабдоминальные итрансвагинальные датчики
Рутинный метод, применяется для
первичной диагностики, для
динамического наблюдения.
15. УЗИ
Расширитьдиагностические
возможности метода
позволяет
гидросонография –
контрастирование полости
матки жидкими средами
(обычно физ.раствор).
16. УЗИ
С помощью этих методов можноопределить точную локализацию
миомы, а также сопутствующие
патологии эндометрия.
Чувствительность методов достигает
100%!
17. УЗИ Гидросонография
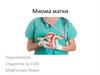
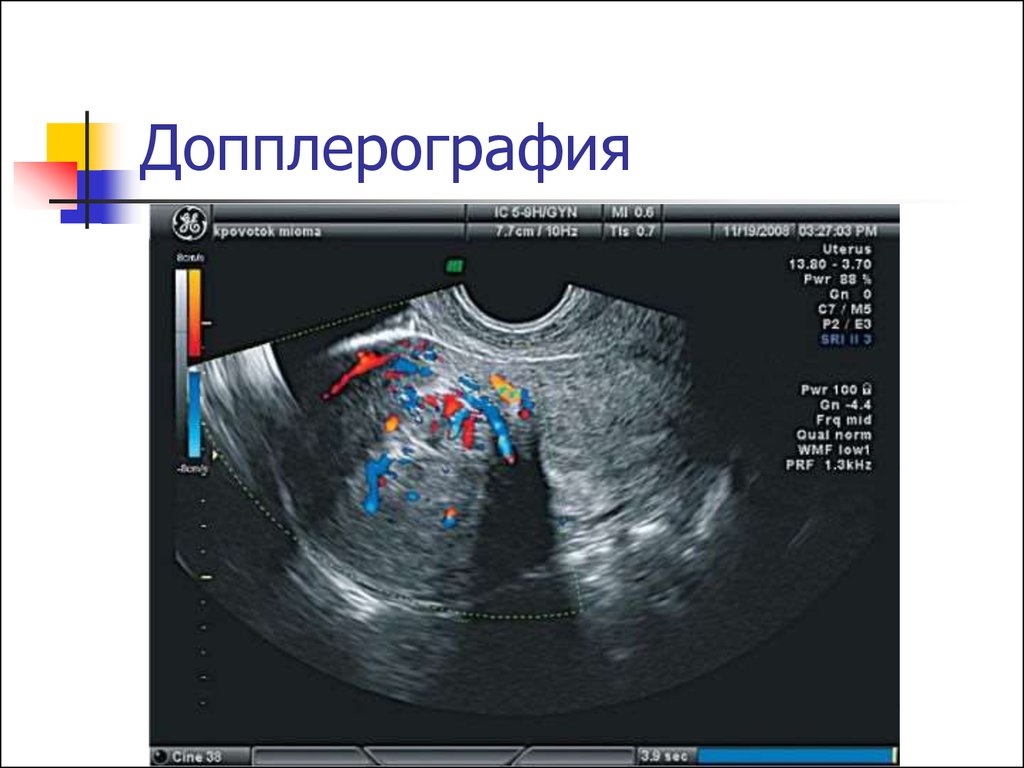
18. Допплерография и ангиография
Позволяют определить особенностикровообращения в миоматозных
узлах перед проведением ЭМА, для
определения типа ММ.
Оценить эффективность ЭМА
Провести диф. диагностику с
саркомой
19. Допплерография
20. Ангиография
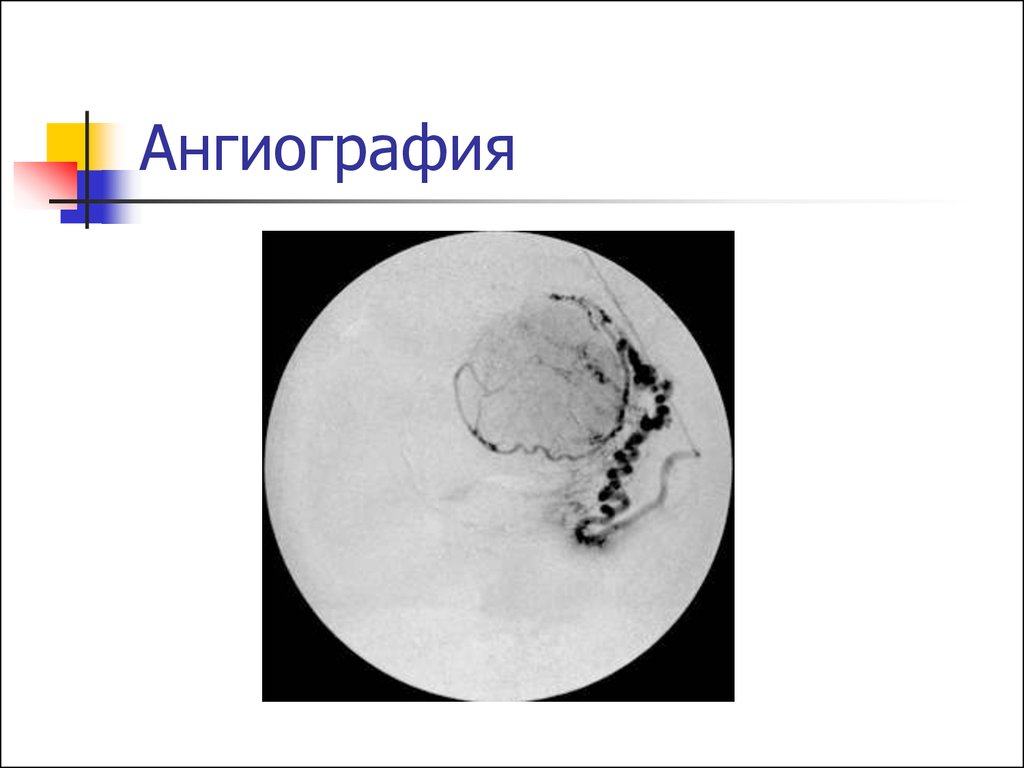
21. Гистероскопия
Золотой стандарт диагностикисубмукозных узлов.
Оценивается тип узла, расположение,
размеры и возможность проведения
трансцервикальной миомэктомии.
22. Гистероскопия
23. ММ при гистероскопии
24. МРТ
Используется для исследованиятопографии миоматозных узлов при
гигантских ММ
Контроль за эффективностью ЭМА
Для проведения ФУЗ-абляции
25. МРТ ММ
26. Диагностическая лапароскопия
В чистом виде, а не как этапоперации, в настоящее время
применяется редко, т.к. метод
травматичный
Проводится с целью
дифференциальной диагностики с
другими опухолями брюшной полости
27. Диагностическая лапароскопия
28. Лечение миомы матки
29.
Миому матки надо начинать лечить смомента ее выявления, избегая
пассивного наблюдения, при этом
лечить надо независимо от ее
размера и максимально щадящим
методом.
30.
Рекомендуется большим вниманиемотноситься к маленьким миоматозным
узлам и в целом рассматривать их
обнаружение как диагностическую
удачу, а не как ничего не значащую
находку.
31. Медикаментозное лечение
Основывается на воспроизведениимедикаментозной псевдоменопаузы
или гипоэстрогении. Целесообразно
для узлов размерами до 3 см, т.к. в
узлах бОльших размеров
гормональные рецепторы часто
отсутствуют.
32. Медикаментозное лечение
Применяются следующие группыпрепаратов:
Антигонадотропины
Агонисты гонадотропин-рилизинг гормона
Антипрогестины
33. Гонадотропины
Даназол, гестринонОбладают антиэстрогенным и
антипрогестероновым эффектом, вызывая
временную аменорею.
Препараты назначают 1 раз в день в
течение 3-5 месяцев.
В ряде случаев аменорея не наступает, а
имеется гипоменструальный синдром
Размер матки уменьшается на 50-60%.
Побочные эффекты наблюдаются редко.
34. Агонисты гонадотропин-рилизинг гормона (аГнРГ)
Агонисты гонадотропинрилизинг гормона (аГнРГ)Бусерелин, трипторелин, лейпрорелин
Блокируют секрецию гонадотропинов и,
следовательно, половых гормонов.
Блокада обратима, после отмены синтез
гонадотропных гормонов восстанавливается
Высказано мнение о прямом влиянии аГнРГ на
ММ – в ней обнаружены рецепторы к ГнРГ
Побочные эффекты связаны с гипоэстрогенией,
поэтому возможно сочетание с небольшими
дозами эстрогенов.
35. Схемы назначения аГнРГ
На 2-3 месяца перед операциеймиомэктомии с целью уменьшения
размеров узлов, сокращения времени
операции и объема кровопотери,
облегчения энуклеации.
Однако это увеличивает число рецидивов,
т.к. маленькие узлы становятся еще
меньше и во время операции обнаружить
их не удается.
36. Схемы назначения аГнРГ
После операции на 3-4 месяца. Приотсутствии предоперационной
терапии – на 6 месяцев.
37. Схемы назначения аГнРГ
В случае отсутствия операции ММбыстро возвращается к
первоначальным размерам в течении
первых 3-4 менструальных циклов.
В таких случаях целесообразно
использовать двухэтапную терапию
38. Двухэтапная терапия
1 этап (регрессивный) – используют аГнРГ сцелью уменьшения объема ММ
2 этап (стабилизирующий) – применяются
низкодозированные КОК с гестагенным
компонентом третьего поколения (логест,
регулон, марвелон). Возможно применение
гормональной рилизинг-системы мирена,
особенно при отсутствии у рожавшей женщины
ближайших репродуктивных планов
39. Антипрогестины
МифепристонСвязывается с прогестероновыми
рецепторами, блокируя их функцию
Главное достоинство препарата –
отсутствие гипоэстрогении
После приема в течение 12 недель
размеры ММ уменьшаются на 50-60%
40. Хирургическое лечение
41. Радикальное (ампутация матки)
Включает гистерэктомиюлапароскопическим и
лапаротомическим доступами.
Лечение по принципу «нет органа –
нет проблем»
Нужно помнить, что в организме
лишних органов нет!
42. Показания:
Большие размеры узла (матка соответствует 14 неделямбеременности)
Растущая миома в постменопаузальном возрасте
(«Нерегрессирующая ММ в постменопаузальном
периоде является маркером онкопатологии органов
репродуктивной системы» Я.В.Бохман, известный
онколог)
Неэффективность других методов
Острое нарушение питания миомы
43. Показания
Нарушение функции соседнихорганов
Шеечная локализация
Маточные кровотечения,
сопровождающиеся хронической
анемией
44. Лапароскопическая гистерэктомия
Ограничениями являются размерматки, превышающий 16-18 недель
беременности, наличие низко
расположенных узлов, особенно по
задней стенке.
Примерно у 40% пациенток,
перенесших гистерэктомию,
развивается постгистерэктомический
синдром
45. Постгистерэктомический синдром
Обусловлен недостаточностьюэстрогенов из-за снижения
овариального кровотока и нарушения
рецепторных взаимодействий в
системе яичники-миометрийэндометрий.
Для его коррекции необходима
гормонзаместительная терапия(ГЗТ)
46. Лапароскопическая гистерэктомия
47. Консервативное лечение
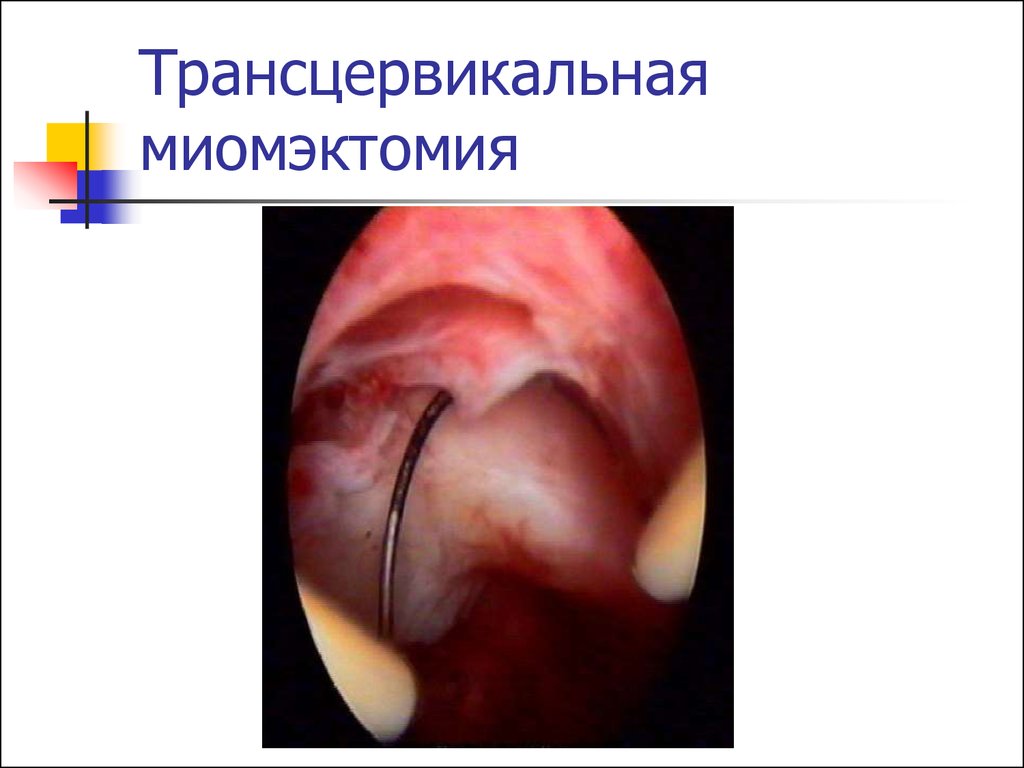
48. Трансцервикальная миомэктомия
Оптимальный метод приподслизистой локализации ММ.
Операция выполняется под
контролем гистероскопа, полость
матки заколняется 5% раствором
глюкозы.
Возможности метода зависят от
величины узла, его формы и типа.
49. Трансцервикальная миомэктомия
Если узел полностью располагается в полостиматки, его диаметр до 10 см – возможно удаление
механическим способом (эндоскопические
ножницы, абортцанг)
Электрохирургическая миомэктомия безопасна
при субмукозных узлах до 5 см в диаметре.
Возможна предоперационная подготовка аГнРГ
для уменьшения узла и формирования капсулы,
что облегчает вылущивание узла.
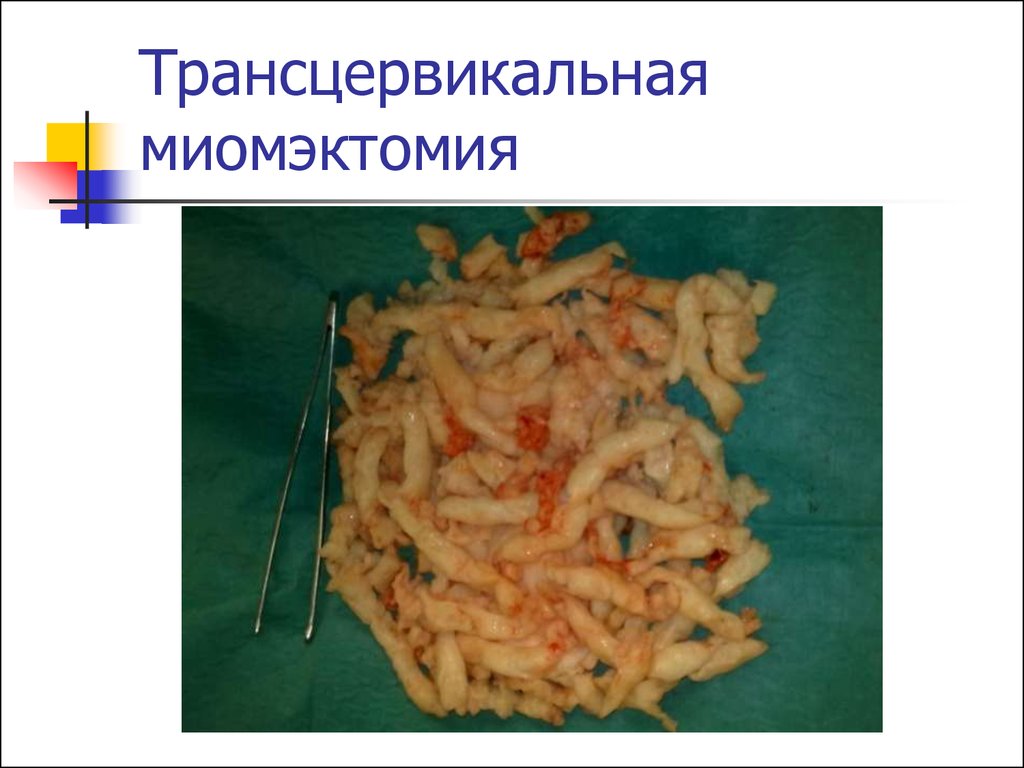
50. Трансцервикальная миомэктомия
51. Трансцервикальная миомэктомия
52. Миомэктомия лапароскопическим доступом
Основным критерием эффективностимиомэктомии следует считать
формирование полноценного рубца,
который будет состоятельным при
последующих беременностях
Для уменьшения ложаузла и снижения
кровопотери показано проведение
предоперационной подготовки аГнРГ.
Утолщение и уплотнение капсулы
облегчает энуклеацию.
Ложе узла должно быть тщательно ушито.
53. Лапароскопическая миомэктомия
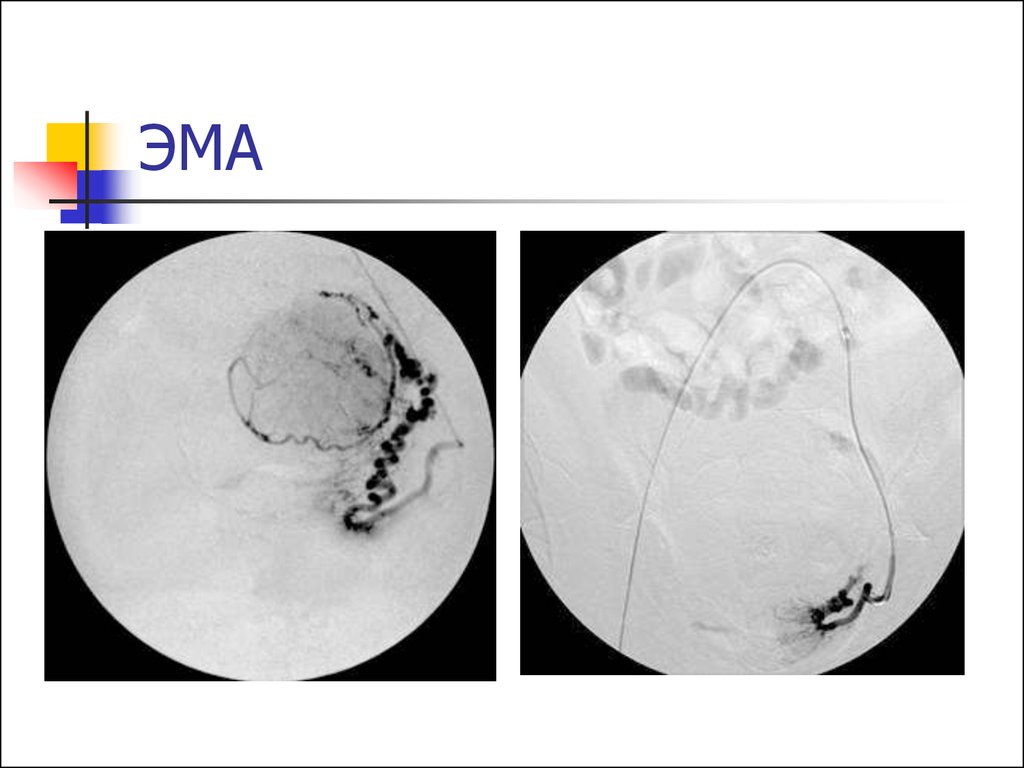
54. Эмболизация маточных артерий
Через пункцию правой бедренной артериивводят тонкий катетер, который под
контролем рентгенотелевидения
проводится непосредственно в маточные
артерии
Затем в ветви маточных артерий вводят
эмболизационный препарат,
препятствующий кровоснабжению ММ.
Продолжительность процедуры 10-20
минут.
55. ЭМА
Клиническая эффективность заключается вуменьшении размеров матки и нормализации
менструальной функции.
Объем ММ к году наблюдения сокращается в 3
раза.
Возможна самопроизвольная экспульсия
(выпадение) в виде некротического детрита.
В случае больших размеров узлов и
невозможности из самостоятельной экспульсии,
целесообразно проведение трансцервикальной
миомэктомии.
56. ЭМА
Возможно миграция миоматозных узловмежмышечно, что считается
благоприятным, т.к. восстанавливается
полость матки и снижается кровопотеря в
менструацию.
Уменьшение размеров субсерозных узлов
позволяет сформировать полноценный
рубец после миомэктомии.
Как и после гистерэктомии, возможно
развитие гипоэстрогении, связанное с
нарушением кровоснабжения в яичниках.
57. ЭМА
58. ЭМА
59. Фокусированная ультразвуковая абляция под контролем МРТ
Сравнительно новый метод леченияММ, применяется в России с 2006
года.
Сущность метода заключается в
воздействии на ткань ММ
высокочастотного УЗ, под действием
которого происходит нагрев и
развивается коагуляционный некроз.
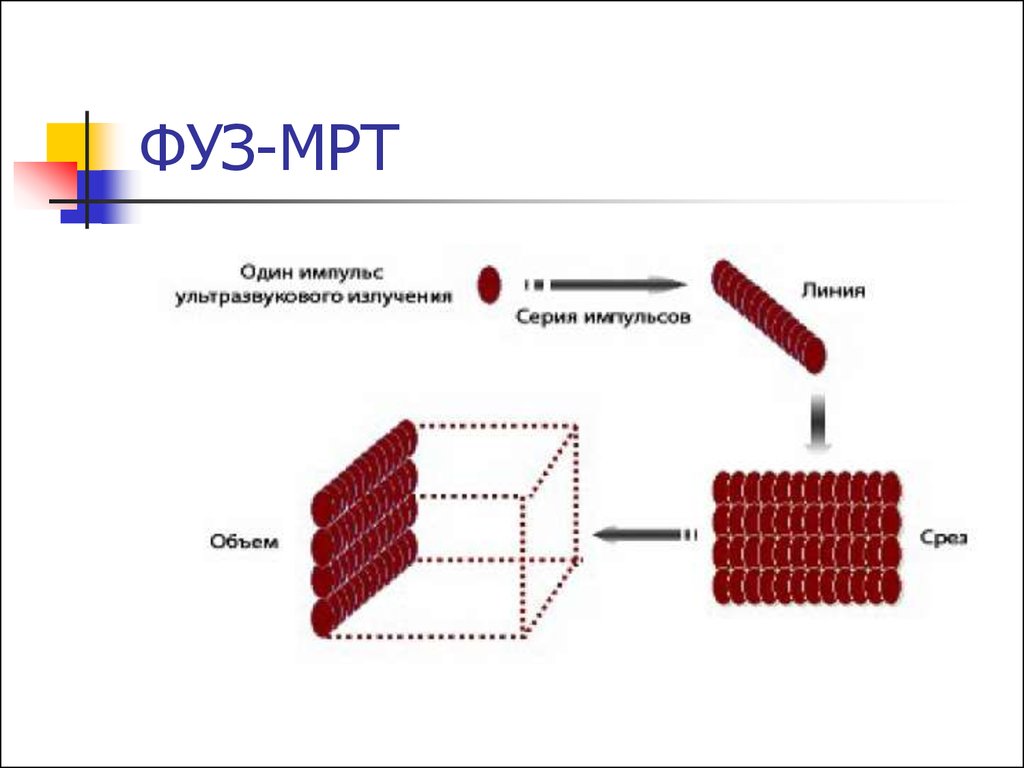
60. ФУЗ-МРТ
Пациентка располагается в положениилежа на животе внутри магнитнорезонансного томографа.
61. ФУЗ-МРТ
Проводится базовое сканирование,врач намечает план операции.
Затем выполняется сама процедура, в
ходе которой УЗ поочередно
воздействуют на определенный
объем ткани.
Продолжительность процедуры 3-5
часов.
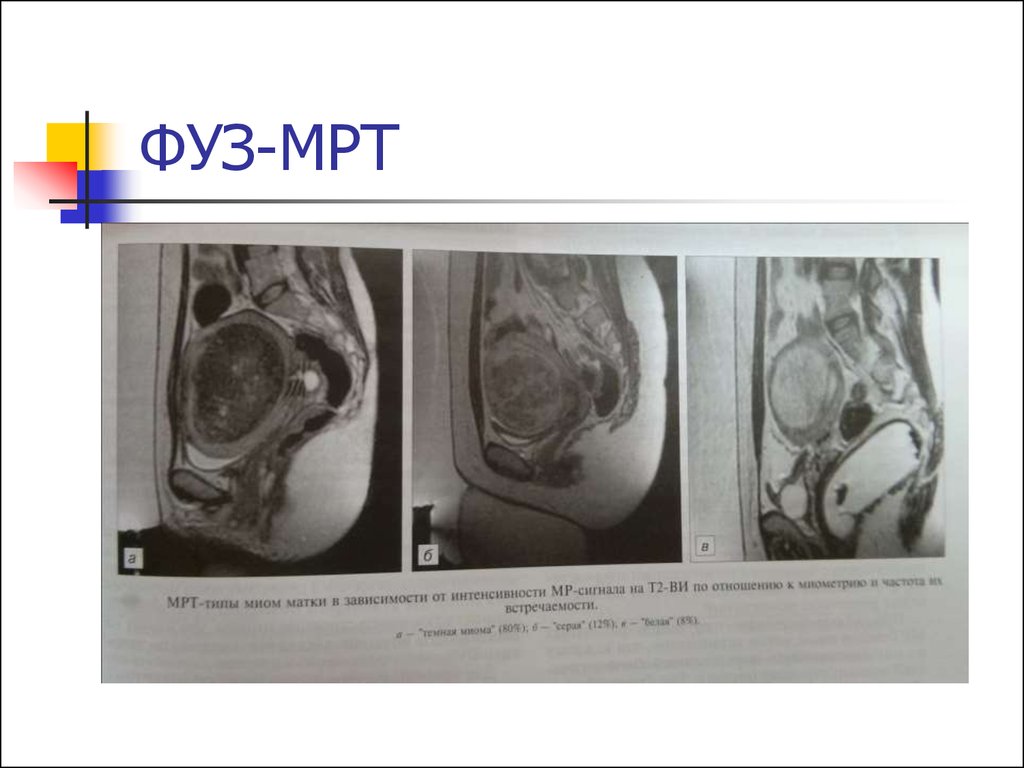
62. ФУЗ-МРТ
Т.к. ультразвук в большей степенипоглощается соединительной
тканью, этот метод практически
неприменим для пролиферирующих
миом. Наибольшая эффективность в
отношении «темных» миом.
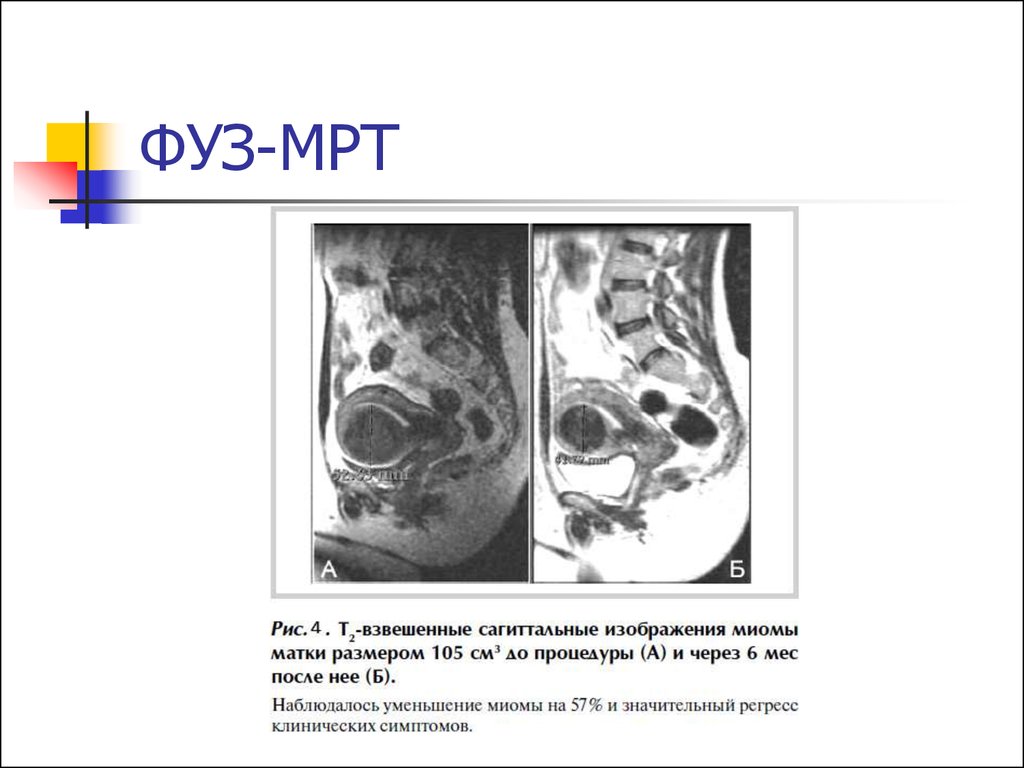
Через 6 месяцев после процедуры
ММ уменьшается в среднем на 50%.

























































 Медицина
Медицина