Похожие презентации:
Кислоты
1.
Что объедняет этирисунки?
2. Кислоты
Состав, классификацияи получение.
3. Что вы знаете о кислотах?
Что вы хотели быузнать о кислотах?
4. Нахождение в природе
Муравей приукусе
впрыскивает в
ранку яд,
содержащий
муравьиную
кислоту
Голожаберные моллюски
в порядке самообороны
выстреливают парами
серной кислоты
Органические
кислоты
входят в
состав
различных
фруктов
5. Кислоты – это сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металлов и кислотных остатков.
Соляная кислотаСерная кислота
Азотная кислота
6. Индикаторы – это вещества, изменяющие свой цвет в растворах кислот и щелочей.
ИндикаторНейтральная
среда
Кислая
среда
Лакмус
Фиолетовый
Красный
Фенолфтал
еин
Метиловый
оранжевый
Бесцветный
Бесцветный
Оранжевый
Красный
Универсаль
ный
индикатор
Желтый
Красный
7.
ПРАВИЛА ТЕХНИКИБЕЗОПАСНОСТИ
Кислота – едкое
вещество!
Попавшие на кожу капли
раствора кислоты немедленно
Разрушает и раздражает смойте сильной струей холодной
воды, а затем обработайте
кожу, слизистые
поврежденную поверхность 2%оболочки.
м раствором питьевой соды.
8.
Лабораторная работаДействие индикатора на
кислоты
Задание:
• проведите опыт, согласно инструкции;
• Сделайте вывод: с помощью каких
индикаторов можно определить кислоту?
Запишите вывод в тетрадь.
9.
По какому признакукислоты разделены на группы?
HF - фтороводородная
HCl - хлороводородная
HBr - бромоводородная
HI - йодоводородная
H2S - сероводородная
HNO3 - азотная
H2SO4 - серная
H2SO3 - сернистая
H2CO3 - угольная
H2SiO3- кремниевая
H3PO4 - фосфорная
10.
По какому признаку кислотыразделены на группы?
HF - фтороводородная
HCl - хлороводородная
HBr - бромоводородная
HI - йодоводородная
HNO3 - азотная
H2S - сероводородная
H2SO4 - серная
H2SO3 - сернистая
H2CO3 - угольная
H2SiO3 - кремниевая
H3PO4 - фосфорная
H3BO3 - борная
11. Классификация кислот:
КислотыБескислородные
Кислородсодержащие
___________________
___________________
_____________________
_____________________
Из перечисленных ниже кислот выпишите
кислородсодержащие и бескислородные кислоты,
определите их основность: HCl, H2CO3, H2S, H3PO4,
HNO3, HBr, H2SO4. Назовите эти кислоты.
12.
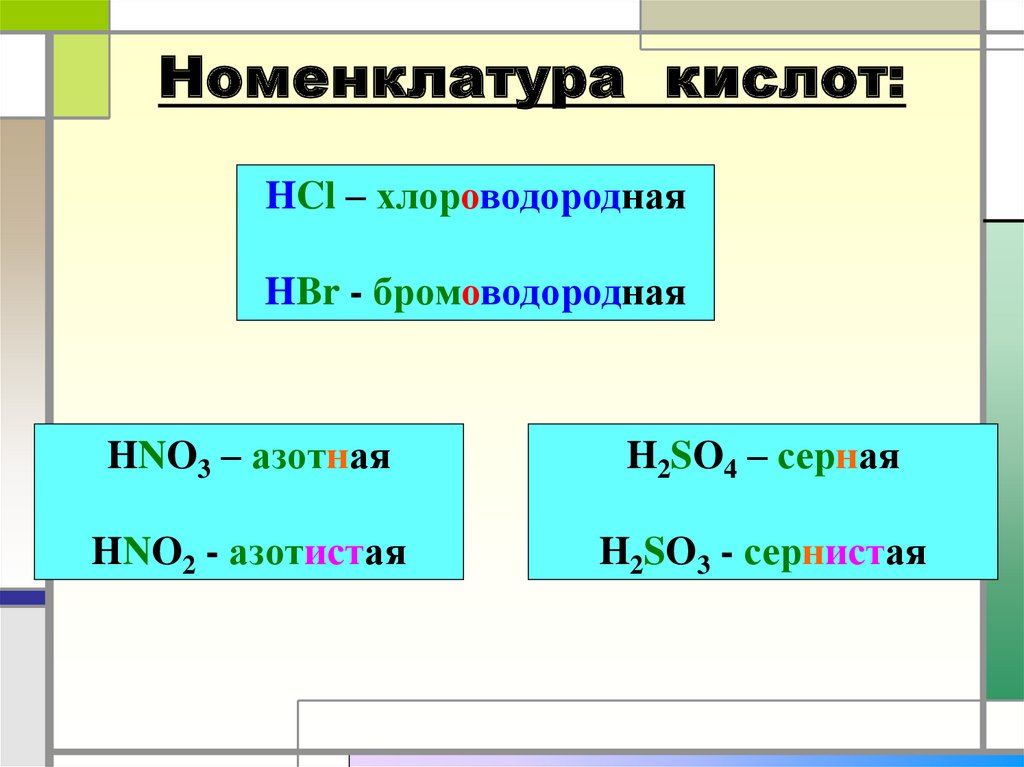
Номенклатура кислот:HCl – хлороводородная
HBr - бромоводородная
HNO3 – азотная
H2SO4 – серная
HNO2 - азотистая
H2SO3 - сернистая
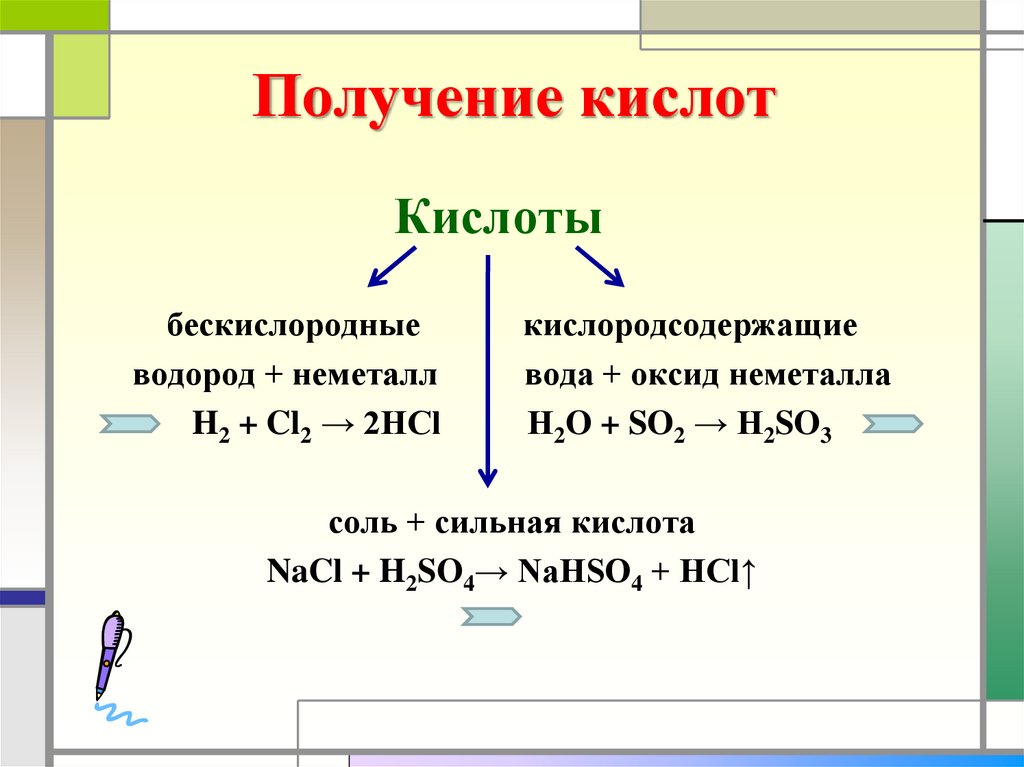
13. Получение кислот
Кислотыбескислородные
водород + неметалл
H2 + Cl2 → 2HCl
кислородсодержащие
вода + оксид неметалла
H2O + SO2 → H2SO3
соль + сильная кислота
NaCl + H2SO4→ NaHSO4 + HCl↑
14.
Составьте уравнения получения следующихкислот: H2SO4 , Н3РO4, H2S. Назовите их и
дайте характеристику.
__________________________________________________
__________________________________________________
__________________________________________________
15. Дополни выражение:
□ Кислоты – это сложные_______ вещества, состоящие из
атомов __________
водорода , способных замещаться на
атомы _________,
металла и _________
кислотных ___________.
остатков
□ Валентность кислотного остатка равна
водорода
количеству атомов ____________.
□ Вещества, изменяющие свою окраску в
индикаторами
кислотах и щелочах, называются __________.
□ В кислой среде метиловый оранжевый, лакмус
и универсальный индикатор окрашиваются в
красный цвет.
__________
16. Выполни задания:
1. Найдите «лишнее» вещество в каждомряду. Поясните.
1. HNO3, HCl, H3PO4
2. H2SiO3, HBr, HI,
3. H2SO4, H2S, H3BO3.
17.
Дан текст, в котором «спрятаны» формулыкислот. Выпишите их и дайте им название.
H2OSOHBrNa2SО3MgBaH2CO3 H2 SO4KOH
HClBaSHKSHH2Na2OH2SКNaClH2SO4
___________________________________
___________________________________
18. Выполни задания:
2. Приведенные на рисунке формулы кислот распределите вследующем порядке:
Кислородсодержащие;
Бескислородные;
Одноосновные;
Двухосновные;
Трехосновные.
19. Самостоятельная работа
Уровень «А»1. Дан текст, в котором «спрятаны» формулы кислот. Выпишите их и
дайте им название.
H2OSOHBrNa2SО3MgBaH2CO3SO4KO
HClBaSHKSHH2Na2OH2SКNaClH2SO4
Уровень «В»
2. Назовите кислоты и дайте им характеристику по плану:
1. Название
2. Наличие кислорода
3. Основность
4. Растворимость
1 вариант - H2SО4
2 вариант – HNO3
Уровень «С»
3. Составьте уравнение получения кислот, укажите тип реакции и
назовите вещества. В формуле кислоты укажите валентность
кислотного остатка, определите ее основность.
1 вариант – соляная, сернистая;
2 вариант – сероводородная, серная.
20. Домашнее задание
§ 47, № 1,2 (устно), 11 (письменно).Творческое задание: сочинить рассказ, сказку
о кислотах.
21.
Рефлексия:•Что нового узнали на уроке?
•Что было особенно интересно?
•В чем возникали трудности?
•С каким настроением вы заканчиваете урок?
Выбрать смайлики:
хорошее
безразличное
грустное


















 Химия
Химия