Похожие презентации:
Карбоновые кислоты
1.
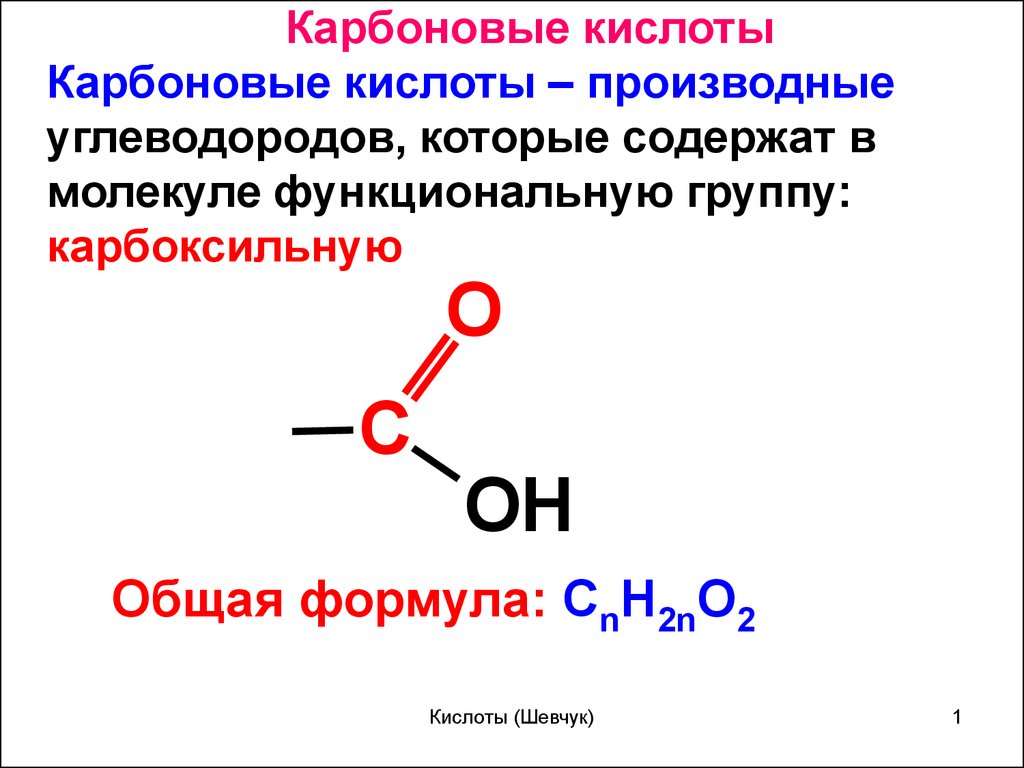
Карбоновые кислотыКарбоновые кислоты – производные
углеводородов, которые содержат в
молекуле функциональную группу:
карбоксильную
O
C
OH
Общая формула: CnH2nO2
Кислоты (Шевчук)
1
2.
Названия кислотНазвание
кислоты
Метановая
(муравьиная)
Этановая
(уксусная)
Пропановая
(пропионовая)
Бутановая
(масляная)
Пентановая
(валериановая)
Гексановая
(капроновая)
Изомасляная
Формула
Н–СООН
СН3–СООН
СН3–СН2–СООН
СН3–СН2–СН2–СООН
СН3–СН2–СН2–СН2–СООН
СН3–СН2–СН2–СН2–СН2–СООН
(СН3)2СН2–СООН
Кислоты (Шевчук)
2
3.
Способы полученияЖЕСТКОЕ ОКИСЛЕНИЕ
1. АЛКАНОВ, АЛКЕНОВ, АЛКИНОВ
(см. выше)
2. боковой
цепочки
аренов
(см.выше)
3. СПИРТОВ и альдегидов (см.
выше)
Кислоты (Шевчук)
3
4.
2. Гидролиз геминальных тригаClлогензамещенных УВ
CH3
Cl C Cl
3Cl2/hv
H2O
-3HCl
O
OH
HO C OH
-H2O
Кислоты (Шевчук)
гемтриол
C
OH
4
5.
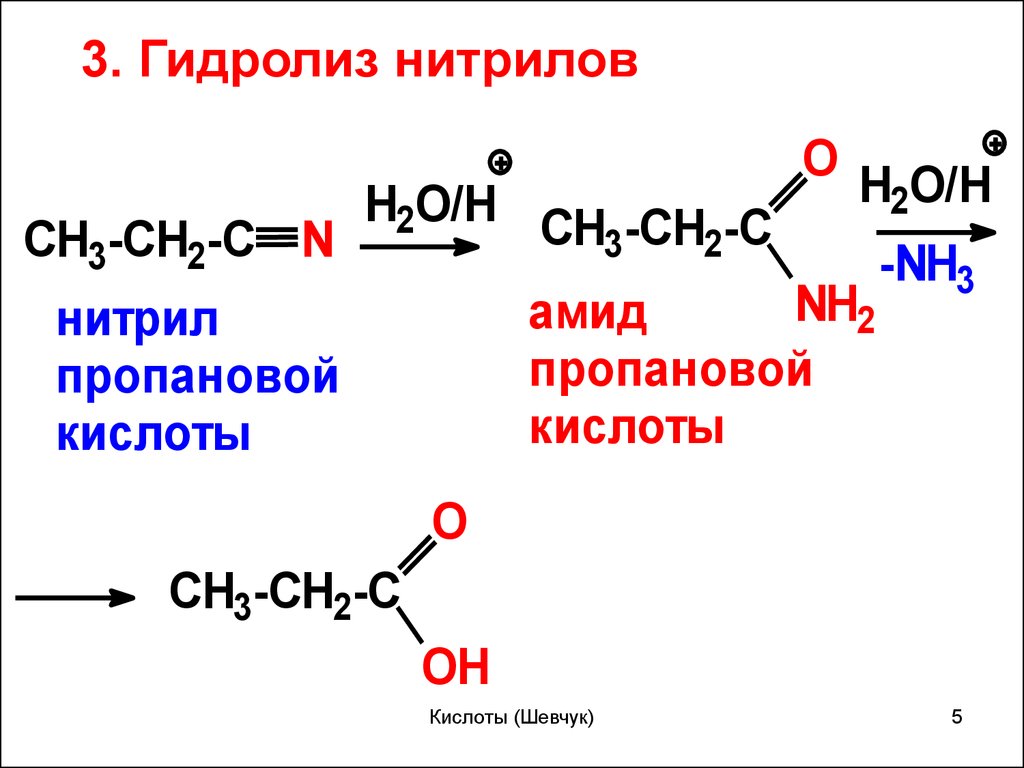
3. Гидролиз нитриловO
H2O/H
H2O/H CH -CH -C
CH3-CH2-C N
3
2
-NH3
NH2
амид
нитрил
пропановой
пропановой
кислоты
кислоты
O
CH3-CH2-C
OH
Кислоты (Шевчук)
5
6.
ФИЗИЧЕСКИЕ СВОЙСТВАС1-С9 - бесцветные жидкости.
Ароматические,
высшие
алифатические,
и
все
дикарбоновые
–
твердые
вещества.
Т. кип. жидких кислот выше, чем
спиртов и альдегидов из-за
образования
водородных
связей:
Кислоты (Шевчук)
6
7.
Низшие членыгомологического ряда
алифатических
монокарбоновых кислот
смешиваются с водой в любых
пропорциях.
Ароматические карбоновые
кислоты плохо растворимы в
воде, но лучше в этаноле.
Кислоты (Шевчук)
7
8.
Химические свойства1. Реакции с участием карбоксильной
группы:
1) Кислотные свойства замещение водорода ОН группы на
атом металла с образованием солей
карбоновых кислот.
Карбоновые кислоты являются более
сильными кислотами, чем спирты и
фенолы
Кислоты (Шевчук)
8
9.
OH3 C
NaOH
C
OH
O
H2O
ONa
ацетат натрия
H3C
C
Кислоты (Шевчук)
9
10.
Качественная реакция накарбоновые кислоты –
реакция с содой →
выделение углекислого
газа
C6H5 C
O
NaHCO3
OH
O
CO2 H2O
ONa
бензоат натрия
C6H5 C
Кислоты (Шевчук)
10
11.
2) пиролиз солей Са и Ва(см. кетоны)
O
O
R C O Ca O C R
o
300
O
R C R
Кислоты (Шевчук)
CaCO3
11
12.
2) Реакции с разрывом связиС-ОН идут с образованием
функциональных производных
кислот:
-галогенангидридов
- ангидридов
-сложных эфиров
- амидов
Кислоты (Шевчук)
12
13.
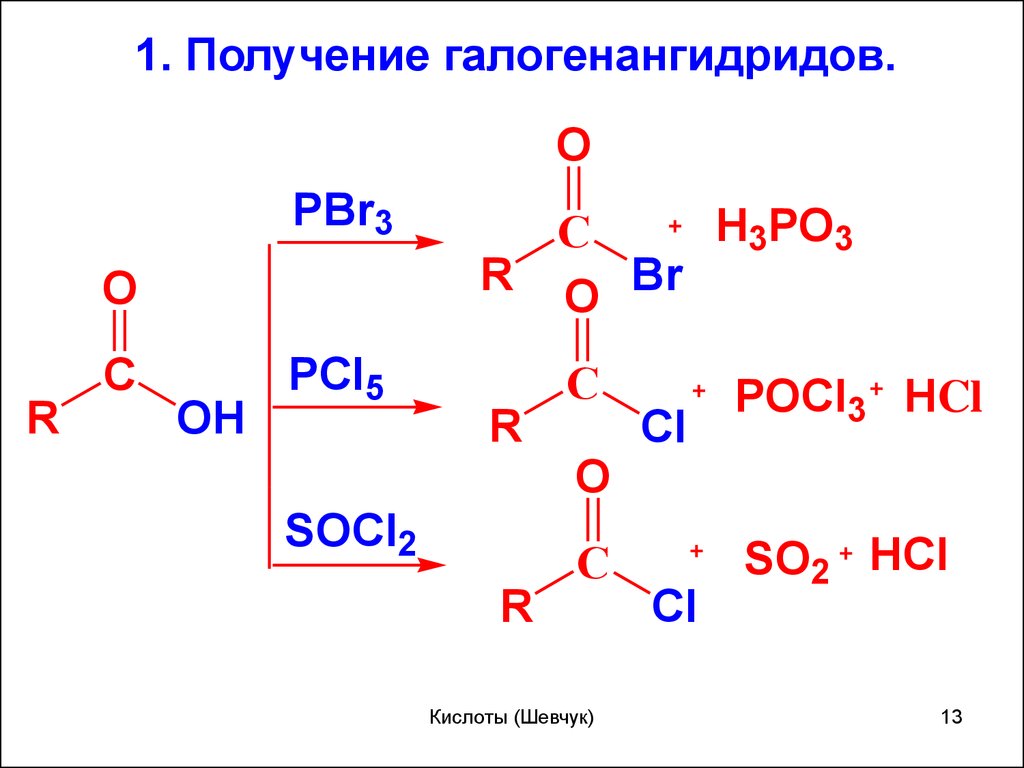
1. Получение галогенангидридов.O
PBr3
O
R
С
OH
PCl5
H3PO3
С
R O Br
R
SOCl2
R
С
O
С
Кислоты (Шевчук)
Cl
Cl
POCl3 HCl
SO2 HCl
13
14.
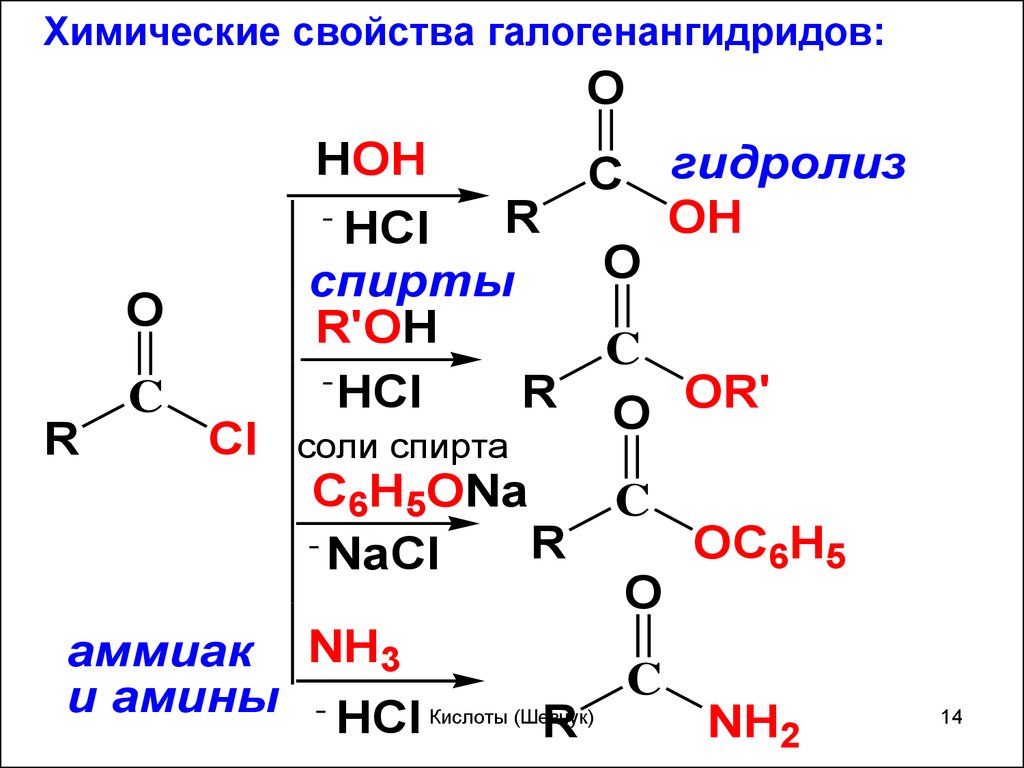
Химические свойства галогенангидридов:O
HOH
R
спирты
R'OH
- HCl
R
- HCl
O
R
C
Cl
соли спирта
C6H5ONa
- NaCl
R
C гидролиз
OH
O
C
OR'
O
C
O
OC6H5
аммиак NH3
и амины - HCl Кислоты (Шевчук) C
R
NH2
14
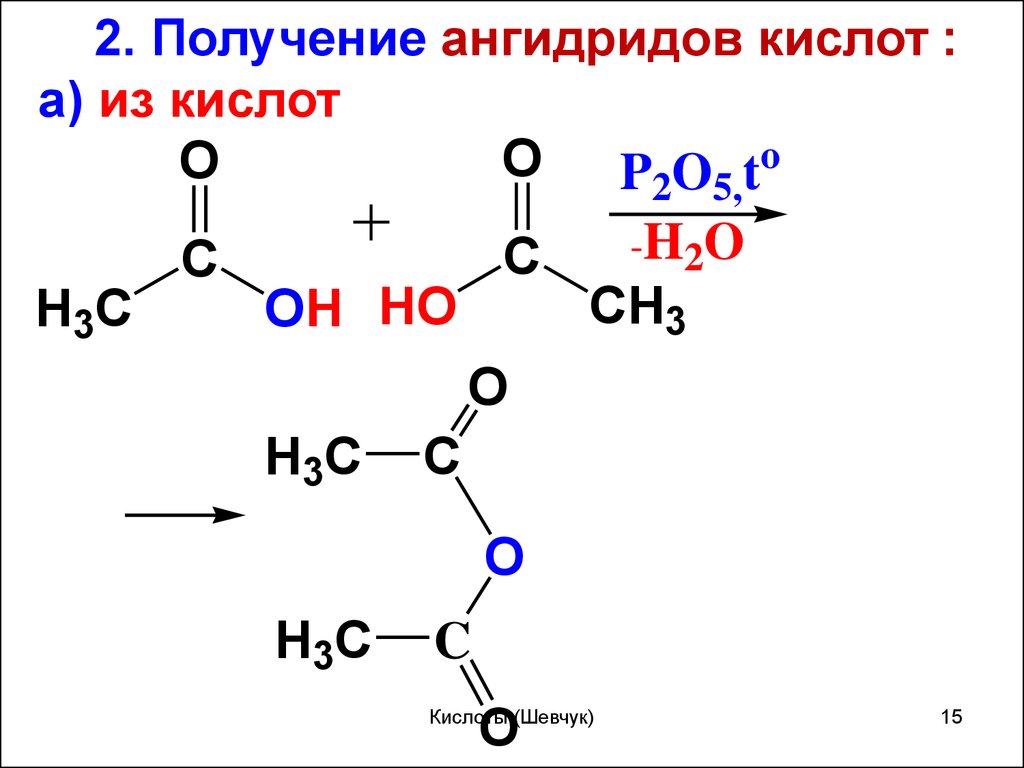
15.
2. Получение ангидридов кислот :а) из кислот
O P2O5,to
O
-H2O
C
C
CH3
H3 C
OH HO
O
H3 C
C
O
H3 C
C
O
Кислоты (Шевчук)
15
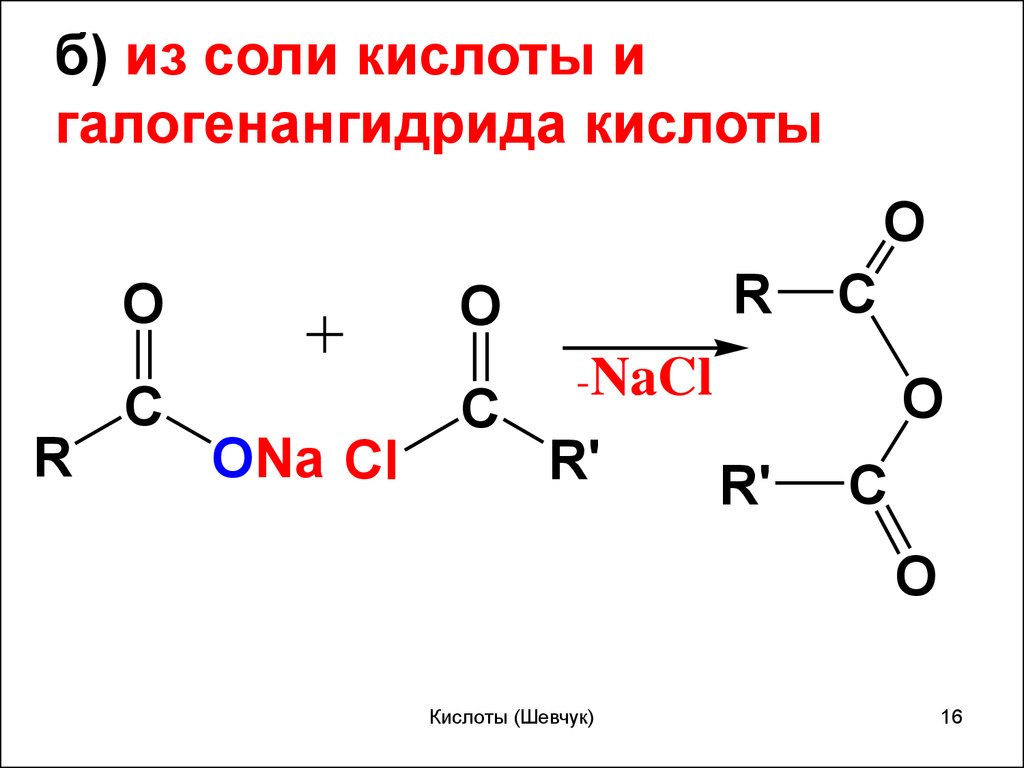
16.
б) из соли кислоты игалогенангидрида кислоты
O
O
R
C
R
O
ONa Cl
C
C
-NaCl
R'
O
R'
C
O
Кислоты (Шевчук)
16
17.
Химические свойства ангидридов кислот:HOH
R
O
R
C
O
R
R'OH
R
C
O
O
O
C
C
OH R
O
OH
гидролиз
O
C
C
OR' R
O
NH3
R
C
NH2
Кислоты (Шевчук)
OH
алкоголиз
O
C
R
OH
аммонолиз 17
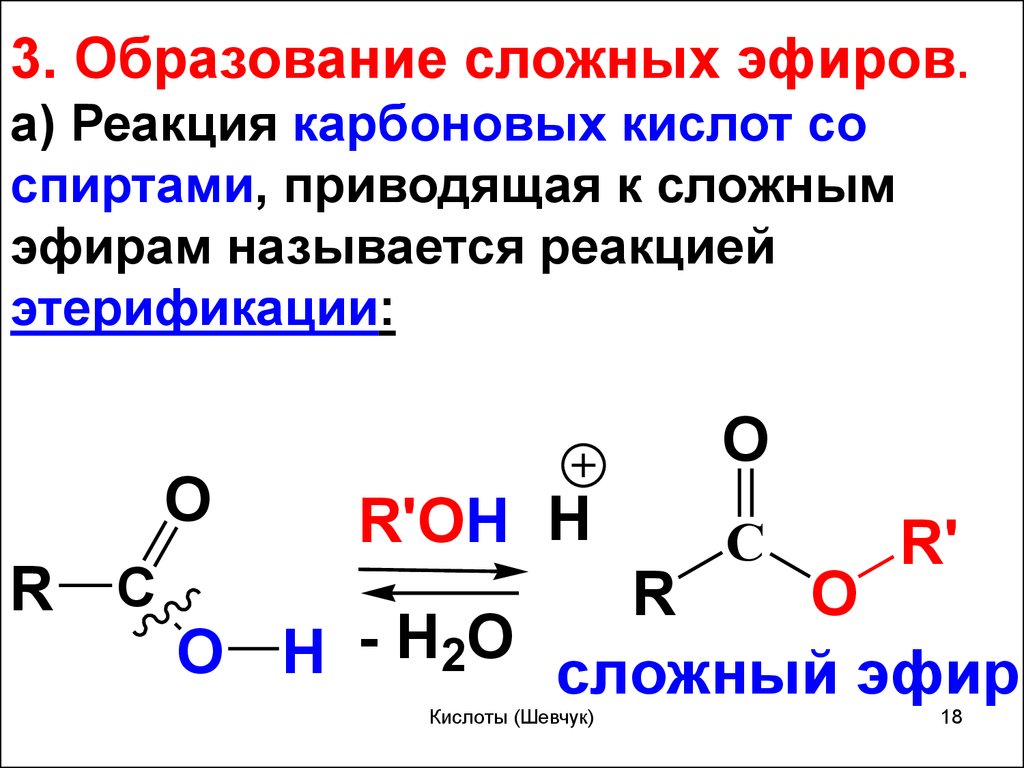
18.
3. Образование сложных эфиров.а) Реакция карбоновых кислот со
спиртами, приводящая к сложным
эфирам называется реакцией
этерификации:
O
R
С
O
R'OH H
С
R'
R
O
O H - H2O сложный эфир
Кислоты (Шевчук)
18
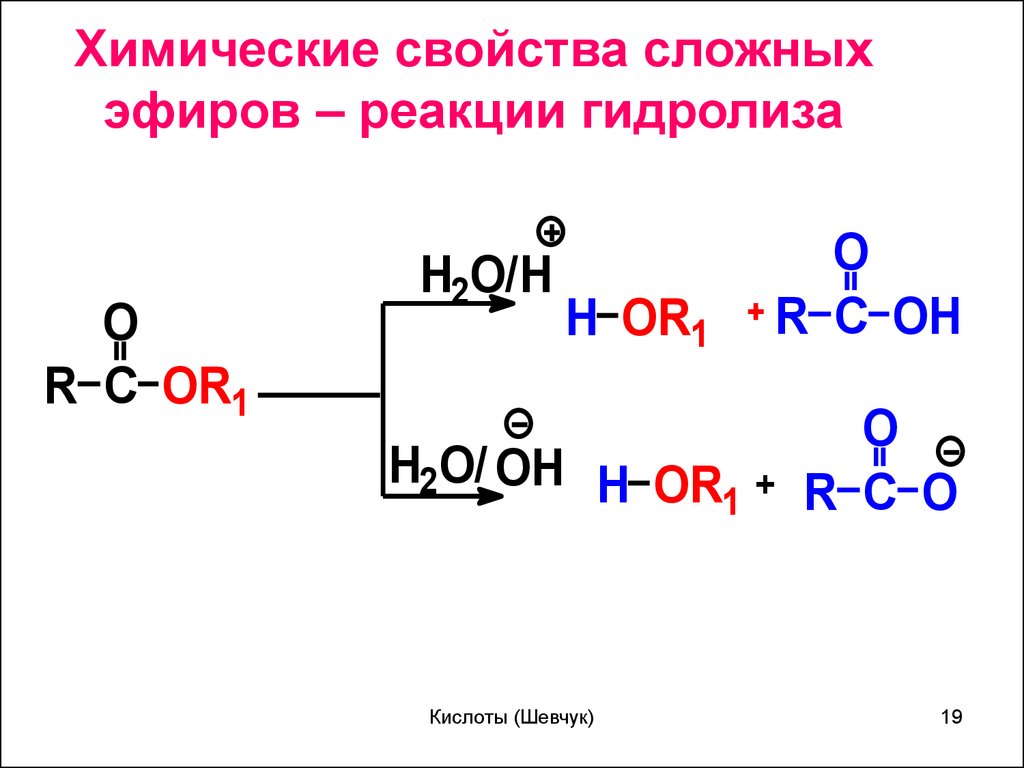
19.
Химические свойства сложныхэфиров – реакции гидролиза
O
R C OR1
H2O/H
H OR1
O
R C OH
H2O/ OH H OR +
1
Кислоты (Шевчук)
O
R C O
19
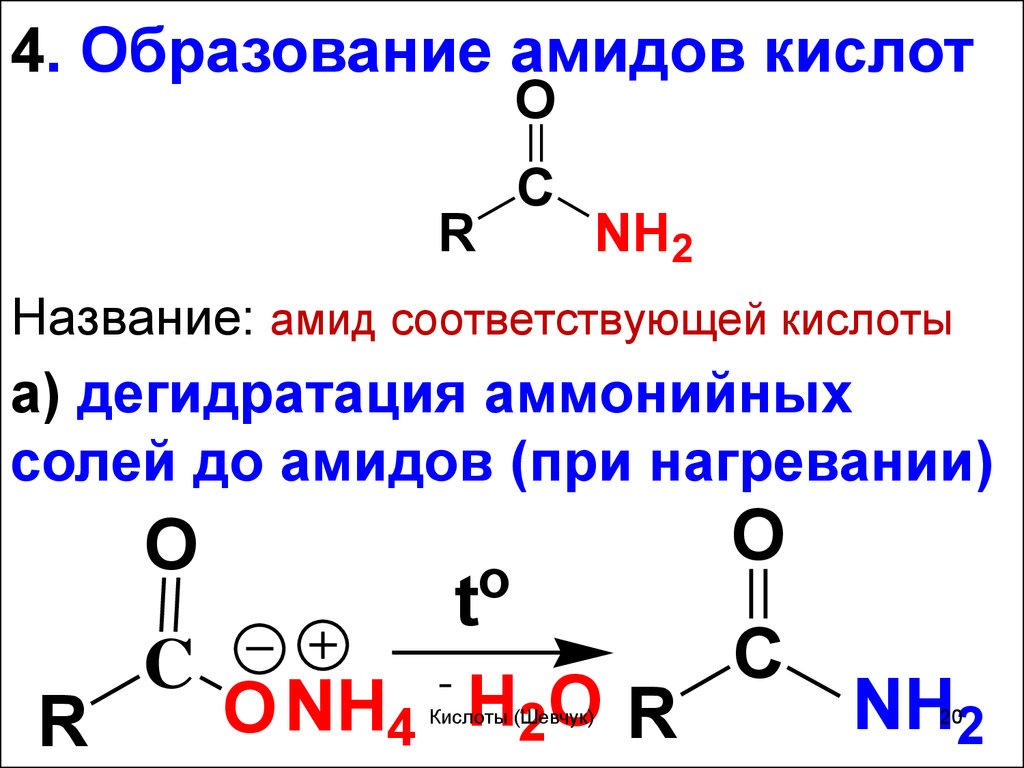
20. Название: амид соответствующей кислоты
4. Образование амидов кислотO
C
R
NH2
Название: амид соответствующей кислоты
а) дегидратация аммонийных
солей до амидов (при нагревании)
O
o
O
t
C
C
H
O
NH2
NH
O
R
2
4
R
Кислоты (Шевчук)
20
21.
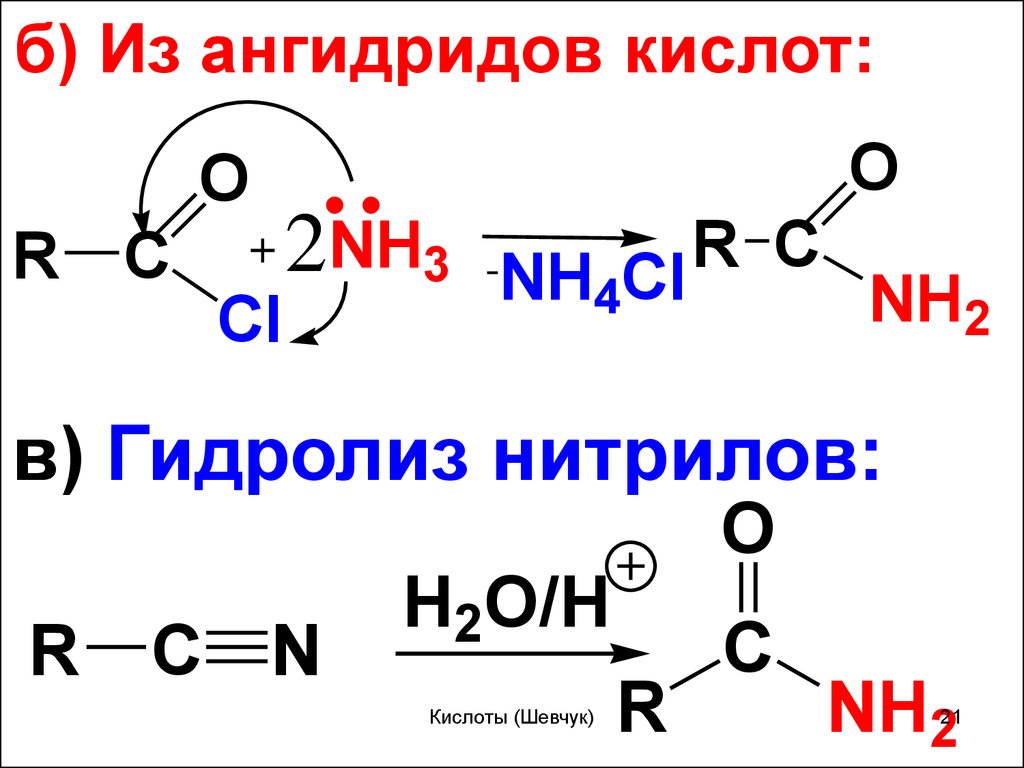
б) Из ангидридов кислот:O
R C
Cl
O
2NH3
-NH
R
C
Cl
4
NH2
в) Гидролиз нитрилов:
R C N
O
H2O/H
Кислоты (Шевчук)
R
C
NH2
21
22.
Химические свойства амидов кислот:HOH R
o
,t
H
O
OH
O
R
C
NH2
NH3 гидролиз
C
O
HOH
NaOH ,to
P2O5 ,to
R
C
NH3 гидролиз
ONa
R C
Кислоты (Шевчук)
дегидратация
NH H2O
22
23.
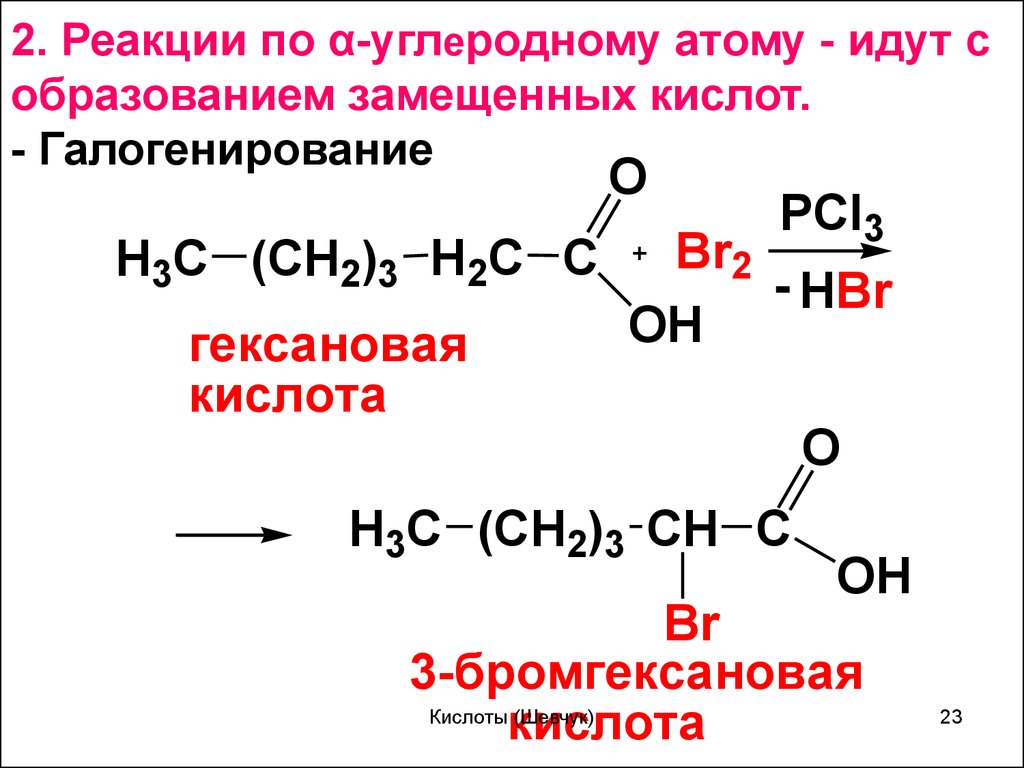
2. Реакции по α-углеродному атому - идут собразованием замещенных кислот.
- Галогенирование
O
H3C (CH2)3 H2C C
гексановая
кислота
PCl3
Br2
- HBr
OH
H3C (CH2)3 CH C
O
OH
Br
3-бромгексановая
кислота
Кислоты (Шевчук)
23
24.
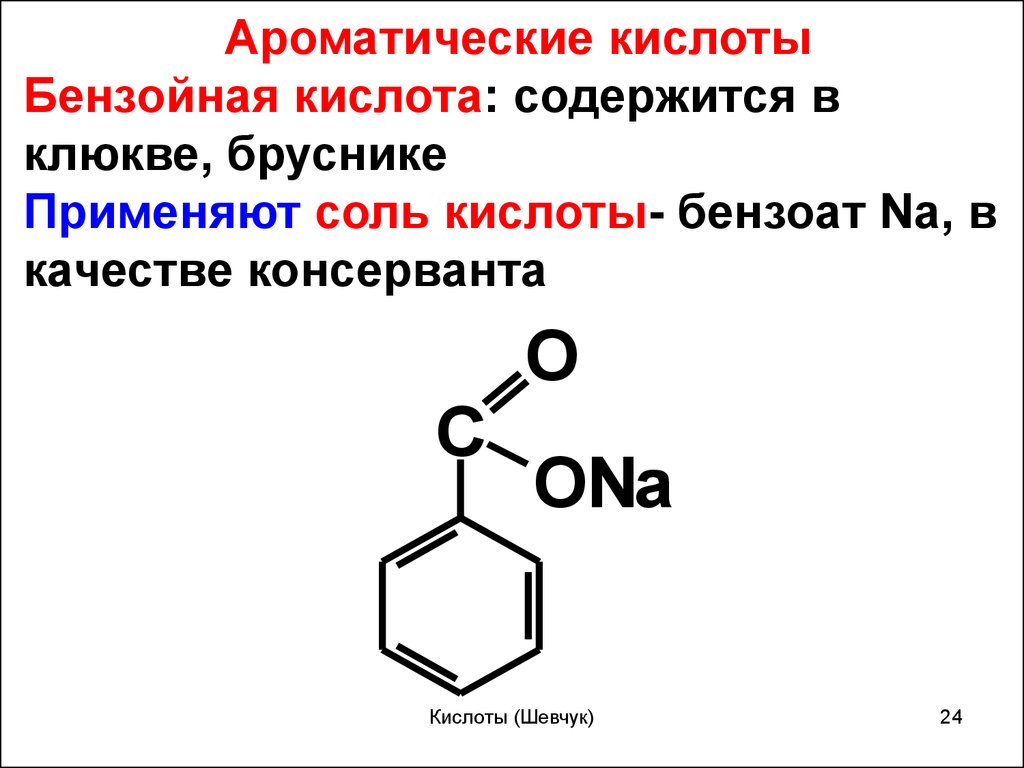
Ароматические кислотыБензойная кислота: содержится в
клюкве, бруснике
Применяют соль кислоты- бензоат Na, в
качестве консерванта
С
O
ONa
Кислоты (Шевчук)
24
25.
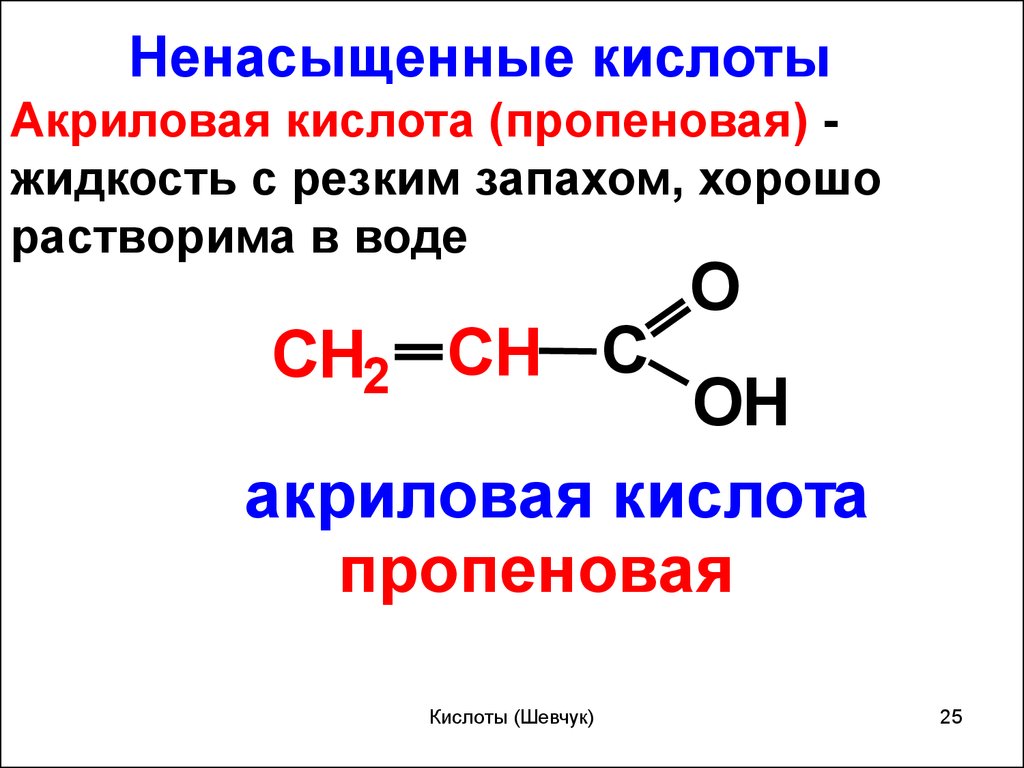
Ненасыщенные кислотыАкриловая кислота (пропеновая) жидкость с резким запахом, хорошо
растворима в воде
CH2 CH C
O
OH
акриловая кислота
пропеновая
Кислоты (Шевчук)
25
26.
Метакриловаяпроизводстве
полимерных
(оргстекла)
CH3
CH2
C C
кислота – в
прозрачных
материалов
O полим.
OH
метакриловая кислота
2-метилпропеновая
Кислоты (Шевчук)
COOH
CH2 C
n
CH3
26
27.
Двухосновные кислоты карбоновые кислоты,содержащие две карбоксильные
группы
Гомологический ряд:
HOOC-COOH – щавелевая, этандиовая
HOOC-CH2-COOH – малоновая, пропандиовая
HOOC-(CH2)2-COOH – янтарная, бутандиовая
HOOC-(CH2)3-COOH – глутаровая, пентандиовая
HOOC-(CH2)4-COOH – адипиновая, гександиовая
Кислоты (Шевчук)
27
28.
COOHCOOH
фталевая
1,2-бензолдикарбоновая
COOH
COOH
терефталевая
1,4-бензолдикарбоновая
Кислоты (Шевчук)
28
29.
Химические свойства:1. Кислотные – образуют с
NaOH, NaHCO3 два ряда
солей: кислые и средние
соли. Кислотные свойства
выше одноосновных кислот,
так как содержат две
карбоксильные группы
Кислоты (Шевчук)
29
30.
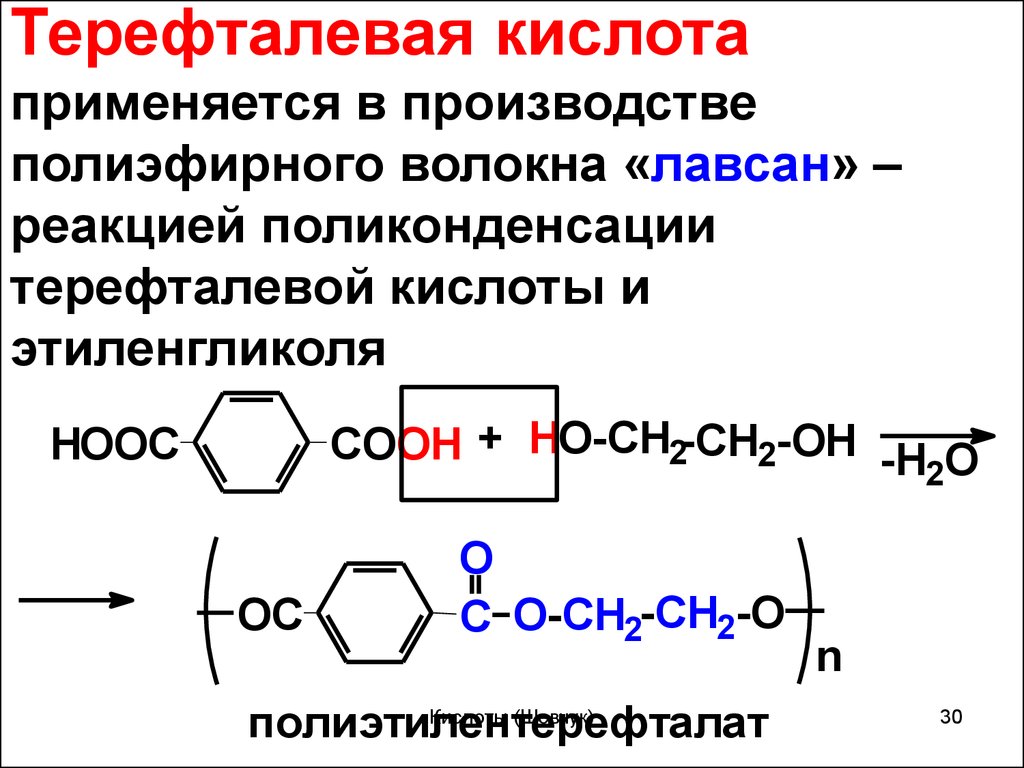
Терефталевая кислотаприменяется в производстве
полиэфирного волокна «лавсан» –
реакцией поликонденсации
терефталевой кислоты и
этиленгликоля
COOH + HO-CH2-CH2-OH -H O
2
HOOC
OC
O
C O-CH2-CH2-O
Кислоты (Шевчук)
полиэтилентерефталат
n
30
31.
Высшие жирные кислотыПальмитиновая- С15Н31СООН, Стеариновая
- С17Н33СООН,
Эти кислоты содержатся жире животных.
Жиры - сложные эфиры глицерина и
высших кислот
Применение:
- в производстве мыла:
- Na-соли этих кислот твердое мыло,
- К-соли - жидкое мыло
- в производстве резины, линолеума,
лаков, краски
Кислоты (Шевчук)
31
32.
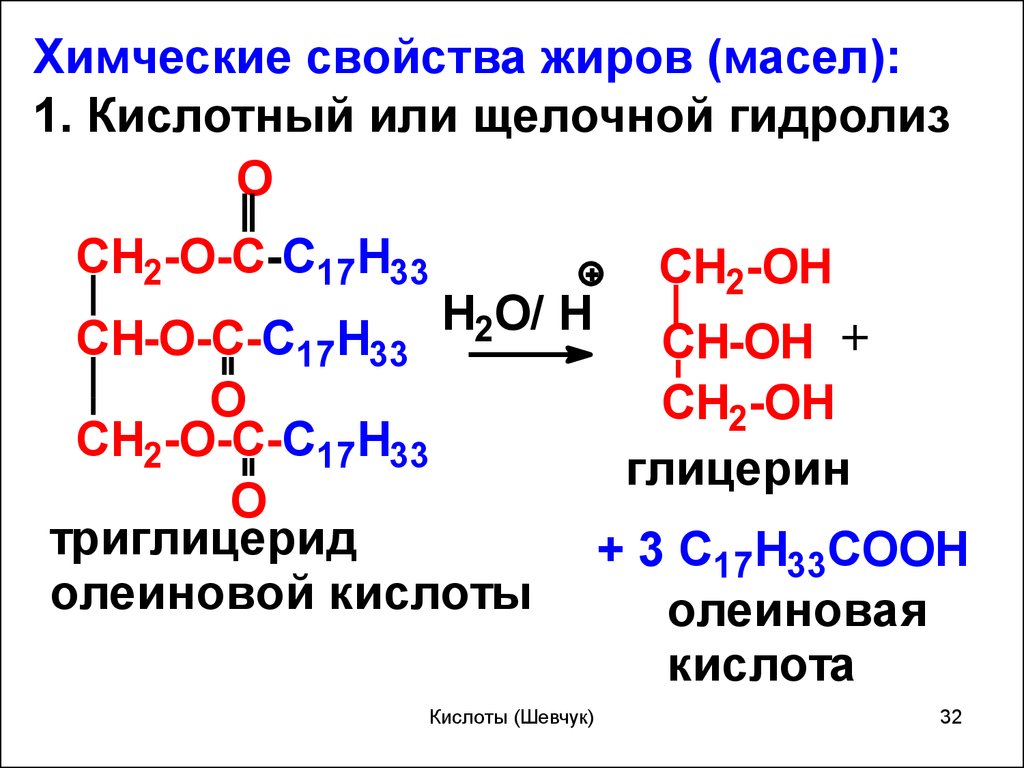
Химческие свойства жиров (масел):1. Кислотный или щелочной гидролиз
O
CH2-O-C-C17H33
Н2O/ H
CH-O-C-C17H33
O
CH2-O-C-C17H33
O
триглицерид
олеиновой кислоты
Кислоты (Шевчук)
CH2-OH
CH-OH +
CH2-OH
глицерин
+ 3 C17H33COOH
олеиновая
кислота
32

















 Химия
Химия








