Похожие презентации:
Второе начало термодинамики и энтропия
1. ВТОРОЕ НАЧАЛО ТЕРМОДИ-НАМИКИ И ЭНТРОПИЯ
ВТОРОЕНАЧАЛО
ТЕРМОДИНАМИКИ И
ЭНТРОПИЯ
2. Проверочная работа
Найти изменение энтропии молей газаВан-дер- Ваальса
2
a
p 2 V b RT
V
при изменении давления и объема от p0 и
V0 до p и V. Молярная теплоем-кость при
постоянном объеме cv const.
3. Проверочная работа
2ap 2 V b RT
V
2
a
RT
TdS cv dT 2 dV pdV cv dT
dV ,
V
V b
dT
R
dS cv
dV ,
T V b
V b
T
S cv ln R ln
,
T0
V0 b
4.
2ap 2 V b
V b
V
S cv ln
R ln
2
V0 b
a
p0 2 V0 b
V0
2a
p 2
V b
V
cv ln
(cv R) ln
2
V0 b
a
p0 2
V0
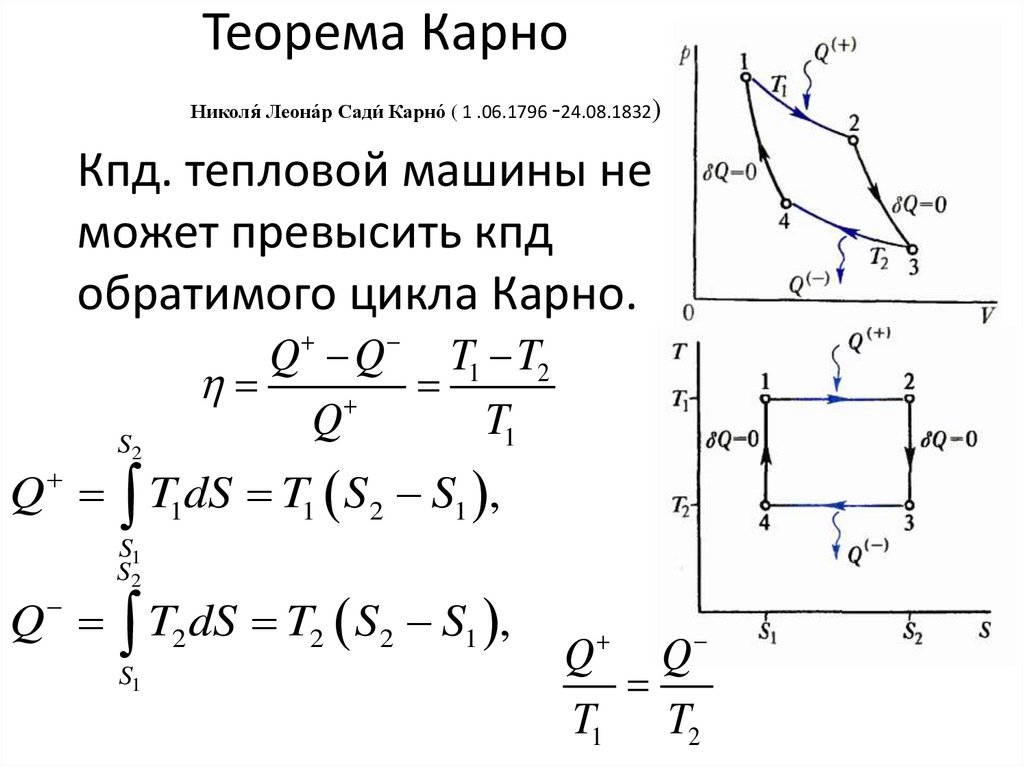
5. Теорема Карно Николя́ Леона́р Сади́ Карно́ ( 1 .06.1796 -24.08.1832)
Теорема КарноНиколя́ Леона́р Сади́ Карно́ ( 1 .06.1796 -24.08.1832)
Кпд. тепловой машины не
может превысить кпд
обратимого цикла Карно.
S2
Q Q T1 T2
Q
T1
Q T1dS T1 S2 S1 ,
S1
S2
Q T2 dS T2 S2 S1 ,
S1
Q Q
T1 T2
6. Формулировка II начала термодинамики
Для любой квазиравновесной, (т.е.участвующей в квазистатическом процессе)
термодинамической системы существует
однозначная функция термодинамического
состояния S, называемая энтропией, такая,
Q
что ее полный дифференциал dS
.
T
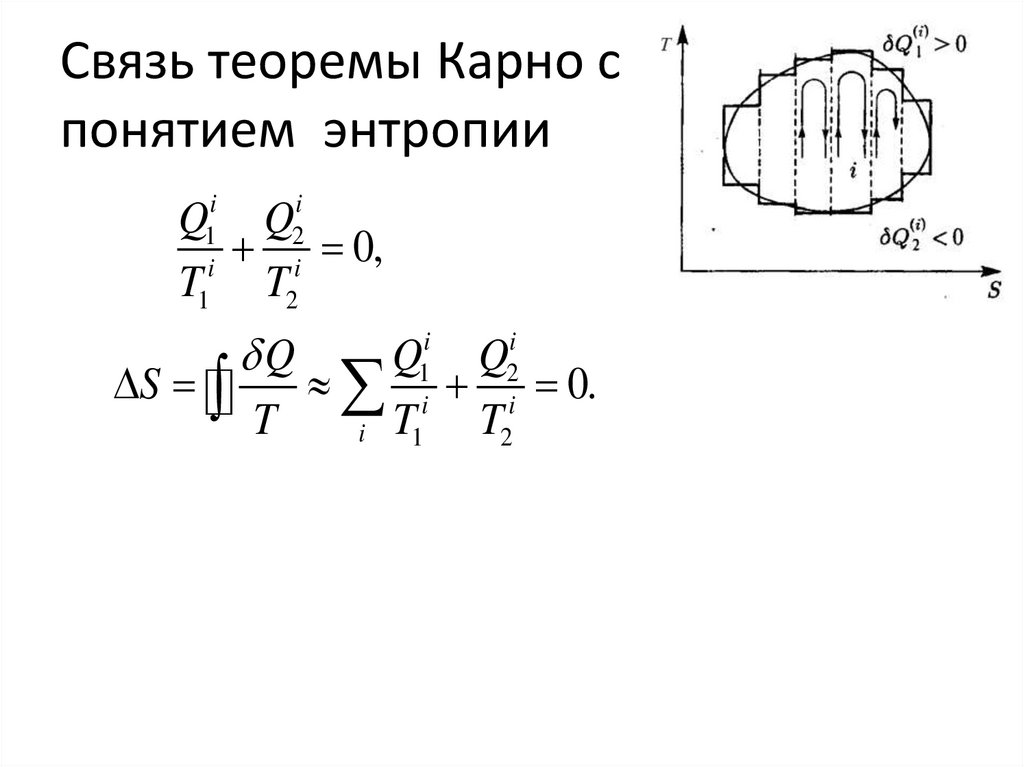
7. Связь теоремы Карно с понятием энтропии
Q1i Q2ii 0,
i
T1 T2
Q Q
Q
S
0.
T
T
i T
i
1
i
1
i
2
i
2
8. Неравенство Клаузиуса
T1 T2 Q QQ
0
0
T1
T T
T
Q
Q
Q
Q
T A B T B A T A B T S A SB 0
i
1
i
1
i
2
i
2
Q
SB S A
,
T
A B
Q 0 SB S A
9. Другие формулировки II HT
• Уи́льям То́мсон, 1-й барон Ке́львин(26.06.1824-17.12.1907)
• Макс Карл Эрнст Людвиг Планк (23.04.18584.10.1947)
Невозможно построить периодически
действующую машину, которая совершала
бы работу за счет охлаждения некоторого
источника тепла (1851).
10. Другие формулировки II HT
• Рудольф Юлиус ЭмануэльКла́узиус (Рудольф Готтлиб) (01.01.182224.08.1888)
Тепло не может само по себе (без
компенсации ) перейти от тела менее
нагретого к более нагретому (1850).
11. Рост энтропии
Q QS S A S B 0
T1 T2
A
T1 T2
B
Энтропия адиабатически
изолированной системы не
убывает.
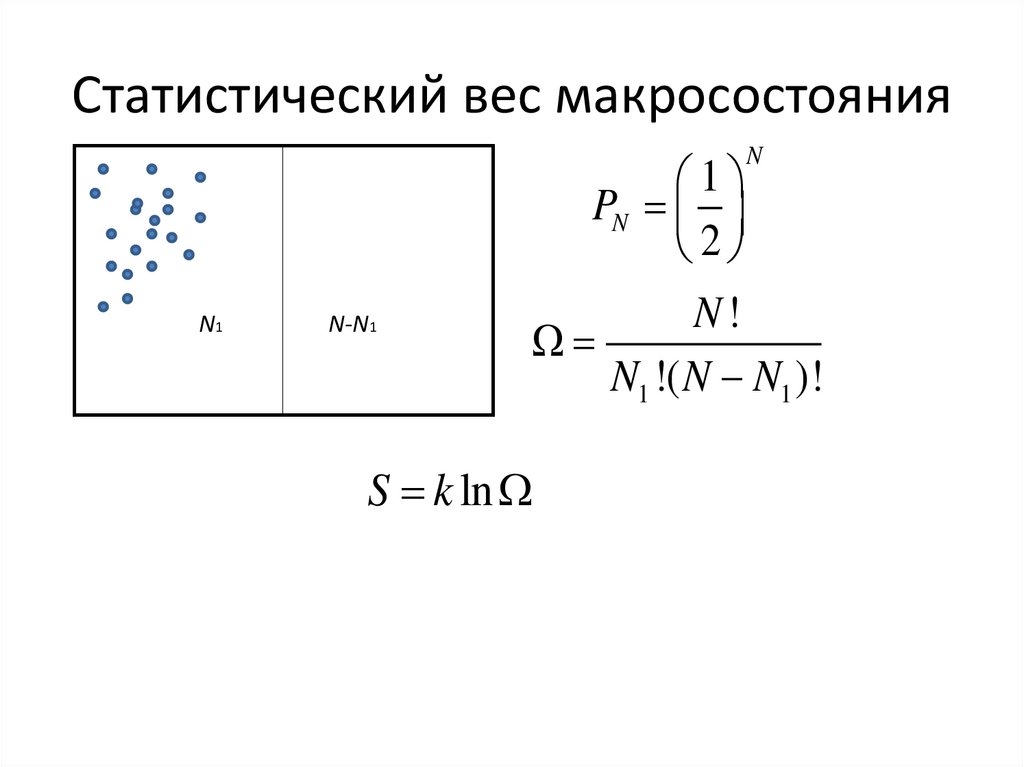
12. Статистический вес макросостояния
NN1
N-N1
1
PN
2
N!
N1 !( N N1 )!
S k ln
13. Молекулярно-кинетическое обоснование (следствие молекулярного хаоса)
n1 nT1 T
14. Н-теорема Больцмана, парадокс Лошмидта.
Величина H
S
P ln Pd 3v ln P
Nk
не может
возрастать.
• Для любой механической системы в силу
обратимости во времени уравнений ньютоновской динамики возможна последовательность состояний с уменьшающейся энтропией.
15. Теорема Пуанкаре о возвращении
Любое состояние динамической системычерез некоторое время повторится с любой
наперед заданной точностью.
Так, для сосуда с размерами 10 см, содержащего 70 молекул газа, время возврата
всех молекул к нахождению в одной половине сосуда порядка возраста Вселенной
1010 лет.
16. Распределение Больцмана и формула Больцмана
( E ) ( E1 ) ( E2 )E E1 E2
E ln ( E ) 0 exp( E)
1/ kT
(S ) (S1 ) (S2 )
S S1 S2
S ln (S ) 0 exp( S )
1/ k
17. Домашнее задание
18.
19.
dVdT
dS cv
R ,
V
T
p V , V RT
RdT 2 VdV
dV 2dV
dV
2 VdV
dS cv
R cv
R
2
V V
V
V
2R
1
2cv R d ln V
R d ln V
Rd ln V
1
1
1
1
S
R ln V C SM
R ln VM C '
1
1
2
20.
21.
S1U
,
TdS dU dA, S U dS dU , , T
U1
cv
2
U S1
dU dU dA,
cv U1
1
2
U S1
A
U
2 cv U1
2
1
1 S1
2 R
2
2
U
U
2 1 U 2 U1
22.
23.
RpV C TV T V , c cv
n 1
T
V
T
R
T
T
S cv ln R ln cv ln
ln c ln
T0
V0
T0 n 1 T0
T0
n
n 1
n 1
0 0
T S S1
S S1
ln
T T0 exp
T0
c
c




















 Физика
Физика








