Похожие презентации:
Комплексные соединения
1. КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
2. Цель:
• Сформировать представление осоставе, строении, номенклатуре,
видах и классификации комплексных
соединений.
• Научить давать названия
комплексным соединениям по
формулам, составлять формулы по
названиям.
3.
Комплексными называютсоединения, содержащие
сложные ионы и молекулы,
способные к существованию
как в кристаллическом виде,
так и в растворе.
4.
Альфред ВЕРНЕР (Werner A.)(12.XII.1866 - 15.XI.1919)
Швейцарский химик Альфред Вернер, лауреат Нобелевской премии.
Его научная деятельность проходила в Цюрихском университете.
Ученый синтезировал много новых комплексных соединений,
систематизировал ранее известные и вновь полученные
комплексные соединения и разработал экспериментальные методы
доказательства его строения
5.
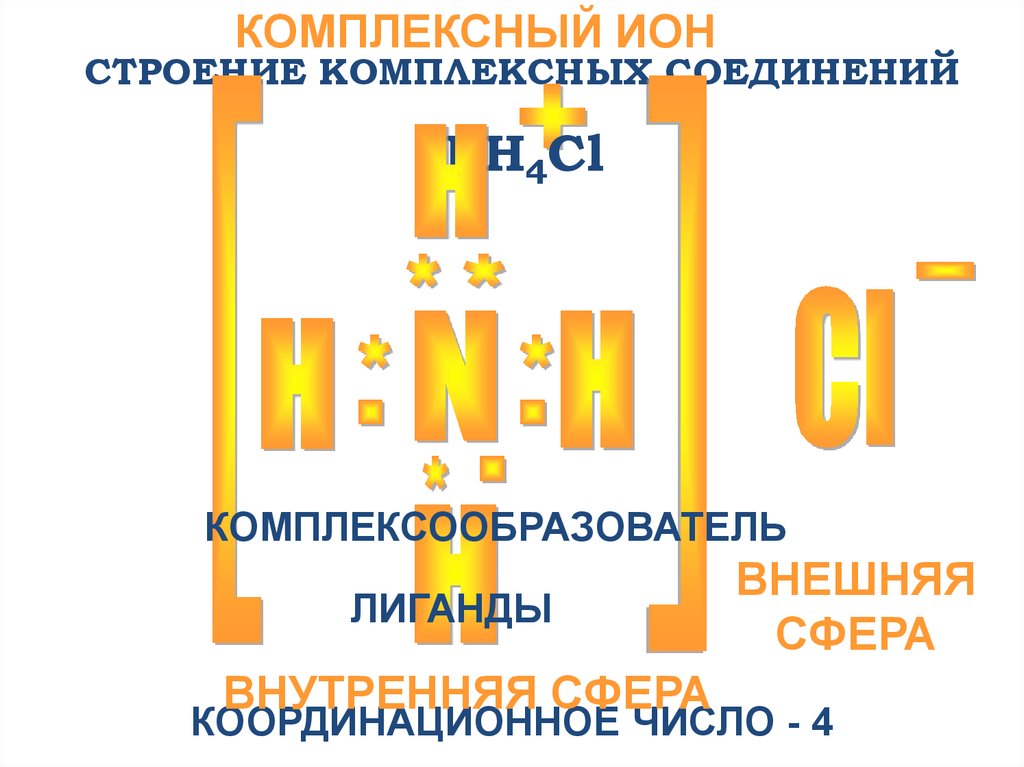
КОМПЛЕКСНЫЙ ИОНСТРОЕНИЕ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ
NH4Cl
КОМПЛЕКСООБРАЗОВАТЕЛЬ
ЛИГАНДЫ
ВНУТРЕННЯЯ СФЕРА
ВНЕШНЯЯ
СФЕРА
КООРДИНАЦИОННОЕ ЧИСЛО - 4
6.
-3+1
-1
[N H 4]Cl
ВНУТРЕННЯЯ СФЕРА:
+
]
[NH
КОМПЛЕКСНЫЙ ИОН
4
-3
КОМПЛЕКСООБРАЗОВАТЕЛЬ N
+
ЛИГАНДЫ H
ВНЕШНЯЯ СФЕРА
АНИОН Cl-
7. Лигандами могут быть: а) полярные молекулы NH3 ; H2O ; CO ; NO б) простые ионы CI- ; Br- ; I- в) сложные ионы CN- ; SCN- ; NO2- ; OH-
Лигандами могут быть:а) полярные молекулы NH3 ;
H2O ; CO ; NO
б) простые ионы CI ; Br ; I
в) сложные ионы CN ; SCN ;
NO ; OH
2
8.
Na+2 [Zn+x (OH)-4 ](+1) ·2 + x + (-1) ·4 = 0
x = 0-2+4
x = +2
Na+[Zn+2(OH)-4]
9.
РАССТАВЬТЕ СТЕПЕНЬ ОКИСЛЕНИЯ ИОНАКОМПЛЕКСООБРАЗОВАТЕЛЯ:
Na3[AlF6]
Ответ: Na+3[Al+3F-6]
K[MgCl3]
Ответ: K+[Mg+2Cl-3]
Na[Al(OH)4] Ответ: Na+[Al+3(OH)-4]
Na4[Fe(CN)6] Ответ:Na+4[Fe+2(CN)-6]
10.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙЧИСЛИТЕЛЬНЫЕ:
23456-
дитритетрапентагекса-
НАЗВАНИЯ ЛИГАНДОВ:
H2O - аква
NH3 - амин
СO - карбонил
OН- - гидроксо(СN)- - циано
(NO3)- - нитро
F-, Cl-, Br-, I- - фторо-, хлоро-,
бромо-, йодо-
11.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙНАЗВАНИЯ АНИОНОВ:
Fe - феррат
Cu - купрат
Ag - аргентат
Au - аурат
Hg - меркурат
Zn - цинкат
Al - алюминат
12.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХ СОЕДИНЕНИЙNa+2[Zn+2 (OH)-4]
гидроксо
цинкат
тетра натрия
[Cr+3(H2O)06] Cl-3
хлорид
гексааква xрома (III)
K+2 [Hg+2 I- 4]
тетрайодомеркурат (II) калия
13.
НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯNa3[AlF6]
Гексафтороалюминат натрия
Na[Al(OH)4]
Тетрагидроксоалюминат натрия
K4[Fe(CN)6]
Гексационоферрат (II) калия
14.
НАЗОВИТЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ[Cu(NH3)4]SO4
Сульфат тетраамминмеди (II)
[Ag(NH3)2]Cl
Хлорид диамминсеребра
[Cr(H2O)6]Cl3
Хлорид гексааквахрома (III)
15.
СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВГексахлороплатинат (IV) калия
Ответ: K2[PtCl6]
Гексагидроксохромат (III) натрия
Ответ: Na3[Cr(OH)6]
16. ХИМИЧЕСКИЕ СВОЙСТВА
• 1. Диссоциация комплексных соединений[Cu(NH3)4]SO4 ↔ [Cu(NH3)4]2+ + SO42комплексный ион
внешн. среды
ион
17. Практическое применение комплексных соединений
• 1) в аналитической химии для определениямногих ионов
• 2) для разделения некоторых металлов
• 3) для получения металлов высокой степени
чистоты (золота, серебра, никеля и др.)
• 4) в качестве красителей
• 5) для устранения жесткости воды
















 Химия
Химия








