Похожие презентации:
Комплексные соединения
1.
NN
Mg
N
О
О
N
О
О
O
2.
Сформировать представления осоставе, строении, свойствах и
номенклатуре комплексных
соединений;
развить навыки определения
степени окисления у
комплексообразователя.
3.
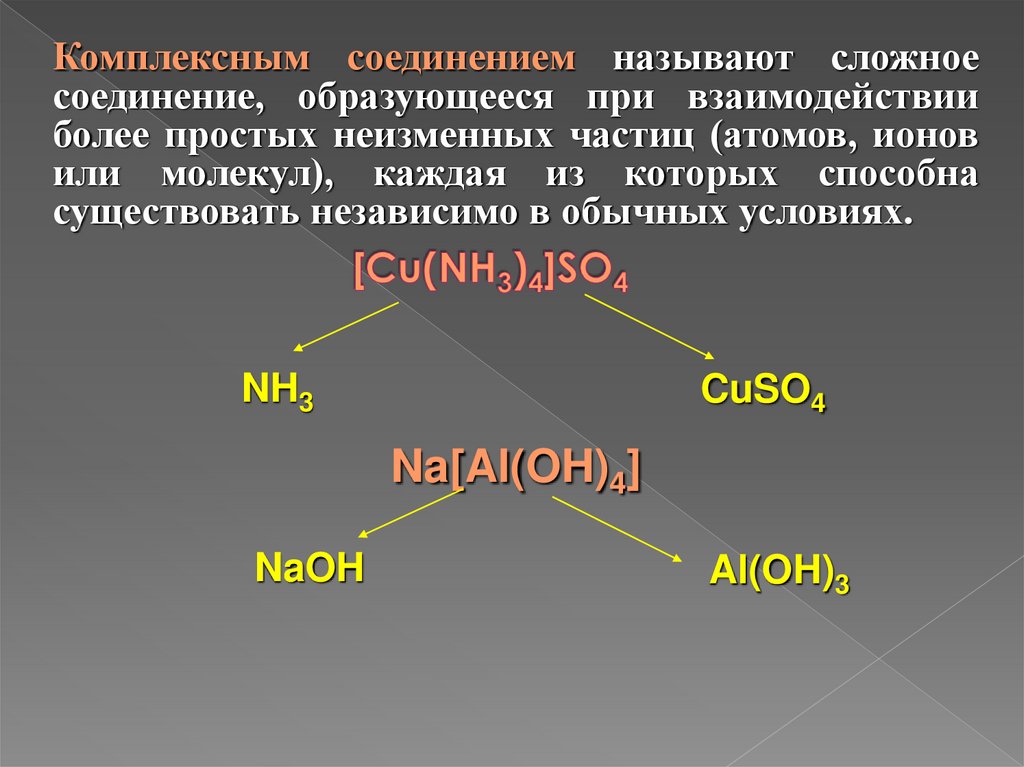
Комплексным соединением называют сложноесоединение, образующееся при взаимодействии
более простых неизменных частиц (атомов, ионов
или молекул), каждая из которых способна
существовать независимо в обычных условиях.
NH3
CuSO4
Na[Al(OH)4]
NaOH
Al(OH)3
4.
Предложена в 1893 г. швейцарскимхимиком, лауреатом Нобелевской
премии, профессором Цюрихского
университета Альфредом Вернером (1866 – 1919)
и дополненная русскими учёными
Л.А Чугаевым, И.Л.Черняевым и
А.А.Гринбергом.
5.
ЧугаевЛев Александрович
Черняев
Илья Ильич
(1873—1922)
(1893—1966)
6.
1+ +3
K[Fe(CN)
Fe
6]
7.
2.Вокруг комплексообразователя расположены
лиганды – частицы, обладающие
неподеленными электронными парами.
Молекулы:
.. ..
H2O,
.. NH3,
Анионы:
CN-, OH-,
Cl-, Br-, NO2-
8.
3. Координационное число (к.ч.) – количестволигандов, которые может присоединять
комплексообразователь.
Координационное
число – в 2 раза
больше чем С.О.
центрального
иона.
+1 (2)
+2
+2 (4, 6)
+2
[Cu(NH
)
]
3 4
+3 (6, 4)
+4 (8, 6)
9.
4. Комплексообразователь и лигандысоставляют внутреннюю сферу
[Cu(NH3)4]+2
комплекса.
10.
Комплексные соединенияклассифицируют
по заряду комплекса
по виду лигандов
по составу внешней сферы
11.
КатионныеНейтральные
[Cr(H2O)4]3+Cl3
[PtCl4(NH3)2]
Катионно анионные
[Cu(NH3)4]2+[PtCl4]2-
Анионные
K2[PtCl6]2-
12.
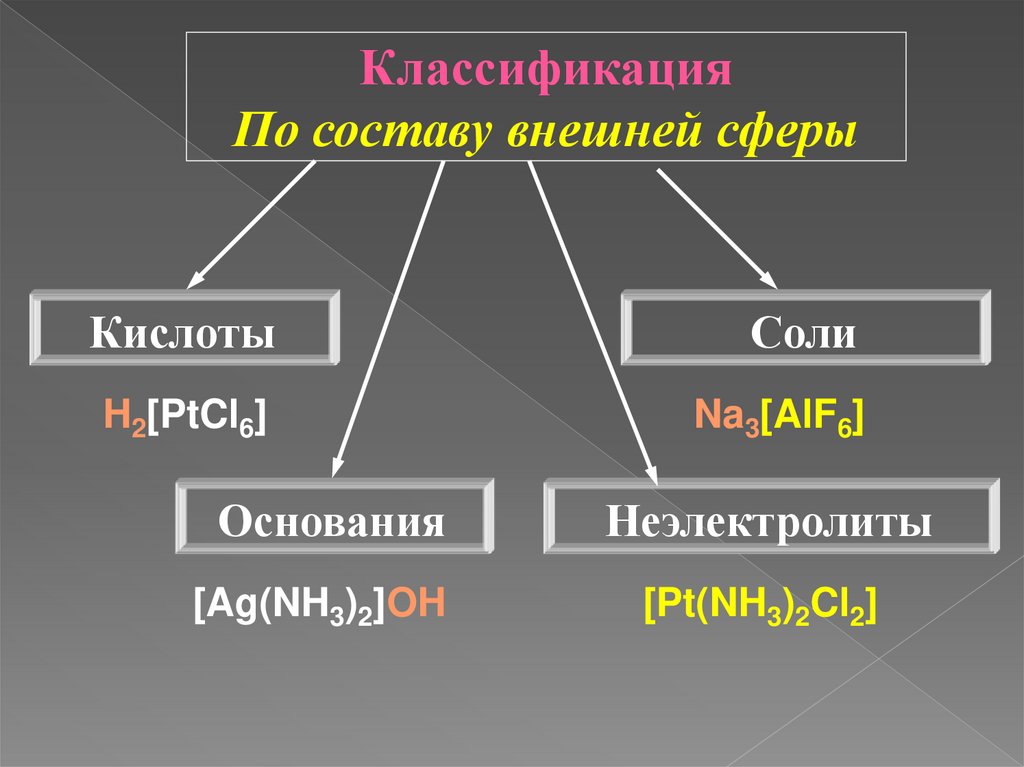
КлассификацияПо составу внешней сферы
Кислоты
Соли
H2[PtCl6]
Na3[AlF6]
Основания
[Ag(NH3)2]OH
Неэлектролиты
[Pt(NH3)2Cl2]
13.
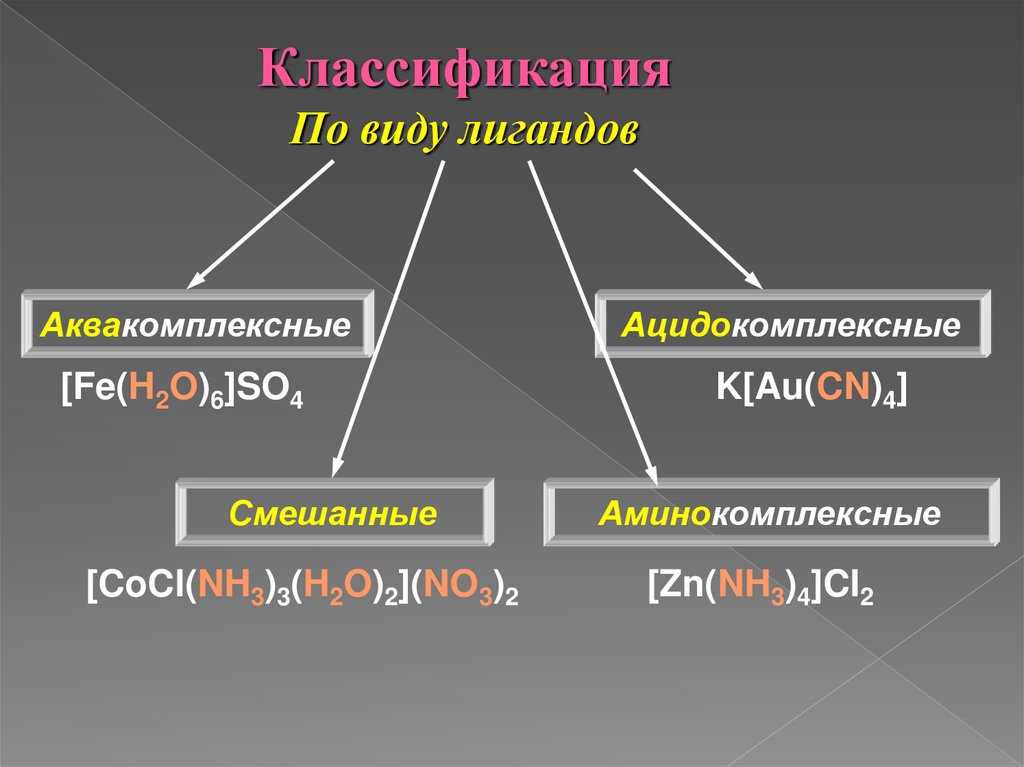
КлассификацияПо виду лигандов
Аквакомплексные
[Fe(H2O)6]SO4
Смешанные
[CoCl(NH3)3(H2O)2](NO3)2
Ацидокомплексные
K[Au(CN)4]
Аминокомплексные
[Zn(NH3)4]Cl2
14.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХСОЕДИНЕНИЙ
ЧИСЛИТЕЛЬНЫЕ:
23-
НАЗВАНИЯ ЛИГАНДОВ:
ди-
H2O – аква-
три-
NH3 – аммин-
4- тетра5- пента6- гекса-
OН- - гидроксо(СN)- - циано(NO2)- - нитроF-, Cl-, Br-, I- - фторо-,
хлоро-, бромо-, йодо-
15.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХСОЕДИНЕНИЙ
НАЗВАНИЯ КОМПЛЕКСНЫХ АНИОНОВ:
+3
Fe - феррат
+2
Cu - купрат
+
Ag - аргентат
+3
Au - аурат
+2
Hg - меркурат
+2
Zn - цинкат
+3
Al - алюминат
От латинского названия
комплексообразователя с
добавлением суффикса
ат
16.
НОМЕНКЛАТУРА КОМПЛЕКСНЫХСОЕДИНЕНИЙ
Na+2[Zn+2 (OH)-4]
тетра натрия
гидроксо
цинкат
[Cr+3(H2O)06] Cl-3
хлорид
гексааква xрома (III)
K+2 [Hg+2 I-4]
тетрайодомеркурат (II) калия
17.
НАЗОВИТЕ КОМПЛЕКСНЫЕСОЕДИНЕНИЯ
Na3[AlF6]
Гексафтороалюминат натрия
Na[Al(OH)4]
Тетрагидроксоалюминат натрия
K4[Fe(CN)6]
Гексационоферрат (II) калия
18.
НАЗОВИТЕ КОМПЛЕКСНЫЕСОЕДИНЕНИЯ
[Cu(NH3)4]SO4
Сульфат тетраамминмеди (II)
[Ag(NH3)2]Cl
Хлорид диамминсеребра
[Cr(H2O)6]Cl3
Хлорид гексааквахрома (III)
19.
СОСТАВЬТЕ ФОРМУЛЫ ВЕЩЕСТВГексахлороплатинат (IV) калия
Ответ: K2 [ PtCl6]
Нитрат гексаакваалюминия
Ответ: [ Аl (H2О)6 ] (NO3)3
Гексагидроксохромат (III) натрия
Ответ: Na3 [Cr (OH)6 ]
Нитрат гексаамминникеля (II)
Ответ: [ Ni (NH3)6] (NO3)2
20.
Комплексные соединенияиспользуются:
-
в аналитической химии
21.
для разделения некоторых металлов иполучения металлов высокой степени чистоты;
-в качестве красителей;
- для устранения жесткости воды;
- в качестве катализаторов важных
биохимических процессов.
- в гальванотехнике;
- в борьбе с коррозией металлов;
- в практике дезактивации;
при производстве веществ с заранее
заданными свойствами в качестве
катализаторов и т.д.
-
22.
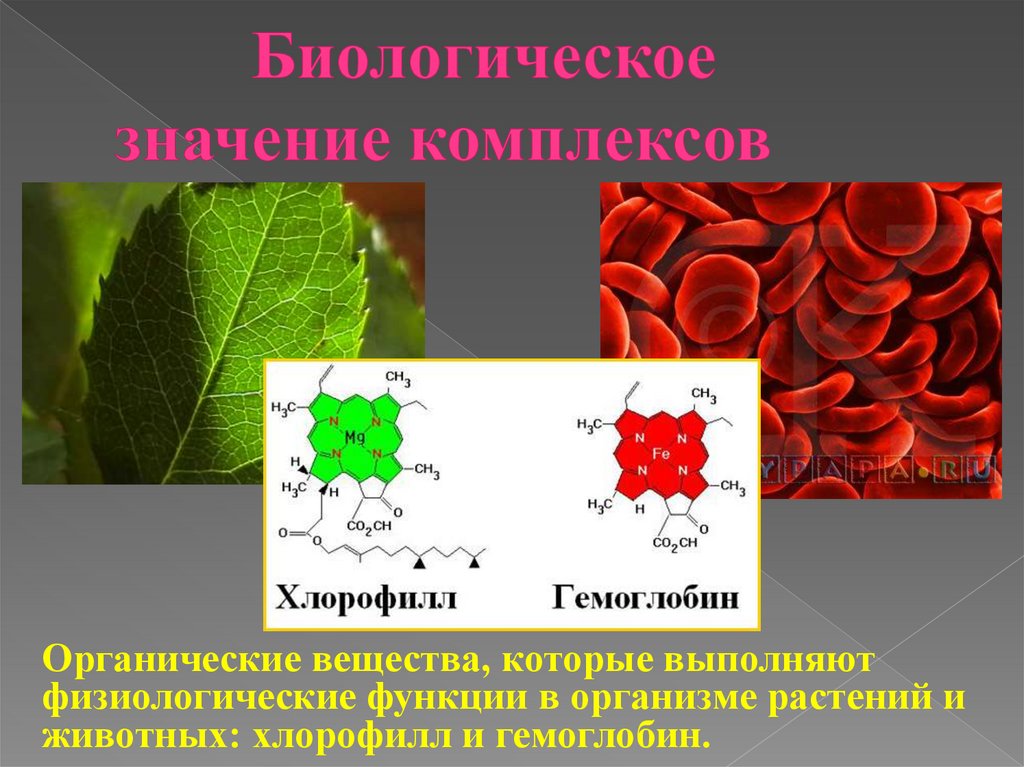
Органические вещества, которые выполняютфизиологические функции в организме растений и
животных: хлорофилл и гемоглобин.


















 Химия
Химия








