Похожие презентации:
Расчеты концентраций жидких лекарственных форм
1. Расчеты концентраций жидких лекарственных форм
2. Медицинские растворы – гомогенные системы, содержащие не менее двух веществ, одним из которых является лекарственное вещество
Растворители:Вода очищенная (ФС.2.2.0020.15)
Неводные растворители:
– летучие (спирт этиловый, эфир медицинский)
– нелетучие (глицерин, жирные и минеральные масла и
т.п.)
Комбинированные (смеси растворителей: этанол с
глицерином, глицерин с димексидом)
Сорастворители – вещества, используемые в составе
комплексных
растворителей
для
повышения
растворимости некоторых трудно растворимых ЛВ
(бензилбензоат – повышение растворимости в маслах,
глицерин, пропиленгликоль – повышение растворимости в
воде).
3.
Большинство растворов готовят растворениемлекарственных веществ в соответствующем
растворителе. Некоторые водные растворы
изготовляют при помощи химических
взаимодействий.
• Стандартизуют растворы
по концентрации действующих веществ
по плотности (ареометр – 20 0С, точность 0,001)
20 t t 20
-поправочный температурный коэффициент (справочная
величина), показывающий изменение плотности при изменении
температуры на 1 0С
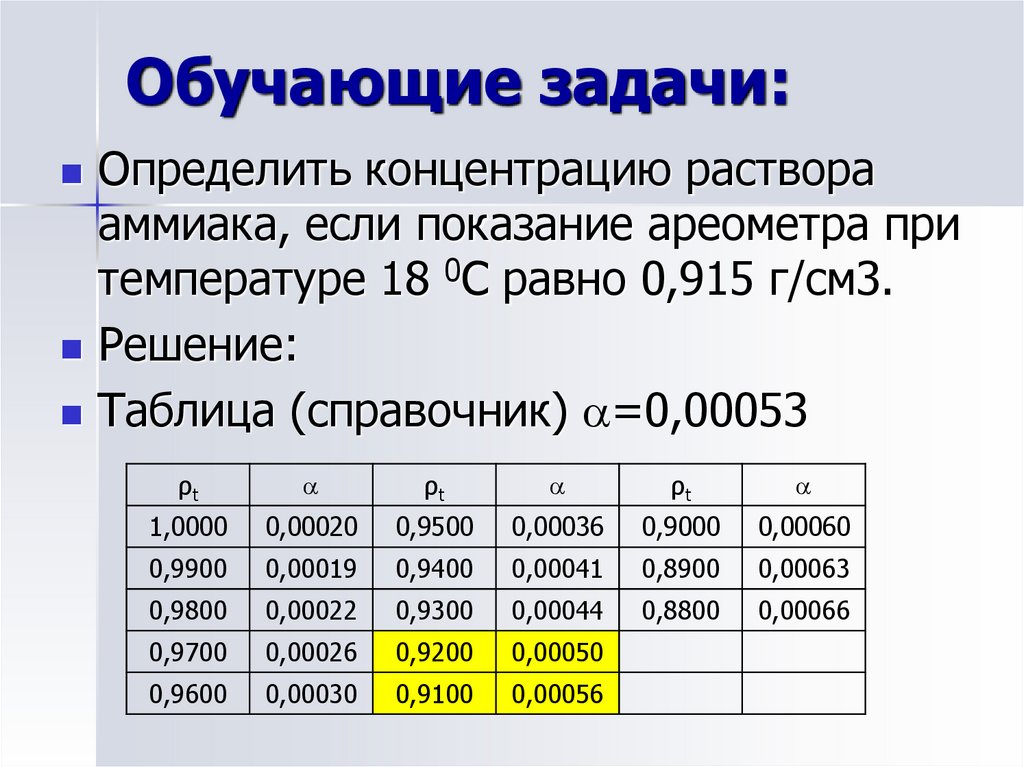
4. Обучающие задачи:
Определить концентрацию растворааммиака, если показание ареометра при
температуре 18 0С равно 0,915 г/см3.
Решение:
Таблица (справочник) =0,00053
ρt
ρt
ρt
1,0000
0,00020
0,9500
0,00036
0,9000
0,00060
0,9900
0,00019
0,9400
0,00041
0,8900
0,00063
0,9800
0,00022
0,9300
0,00044
0,8800
0,00066
0,9700
0,00026
0,9200
0,00050
0,9600
0,00030
0,9100
0,00056
5. Обучающие задачи:
Расчет плотности раствора аммиака при 20 0С
20 t t 20 0,915 0,00053 2 0,9139
По таблице плотностей
• 0,9164 г/см3 - 22%
• 0,9131 г/см3 - 23%
• т.е. 1%
- 0,0033 г/см3
х
- 0,0008
с=23%-0,24%=22,76%
х=0,24%
Ответ: концентрация раствора аммиака 22,76%
6. Самостоятельно на занятии:
Показание ареометра при 15 0С всоляной кислоте 1,090. Чему равна
концентрация кислоты?
Справочные данные:
ρt
ρt
ρt
1,0000
0,00021
1,0600
0,00036
0,1200
0,00052
1,0200
0,00026
1,0800
0,00041
1,1400
0,00053
1,0400
0,00031
1,1000
0,00046
1,1600
0,00064
1,1800
0,00070
температурная поправка равна 0,000435
7.
Лесина Ю.А.Ответ: плотность при 20 0С 1,0878, концентрация 18,0 %
7
8.
ЖЛФ могут быть изготовлены в :Концентрации по массе, которая
показывает какое
количество килограммов (или г) ЛВ содержится в
100 кг (или г) раствора.
Концентрации по объему, которая показывает,
какое количество литров (или мл) ЛВ содержится в
100 л (или мл) раствора при 20 градусах Цельсия.
Массо-объемная концентрация, которая
показывает, какое количество килограммов (или
граммов) ЛВ содержится в 100 л (или мл) раствора
при 20 градусах Цельсия.
9. Укрепление и разбавление растворов
x – необходимое количество крепкого раствора(кг, л)
y –
количество разбавителя (кг, л)
m, V – количество или объем раствора требуемой
концентрации (кг, л)
а – концентрация крепкого раствора (%масс, %об.)
b – требуемая концентрация (% масс, %об.)
с – концентрация слабого раствора (% масс, %об.)
а>b>c
Лесина Ю.А.
9
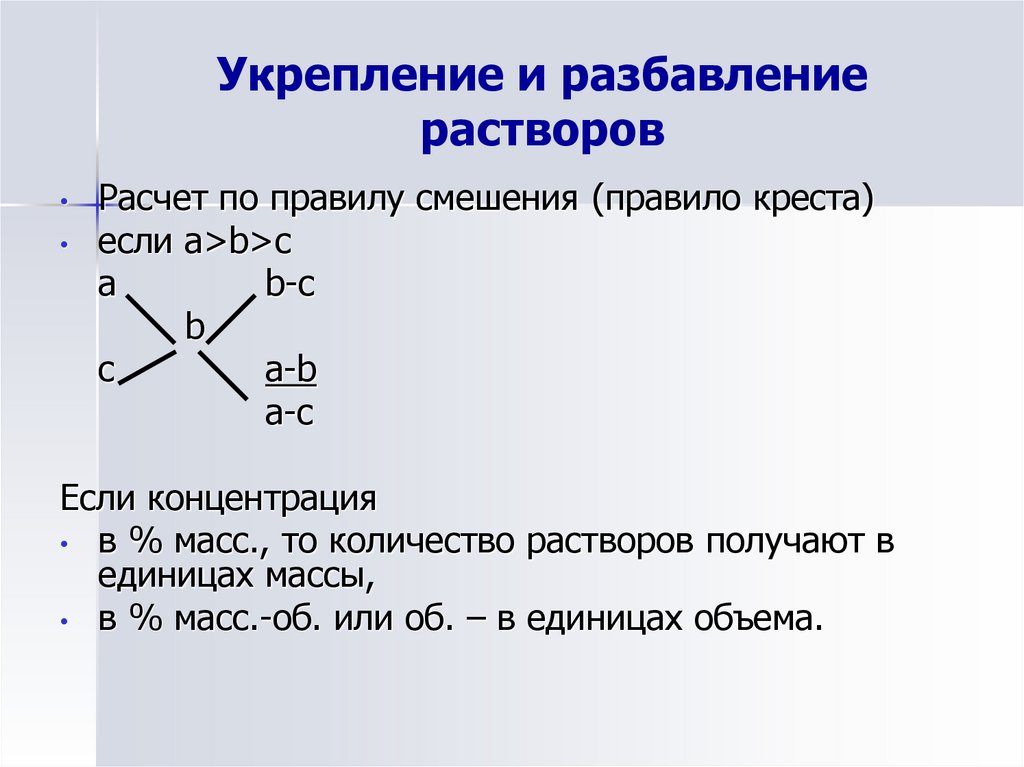
10. Укрепление и разбавление растворов
Расчет по правилу смешения (правило креста)
если а>b>c
a
b-c
b
c
a-b
a-c
Если концентрация
• в % масс., то количество растворов получают в
единицах массы,
• в % масс.-об. или об. – в единицах объема.
11. Укрепление и разбавление растворов
Расчет разбавления• по массе
или
объему:
b Если разбавителем является растворитель
b
х m
х V
a
a
b с
х m
a с
y m x
Если разбавителем является
раствор с меньшей концентрацией
b с
х V
a с
y V x
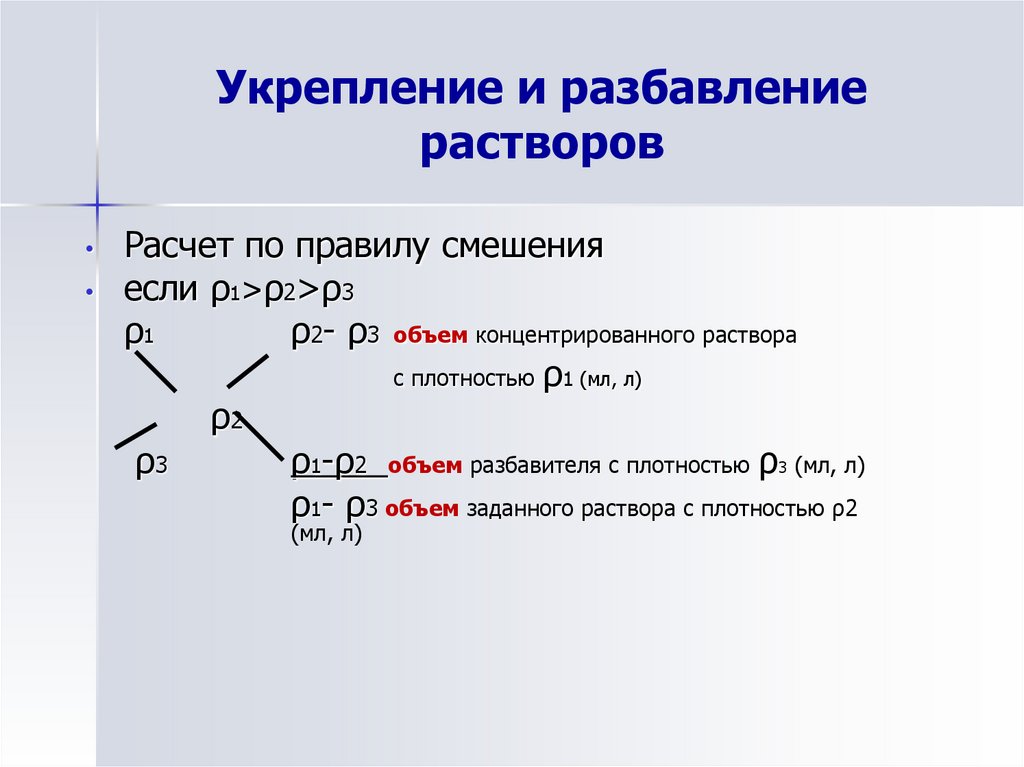
12. Укрепление и разбавление растворов
Расчет по правилу смешения
если ρ1>ρ2>ρ3
ρ1
ρ2- ρ3 объем концентрированного раствора
с плотностью ρ1 (мл, л)
ρ2
ρ3
ρ1-ρ2 объем разбавителя с плотностью ρ3 (мл, л)
ρ1- ρ3 объем заданного раствора с плотностью ρ2
(мл, л)
13. Обучающие задачи:
Сколько нужно взять 18,0 % солянойкислоты для приготовления 3,6 кг 8,3%
раствора?
Решение по правилу смешения:
18,0%
8,3 кг масса 18% раствора
8,3%
0%
9,7 кг
масса разбавителя (вода)
18,0 кг масса разбавленного
раствора
14. Обучающие задачи:
Составляем пропорцию:18,0 кг содержат 8,3 кг 18% НСl
3,6 кг х кг
х=3,6 8,3/18,0=1,66 кг
Ответ: 1,66 кг 18,0 % соляной
кислоты необходимо для
приготовления 3,6 кг 8,3%
раствора.
15. Обучающие задачи:
Сколько нужно взять 18,0% солянойкислоты для приготовления 3,6 кг
8,3% раствора?
Решение расчет по массе:
b
8,3
х m 3,6
1,66кг
a
18
16. Разбавление водно-спиртовых растворов
Разбавление водноспиртовых растворовКонцентрация этанола выражается в объемных
процентах (%) и в процентах по массе (%масс.).
Если нет специального обозначения,
подразумеваются объемные проценты.
В производственных условиях этанол (96,296,7%) разводят по массе (контракция!!!), для
чего объемную концентрацию этанола
переводят в проценты по массе
(Алкоголеметрическая таблица 1, ГФ XI,
стр.303-314) и проводят расчет по формуле
или правилу смешения.
17.
При смешивании спирта и водысохраняется закон сохранения массы, но
объем смеси не равен сумме объемов
спирта и воды. Явление уменьшения
объема (сжатие) называется
КОНТРАКЦИЕЙ.
Например: 60 л абсолютного
(безводного) спирта и 40 л воды дают
не 100 л раствора, а 96,64 л.
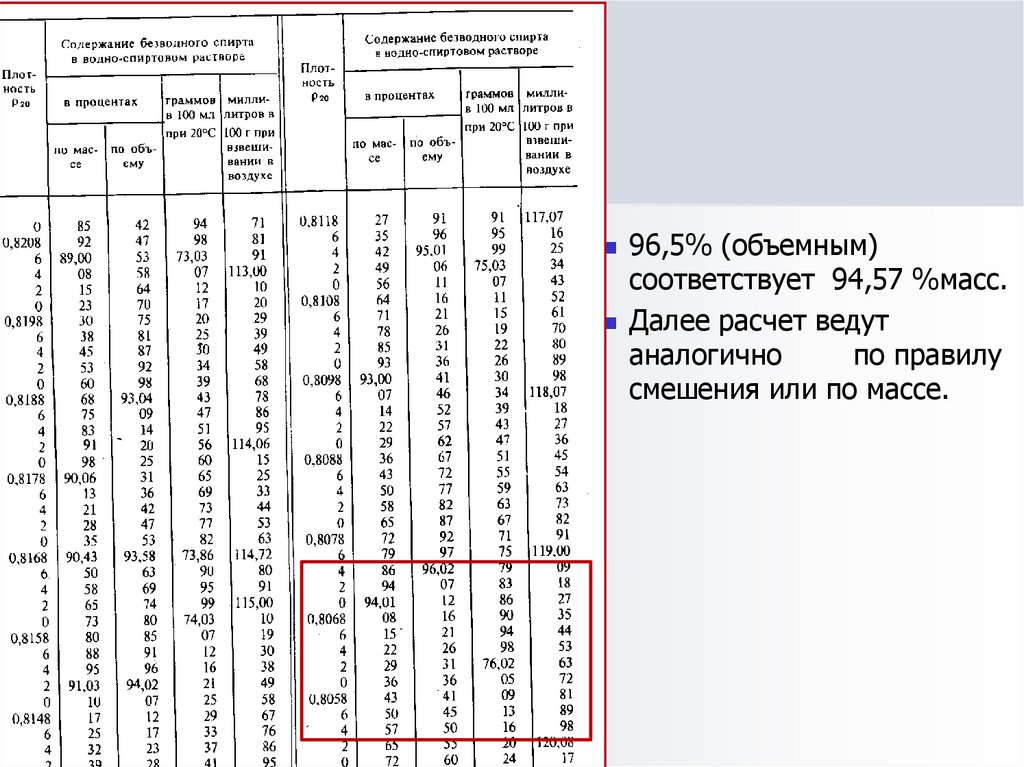
18.
96,5% (объемным)соответствует 94,57 %масс.
Далее расчет ведут
аналогично
по правилу
смешения или по массе.
19. Обучающие задачи (самостоятельное решение на занятии):
Сколько потребуется 96,5 % этанола и воды, чтобыприготовить 60 кг 70% этанола?
Получено 240 мл раствора основного ацетата алюминия
плотностью 1,050 г/см3. Сколько нужно добавить воды, чтобы
получить препарат плотностью 1,048 г/см3?
Какое количество раствора ацетата алюминия с плотностью
1,052 г/см3 потребуется для укрепления 2 кг раствора
основного ацетата алюминия плотностью 1,040 г/см3, чтобы
получить раствор плотностью 1,048 г/см3?
Сколько следует взять раствора основного ацетата свинца
плотностью 1,330 г/см3, чтобы получить 3 кг раствора
плотностью 1,230 г/см3?















 Медицина
Медицина








