Похожие презентации:
Обмен белков-2
1. КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМИИ
Лекция по теме:«Обмен белков–2»
Краснодар
2009
2.
РЕГУЛЯЦИЯ ПРОЦЕССОВПЕРЕВАРИВАНИЯ БЕЛКОВ
ГОРМОН
ГАСТРИН
ЭНТЕРОГАСТРОН
СЕКРЕТИН
МЕСТО
ВЫРАБОТКИ
ПИЛОРИЧЕСКАЯ
ЧАСТЬ ЖЕЛУДКА
12-ПЕРСТНАЯ
КИШКА
12-ПЕРСТНАЯ
КИШКА, ТОЩАЯ
ХОЛЕЦИСТОКИНИН
ТОНКИЙ
КИШЕЧНИК
ВАЗОАКТИВНЫЙ
ИНТЕСТЕНАЛЬНЫЙ ПЕПТИД
(ВИП)
ПАНКРЕОТИЧЕС КИЙ ПОЛИПЕПТИД
(ПП)
ТОНКИЙ
КИШЕЧНИК
ТОНКИЙ
КИШЕЧНИК
БИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ
УСИЛИВАЕТ СИНТЕЗ СОЛЯНОЙ
КИСЛОТЫ
ТОРМОЗИТ ВЫРАБОТКУ НСI И
ПЕПСИНА
УСИЛИВАЕТ СИНТЕЗ
БИКАРБОНАТОВ И ЖИДКОЙ
ЧАСТИ ПАНКРЕАТИЧЕСКОГО
СОКА
УСИЛИВАЕТ СИНТЕЗ
ПАНКРЕОТИЧЕСКИХ
ФЕРМЕНТОВ
СТИМУЛИРУЕТ СИНТЕЗ
БИКАРБОНАТОВ ВЫРАБОТКУ
ЖЕЛЧИ, ТОРМОЗИТ ДЕЯТЕЛЬНОСТЬ ЖЕЛУДОЧНЫХ ЖЕЛЕЗ
ТОРМОЗИТ ВЫРАБОТКУ ПАНКРЕАТИЧЕСКИХ
ФЕРМЕНТОВ
3. Катаболизм аминокислот
ОБЩИЕ ПУТИКАТАБОЛИЗМА
СО2
R
ИНДИВИДУАЛЬНЫЕ
ПУТИ
КАТАБОЛИЗМА
СН COOH
NH2
потеря
аминогруппы
- NH3
карбоновые
кислоты
декарбоксилирование
биогенные
амины
нии
м
а
дез вание
ро
- NH2
п ер
еа
ров миниани
е
-кетокислоты
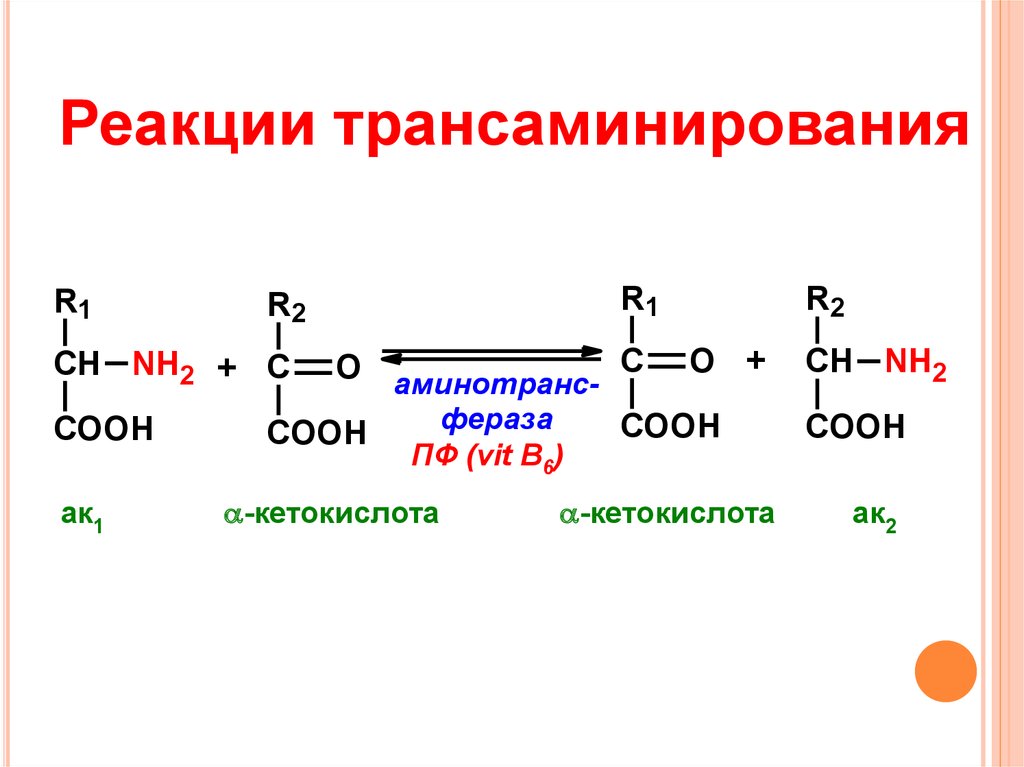
4. Реакции трансаминирования
R1R1
R2
O аминотранс- С O +
фераза
COOH
COOH
R2
СН NH2 + С
СН NH2
COOH
COOH
ак1
ПФ (vit B6)
-кетокислота
-кетокислота
ак2
5. Реакции трансаминирования
6. Присоединение ПФ к активному центру аминотрансферазы
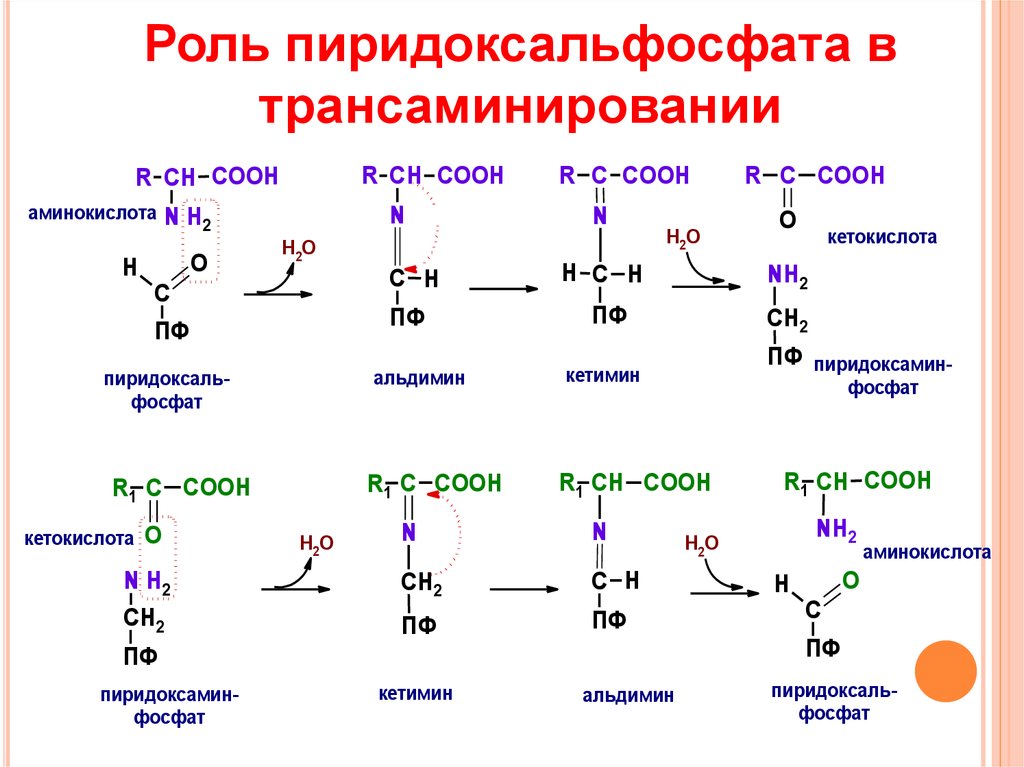
7. Роль пиридоксальфосфата в трансаминировании
R СН COOHR СН COOH
аминокислота
H
N Н2
O
N
Н2О
С
ПФ
ПФ
СН2
С H
СН2
ПФ
ПФ
R1 СН COOH
NН2
Н2О
H
аминокислота
O
С
ПФ
ПФ
кетимин
фосфат
R1 СН COOH
СН2
пиридоксаминфосфат
ПФ пиридоксамин-
кетимин
N Н2
Н2О
кетокислота
ПФ
N
O
O
NН2
N
кетокислота
Н2О
H С H
R1 С COOH
R1 С COOH
N
R С COOH
С H
альдимин
пиридоксальфосфат
R С COOH
альдимин
пиридоксальфосфат
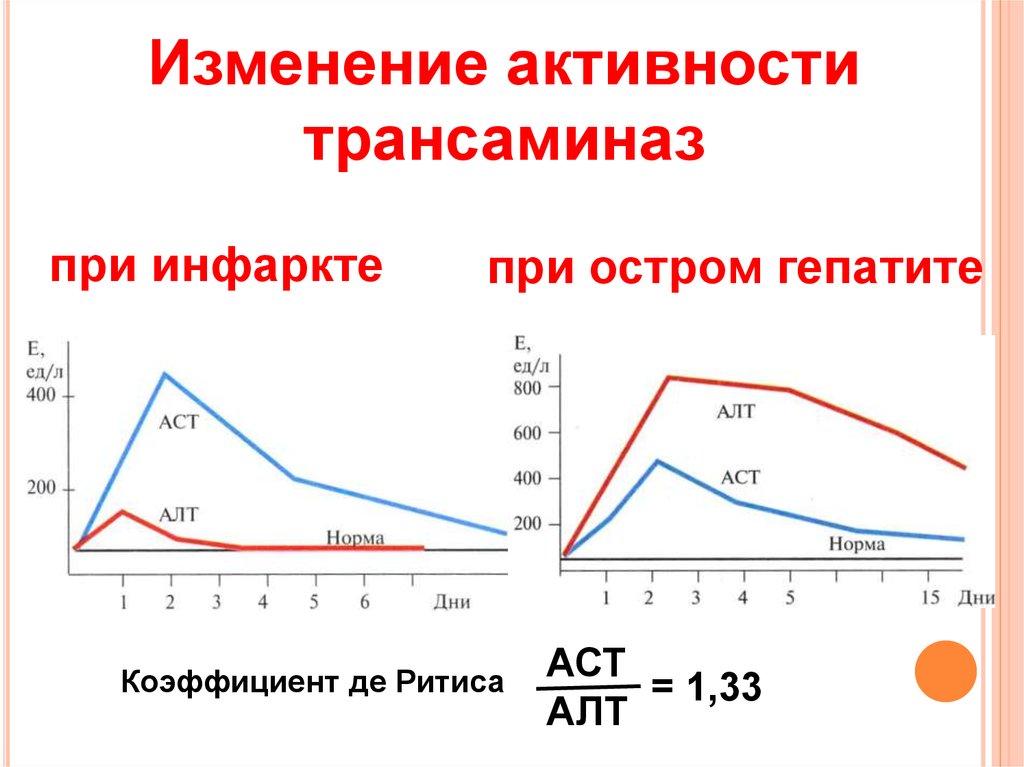
8. Изменение активности трансаминаз
при инфарктепри остром гепатите
Коэффициент де Ритиса
АСТ
= 1,33
АЛТ
9. Типы реакций дезаминирования
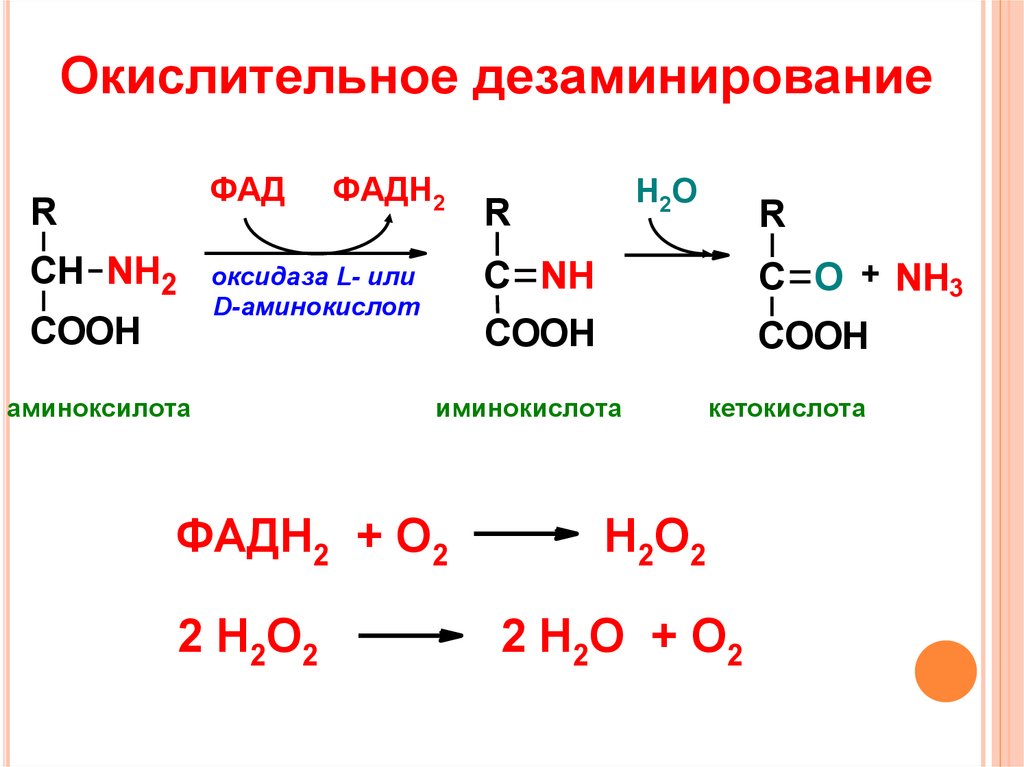
10. Окислительное дезаминирование
ФАДR
СН NH2
COOH
ФАДН2
оксидаза L- или
D-аминокислот
аминоксилота
R
R
С NH
С O + NH3
COOH
COOH
иминокислота
ФАДН2 + О2
2 Н2О2
Н2О
кетокислота
Н2О2
2 Н2О + О2
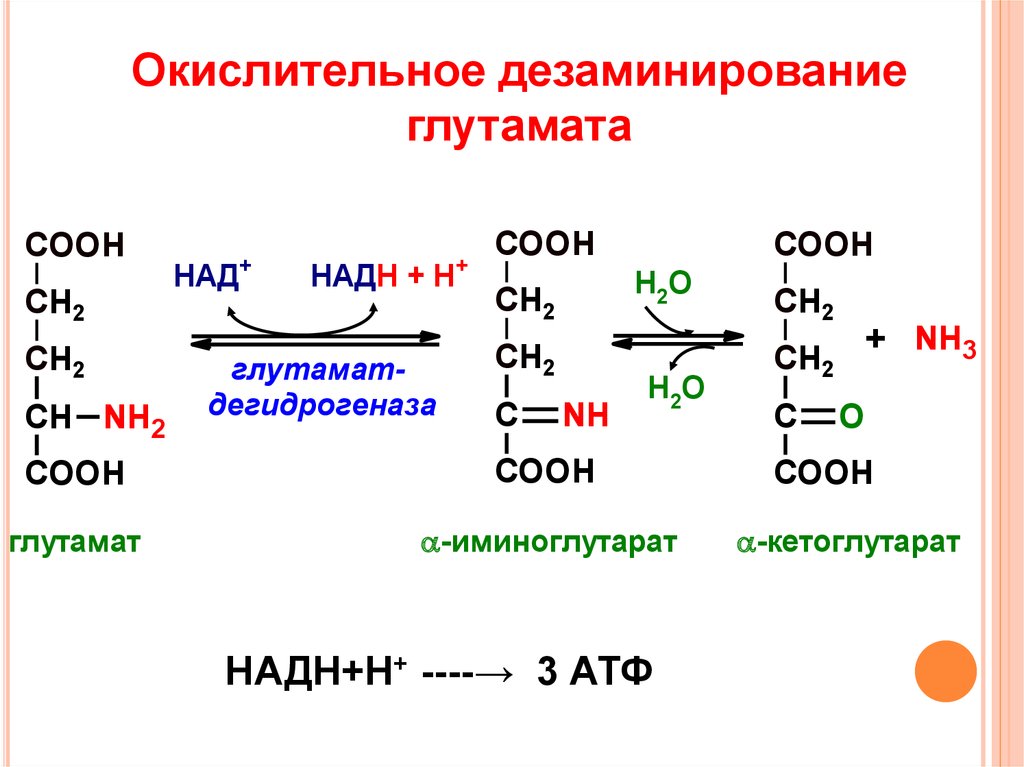
11. Окислительное дезаминирование глутамата
COOHCH2
CH2
СН NH2
COOH
глутамат
+
НАД
НАДН + Н
глутаматдегидрогеназа
+
COOH
Н2О
CH2
CH2
С
COOH
NH
Н2О
COOH
-иминоглутарат
НАДН+Н+ ----→ 3 АТФ
CH2
+ NH3
CH2
С
O
COOH
-кетоглутарат
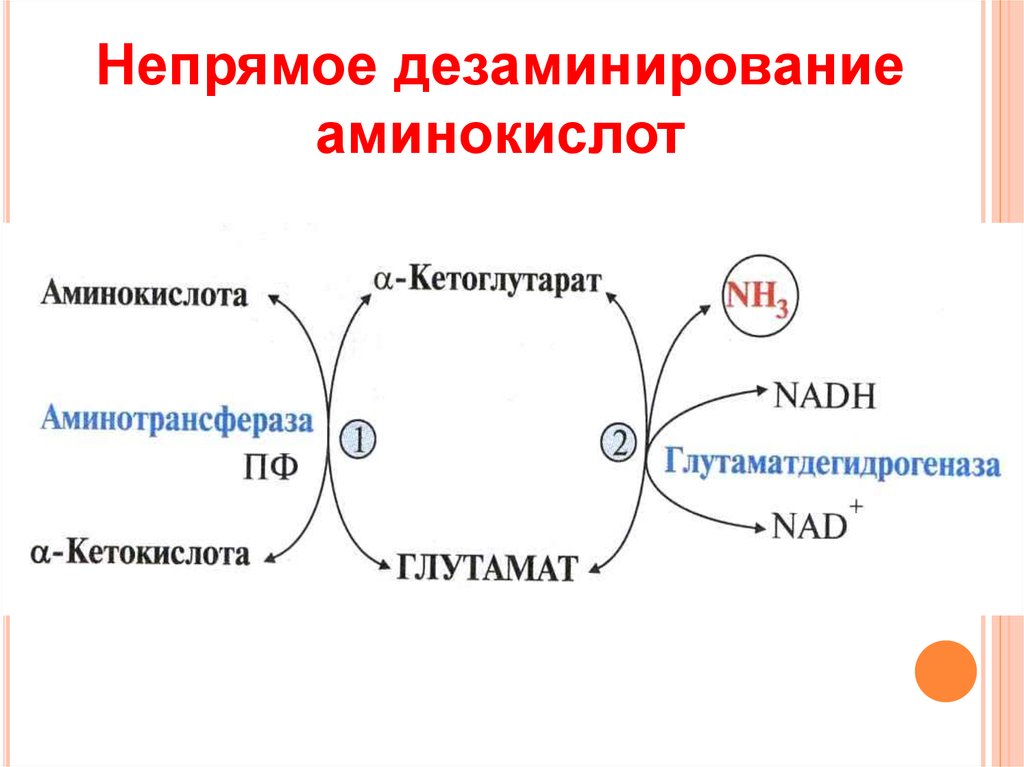
12. Непрямое дезаминирование аминокислот
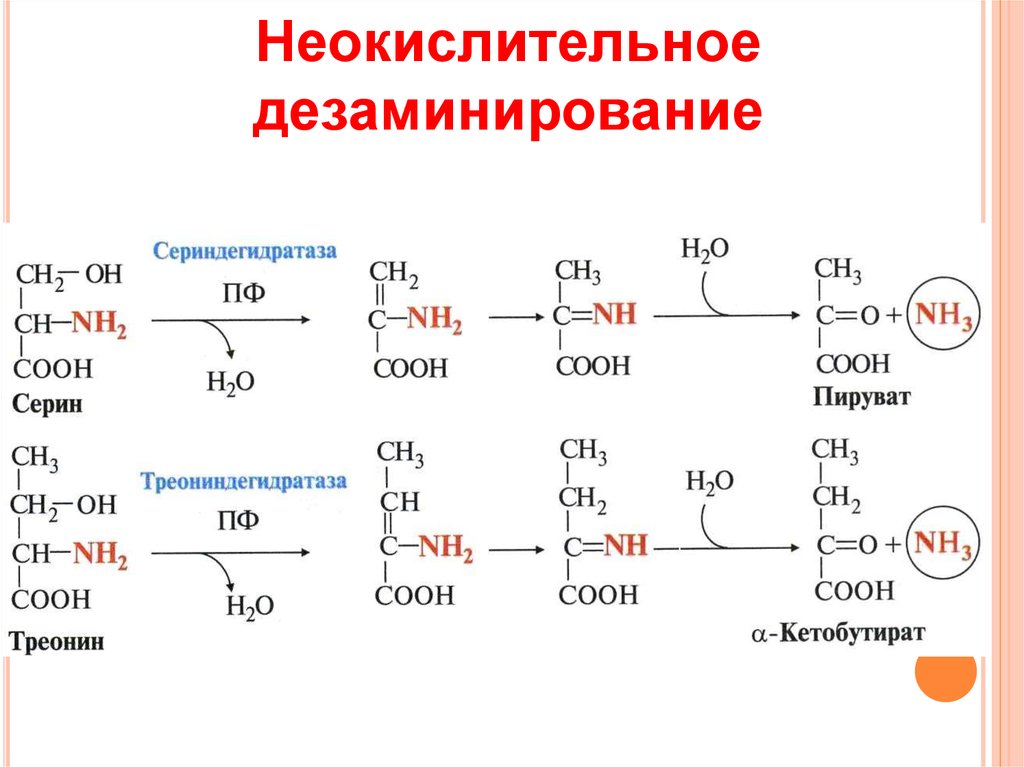
13. Неокислительное дезаминирование
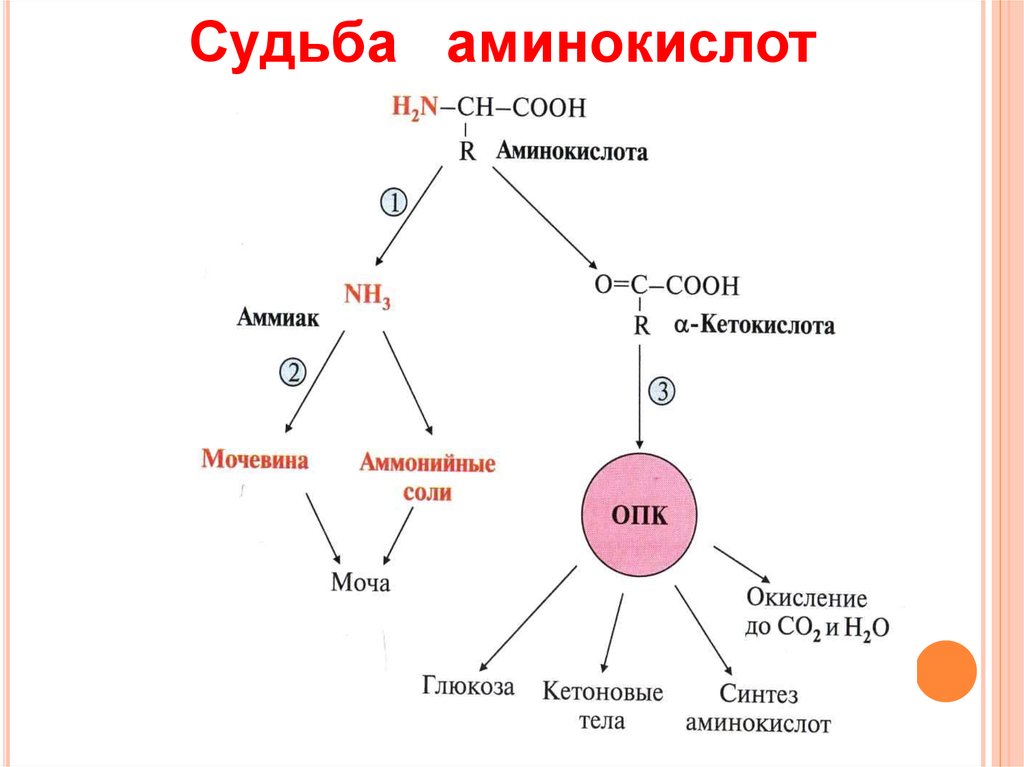
14. Судьба аминокислот
15. Реакции декарбоксилирования
СО2R СН COO H
NH2
декарбоксилаза
ПФ (vit B6)
аминоксилота
COOH
СН2
СН2
СН NH2
COOH
глу
R СН2 NH2
биогенный амин
СО 2
декарбоксилаза
ПФ (vit B6)
COOH
СН2
СН2
СН2 NH2
-аминомасляная к-та
(ГАМК)
16. Декарбоксилирование гетероциклических аминокислот
СН 2N
СН COOH
NH2
NH
гистидин
СО2
СН 2 СН 2
N
гистидиндекарбоксилаза
ПФ (vit B6)
NH2
NH
гистамин
СН 2 СН COOH
NH2
NH
триптофан
1/2 О2
гидроксилаза
СО2
HO
СН 2 СН COOH
NH
NH2
декарбоксилаза
HO
СН 2 СН 2
NH
NH2
ПФ (vit B6)
5-окситриптофан
серотонин
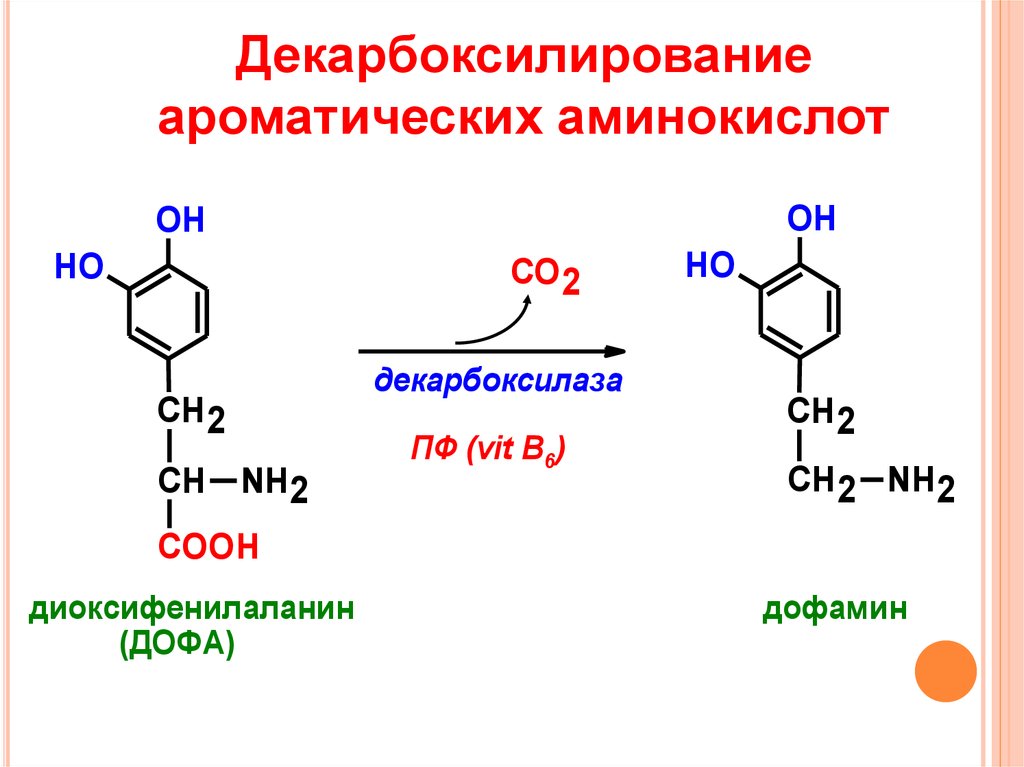
17. Декарбоксилирование ароматических аминокислот
OHOH
СО2
HO
СН 2
СН NH2
декарбоксилаза
ПФ (vit B6)
HO
СН 2
СН 2 NH2
COOH
диоксифенилаланин
(ДОФА)
дофамин
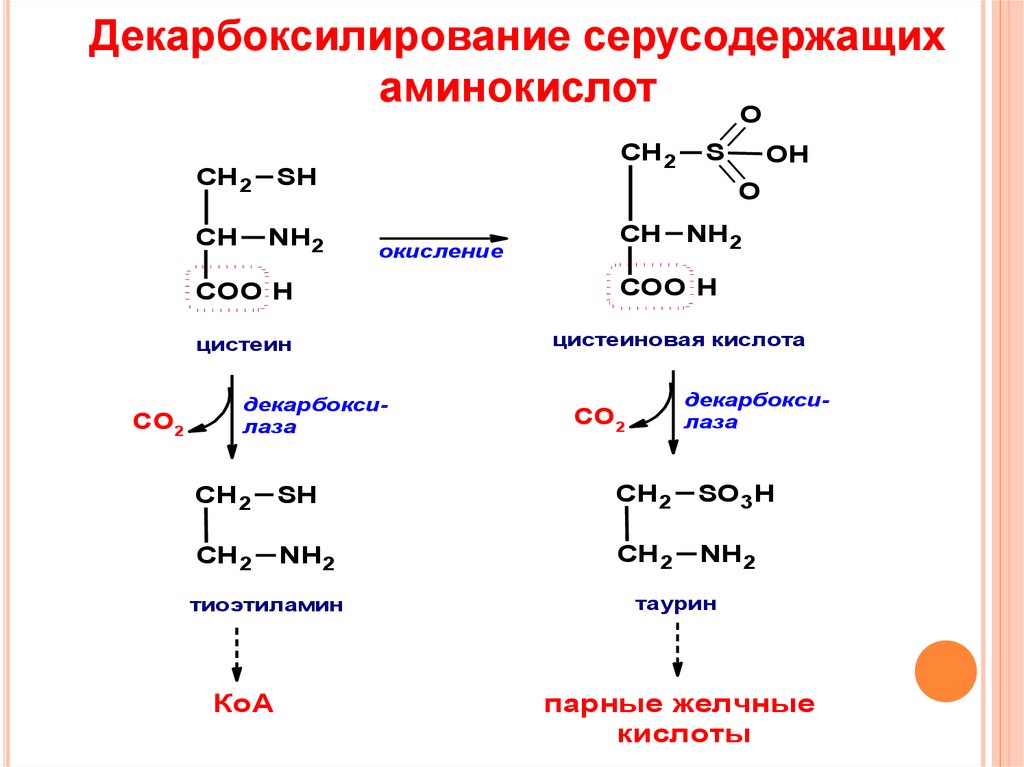
18. Декарбоксилирование серусодержащих аминокислот
OСН 2
СН
СН 2
SH
NH2
OH
O
окисление
COO H
цистеин
СО2
S
декарбоксилаза
СН
NH2
COO H
цистеиновая кислота
декарбоксилаза
СО2
СН 2
SH
СН 2
SO 3H
СН 2
NH2
СН 2
NH2
тиоэтиламин
КоА
таурин
парные желчные
кислоты
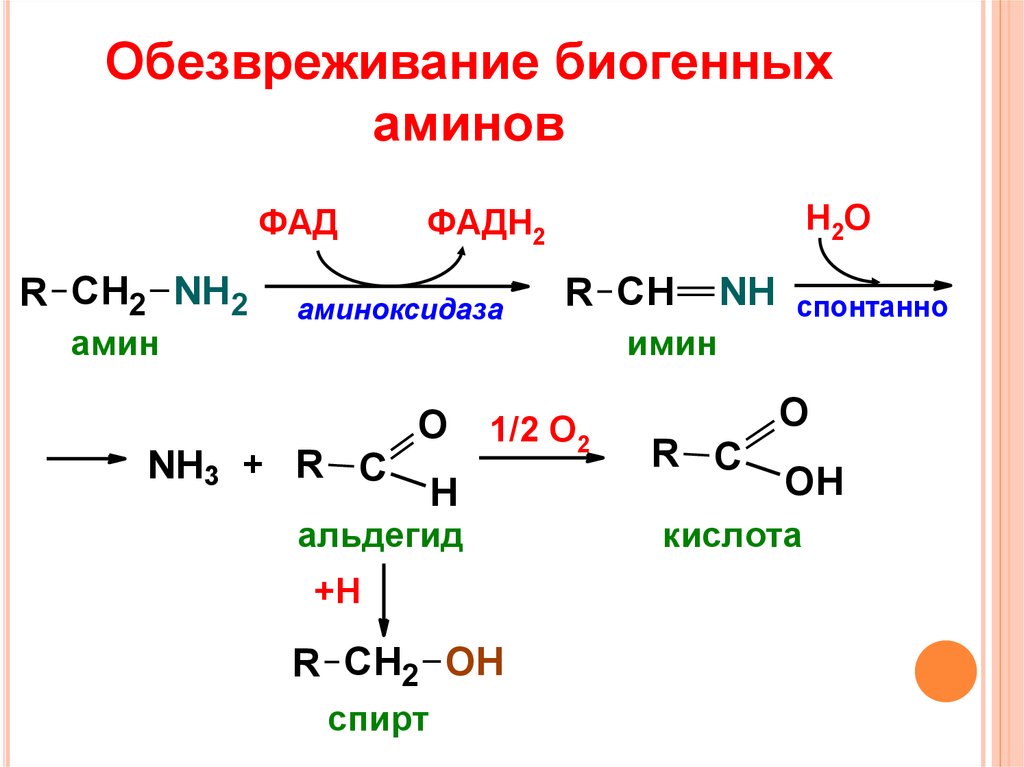
19. Обезвреживание биогенных аминов
ФАДR СН2 NH2
амин
аминоксидаза
NH3 + R С
Н2О
ФАДН2
O
1/2 О2
H
альдегид
+Н
R СН2 OH
спирт
R СН
NH
имин
спонтанно
O
R С
ОН
кислота








 Биология
Биология








