Похожие презентации:
Цикл азота в биосфере
1.
Цикл азота в биосфере2. Промышленное получение аммиака
Фриц Габер, Карл Бош – Нобелевскаяпремия 1918 и 1931 за создание
технологии промышленного получения
аммиака
+5000С, 300-350 атм.
3.
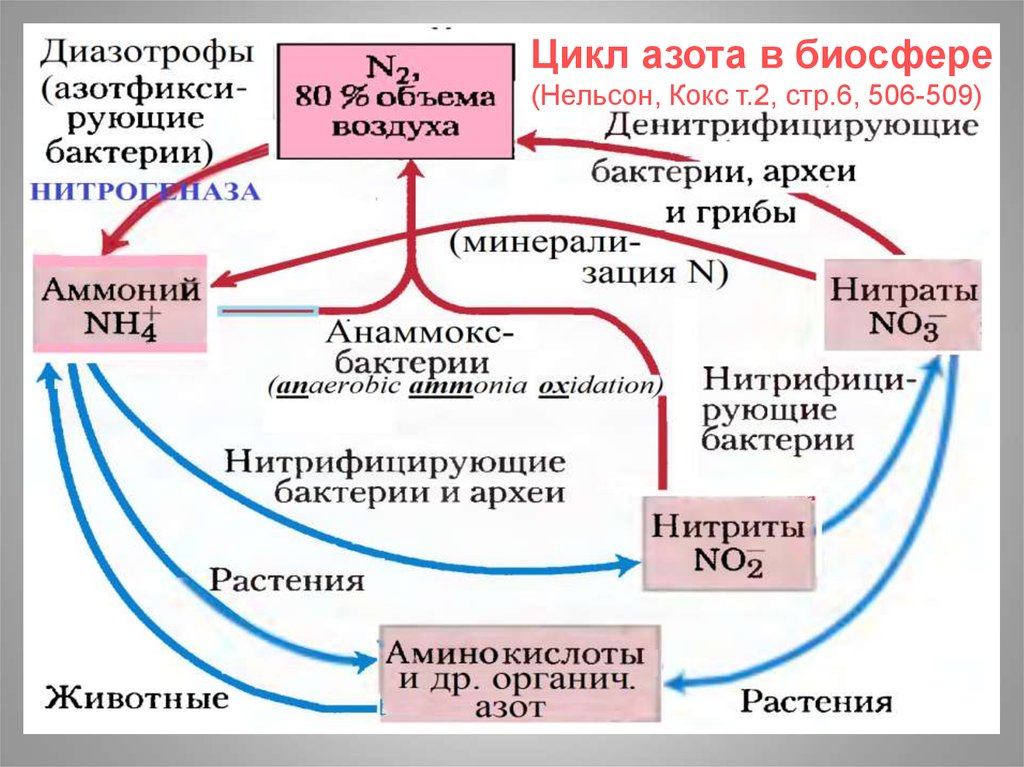
Цикл азота в биосфере(Нельсон, Кокс т.2, стр.6, 506-509)
4.
Биологическая фиксациямолекулярного азота
воздуха
5. Азотофиксирующие организмы НИТРОГЕНАЗА
БАКТЕРИИ - диазотрофы:• - свободноживущие (рр.
Azotobacter, Clostridium, все
фотосинтезирующие, ряд
АРХЕЙ…)
• - в симбиозе или ассоциации
с растениями (рр. Rhizobium,
Azospirillum, Anabaena, Frankia …)
• - в кишечнике животных
(р. Кlebsiella…)
60% N в теле термита –
продукт азотфиксации
бактерий пищеварительного тракта
•Azotobacter
Rhizobium на люпине
6.
7. Нитрогеназный комплекс
• Азоферредоксин (дегидрогеназа(или редуктаза) динитрогеназы,
она же Fe-белок) - димер
• Молибдоферредоксин
(динитрогеназа, FeMo-белок) тетрамер, имеет 2 центра
связывания Fe-белка
У Clostridium, Azotobacter и Anabaena
бывают нитрогеназы, содержащие
ванадий, у Azotobacter, Rhodobacter и
Rhodopseudomonas – содержащие Fe.
8. Кластеры нитрогеназы
9.
10. FeMo-кофактор
• Серый цвет – атомы Fe (7),желтые – S (9), черные – С,
подписан Мо (1), обведен
голубым – недавно
выявленный С.
11. Работа нитрогеназы
У Rhizobium для восстановления1N2 может идти от 12 до 35 АТФ
Побочная реакция при азотфиксации –
восстановление Н+ до Н2.
В результате только 40-60% всего потока е- через
нитрогеназу передается на N2.
12.
13.
(Редуктазадинитрогеназы)
(Динитрогеназа)
14. Работа нитрогеназы
N2 + 8H+ + 8e + 16АТФ→ 2NH3 + H2 + 16АДФ + 16Фн15.
16. Легоглобины – защита от О2
Из люпинаМиоглобин кашалота
17. РАСТЕНИЕ: поглощение и переработка NH4+ из почвы (или от симбионтов)
• 2 типа транспортных систем:если аммония мало – система высокого сродства
(аммонийный транспортер АМТ, антипорт с Н+),
несколько разных АМТ.
если аммония много – система низкого сродства (ионный
канал).
Внутри растения – аминирование, амидирование
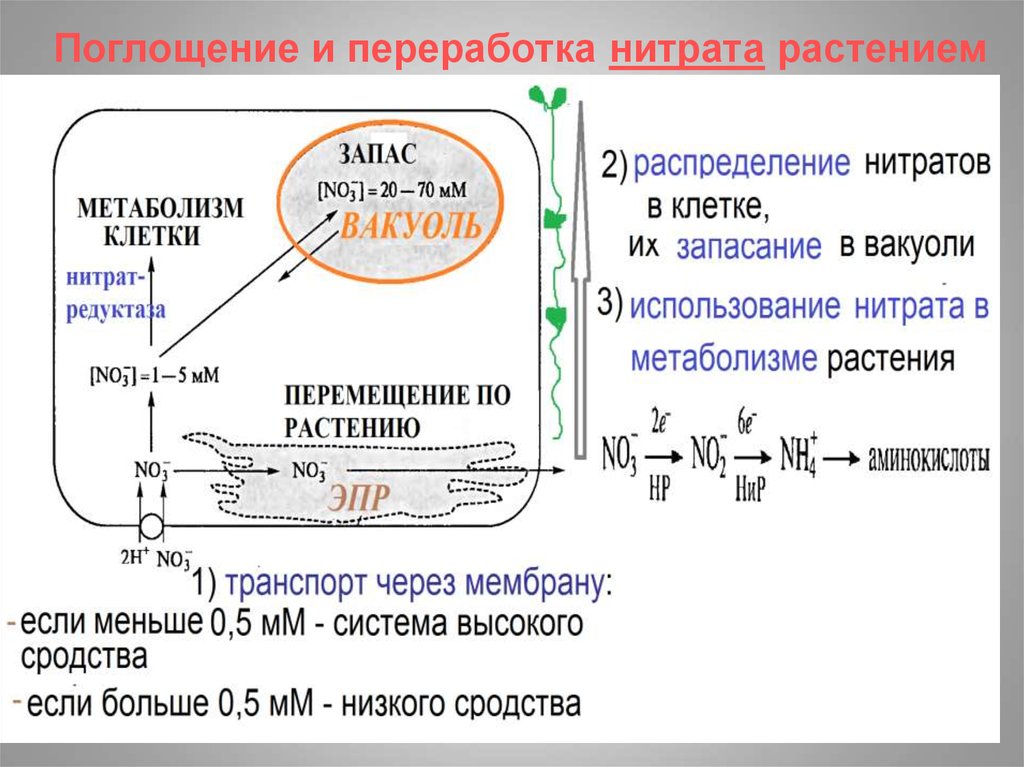
18. Поглощение и переработка нитрата растением
19. Нитратредуктаза КФ 1.6.6.1 – металлофлавопротеин, гомоди- или тетрамер
1 субъединица (на рис.) ~1000 а-к-т+ ФАД + гем (цитохром b5) + молибдоптерин
У высших растений –
в цитозоле.
Есть отдельные центры связывания для НАДН и NO3-
20. Нитритредуктаза КФ 1.7.7.1
• Мономер из 2х доменов.Кофакторы – 2 FeSцентра и сирогем
Фд – белок ферредоксин в
окисленном или восстановленном
состоянии
21.
нитраты и нитритыРекомендации ВОЗ - в сутки не более 3,7 мг
нитратов на 1 кг массы тела, нитритов – 0,2
мг на кг (именно по аниону),
250 мг нитратов, безопасных для условного
едока массой в 70 кг = 350 мг NaNO3
Нормы в Германии 50-100 мг в сутки,
в большинстве стран СНГ – 300-320 мг
в США – 400-500 мг.
22. Типы токсического воздействия на организм человека
Взрослые: Острое отравление 1–4 г,ТОКСИЧНОСТЬ
смерть 8 -14 г
• Первичная - самого нитрат-иона;
• Вторичная - нитрит-иона,
• Третичная – действие нитрозаминов,
образовавшихся из нитритов.
• Кроме того, при метаболизме нитратов
в организме возникает NO,
обладающий сигнальным действием.
23.
24.
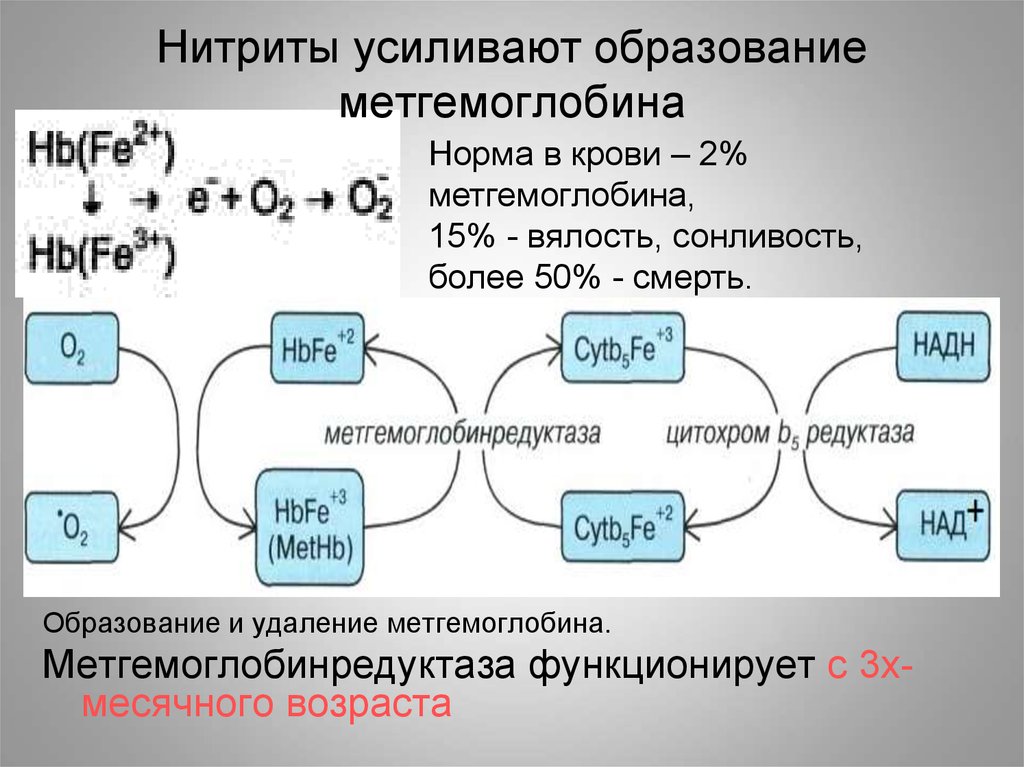
25. Нитриты усиливают образование метгемоглобина
Норма в крови – 2%метгемоглобина,
15% - вялость, сонливость,
более 50% - смерть.
Образование и удаление метгемоглобина.
Метгемоглобинредуктаза функционирует с 3хмесячного возраста
26. Нитрозамины и их образование
• Нитрозамины – это соединения сгруппировкой =N-N=O
Например, нитрит-ион в водной среде даст
азотистую кислоту. Она при
взаимодействии с аминами может дать
нитрозамин.
НNO2 + (C2H5)2NH =>
=>(C2H5)2N-N=O + N2 + H2O
27. Нитрозамины нарушают ДНК
28.
Уровень накопления нитратов в овощахCодержание
нитратов
Низкое 10150 мг/кг
Среднее
150-700
мг/кг
Высокое
700-1500
мг/кг
Виды овощных культур
Горох, томаты, сладкий стручковый перец, чеснок, картофель,
репчатый лук, поздняя морковь
Огурцы, поздняя белокочанная капуста, зеленый лук в
открытом грунте, тыква, кабачки, патиссоны, лук-порей,
щавель, ранняя морковь, корнеплоды петрушки, лук-батун,
цветная капуста (осенью)
Ранняя цветная и белокочанная капуста, столовая свекла,
капуста брокколи, корневой сельдерей, брюква, кольраби,
ревень, репа, хрен, редис и редька в открытом грунте,
зеленый лук в защищенном грунте.
МаксиСалат, пекинская капуста, мангольд (листовая свекла), шпинат,
мальное
укроп, редис в защищенном грунте, листья столовой
1500-4000
мг/кг
свеклы и петрушки, листовой сельдерей.
29. Проблема нитратов в пище
УправлениеРоспотребнадзора по
Нижегородской области, 2018:
превышение по нитратам из
2000 взятых проб – в 12 .
Снято с реализации
несколько партий
плодоовощной продукции
объемом свыше 3 тонн.
Следует приобретать плодоовощную продукцию только в специально оборудованных и
отведенных для этих целей органами местного самоуправления местах уличной
торговли (при этом на вывеске должно быть указано наименование предприятия, его
юридический адрес, ФИО индивидуального предпринимателя, продавец должен
находиться в чистой санитарной одежде и иметь при себе бейджик с указанием ФИО и
личную медицинскую книжку), а также на организованных рынках, ярмарках и в
стационарной торговой сети.
30.
31. Пути синтеза белковых аминокислот
• 1) прямое восстановительное аминирование• 1а) – образование амидов
• 2) переаминирование
• 3) ферментативные превращения
32. Семейства белковых аминокислот по путям синтеза
1) Семейства 1 – 4 (на основе αкетоглутаровой к-ты, ПВК, 3-ФГК и ЩУКсоответственно).
2) Гистидин
3) Семейство 5. Ароматические аминокислоты
(шикиматный путь)
ВНИМАНИЕ! Есть НЕЗАМЕНИМЫЕ аминокислоты – путь синтеза
не равлизуется у данного организма.
33.
Катаболизмаминокислот
34. Катаболизм аминокислот
ОБЩИЕ ПУТИКАТАБОЛИЗМА
СО2
R
ИНДИВИДУАЛЬНЫЕ
ПУТИ
КАТАБОЛИЗМА
СН COOH
биогенные
амины
NH2
потеря
аминогруппы
- NH3
карбоновые
кислоты
декарбоксилирование
нии
м
а
дез вание
ро
- NH2
п ер
еа
ров миниани
е
-кетокислоты
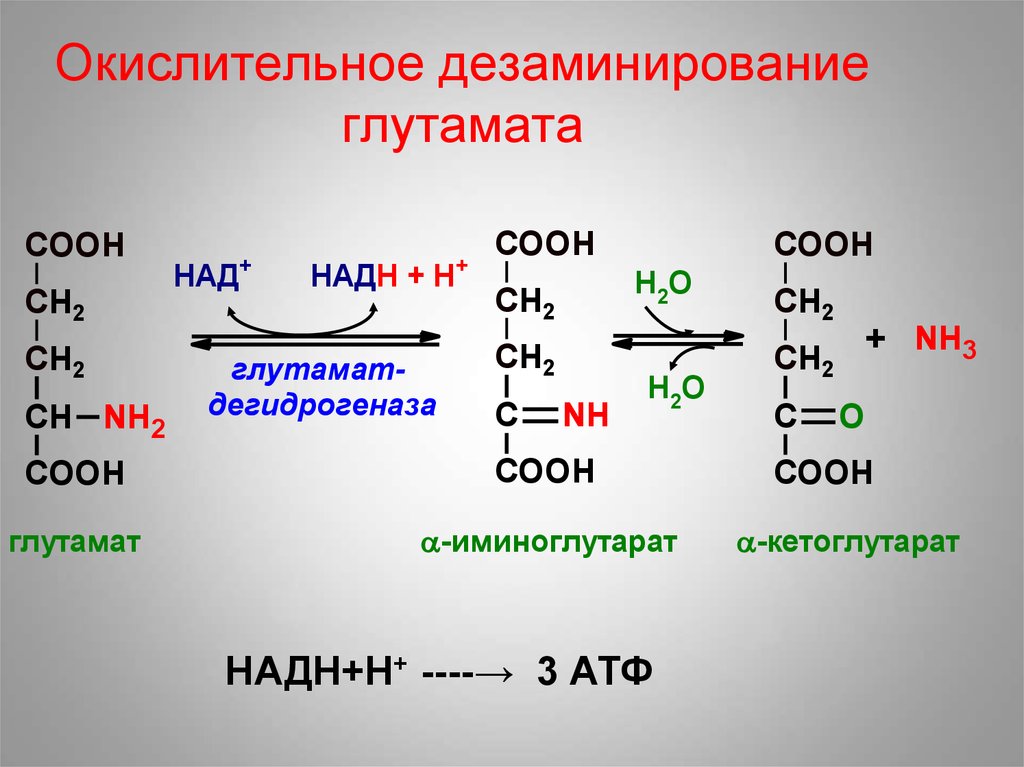
35. Окислительное дезаминирование глутамата
COOHCH2
CH2
СН NH2
COOH
глутамат
+
НАД
НАДН + Н
глутаматдегидрогеназа
+
COOH
Н2О
CH2
CH2
С
COOH
NH
Н2О
COOH
-иминоглутарат
НАДН+Н+ ----→ 3 АТФ
CH2
+ NH3
CH2
С
O
COOH
-кетоглутарат
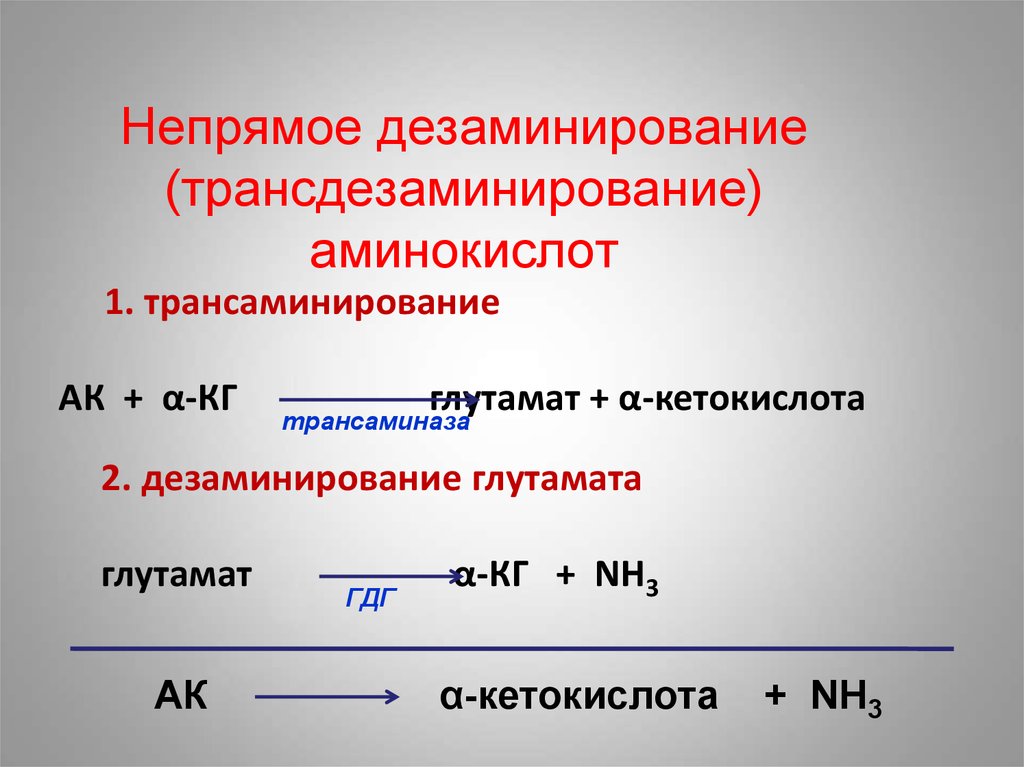
36. Непрямое дезаминирование (трансдезаминирование) аминокислот
1. трансаминированиеАК + α-КГ
глутамат + α-кетокислота
трансаминаза
2. дезаминирование глутамата
глутамат
АК
ГДГ
α-КГ + NH3
α-кетокислота
+ NH3
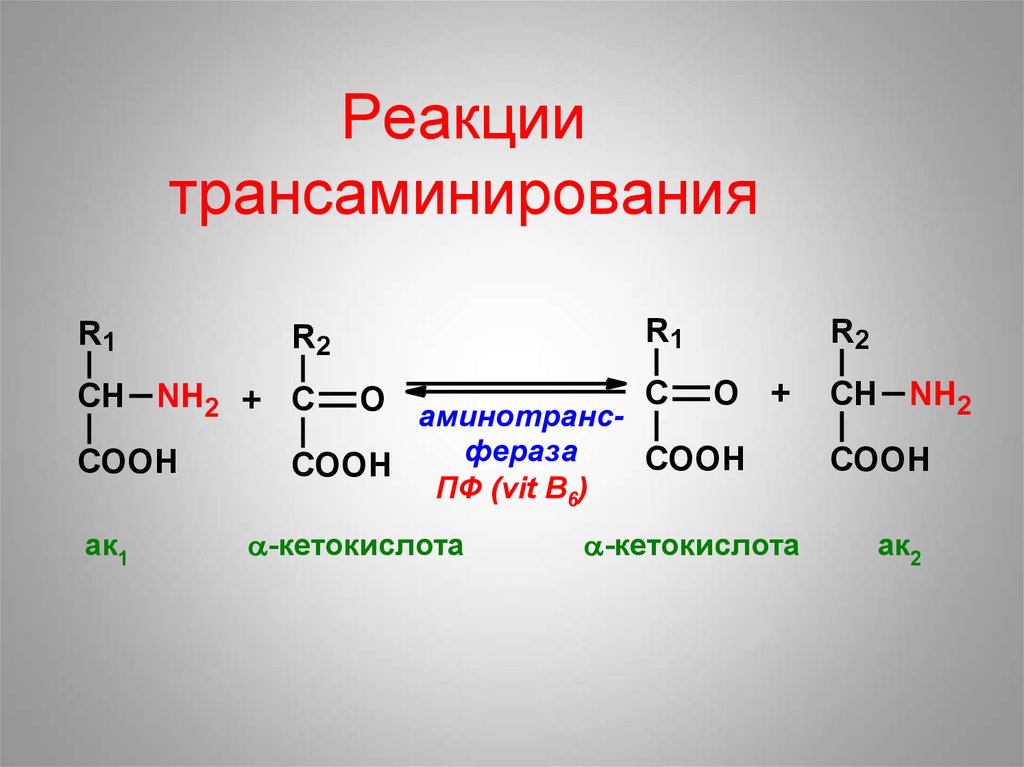
37. Реакции трансаминирования
R1R1
R2
O аминотранс- С O +
фераза
COOH
COOH
R2
СН NH2 + С
СН NH2
COOH
COOH
ак1
ПФ (vit B6)
-кетокислота
-кетокислота
ак2
38. Реакции декарбоксилирования
СО2R СН COO H
NH2
декарбоксилаза
ПФ (vit B6)
аминоксилота
COOH
СН2
СН2
СН NH2
COOH
глу
R СН2 NH2
биогенный амин
СО 2
декарбоксилаза
ПФ (vit B6)
COOH
СН2
СН2
СН2 NH2
-аминомасляная к-та
(ГАМК)
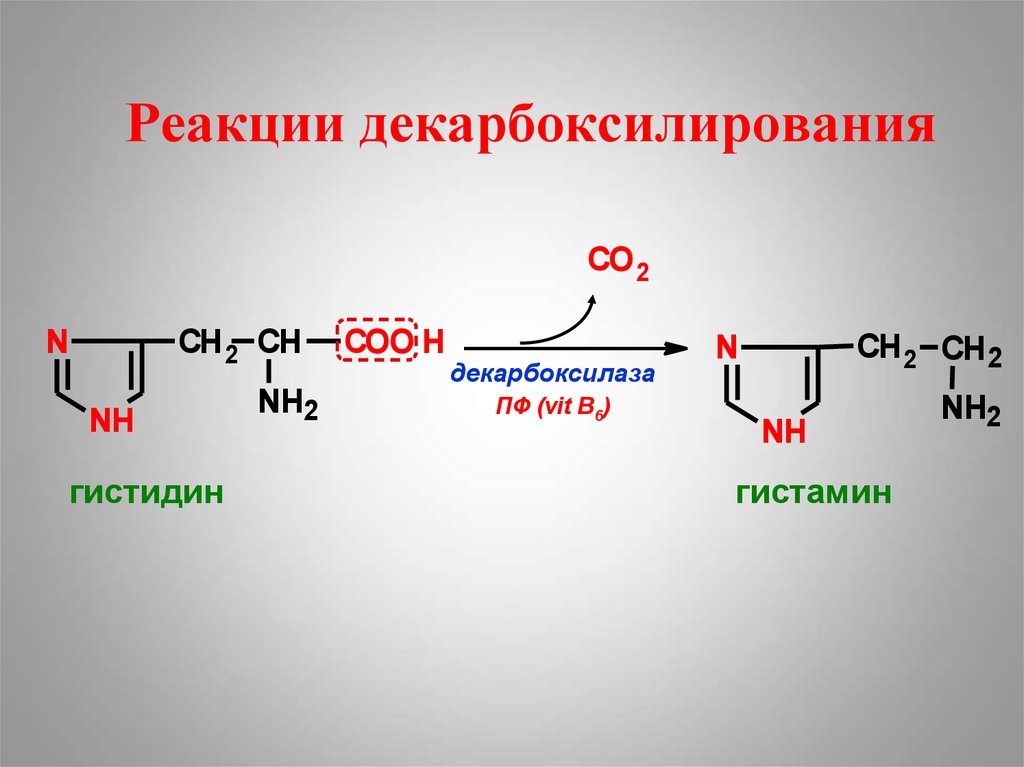
39. Реакции декарбоксилирования
CO 2СН 2 СН
N
NH
гистидин
NH2
COO H
декарбоксилаза
ПФ (vit B6)
СН 2 СН 2
N
NH
гистамин
NH2
40. Реакции декарбоксилирования
OHOH
СО2
HO
декарбоксилаза
СН2
СН
NH2
ПФ (vit B6)
HO
СН2
СН2 NH2
COOH
диоксифенилаланин
дофамин
41. Реакции декарбоксилирования
СН2 СН COOHNH2
NH
триптофан
1/2 О2
гидроксилаза
СО2
HO
СН2 СН COOH
NH
NH2
декарбоксилаза
HO
СН2 СН2
NH2
NH
ПФ (vit B6)
5-окситриптофан
серотонин
42.
Выведение аммиака43.
Пути выведения аммиакав зависимости от
систематического
положения и
экологических условий
обитания организмов
44.
45.
46.
47.
Конечные продуктыкатаболизма некоторых
сложных белков человека
и животных







































 Биология
Биология








