Похожие презентации:
Реакции ионного обмена и условия их протекания
1. Тема урока:
Реакции ионного обмена иусловия их протекания.
2. Цель урока:
Изучение реакций ионного обмена иусловий их протекания.
3. Эпиграф
Три пути ведут к познанию: путьразмышления – самый благородный,
путь подражания – самый лёгкий, путь
опыта – самый горький!
4. Ответьте на вопросы
1.Какие вещества называютсяэлектролитами? Приведите примеры.
2. Какие вещества называются
неэлектролитами? Приведите примеры.
3. В каком году и кто разработал теорию
электролитической диссоциации?
5. Выполните задания
1.Перечисленные вещества разделитена 2 столбика: в один запишите
электролиты, в другой – неэлектролиты:
р-р КОН, тв.КОН, крист. сахара, Н2SO4,
спирт, дист.вода.
2. Запишите уравнение диссоциации
следующих веществ: КNO3, Ba(OH)2,
HCL, H2SO4
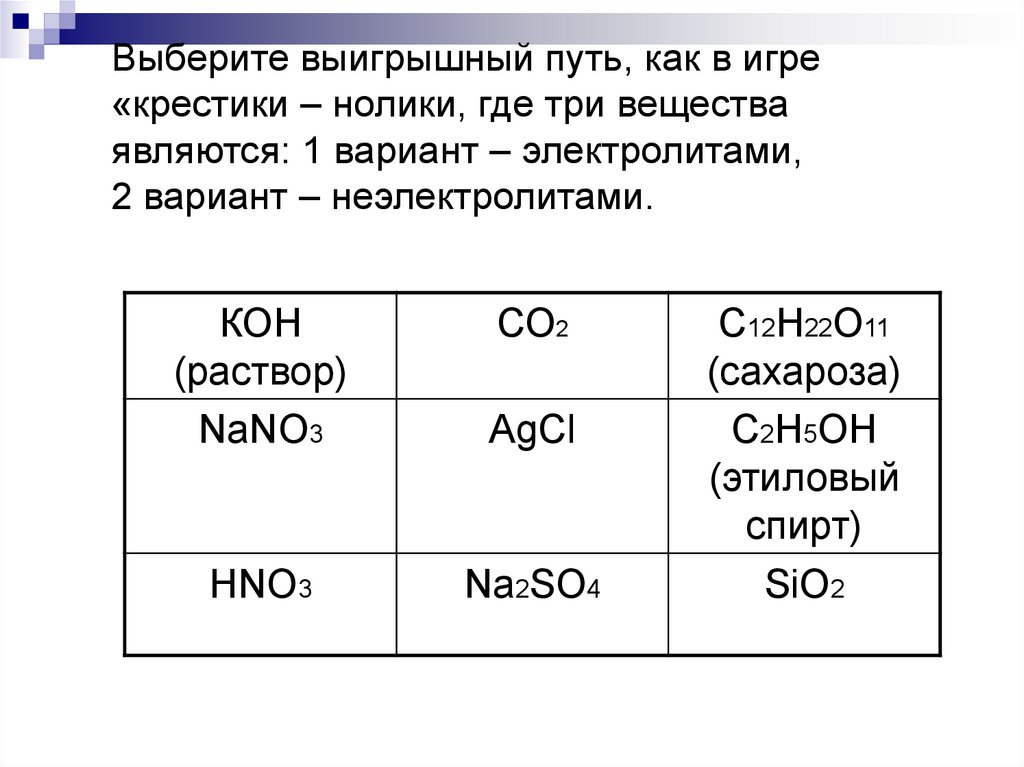
6. Выберите выигрышный путь, как в игре «крестики – нолики, где три вещества являются: 1 вариант – электролитами, 2 вариант –
неэлектролитами.КОН
(раствор)
NaNO3
СО2
AgCl
HNO3
Na2SO4
С12Н22О11
(сахароза)
C2H5OH
(этиловый
спирт)
SiO2
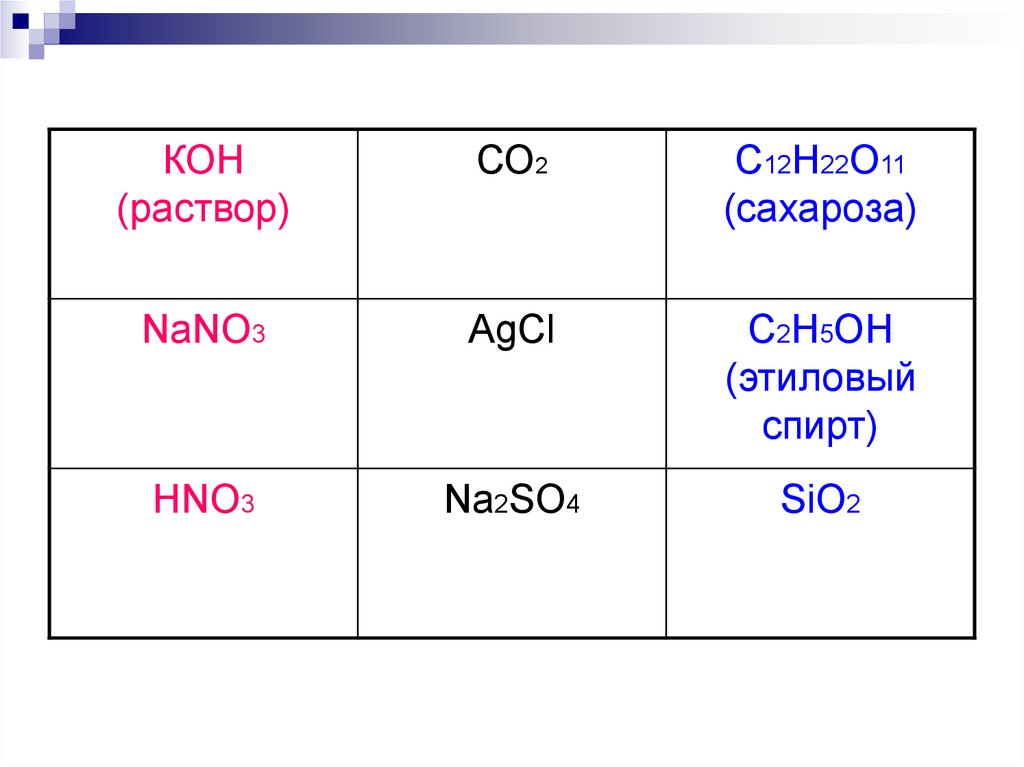
7.
КОН(раствор)
СО2
С12Н22О11
(сахароза)
NaNO3
AgCl
C2H5OH
(этиловый
спирт)
HNO3
Na2SO4
SiO2
8. Реакции между ионами называются ионными реакциями, а уравнения таких реакций – ионными уравнениями.
9. Реакции ионного обмена протекают до конца в случае
Выпаденияосадка
Выделения газа
Образования
малодиссоциирующего
вещества
10. Правила составления ионных уравнений
Простые вещества, оксиды, а также нерастворимыекислоты, основания, соли не диссоциируют.
Для реакции берут растворы веществ, поэтому даже
малорастворимые вещества находятся в растворах в
виде ионов.
Если в результате реакции образовалось
малорастворимое вещество, то при записи ионного
уравнения его считают нерастворимым.
11. Алгоритм составления ионного уравнения
Записать молекулярное уравнение реакции.С помощью таблицы растворимости
определить растворимость каждого
вещества.
Составить полное ионное уравнение
Составить сокращенное ионное уравнение
(найти одинаковые ионы и сократить их слева
и справа)
12. Лабораторная работа Тема: Реакции ионного обмена
1 группаВзаимодействие
растворов NaOH и
CuSO4
2 группа
Взаимодействие
растворов Na2CO3 и HCl
3 группа
Взаимодействие
растворов NaOH и HCl
13. Заполните таблицу
Исходныевещества
Признак
реакции
Уравнение Вывод
реакции
14. Вывод урока
ЗнаюХочу узнать
Узнал
15. Оцените свою работу по направлениям
«Я» - как я себя чувствовал в процессеурока, доволен ли я своей работой;
«Мы» - насколько комфортно и
эффективно мне было работать в
группе;
«Дело» - достиг ли я цели обучения, в
чём испытал затруднения, как
преодолеть проблемы.













 Химия
Химия








