Похожие презентации:
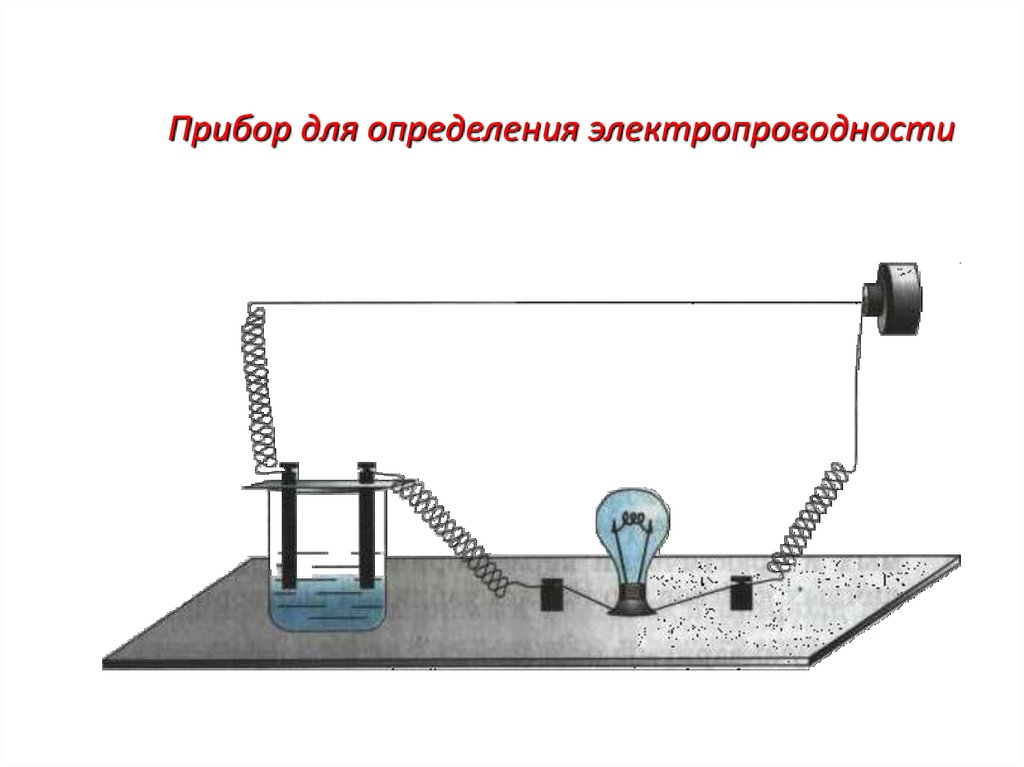
Прибор для определения электропроводности
1. Прибор для определения электропроводности
2. Электролитическая диссоциация
3. Цель урока:
• Познакомиться с процессами,происходящими в растворах
• Изучить механизм диссоциации
4.
Задачи урока:1. узнать, что такое электролитическая
диссоциация.
2. изучить механизм электролитической
диссоциации
5.
«Сами трудясь, вы многое сделаете длясебя и для близких, а если при труде успеха
не будет, будет неудача, не беда, попробуйте ещё»
Д.И.Менделеев
6. http://fcior.edu.ru/card/9262/laboratornaya-rabota-elektrolity-i-neelektrolity.html
Лабораторная работа:Электролиты и неэлектролиты.
HTTP://FCIOR.EDU.RU/CARD/9262/LABORATORNAYARABOTA-ELEKTROLITY-I-NEELEKTROLITY.HTML
7.
Знаете ли вы?Даже в медицине используют
понятие « электролит». Термин
"содержание электролитов в сыворотке
крови означает содержание отдельных
ионов (натрия, калия, хлора, бикарбоната
и т.д.) в циркулирующей крови человека.
Оксфордский толковый словарь общей медицины, 2002 г.
8. С. Аррениус, 1887г.:
Причинаэлектропроводности ─
наличие растворе ионов,
которые образуются
при растворении
электролита в воде
9.
• Процесс распада электролита наионы в растворе называется
электролитической диссоциацией
(от лат. dissociatio – «разделение»)
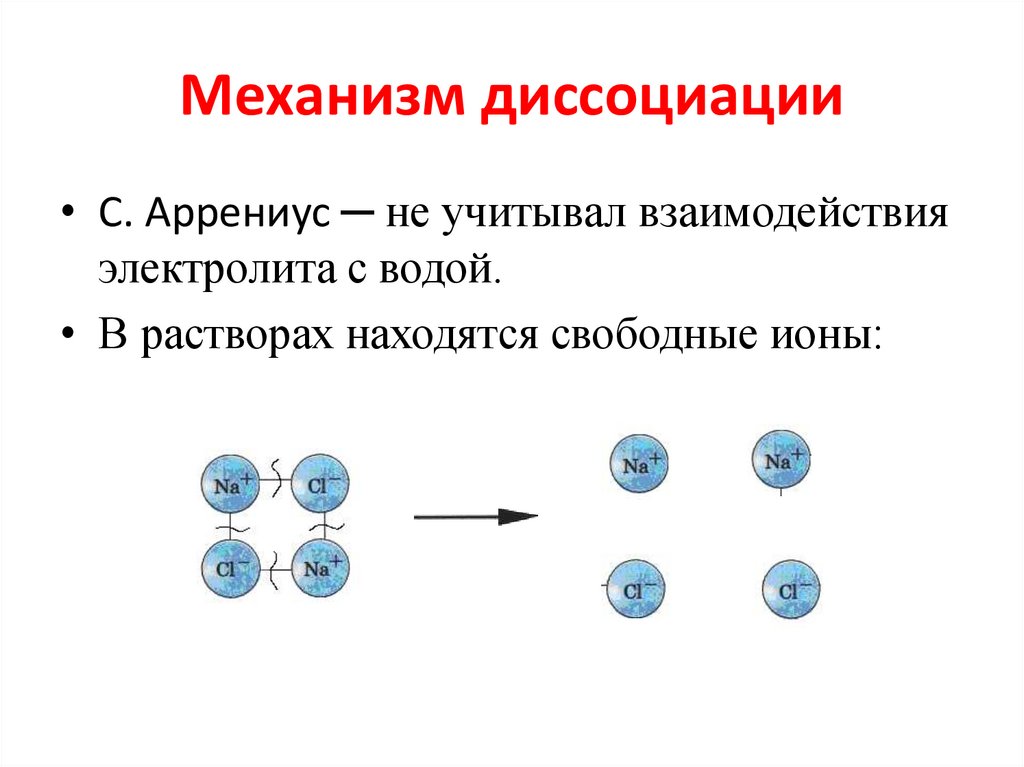
10. Механизм диссоциации
• С. Аррениус ─ не учитывал взаимодействияэлектролита с водой.
• В растворах находятся свободные ионы:
11. Ионы
катионыанионы
(+)
(─)
12.
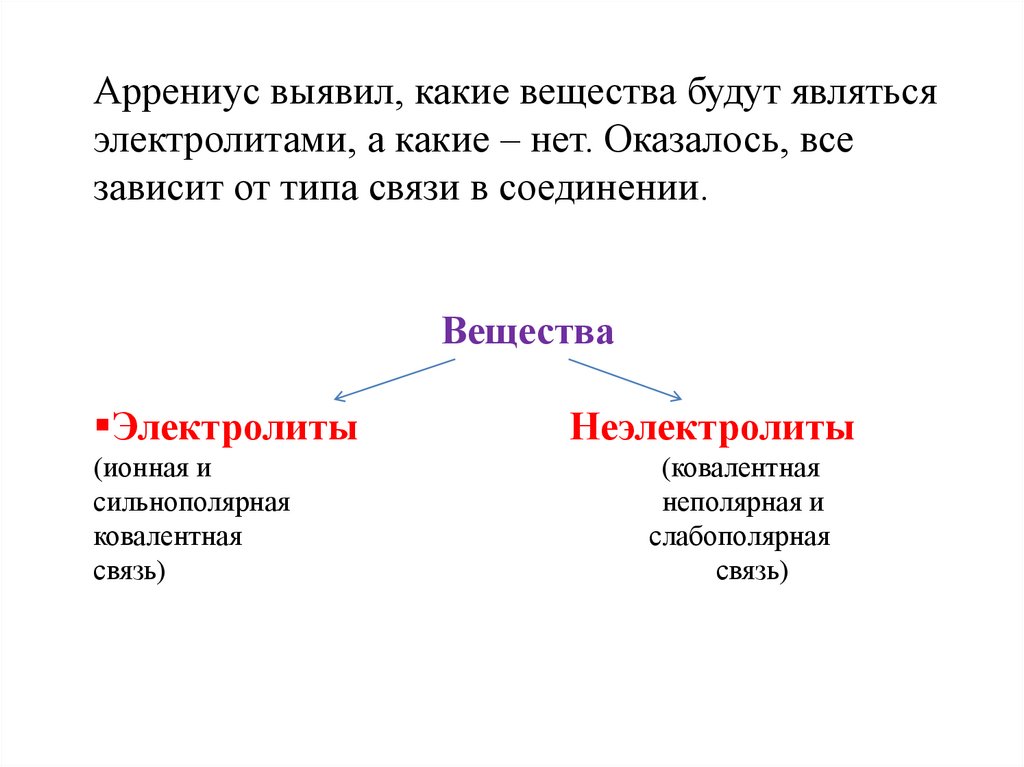
Аррениус выявил, какие вещества будут являтьсяэлектролитами, а какие – нет. Оказалось, все
зависит от типа связи в соединении.
Вещества
Электролиты
(ионная и
сильнополярная
ковалентная
связь)
Неэлектролиты
(ковалентная
неполярная и
слабополярная
связь)
13. Д.И. Менделеев
В растворах находятся несвободные, а
гидратированные ионы
Д.И. Менделеев
И.А. Каблуков
В.А. Кистяковский
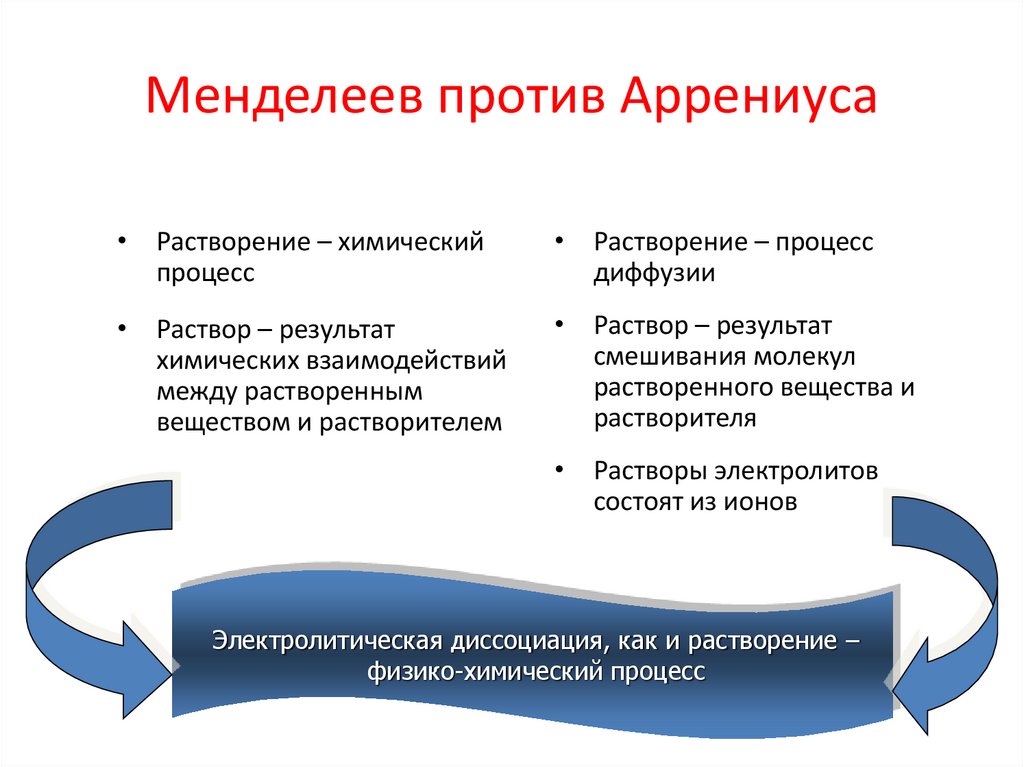
14. Менделеев против Аррениуса
• Растворение – химическийпроцесс
• Растворение – процесс
диффузии
• Раствор – результат
химических взаимодействий
между растворенным
веществом и растворителем
• Раствор – результат
смешивания молекул
растворенного вещества и
растворителя
• Растворы электролитов
состоят из ионов
Электролитическая диссоциация, как и растворение –
физико-химический процесс
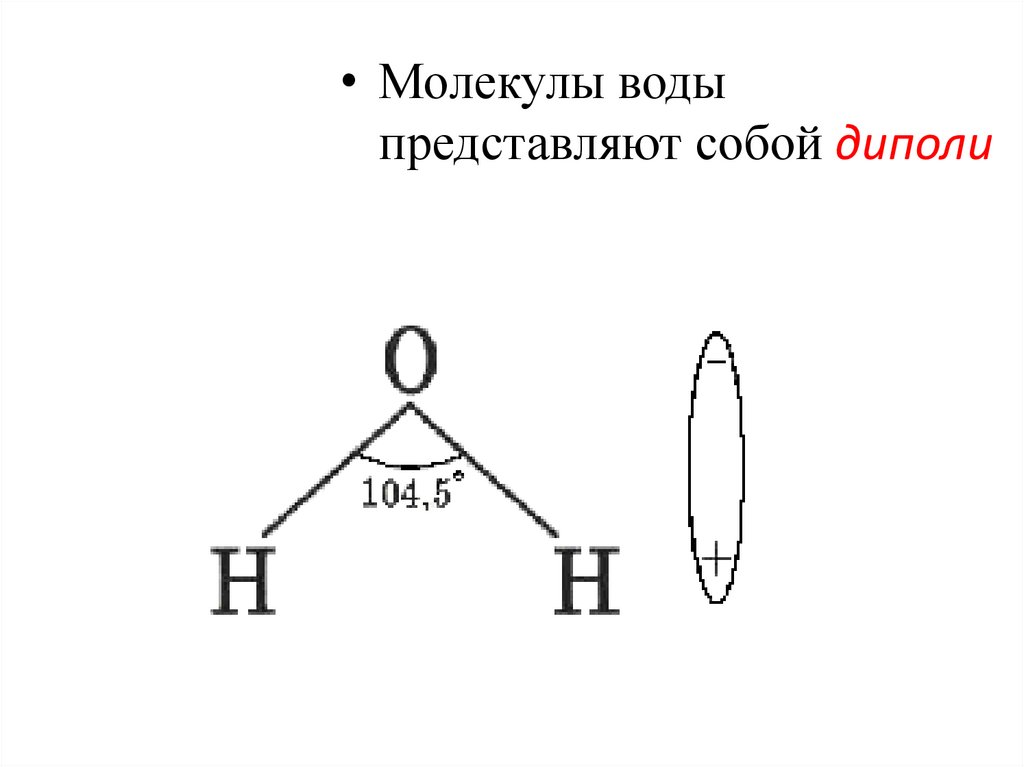
15.
• Молекулы водыпредставляют собой диполи
16.
Это интересно……Если бы молекулы воды были построены более
симметрично они не были бы полярные, и тогда весь
облик Земли изменился бы до неузнаваемости:
океаны испарились, и вокруг земного шара
образовалась атмосфера из водяного пара с
незначительной примесью других газов. Что привело
бы к исчезновению жизни на Земле.
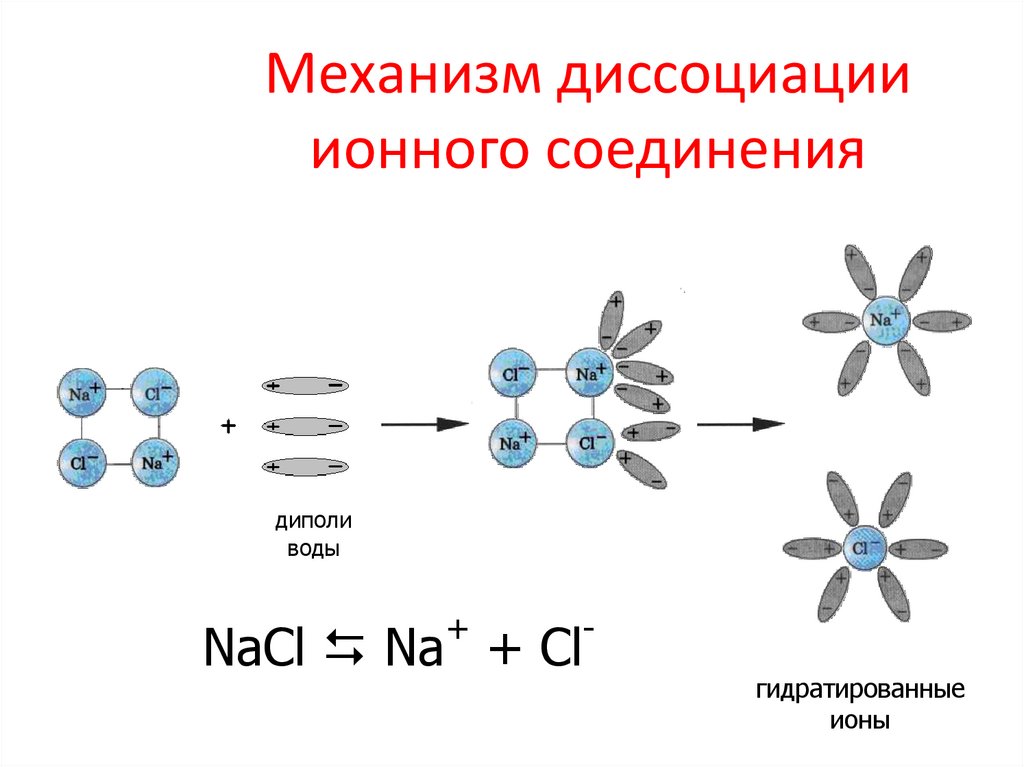
17. Механизм диссоциации ионного соединения
диполиводы
+
NaCl Na + Cl
гидратированные
ионы
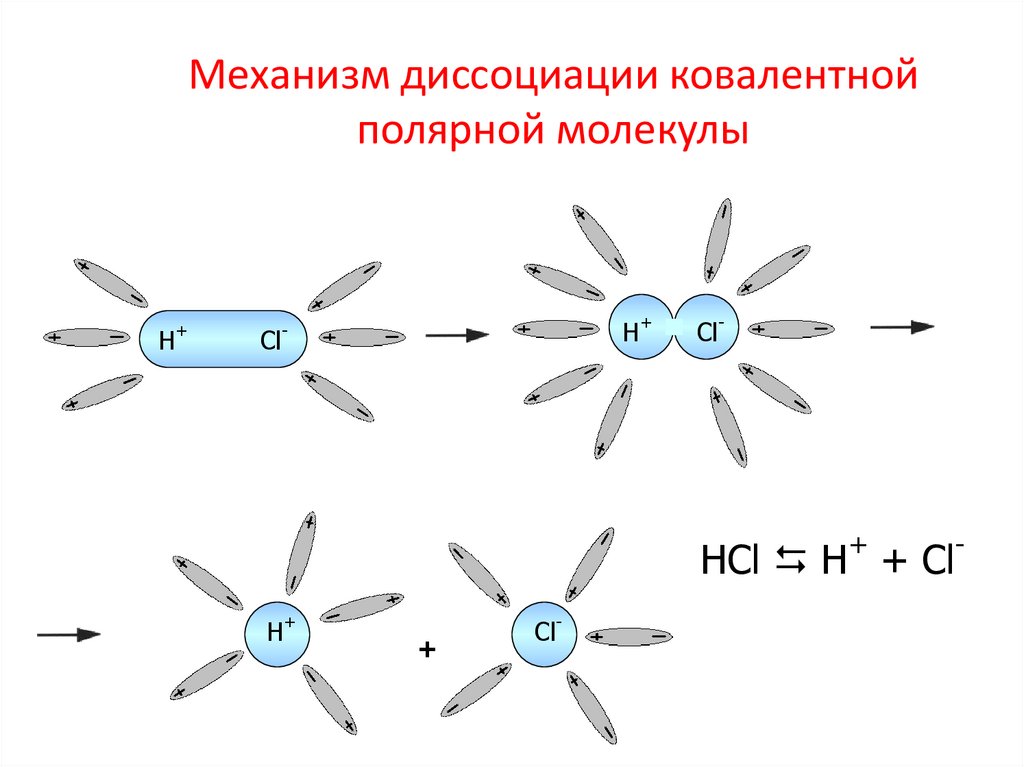
18. Механизм диссоциации ковалентной полярной молекулы
+H
H+
-
Cl
Cl-
+
HCl H + Cl
H+
+
Cl-
-
19. Этапы диссоциации: 1. Ориентация 2. Гидратация 3. Диссоциация
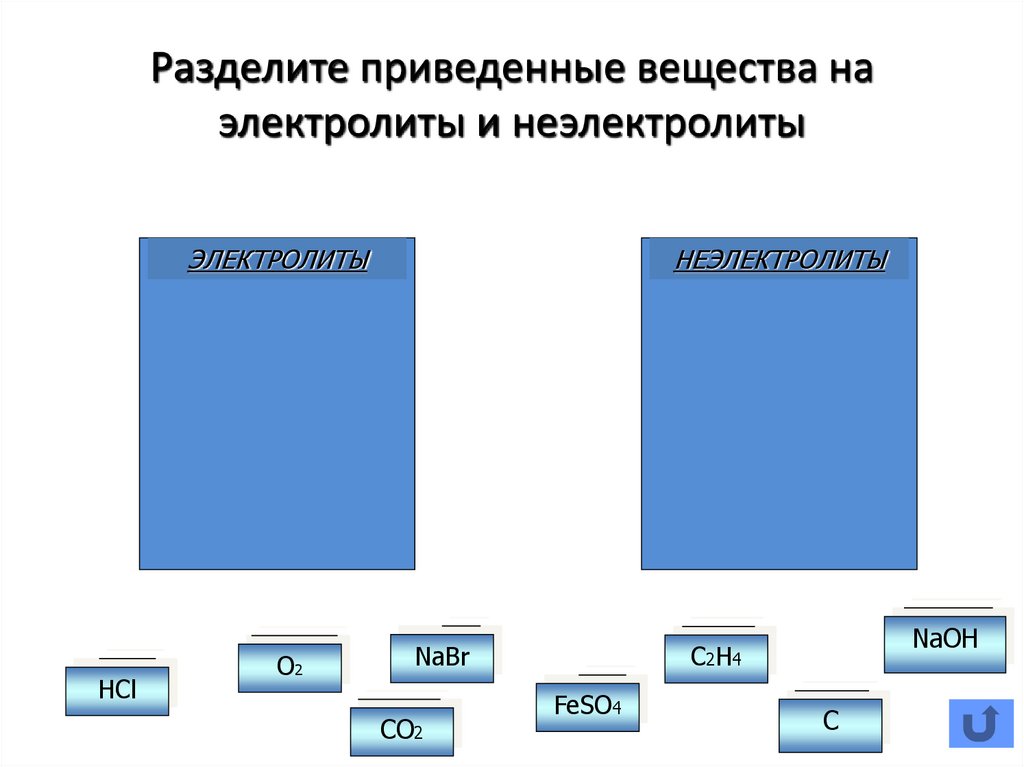
20. Разделите приведенные вещества на электролиты и неэлектролиты
ЭЛЕКТРОЛИТЫHCl
O2
НЕЭЛЕКТРОЛИТЫ
NaBr
CO2
NaOH
C2H4
FeSO4
C
21. Домашнее задание
– § 36, упр. 1, 5 (базовый уровень);+упр. 2,3 (повышенный уровень)
– Выполнить задание в интерактивном
режиме
http://fcior.edu.ru/card/14154/testypo-teme-elektrolity-ineelektrolity.html
• ( по желанию)













 Химия
Химия








