Похожие презентации:
Клиническая фармакокинетика и фармакодинамика лекарственных средств
1.
2.
Цель медицины – действие, а не ожидание. Угрозаошибиться в диагнозе всегда большая, но еще
сильнее угроза рисковать жизнью больного,
оставив его без лечения.
К. Бернар
3.
По определению ВОЗ,клиническая
фармакология – наука, которая занимается
изучением лекарственных средств в применении к
человеку.
Цель – это оптимизация фармакотерапии человека,
то есть сделать ее максимально эффективной и
безопасной.
4.
Составляющие клиническойфармакологии
Клиническая фармакокинетика
Клиническая фармакодинамика
Терапевтическя оценка
Молекулярная фармакокинетика
Фармакогенетика
Фармакоэкономика
Фармакоэпидемиология
5.
Клиническая фармакологияв ХХ веке изучала
ФАРМАКОДИНАМИКУ
ФАРМАКОКИНЕТИКУ
ЛС
ДОЛЖНА БЫЛА
ОБЕСПЕЧИТЬ
ЭФФЕКТИВНОСТЬ
И БЕЗОПАСНОСТЬ
ФАРМАКОТЕРАПИИ
ВЗАИМОДЕЙСТВИЕ
ЛЕКАРСТВЕННЫХ
СРЕДСТВ
НЕЖЕЛАТЕЛЬНЫЕ
ЛЕКАРСТВЕННЫЕ
РЕАКЦИИ
6.
Клиническая фармакологияв ХХI веке
ФАРМАКОКИНЕТИКА
НЕЖЕЛАТЕЛЬНЫЕ
ЛЕКАРСТВЕННЫЕ
РЕАКЦИИ
ФАРМАКОЭПИДЕМИОЛОГИЯ
ФАРМАКОДИНАМИКА
КЛИНИЧЕСКАЯ
ФАРМАКОЛОГИЯ
ФАРМАКОГЕНЕТИКА
ФАРМАКОГЕНОМИКА
КФ ДОЛЖНА ОБЕСПЕЧИТЬ
ЭФФЕКТИВНОСТЬ И
БЕЗОПАСНОСТЬ
ФАРМАКОТЕРАПИИ
ВЗАИМОДЕЙСТВИЕ
ЛЕКАРСТВЕННЫХ
СРЕДСТВ
ФАРМАКОЭКОНОМИКА
7.
Задачи клинической фармакологииВыбор лекарственного средства для лечения
конкретного больного
Определение оптимальной лекарственной
формы, пути введения, дозы и режима
дозирования
Наблюдение за действием лекарственного
средства на конкретного больного
Предупреждение и устранение побочных
реакций и нежелательных последствий
взаимодействия лекарственных веществ
Клинические испытания новых
фармакологических средств
8.
ЛЕКАРСТВЕННОЕ ВЕЩЕСТВО (ДЕЙСТВУЮЩЕЕВЕЩЕСТВО, СУБСТАНЦИЯ) – биологически активное
вещество, которое может изменять состояние и
функции организма или имеют профилактическое,
диагностическое или лечебное действие и
используются для производства готовых
лекарственных средств
9.
Международное непатентованноеназвание – утверждается
официальными органами
здравоохранения и используется в
национальных и международных
фармакопеях (Цефтриаксон)
Торговое (фирменное) название – название,
которое является коммерческой
собственностью фармацевтической фирмы
(Форцеф, лонгацеф, цефтрон, цефсон,
триаксон,роцефин, офрамакс)
10.
Патентная защита позволяет патентообладателюпродавать новое средство определенный период
времени.
Как только срок патентной защиты исчезает,
препарат может появиться в продаже как
дженерик под непатентованным названием или
как препарат –преемник под другими торговыми
названиями.
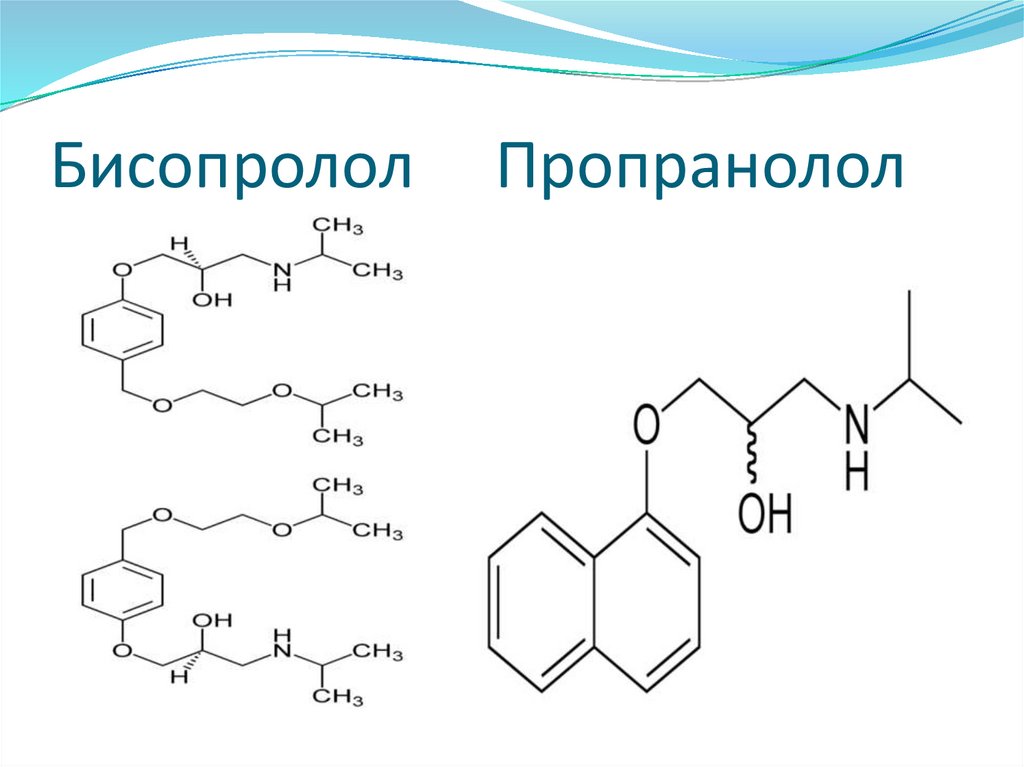
Новый препарат может содержать новый
активный ингредиент или является аналогом
средства (либо препаратом той же группы) со
слегка измененной химической структурой
(вещества-аналоги –β-блокаторы)
11.
БисопрололПропранолол
12.
Оригинальные (брендовые)лекарственные препараты –
препараты, которые имеют
(имели) патентную защиту;
исключительная
собственность компании,
которая их разработала и
(или) имеет лицензию на его
производство.
Брендовые препараты –
наиболее новые и лучше
всего изученные
лекарственные препараты.
Например: плавикс
(клопидогрель)
13.
Генерические лекарственныепрепараты – копии оригинальных
препаратов, которые выпускаются после
истечения срока действия патента на
оригинальный препарат
содержат то же активное вещество, что и оригинальный
лекарственный препарат
идентичны оригинальному лекарственному препарату по
силе действия
имеют ту же лекарственную форму и путь введения, что и
оригинальный лекарственный препарат
имеют те же показания к применению, что и оригинальный
лекарственный препарат
Биоэквивалентны оригинальному лекарственному
препарату
14.
Клиническая фармакокинетикаэто
раздел клинической фармакологии, изучающий
пути введения ЛС в организм здорового и
больного
человека,
их
распределение,
биотрансформацию и выведение ЛС.
-
Главная задача фармакокинетики повышение эффективности, а также снижение
частоты и выраженности побочных эффектов
медикаментозной терапии.
Кинетика отвечает на вопрос : «Что организм
делает с лекарством?»
15.
Основные фармакокинетическиепараметры
Кажущийся объем распределения (Vd) - гипотетический
объем жидкости организма, необходимый для
равномерного распределения всего количества ЛС (дозы) в
концентрации, аналогичной таковой в плазме крови.
Измеряется в л/кг. Служит для подбора нагрузочной дозы
Максимальная концентрация С max и время
наступления максимальной концентрации Тmax- при
поступлении ЛС в системный кровоток (при
внесосудистом введении) его концентрация достигает
значения С max в момент Тmax, затем начинает
снижаться.
16.
Биодоступность - часть дозы ЛС, выраженная впроцентах, поступившая в системный кровоток
после внесосудистого введения.
Биодоступность лекарственного средства выражают
в процентах и при введении непосредственно в
кровь принимают за 100 %, служит для подбора
дозы ЛС при внесосудистом (например
пероральном ) приеме.
17.
БиоэквивалентностьДва лекарственных препарата являются
биоэквивалентными в тех случаях, когда дают одинаковую
концентрацию действующих веществ в крови и тканях
организма при введении препаратов в равной дозе.
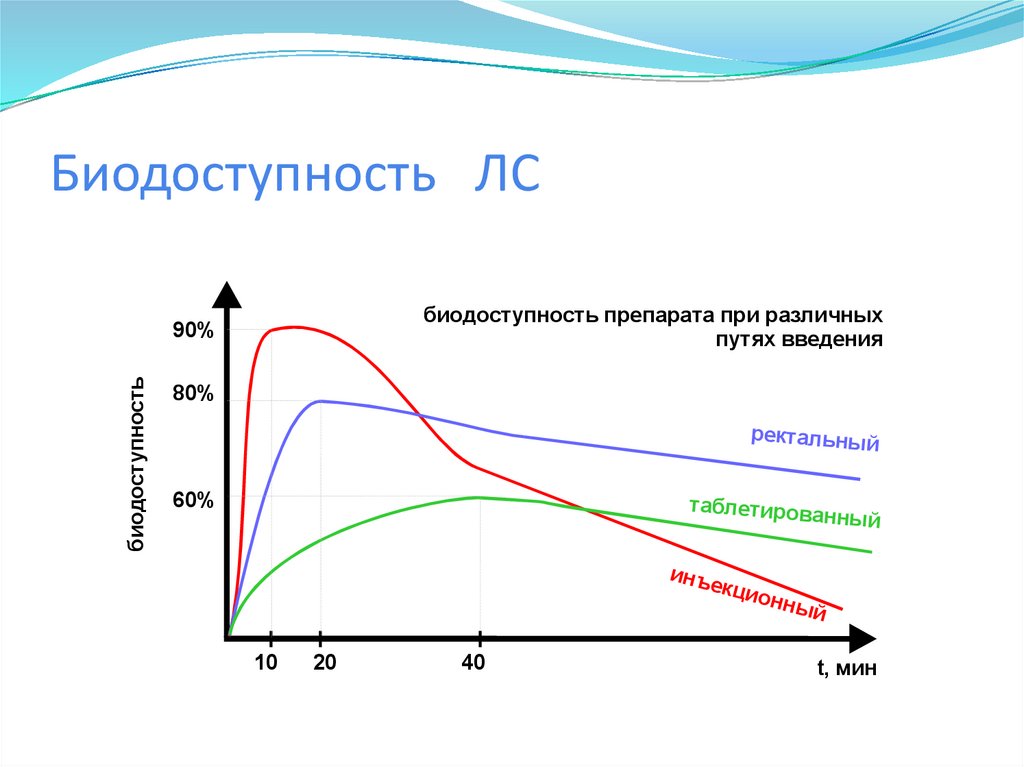
18.
Биодоступность ЛСбиодоступность препарата при различных
путях введения
биодоступность
90%
80%
ректальный
60%
таблетирова
инъ
ек
10
20
40
нный
цион
ный
t, мин
19.
Основные фармакокинетическиепараметры
Период полувыведения (Т1 / 2) - время, необходимое
для снижения концентрации препарата в крови на 50%
в результате элиминационных процессов.
Служит для определения промежутка времени,
необходимого для достижения равновесной
концентрации ЛС в крови ( обычно 3-5 Т1/2). Может
использоваться для оценки выведения ЛС, но менее
точен и информативен, чем общий клиренс
20.
Концентрация лекарственного вещества в организмезависит от времени
Такие процессы, как всасывание и выведение обладают
экспоненциальными характеристиками.
Экспоненциальный рост — возрастание величины, когда
скорость роста пропорциональна значению самой
величины. Для любой экспоненциально растущей
величины чем большее значение она принимает, тем
быстрее растёт. Также это означает, что величина
зависимой переменной и скорость её роста прямо
пропорциональны.
В отношении всасывания: количество препарата ,
всасывающегося за единицу времени зависит от разницы
концентраций (закон Фика)
21.
Общий клиренсОбщий клиренс (CL) - объем плазмы или крови,
полностью освобождающийся от препарата в единицу
времени. Этот показатель количественно характеризует
выведение ЛС и измеряется в мл/мин.
Общий клиренс представляет сумму печеночного и
почечного клиренсов.
Печеночный клиренс характеризует биотрансформацию ЛС
в печени (метаболический клиренс) и выведение с желчью
(желчный) клиренс.
Почечный клиренс отражает выведение ЛС с мочой
22.
Клиренс служит для подбора поддерживающейдозы, зависит от функционального состояния
органа выведения и скорости доставки ЛС к нему
Константа скорости элиминации (Кel)-процент
снижения концентрации вещества в крови за
единицу времени.
23.
Расчет нагрузочной и поддерживающей дозD нагр= V∙C, где D нагр – нагрузочная доза, V – объем
распределения, C – концентрация ЛС в плазме
D поддер=Cl∙Css, где D поддер – поддерживающая доза,Cl
– общий клиренс, Css – равновесная концентрация
24.
Эффективность лекарства определяется путем еговведения.
Энтеральный путь введения: пероральный ( самый
распространенный и доступный), сублингвальный,
ректальный
Парентеральные пути введения:
Инъекционные (внутриартериальный, внутривенный,
внутрикожный, подкожный, внутримышечный,
внутрисердечный, внутрисуставный и др.)
Неинъекционные (ингаляционный, трансдермальный,
конъюнктивальный, в виде липосом, путем
электрофореза)
25.
Механизмы всасыванияПри энтеральном введении всасывание реализуется посредством
пассивной диффузии, активного транспорта, фильтрации через
поры, пиноцитоза.
Пассивная диффузия – основной метод, не требует затрат
энергии.
Жирорастворимые ЛС всасываются быстрее водорастворимых
При пассивной диффузии ЛС сначала проникает в жидкость на
поверхности клеточной мембраны, затем растворяется в ее
липидном слое, проникает в водную фазу на внутренней
поверхности мембраны
Активный транспорт требует затрат энергии, характерен для
всасывания аминокислот , сахаров, витаминов
Фильтрация через поры характерно для ЛС с молекулярной
массой менее 100Да
Пиноцитоз – поглощение вещества клеточной мембраной
26.
Связывание ЛП с белками плазмыЭффективность препарата зависит от степени его связывания с
белками плазмы. Чем меньше препарат связывается, тем
больший он оказывает эффект. Основными белками крови, с
которыми связываются с лекарства, являются альбумины,
липопротеины, гликопротеины, глобулины(α, β, γ).
Препараты находятся в крови в двух формах: связанной и
несвязанной. В зависимости от сродства конкретного препарата
к белкам плазмы, доля лекарства может перейти в связанную с
белками плазмы форму, а оставшаяся часть останется
несвязанной. Если связывания с белками обратимо, то
связанная и несвязанная формы будут находиться
в химическом равновесии таким образом:
Белки + лекарства ⇌ комплекс белок-лекарство
27.
Именно несвязанная доля лекарства будетоказывать терапевтический эффект. Также эта
часть может быть подвергнута биотрансформации
и/или элиминации. Например, «связанная
часть» антикоагулянта варфарина составляет 97 %.
Это означает, что из всего введеного в организм
варфарина , 97 % связано с белками крови.
Оставшиеся 3 % (часть несвязанная) препарата
проявляют активность и могут быть выведены.
28.
Связывание с белками может влиять на периодполувыведения лекарств.
Связанная часть выступает в качестве резервуара
или депо, из которого препарат медленно
выделяется в виде свободной формы.
В то время, как несвязанная часть
метаболизируется и/или выводится из организма,
связанная часть будет высвобождаться для
поддержания равновесия.
29.
Использование двух препаратов в одно и тожевремя может повлиять на их связывание с белками
плазмы.
Например, предположим, что лекарство А и
лекарство Б способны связываться с белками.
Если мы введем лекарство А, оно свяжется с
белками. Но если мы также введем лекарство Б, то
оно может вытеснить лекарство А, и повысить тем
самым его несвязанную долю.
Это может усиливать активность лекарств, так как
только несвязанные фракции могут проявлять
активность.
30.
Эффект связывания с белками является наиболее значимым дляпрепаратов, которые обладают большим сродством (> 95 %) и
имеют низкий терапевтический индекс таких как варфарин.
Низкий терапевтический индекс свидетельствует о том, что
существует высокий риск токсического эффекта при
применении препарата.
Так как варфарин является антикоагулянтом с низким
терапевтическим индексом, то он может вызвать кровотечение,
если не поддерживается его правильный уровень доступности.
Если пациент принимает варфарин одновременно с другими
препаратами, которые вытесняют варфарин из белков плазмы,
таких как сульфаниламиды, это может привести к повышению
риска кровотечения.
31.
Метаболизм (биотрансформация) ЛСМетаболизм ЛС – химические превращения ЛС в
организме, снижается липофильность, повышается
гидрофильность,изменяется фармакологическая
активность.
Изменение фармакологической активности идет в двух
направлениях
ЛС теряет активность, превращается в неактивное
(большинство ЛС)
Фармакологически активное вещество превращается в
другое активное вещество
Неактивные вещества (пролекарства) превращаются в
активные (эналаприл, периндоприл, рамиприл)
32.
Метаболизм ЛСКлассифицируют преимущественно по типу химических реакций,
лежащих в основе преобразования данного соединения
Реакции 1 фазы биотрансформации ЛС обычно несинтетические,
реакции 2 фазы - синтетические.
Все несинтетические реакции можно разделить на 2 группы:
а) Реакции, катализируемые ферментами эндоплазматической сети
(микросомальными) - гемопротеин цитохром Р450.
б) Реакции, катализируемые ферментами другой локализации
(немикросомальными)
При несинтетических реакциях происходит перестройка молекул
субстрата с образованием функциональных групп, повышающих
гидрофильность соединения. К несинтетическим реакциям относят:
реакции окисления (гидроксилирования, присоединения,
восстановления и гидролиза.
33.
Основными ферментами системыбиотрансформации ЛС являются
изоферменты цитохрома Р-450,
локализованные в гепатоцитах
34.
Цитохром Р450 представляет комплекс белка сковалентно связанным гемом (металлопротеином),
обеспечивающим присоединение кислорода.
Гем, в свою очередь, является комплексом
протопорфирина IX и двувалентного атома железа.
Число 450 обозначает, что восстановленный гем,
связанный с СО, отличается максимумом
поглощения света при длине волны 450 нм.
35.
Цитохромы Р-450 участвуют не только в метаболизме лекарств,но и в превращении гемоглобина в билирубин, синтезе стероидов и
др.
Все изоформы цитохрома Р-450 объединены в семейства CYP1,
CYP2, CYP3. Внутри семейств выделены подсемейства A, B, C, D,
E. В пределах подсемейств изоформы обозначены порядковым
номером.
Например, CYP2C19 — наименование 19-го по порядку
цитохрома подсемейства «С», семейства «2». Всего существует
около 250 различных видов цитохрома Р-450, из них примерно 50 —
в организме человека и только шесть из них (CYP1A2, CYP2C9,
CYP2C19, CYP2D6, CYP2E1, CYP3A4) имеют отношение к
метаболизму лекарств.
36.
На активность цитохромов Р-450оказывает влияние множество факторов
— курение, алкоголь, возраст, генетика,
питание, болезни. Эти факторы отвечают
за формирование индивидуальных
особенностей работы ферментов Р-450 и
определяют эффекты лекарственного
взаимодействия у конкретного пациента.
37.
Микросомальная система оксидазФерменты расположены на мембранах эндоплазматического
ретикулума клеток печени, ответственные за окислительный
метаболизм - оксидазы со смешанной функцией
(монооксигеназы)
Основную роль играют изоферменты цитохрома Р 450
Различают 17 семейств, 39 подсемейств
Основные изоферменты – 1А1, 1А2, 2А6, 2А6, 2В6, 2Д6,
2С19, 3А4.
Содержание 3А4 составляет 28% в печени
Субстраты 3А4 – азитромицин, алкалоиды спорыньи,
амиодарон, амлодипин, аторвастатин, верапамил,
галореридол. гидрокортизон, дексаметазон, карбамазепин,
диазепам и многие другие.
38.
Реакции 2 фазы биотрансформации (синтетические)В их основе лежит конъюгация ЛС с эндогенными
субстратами (глюкуроновой кислотой, глутамином,
сульфатом, глутатионом, глицином, метильными группами
и водой).
Необходимо учитывать, что ацетилирование и
метилирование ЛС происходит с участием гидроксильной,
карбоксильной, аминной, эпоксидной и других
функциональных групп. После завершения этой реакции
молекула препарата становится более полярной, лучше
выводится из организма.
Как правило, только после второй фазы биотрансформации
образуются неактивные или мало активные соединения,
поэтому именно синтетические реакции можно считать
настоящими реакциями детоксикации
ксенобиотиков, в т.ч. и лекарственных средств.
39.
Основные пути выведения ЛС из организмаПуть выведения
Механизмы выведения
ЛС
С мочой
Клубочковая фильтрация,
активная канальцевая
секреция
Большинство ЛС в не
связанной с белками
форме
С желчью
Активный транспорт,
пассивная диффузия,
пиноцитоз
Дигитоксин,
пенициллины,
тетрациклины,
стрептомицин, хинин,
стрихнин
Через кишечник
Пассивная диффузия,
желчная секреция без
реабсорбции
Доксициклин,
ионизированные
органические кислоты
Со слюной
Пассивная диффузия,
активный транспорт
Пенициллины,
сульфаниламиды,
салицилаты
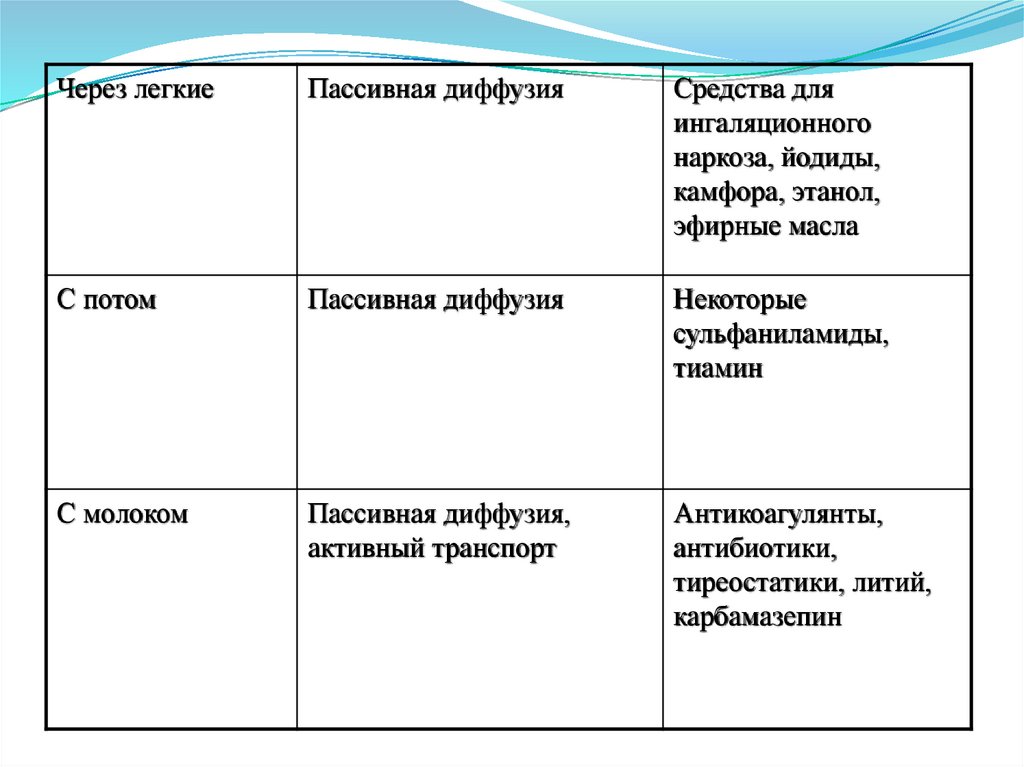
40.
Через легкиеПассивная диффузия
Средства для
ингаляционного
наркоза, йодиды,
камфора, этанол,
эфирные масла
С потом
Пассивная диффузия
Некоторые
сульфаниламиды,
тиамин
С молоком
Пассивная диффузия,
активный транспорт
Антикоагулянты,
антибиотики,
тиреостатики, литий,
карбамазепин
41.
Фармакодинамика включает механизмразвития, характер, силу и продолжительность
фармакологических эффектов ЛС.
Лекарственные средства модифицируют
функции молекул-мишеней (рецепторов,
эффекторов, ферментов, вторичных
переносчиков), что в конечном итоге и
приводит к усилению, ослаблению или
стабилизации реакций организма.
Фармакодинамика отвечает на вопрос: «Как
лекарство вмешивается в регуляцию функций
организма?»
42.
Клинические аспекты фармакодинамикиПодавляющее большинство
лекарств оказывают свое
лечебное действие путем
изменения деятельности
физиологических систем
различных клеток организм,
так как многие ЛС похожи
на биологически активные
вещества (ацетилхолин,
норадреналин, гистамин)
43.
44.
Расшифрованы молекулы-мишени ЛС1. Ионные каналы;
2. Неспецифические белки и липиды
3. Рецепторы:
Мембранные (рецепторы I – III типов);
Внутриклеточные (рецепторы IV типа);
Иммуноглобулиновые;
4. Ферменты
5. Неорганические соединения (HCl, металлы);
6. На чужеродных организмах (микроорганизмы).
45.
В органе - мишени ЛС могут:1. Связываться со специфическими рецепторами,
что определяет клинический эффект данного
препарата.
2. Связываться с неспецифическими рецепторами,
обычно с белками тканей.
3. Оставаться в свободной (несвязанной)
растворимой форме.
4. Вернуться в плазму крови в неизмененном виде.
5. Подвергнуться биотрансформации (метаболизму).
6. Выделяться в неизменном виде.
46.
Изучены четыре типа рецепторов1 тип. Рецепторы-ионные каналы(н-холинорецептор :нхолиномиметики:цититон;н -холиноблокаторы: ганглиоблокирующие
средства: бензогексоний; пентамин;
ГАМК-рецепторы –снотворные , антиэпилептические,
противопаркинсонические при др.);
2 тип. Рецепторы наиболее распространены в организме,
вазопрессиновые ( десмопрессин), ангиотензиновые (лозартан,
ирбесартан, кандесартан, валсартан) α,β – адренергические, м –
холинорецепторные, дофаминовые (селективные агонисты D2дофаминовых рецепторов ( прамипексол , ропинирол), опиатные агонисты (морфин, фентанил, промедол), агонисты-антагонисты
(буторфанол, пентазоцин, бунренорфин. трамадол), антагонисты
(налоксон, налтрексон), гистаминовые (супрастин, кларитин, зиртек,
телфаст), аденозиновые (АТФ, дипиридамол, кофеин, теофиллин)
47.
3 тип. Рецепторы с тирозинкиназной активностью,рецепторы пептидных гормонов, регулирующих
рост, дифференцировку, развитие .
(рецепторы инсулина, глюкогона, гормонов
гипоталамуса, гипофиза, эритропоэтина и др.);
4 тип. Внутриклеточные рецепторы
(рецепторы стероидных, тиреоидных
гормонов, ретиноидов, витамина Д).
48.
49.
50.
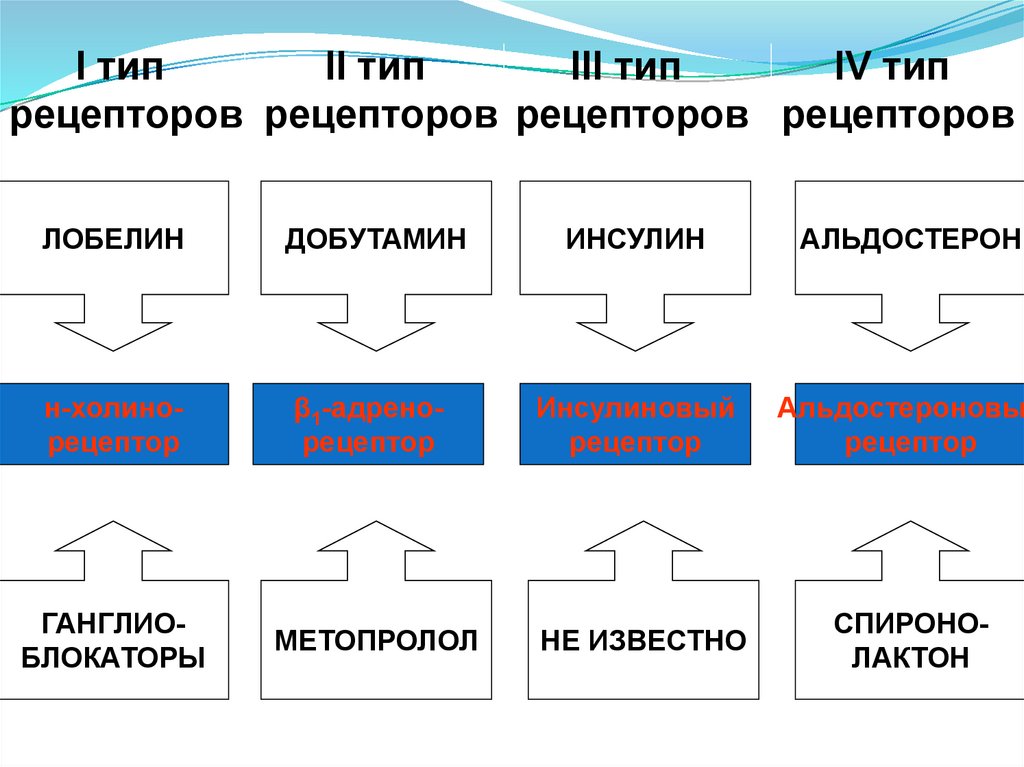
I типII тип
III тип
IV тип
рецепторов рецепторов рецепторов рецепторов
ЛОБЕЛИН
ДОБУТАМИН
ИНСУЛИН
АЛЬДОСТЕРОН
агонист
агонист
агонист
агонист
н-холинорецептор
β1-адренорецептор
Инсулиновый
рецептор
Альдостероновы
рецептор
антагонист
антагонист
антагонист
антагонист
ГАНГЛИОБЛОКАТОРЫ
МЕТОПРОЛОЛ
НЕ ИЗВЕСТНО
СПИРОНОЛАКТОН
51.
Типичные механизмы действия ЛС-Рецепторные взаимодействия:
Воздействие на активный центр рецептора (средства влияния
на ВНС, на потенциал зависимые и лиганд зависимые каналы)
Например: Рецептор 1-го типа – н-холинорецептор, при
связывании с ЛС расширяется канал, пронизывающий
мембрану, облегчается прохождение Na+, деполяризуется
мембрана.
Конформационные сдвиги регуляторных участков рецептора
(бензодиазепины, сердечные гликозиды)
-Угнетение или активация внутриклеточных или внеклеточных
ферментов (АХЭ средства, иАПФ, ИМАО)
-Взаимодействие с геномом (стероидные гормоны и их аналоги,
витамины А, D)
52.
Нерецепторные взаимодействия:-Нарушение структуры макромолекул
(противоопухолевые средства, иммунодепрессанты,
антибиотики, антисептики)
-Конкурентная блокада образования эндогенных
соединений (антиметаболиты)
-Субстратное усиление (леводопа)
-Прямое взаимодействие с эндогенными,
экзогенными соединениями (антациды,
хелатообразующие соединения, некоторые антидоты)
53.
Принципы дозирования ЛСЭффективная концентрация - концентрация препарата,
что обеспечивает наибольший терапевтический эффект.
Существует определенный диапазон эффективных
концентраций (терапевтический диапазон), нижней
границей которого является минимальная терапевтическая
концентрация, а верхней - максимально переносимая
(минимальная токсичная).
Для антибиотиков определяют минимальную угнетающую
концентрацию (МПК) для определенного типа
микрооргагизмив.
Целевая концентрация (ТС) - концентрация препарата в
плазме крови, которая будет обеспечивать требуемый
эффект.
54.
Доза - количество препарата, вводимого ворганизм пациента и выражается в весовых
единицах, объемных (для газов) или единицах
действия (для препаратов биологической природы).
Для более точного дозирования лекарств, дозы
рассчитываются с погрешностью на массу или
площадь поверхности тела. Для препаратов,
вводимых в / в, используют понятие скорость ввода определяет дозу препарата, который поступает в
организм за определенный промежуток времени (мкг
/ мин.)
Например: норэпинефрин 8-12мкг/мин,
поддерживающая 2-4 мкг/мин
55.
По влиянию на рецепторы ЛСделят на 3 типа
Агонисты - при связывании с рецептором активируют
его и вызывают эффекты, свойственные
естественным лигандам (стимулирующее влияние)
Антагонисты - при связывании с рецептором не
активируют его, но препятствуют действию
природных лигандов (блокирующее или
ингибирующее влияние)
Агонисты-антагонисты - имеют слабое
стимулирующее влияние на рецепторы, однако при
этом блокируют действие эндогенных активаторов.
56.
Особенности рецепторноговзаимодействия
Аффинитет - способность лиганда к связыванию с рецептором
(степень сродства с ним). Чем выше аффинитет, тем лучше
связывание с рецептором при одинаковых концентрациях (играет
важную роль при конкуренции лекарств за один и тот же
рецептор)
Эффективность (максимальная эффективность) - сила
фармакологического действия, зависит не от активности, а от
особенностей взаимодействия с рецепторами и работы
пострецепторных механизмов (вторичных посредников,
регуляторов). Максимальная эффективность определяет границу,
за которой дальнейшее увеличение дозы не вызывает прироста
обратной .
реакции.
Селективность - выборочное действие препаратов
57.
Виды действия ЛС на организмМестное действие означает эффект, который развивается в месте
введения или всасывание препаратов (антациды, гастроцитопротекторы,
ингаляционные кортикостероиды, бронхолитики, анестетики)
Рефлекторное действие означает, что лечебный эффект препаратов
опосредуется физиологическими реакциями нервной системы, которые
связанные, например, с раздражением чувствительных окончаний в
коже, слизистых оболочках или стенках сосудов (раздражающие,
отхаркивающие или слабительные средства)
Резорбтивное (системное) действие - эффект, развивающийся после
всасывания и попадания препаратов в кровь.
В отношении воздействия на нервную систему выделяют центральное
(на ЦНС) и периферическое (на другие звенья системы) действие ЛС.
Используют термины прямого или первичного и опосредованного или
вторичного действия.
58.
Характер, сила и длительностьдействия ЛС
По фармакологическим эффектам все ЛС можно разделить
на оказывающих специфическое и неспецифичное
действие.
Препараты неспецифичного действия вызывают широкий
спектр фармакологических эффектов: витамины, глюкоза,
аминокислоты, макро- и микроэлементы, адаптогены
растительного происхождения (препараты женьшеня,
элеутероккока).
Если ЛС влияет как агонист или антагонист на
рецепторные системы , его действие рааматривают как
специфичное ( например, атропин, атенолол)
59.
При введении ЛС возможны следующиереакции
Ожидаемый фармакологический ответ
Гиперреактивность- повышенная чувствительность
организма к вводимому ЛС
Толерантность – снижение чувствительности к
применяемому ЛС (при длительном приеме β2 –
адреномиметиков)
Идиосинкразия - непереносимость к данному ЛС
Тахифилаксия - быстро развившаяся толерантность (
к нитратам при непрерывном применении)
60.
Взаимосвязь между фармакокинетикой ифармакодинамикой
Концентрация ЛС в плазме крови зависит от
введенной дозы и определяется его
фармакокинетикой ( всасыванием,
распределением, биотрансформацией,
экскрецией), а последовательность
биологических реакций характеризует
фармакодинамику.
























































 Медицина
Медицина








