Похожие презентации:
Введение. Фармакокинетика и фармакодинамика лекарственных средств
1.
ГМУ г. СемейКафедра фармакологии имени д.м.н., профессора Мусина М.Н.
Лекция № 1
Тема: Введение. Фармакокинетика и фармакодинамика
лекарственных средств.
2018 - 2019 уч.г.
10.05.2024
1
2.
План лекции• Введение
• Основная часть
- Разделы фармакологии
-Принципы классификации лекарственных средств
-Фармакокинетика и фармакодинамика лекарственных
средств
- Взаимодействие и побочные эффекты лекарственных средств
• Заключение, контрольные вопросы, использованная
литература
10.05.2024
2
3.
Фармакология- это медико-биологическаянаука о действии ЛВ на живые организмы,
судьбе лекарств в организме, принципах
создания новых лекарственных средств.
От греческих слов pharmacon – лекарство, logos
– учение
10.05.2024
3
4.
Место фармакологии среди другихбиологических наук
• Фармакология оказывает влияние на развитие
физиологии и биохимии.
• Химиотерапия – лечение инфекций.
• Агрохимия – лечение растений.
• Ветеринарная (экспериментальная) фармакология –
лечение животных.
• Клиническая фармакология – лечение человека.
10.05.2024
4
5.
История фармакологии• Общее описание лекарственных средств и список около 400
лекарственных растений было дано в Древней Греции за 500 лет
до Гиппократа Диоскоридом
• Более подробное описание лекарственных средства было
проведено Гиппократом (377-460 до нашей эры)
• Клавдий Гален (127-200 гг. д. н. э.). описал лекарственные
растения, разработал различные формы и приемы изготовления
препаратов
• Абу-Али-Ибин Сина (Авиценна) (980 - 1037) Во втором томе
“Канона медицины ” приводится описание (с рисунками)
лекарственных растений, а в пятом томе способы применения
особо редких растений при различных болезненных состояниях…
10.05.2024
5
6.
• В IX в. арабы систематизировали и стандартизировалипрепараты. Были созданы книги по фармакопее.
• В XV в. в Италии издана первая печатная фармакопея,
затем в Англии и Франции (XVII в.), в России (XVIII в.), в
США (XIX в.).
• В середине XIX в. в Тарту организована первая
лаборатория экспериментальной фармакологии.
Внедрены средства для наркоза (эфир, хлороформ, закись
азота).
• В начале ХХ в. сформулированы основные принципы
химиотерапии инфекций, синтезирован
противосифилитический препарат сальварсан, витамин
В1, антиаритмик хинидин.
10.05.2024
6
7.
• В 20-е годы получен инсулин и пенициллин.• В 30-е годы установлено антибактериальное действие
сульфаниламидов.
• В 40-е годы внедрены в практику пенициллин, стрептомицин и
другие антибиотики.
• В 50-е годы созданы психотропные средства (аминазин,
мепробамат, имипрамин и др.), противодиабетические
таблетки, бета-блокаторы, анаболические стероиды,
противоопухолевые и контрацептивные средства.
• В 60-е годы -полусинтетическиепенициллины, цефалоспорины
и рифамицин. Получены блокаторы кальциевых каналов и
гистаминовых Н2-рецепторов, нестероидные
противовоспалительные средства, транквилизаторы.
10.05.2024
7
8.
• В 70-е годы внедряются в практику простагландины, блокаторыангиотензиновых рецепторов и ингибиторов
ангиотензинпревращающего фермента, протиивовирусный
препарат ацикловир, ингибиторы синтеза холестерина
(статины).
• В 80-е годы созданы противоязвенные препараты (омепразол),
выделены натрийуретические факторы, фибринолитик
(фибринолизин), получены фторхинолоны, препарат против
СПИДа (зидовудин), получен инсулин человека.
• В 90-е годы внедрены колониестимулирующие факторы,
избирательные ингибиторы циклооксигеназы-2, блокаторы
ангиотензиновых рецепторов (лозартан). Открыта роль окиси
азота (NO) в действии нитратов. Получены новые
цефалоспорины и макролиды.
• В 2015 г создан новый Казахстанский национальный формуляр
www.knf.kz
10.05.2024
8
9.
Современная История фармакологии• С ХVІІІ века в России начала развиваться фармацевтическая
наука. Первый учебник появился 1783 году под названием
«Врачебное веществословие или описание целительных
растений...» Н.Максимович-Амбодика.
• Основоположником российской фармаколгии является
Н.П.Кравков (1865-1924) написавший первый учебник
«Основа фармакологи» 1904 году.
• В начальный период Советской власти внесли большой вклад
в фармакологическую науку М.П.Николоаев, Н.В.Лазарев,
С.В.Аничков, В.В.Закусов и другие
10.05.2024
9
10.
• В последние годы авторами многих учебников пофармакологии были М.Д.Машковский (Лекарственные
средства), П.В.Сергеев (Молекулярлярная
фармакология) В.Г.Кукес (Клиническая фармакология),
Д.А.Харкевич (Фармакология) и др.
• В Республике Казахстан известны ученые профессора
фармакологи, члены НАН РК, академики
Р.С.Кузденбаева, И.Р.Кулмагамбетов и профессора
Д.Д.Мухамбетов, М.Н.Мусин, А.Е.Гуляев, С.К.Жаугашева,
Г.М.Пичхадзе, Х.Д.Рахимов, Н.Ж.Орманов,
Н.М.Мавлюдова, Т.М.Мажитов и др. внесшие вклад в
развитие фармакологической науки страны.
10.05.2024
10
11.
В нашем УниверситетеКафедра фармакологии организована в Семипалатинском
медицинском институте в 1955-1956 учебном году (Гребнева Л.А, А.А.
Алтымышев, который в последующем стал видным ученым, д.м.н.,
профессор, академик Киргизской Академии наук.
• С 1962 г. кафедрой руководил к.м.н., доцент К.О. Оралбаев,
• 1971 г. – д.м.н. профессор М.Д. Гаевый. Под их руководством был
защищены ряд диссертаций, основным направлением которых было
изучение фармакологии мозгового кровообращения.
• С 1975 по 1979 гг. кафедрой руководил к.м.н., доцент Е.О. Омарханов.
• С 1979 по 1980 гг. руководил кафедрой доцент С.П.Трофименко.
10.05.2024
11
12.
Мусин Марат Нукенович10.05.2024
• С 1980-2015 гг. кафедру фармакологии в
ГМУг.Семей возглавлял д.м.н., профессор, членкорреспондент Академии медицинских наук РК
Мусин Марат Нукенович.
• На кафедре с 1972 г.
• В 1975 году в г. Киев защитил кандидатскую
диссертацию на тему: «Фармакологическое
изучение полифенольного препарата, полученного
из мяты перечной»,
• В 1993 г. в г. Москва на базе института
фармакологии АМН СССР защитил докторскую
диссертацию на тему: «Фармакологическое
изучение противоаритмических свойств нового
класса соединений – 1,2-замещенных пирролов».
• Под его руководством защищены 2 докторские 5
кандидатских диссертаций, 2 магистерских 12
диссертаций
13.
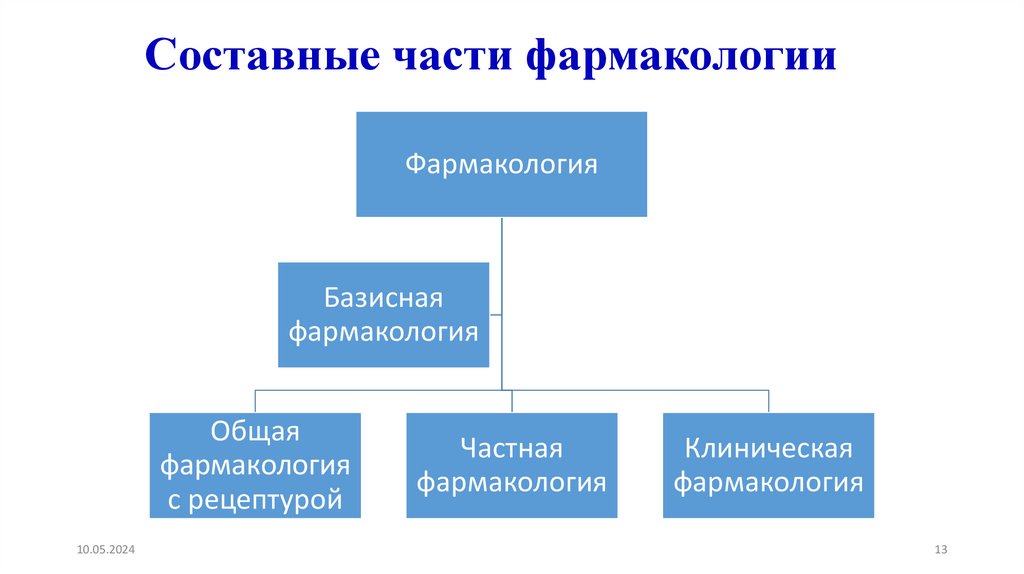
Составные части фармакологииФармакология
Базисная
фармакология
Общая
фармакология
с рецептурой
10.05.2024
Частная
фармакология
Клиническая
фармакология
13
14.
Лекарственное средство• Любое вещество, действующее на живой организм и
используемое для лечения, профилактики или
диагностики болезней.
• Вещество или их смесь, которые будучи введены в живой
организм, изменяют его функцию или функции (ВОЗ).
• Вещество, соответствующее международным стандартам,
допущенное государственным фармакологическим
комитетом для медицинского применения.
10.05.2024
14
15.
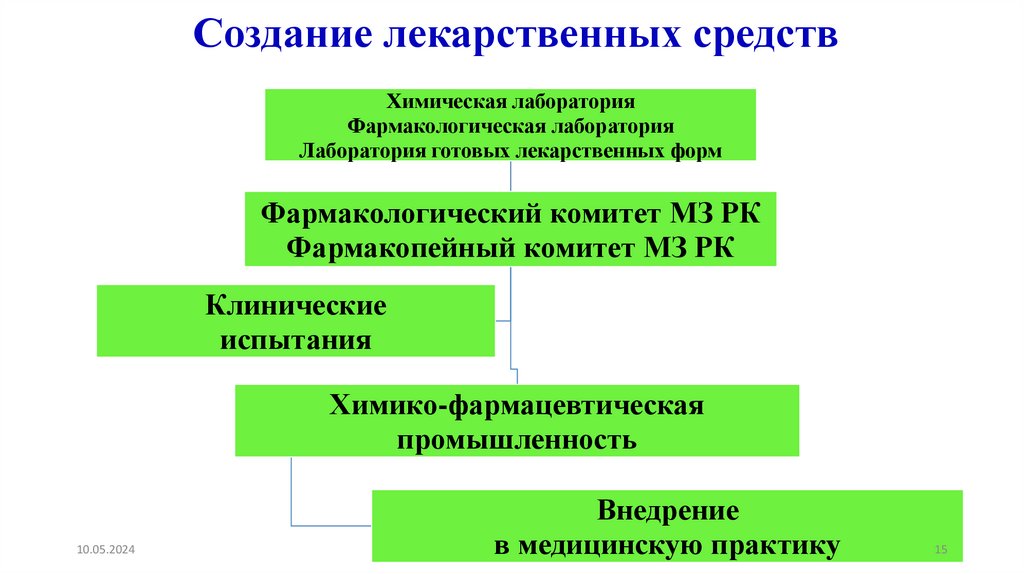
Создание лекарственных средствХимическая лаборатория
Фармакологическая лаборатория
Лаборатория готовых лекарственных форм
Фармакологический комитет МЗ РК
Фармакопейный комитет МЗ РК
Клинические
испытания
Химико-фармацевтическая
промышленность
10.05.2024
Внедрение
в медицинскую практику
15
16.
Поиск новыхЛС• Химический синтез
• Направленный синтез
• Воспроизведение биогенных веществ
• Создание антиметаболитов
• Модификация молекул известных средств
• Изучение структуры рецептора
• Синтез пролекарств
• Эмпирический путь
• Случайные находки
• Скрининг
• Выделение веществ из лекарственного сырья
• Животного происхождения (апипрепараты)
• Растительного происхождения
• Из минералов
• Биотехнология (клеточная и генная инженерия)
10.05.2024
16
17.
Фармакологическое исследование(экспериментальная фармакология)
• Изучение фармакодинамики веществ
• Специфическая активность
• Длительность эффекта
• Механизм действия
• Локализация действия
• Изучение фармакодинамики препарата
• Всасывание
• Распределение
• Метаболизм в организме
• Выведение
• Изучение безопасности
• Побочные эффекты
• Токсичность
• Тератогенность, мутагенность, канцерогенность
10.05.2024
17
18.
Принципы клинического испытания• Подбор популяции больных с точным диагнозом болезни
• Контрольная группа больных
• Аналогичные дозировки препаратов
• Фармакокинетические исследования
• Количественная оценка эффектов
• Использование плацебо и рандомизированного
исследования
• Сравнение с эталонными препаратами данной группы
• Соблюдение
этических принципов (информированное согласие больного)
10.05.2024
18
19.
Фазы клинического испытания лекарств1 фаза. На группе здоровых добровольцев устанавливаются
оптимальные дозировки, исследуются всасываемость, метаболизм
и период полувыведения.
2 фаза. На 100-200 больных изучают фармакодинамику,
фармакокинетику и побочные эффекты.
3 фаза. Рандомизированное контролируемое испытание на
тысячах больных с целью изучения эффективности и безопасности
лекарства, уточнения показаний и противопоказаний.
4 фаза. Широкое исследование на большом количестве больных
побочных эффектов и токсичности препарата.
10.05.2024
16
19
20.
Основные разделы фармакологии• Общая фармакология изучает общие закономерности
взаимодействия лекарственных веществ с живыми организмами.
• Частная фармакология рассматривает отдельные
фармакологические группы и препараты.
• Фармакодинамика изучает механизм действия лекарства и
фармакологические эффекты.
• Фармакокинетика изучает всасывание, метаболизм,
распределение, связь с белками и выведение лекарства.
• Показания к применению и возможные побочные эффекты
отдельных препаратов.
10.05.2024
17
20
21.
Принципы классификации ЛС• Системный принцип
• Средства, регулирующие функции нервной системы
• Средства, регулирующие функции исполнительных
органов и их систем
• Средства, регулирующие процессы обмена веществ
• По патологическим процессам
• Средства для лечения атеросклероза
• Средства для лечения воспаления
• Средства для лечения инфекций
• Средства для лечения опухолей
10.05.2024
18
21
22.
Классификация ЛС• Классификация по алфавиту (В основу этой классификации положен
принцип размещения наименований лекарственных средств в
алфавитном порядке русский и латинский языки).
• Химическая классификация. (В основе ее лежит химическая структура
лекарственных веществ. Например, производные имидазола: бендазол,
клотримазол, метронидазол; производные фенотиазина: хлорпромазин,
этапиразин; производные
метилксантина: кофеин, теофиллин,
теобромин).
• Фармакологическая классификация. (Делятся на разряд - классы –
группы – подгруппы)
• Фармакотерапевтическая классификация. (В ее основу положены
заболевания, при которых применяются конкретные лекарственные
средства)
• Классификация CAS (Chemical Abstracts Service).
(Например,
Регистровый номер CAS азитромицина 83905-01-5)
10.05.2024
22
23.
Фармакокинетика (ФК )Изучает движение ЛВ в организме, то есть:
- пути введения,
- всасывание,
- распределение,
- депонирование,
- метаболическое превращение (биотрансформация),
- выведение (элиминация).
• ФК греческое слово, PHARMACON - лекарство, KINEO
- двигать.
10.05.2024
23
24.
Пути введения ЛС• Энтеральные ( через рот, под язык, ректально)
• Парентеральные ( в/в, в/а, в/м, п/к, в/к, ингаляции,
интратекальное или субарахноидальное введение,
местное применение, внутриматочное, введение в
мочевой пузырь, внутрибрюшинное и т.д.
10.05.2024
24
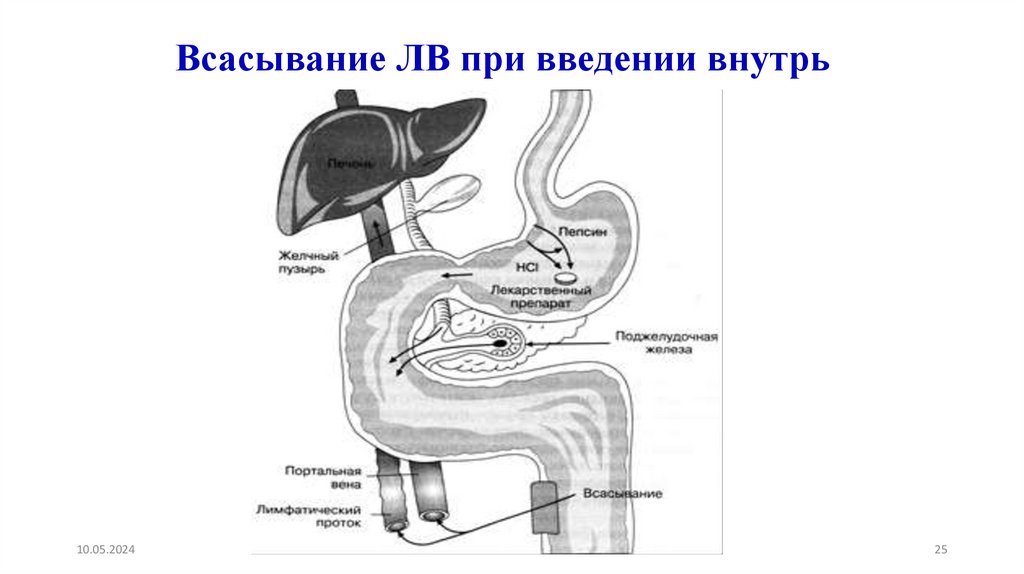
25.
Всасывание ЛВ при введении внутрь10.05.2024
25
26.
АБСОРБЦИЯ– (ABSORBEO – всасываю) называется прохождение,
проникновение лекарств через биологические мембраны.
Механизмы абсорбции:
Известны несколько механизмов, посредством которых ЛС
преодолевают тканевые барьеры.
1 группа - ПАССИВНЫЕ МЕХАНИЗМЫ, осуществляемые по
градиенту концентрации веществ (из мест с большим
концентрационным потенциалом в область более низкой
концентрации), без затраты энергии;
2 группа - АКТИВНЫЙ ТРАНСПОРТ ЛС, в отличии от пассивных
механизмов, с затратой метаболической энергии и может
осуществляется против градиента концентрации.
10.05.2024
26
27.
Основные способы проникновения веществ черезбиологические мембраны
Rang H.P.et al. Pharmacology. – Ln, 2003, с изм.
10.05.2024
27
28.
Пассивные механизмы абсорбции1.Фильтрация через поры мембран, через каналы
(облегченная диффузия) – пассивная диффузия через
«водные поры» для молекул с массой 100-150
Дальтон (вода, литий, этанол, мочевина)
2. Второй путь пассивная диффузия – по градиенту
концентрации путем растворения в липидах
мембран. Для липофильных, малоионизированных
и недиссоциированных лекарств.
10.05.2024
28
29.
Константа ионизации рКа• Если ЛВ при значениях pH, свойственных средам
организма,
находится
главным
образом
в
неионизированном виде (то есть в липофильной
форме) оно хорошо проникает через биологические
мембраны.
• Величина pKa - это тот показатель pH, при котором
диссоциирует 50% молекул вещества.
• Этот показатель определяет степень диссоциации
ксенобиотика, то есть чужеродного организму
соединения.
10.05.2024
29
30.
Формула Гендерсона-Гассельбаха:• степень диссоциации (ионизации) определяется согласно
формуле Хендерсона-Хассельбаха:
• а) ДЛЯ СЛАБЫХ КИСЛОТ:
неионизированная форма
lg ---------------------------------------------- = pKa - pH;
ионизированная форма
• б) ДЛЯ СЛАБЫХ ОСНОВАНИЙ:
ионизированная форма
lg------------------------------------------------ = pKa - pH.
неионизированная форма
10.05.2024
30
31.
• Аспирин слабая кислота (pKa = 3, 5) Хорошо всасывается в желудке и плохо вкишечнике, т.к. рН в желудке 1,5-2,5 в 12пк 5,0-6,0, в тонком кишечнике 8,0.
• Стрептомицин, канамицин - это ЛС со свойствами сильных щелочей, поэтому
всасывание их из желудочно-кишечного тракта незначительно и непостоянно.
Вводятся только парентерально.
• Некоторые ЛС практически полностью инактивируются ферментами ЖКТ.
(белковые или полипептидные вещества: кортикотропин, вазопрессин,
инсулин и др.), а также некоторые гормональные препараты (прогестерон,
тестостерон, альдостерон).
• Соли желчных кислот могут ускорить всасывание или замедлить его при
образовании нерастворимых комплексов (например, нистатин, полимиксин,
ванкомицин).
Вывод: Те лекарства, которые не проникают через липидный слой клеток,
необходимо вводить только внутривенно.
10.05.2024
31
32.
АКТИВНЫЙ ТРАНСПОРТ.• всасывание происходит с помощью специальных носителей переносчиков, белков-ферментов или транспортных белков.
• перенос аминокислот (сахаров, пиримидиновых оснований)
через гематоэнцефалический барьер, плаценту,
• слабых кислот - в проксимальных канальцах почек.
Пиноцитоз.
• ЛС с молекулярной массой свыше 1000 Дальтон, входят в клетку
путем поглощения внеклеточного материала мембранными
везикулами
( вит В12- цианокобаламин, ЛС с полипептидной структурой, с
внутренним фактором Касла, белки, жирные кислоты,
жирорастворимые витамины А,Д,Е,К)
10.05.2024
32
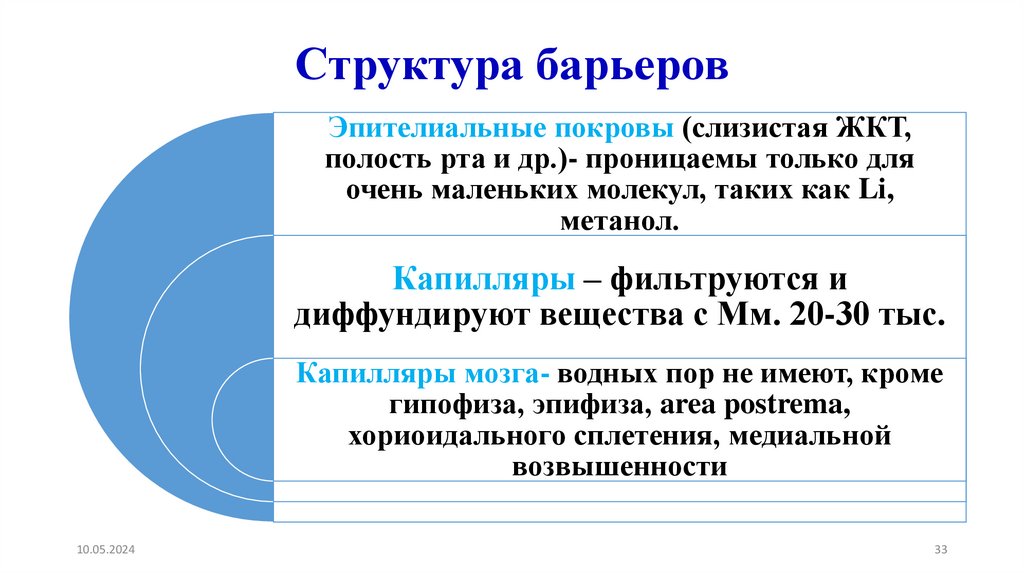
33.
Структура барьеровЭпителиальные покровы (слизистая ЖКТ,
полость рта и др.)- проницаемы только для
очень маленьких молекул, таких как Li,
метанол.
Капилляры – фильтруются и
диффундируют вещества с Мм. 20-30 тыс.
Капилляры мозга- водных пор не имеют, кроме
гипофиза, эпифиза, area postrema,
хориоидального сплетения, медиальной
возвышенности
10.05.2024
33
34.
Выводы:• Всасывание гидрофильных, ионизированных веществ
через эпителий слизистых оболочек ограничено
• Эти соединения могут свободно входить и выходить из
кровеносного русла по законам диффузии (кроме
леводопа, который проникает в клетку с помощью
активного транспорта)
• Их выведение осуществляется почками.
10.05.2024
34
35.
Диффузия в липидахОсновной механизм переноса через клеточную мембрану
( эпителий, клетки органов-мишеней)
Осуществляется пассивно.
Движущая сила – броуновское движение молекул
Основные условия – растворимость в липидах
- градиент концентрации
Ограничения – очень низкая растворимость в воде, эти молекулы
не могут образовать общей фазы с водой вне мембраны.
10.05.2024
35
36.
Выводы:1. Диффузии в липидах легко подвергаются
жирорастворимые неполярные вещества, трудно –
гидрофильные вещества и ионы.
2. Жирорастворимые неполярные вещества хорошо
проникают через ГЭБ и плаценту
3. В почках они подвергаются обратной реабсорбции в
кровь
10.05.2024
36
37.
РАСПРЕДЕЛЕНИЕ ЛВ В ОРГАНИЗМЕ• Гидрофильность
• Липофильность
• Интенсивность регионарного кровотока.
Гистогематические барьеры:
• Гематоэнцефалический
• Гематоофтальмический
• Гематотестикулярный
• Плацентарный
10.05.2024
37
38.
ДЕПОНИРОВАНИЕ ЛВ В ОРГАНИЗМЕДЕПОНИРОВАНИЕ - это обратимое связывание ЛВ с
белками, фосфолипидами и нуклеопротеинами клеток.
Л В + белок <=> комплекс ЛВ-белок.
• клеточные депо - за счет связывания лекарственного
вещества
с
внутриклеточными
белками,
нуклепротеидами, фосфолипидами.
• жировые депо – за счет липофильности некоторых
средств
10.05.2024
38
39.
БИОТРАНСФОРМАЦИЯ ЛВ• Биотрансформация (метаболизм) — изменение химической
структуры лекарственных веществ и их физико-химических
свойств под действием ферментов организма.
Основные виды метаболизма ЛВ:
• несинтетические реакции (метаболическая трансформация) окисление, восстановление, гидролиз;
• синтетические реакции (конъюгация) - конъюгация с остатком
серной кислоты, конъюгация с остатком глюкуроновой кислоты,
конъюгация
с
остатками
α-аминокислот
(глицином,
глутамином), метилирование, ацетилирование.
10.05.2024
39
40.
Несинтетические реакцииа) Основная группа реакций, по которым биотрансформируются
большинство лекарственных средств, это реакции катализируемые
ферментами эндоплазматического ретикулума гепатоцитов или
МИКРОСОМАЛЬНЫЕ реакции;
б) Реакции, катализируемые ферментами
НЕМИКРОСОМАЛЬНЫЕ реакции.
10.05.2024
другой
локализации,
40
41.
Синтетические реакции- образование парных эфиров ЛС с глюкуроновой, серной, уксусной
кислотами, а также с глицином и глутатионом.
Происходит создание высокополярных соединений, которые:
А) хорошо растворимы в воде,
Б) мало растворимы в липидах,
В) плохо проникающих в ткани,
Г) в большинстве случаев фармакологически неактивны.
10.05.2024
41
42.
ВЫВЕДЕНИЕ ЛВ ИЗ ОРГАНИЗМА• Основные пути экскреции : почки, печень, ЖКТ, легкие, кожа,
слюнные железы, потовые железы, молоко матери.
• Почечная экскреция ( клубочковая фильтрация, активная секреция в
проксимальных канальцах и канальцевая реабсорбция) .
• Выведение через желудочно-кишечный тракт
• Совокупность процессов, в результате которых активное
лекарственное вещество удаляется из организма называется
элиминация,
которое
объединяет
два
процесса:
биотрансформацию и выведение.
• Количественно процесс
элиминации характеризуется рядом
фармакокинетических параметров.
10.05.2024
42
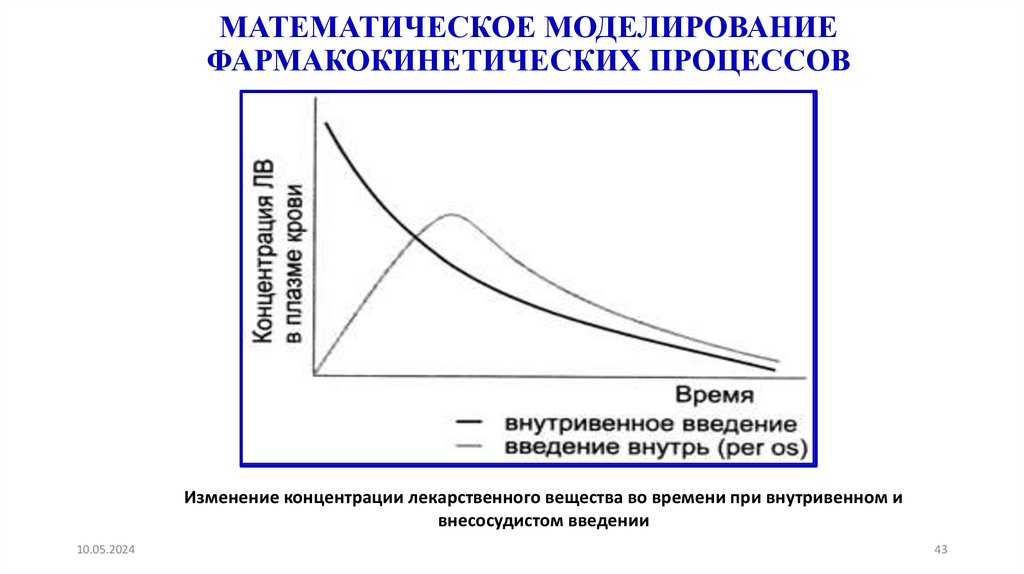
43.
МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕФАРМАКОКИНЕТИЧЕСКИХ ПРОЦЕССОВ
Изменение концентрации лекарственного вещества во времени при внутривенном и
внесосудистом введении
10.05.2024
43
44.
Однокамерная фармакокинетическая модель.Vd (volume of distribution) – объем распределения вещества в камере;
D – количество вещества, введенное в камеру;
Со – начальная концентрация вещества в камере.
10.05.2024
44
45.
Кажущийся объем распределения• гипотетический объем жидкости организма, в
котором лекарственное вещество распределено
равномерно и при этом находится в концентрации,
равной концентрации данного вещества в плазме
крови (Ср).
• Vd = Q/Cp
• где Q - количество вещества в организме при
концентрации в плазме крови Ср.
10.05.2024
45
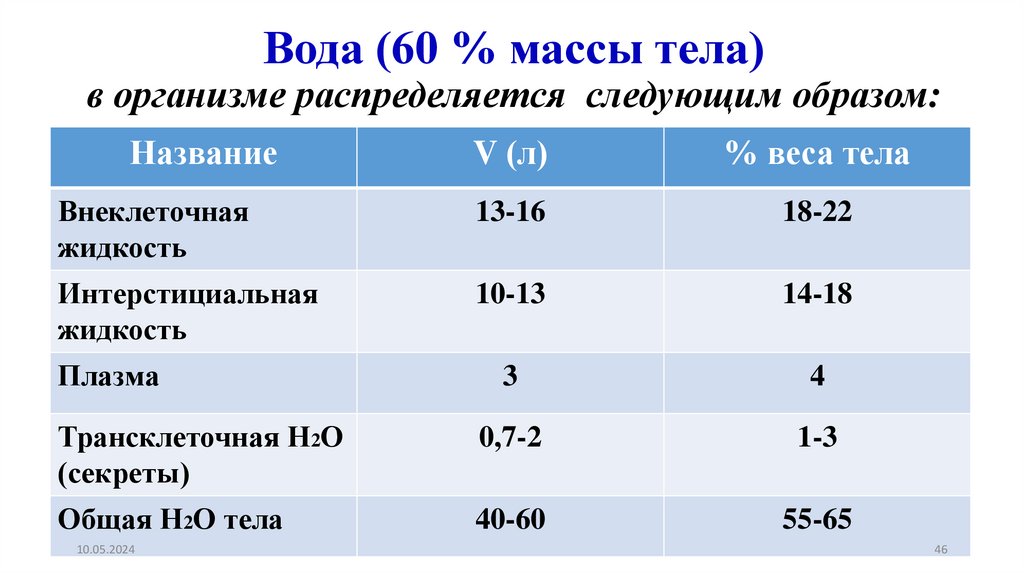
46.
Вода (60 % массы тела)в организме распределяется следующим образом:
Название
V (л)
% веса тела
Внеклеточная
жидкость
13-16
18-22
Интерстициальная
жидкость
10-13
14-18
3
4
Трансклеточная Н2О
(секреты)
0,7-2
1-3
Общая Н2О тела
40-60
55-65
Плазма
10.05.2024
46
47.
Выводы:Показывает, в каком соотношении распределяется вещество между
жидкостями
организма
(плазмой
крови,
интерстициальной,
внутриклеточной жидкостями).
если величина Vd какого-либо вещества имеет значение,
приблизительно равное 3 л (средний объем плазмы крови), значит,
данное вещество преимущественно находится в плазме крови (гепарин,
Vd около 4л) - 1 вариант.
Если Vd = 15 л (сумма средних объемов плазмы крови и
интерстициальной жидкости), вещество преимущественно находится в
плазме крови и интерстициальной жидкости (во внеклеточной
жидкости), гидрофильное и не проникает внутрь клеток – 2 вариант.
Если Vd = 40 л (средний объем всех жидкостей организма)- значит ЛВ
находятся как во внеклеточной, так и во внутриклеточной жидкостях
организма, т.е. проникают через мембраны клеток. В основном так
распределяются в организме липофильные неполярные соединения- 3
вариант.
10.05.2024
47
48.
Варианты объема распределения:1-й вариант:
Vd= VН2О – препарат равномерно распределяется в водных
отсеках
Клиническое значение:
Дозирование препрата должно осуществляться с учетом
массы тела
В случае предозировки препарата объективным
диагностическим критерием служит определение его
содержания в плазме крови
Гемодиализ при интоксикациях – эффективная мера
На доклиническом этапе нет смысла проводить исследования
по его накоплению в различных органах и тканях
10.05.2024
48
49.
Варианты объема распределения:2-й вариант:
• Vd ≤ VН2О – секвестрация в плазме и
межклеточной жидкости
Клиническое значение:
дозирование
препарата
осуществляется
относительно «идеальной массы тела» без учета
излишков веса
Интоксикации препаратами с очень маленьким
объемом распределения редки .
10.05.2024
49
50.
Варианты объема распределения:3 -й вариант:
Vd ≥ VН2О – секвестрация в тканях ( в частности
депонирование)
Клиническое значение:
дозирование препарата осуществляется с учетом массы тела
В случае интоксикации определение его концентрации в плазме
крови не является объективным критерием
Гемодиализ неэффективен
Препараты способны к кумуляции
Доклинические исследования должны включать эксперименты
по «поиску»мест депонирования препарата
10.05.2024
50
51.
Факторы влияющие на Vd :1. На скорость распределения:
-проницаемость мембран
-скорость кровотока
Центральная камера: кровь и хорошо кровоснабжаемые
органы (почки, мозг, легкие, надпочечники, печень, сердце,
селезенка, ЩЖ)
Периферическая камера: мышцы, слизистые оболочки, кожа,
жировая, костная ткани, волосы, ногти
2. На степень распределения:
- липофильность/гидрофильность
- степень ионизации
- степень связывания с белками крови
- внутриклеточное связывание
10.05.2024
51
52.
ЭлиминацияЭто снижение концентрации ЛВ путем двух процессов:
биотрансформации и экскреции.
Для большинства лекарственных веществ скорость
элиминации зависит от концентрации вещества (чем
меньше концентрация вещества, тем меньше скорость
элиминации).
Основные параметры, характеризующие процесс
элиминации: константа скорости элиминации (kel, ke ) и
период полуэлиминации (t1/2).
10.05.2024
52
53.
ЭлиминацияКлиренс – константа, индивидуальная для каждого вещества
скорость
элимин.
к-во/время
объем
CL= ------------- = ---------------- = ---------------- = мл/час (л/час)
концентр.
к-во/ объем
время
Клиренс – объем распредленеия, освобождающийся от
вещества за единицу времени
Клиренс – главный параметр для управления режимом
дозирования
Клиренс аддитивен: CL общ= CL поч + CL печ.+ CL др .
10.05.2024
53
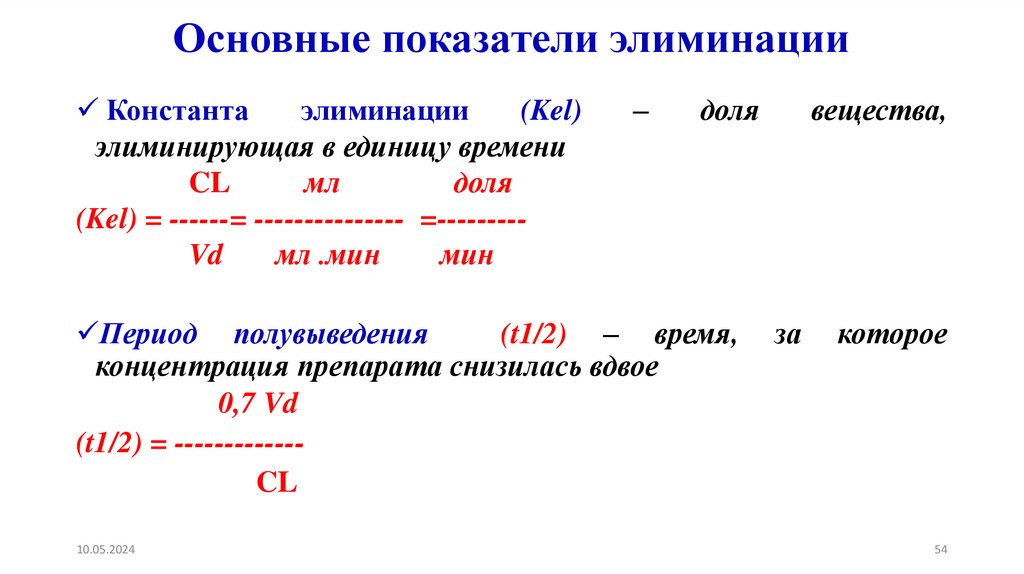
54.
Основные показатели элиминацииКонстанта
элиминации
(Kel)
элиминирующая в единицу времени
CL
мл
доля
(Kel) = ------= --------------- =--------Vd
мл .мин
мин
–
доля
Период полувыведения
(t1/2) – время,
концентрация препарата снизилась вдвое
0,7 Vd
(t1/2) = ------------CL
10.05.2024
вещества,
за
которое
54
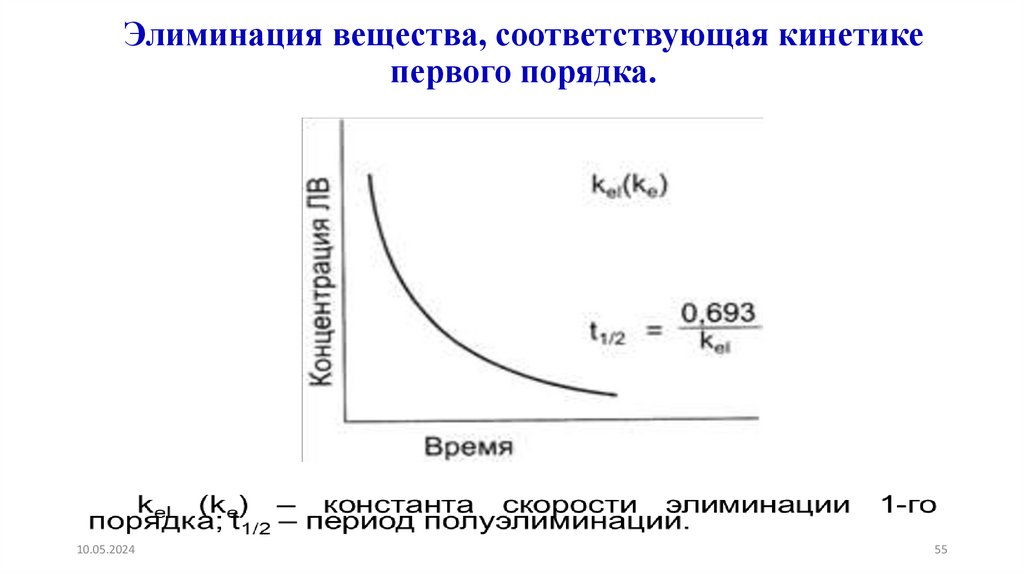
55.
Элиминация вещества, соответствующая кинетикепервого порядка.
10.05.2024
55
56.
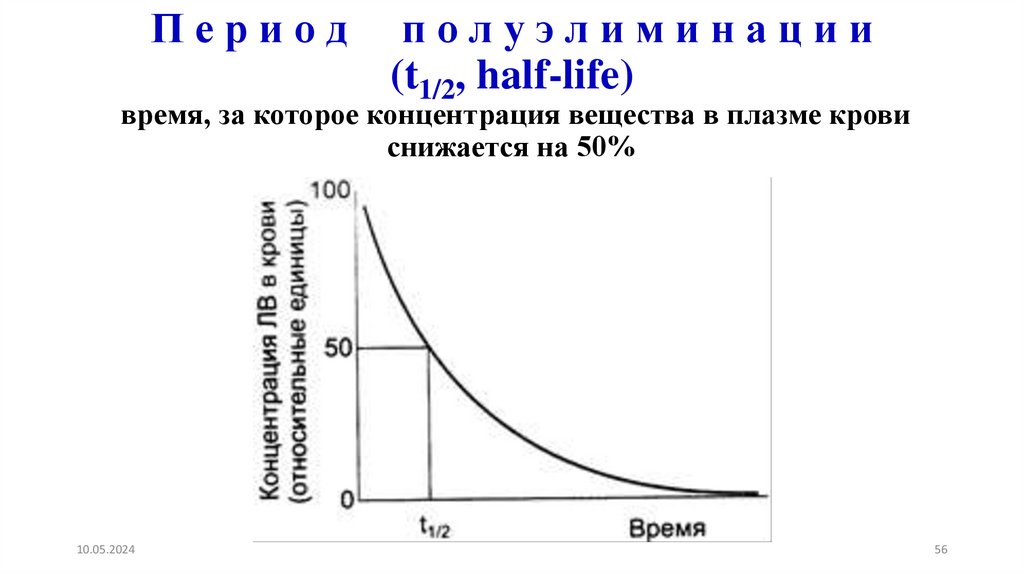
Периодполуэлиминации
(t1/2, half-life)
время, за которое концентрация вещества в плазме крови
снижается на 50%
10.05.2024
56
57.
Клиническое значение (t1/2)Служит для определения интервала дозирования
препаратов
Можно прогнозировать время наступления эффекта
при назначении ПД препарата
Служит ориентиром для установления времени
прекращения действия и выведения препарата из
организма
10.05.2024
57
58.
Двухкамерная фармакокинетическая модель.10.05.2024
58
59.
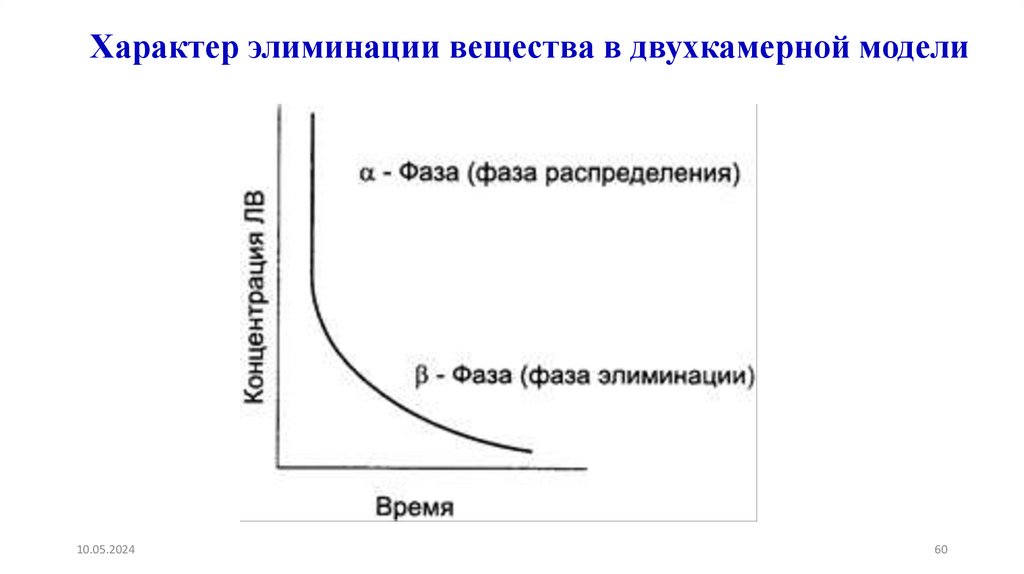
В этой модели организм представляют в виде двух сообщающихся междусобой камер. Одна из камер этой модели называется центральной и представляет
плазму крови и хорошо перфузируемые органы (сердце, печень, почки, легкие), а
другая, называемая периферической, представляет плохо перфузируемые ткани
(кожу, жировую, мышечную ткани).
Вещество вводят в центральную камеру, где оно мгновенно и равномерно
распределяется и откуда затем проникает в периферическую камеру. Этот период
обозначается как фаза распределения, или α-фаза. Затем вещество
перераспределяется из периферической камеры в центральную и удаляется из
нее вследствие элиминации. Эта фаза (фаза элиминации) обозначается как βфаза. α-Фаза характеризуется параметром, который называется периодом
полураспределения — t1/2α, а характеристикой β-фазы является собственно
период полуэлиминации, обозначаемый как t1/2β. Период полураспределения, как
правило, меньше периода полуэлиминации, так как вещество распределяется из
центральной камеры в периферическую быстрее, чем элиминируется.
10.05.2024
59
60.
Характер элиминации вещества в двухкамерной модели10.05.2024
60
61.
Клиренсфармакокинетический параметр, который характеризует скорость
освобождения организма от лекарственного вещества
различают метаболический (Clmet) и экскреторный клиренс (Сехсг) .
системный (общий) клиренс (Clt, total cleance): Clmet+ Cexcr = Clt.
Clt численно равен объему распределения, который освобождается
от вещества в единицу времени (размерность — объем в единицу
времени, например, мл/мин, л/ч, иногда с учетом массы тела,
например, мл/кг/мин): Clt = Vdkel.
Clt = Скорость элиминации вещества
C
где С - это концентрация ЛВ
10.05.2024
61
62.
Почечный клиренс ЛСМеханизмы:
• Фильтрация (мм < 65000)
• Активная секреция в проксимальных канальцах
• Реабсоорбция
Фильтрация- основной механизм выведения
Фильтруются не связанные с белками формы ЛС. Зависист от
фильтрационной способности почек и кровотока
Лимитирующий фактор – размер молекул (мм не более 65000)
• Скорость фильтрации определяют по клиренсу креатинина (норома
80-120 мл/мин)
• Гемодиализ «воспроизводит» процесс гломерулярной фильтрации
10.05.2024
62
63.
Почечный клиренс (продолжение)Секреция
осуществляется в проксимальных тубулах с участием переносчиков
Энергозависисма (активный процесс) против градиента концентрации
Эффективна для ионизированных соединений
Конкуренция за переносчики между ЛС
Угнетается ингибиторами энергетического обмена
Лимитируется возможностями транспортных систем
Реабсорбция
Осуществляется в дистальных канальцах
Реабсорбируются неполярные липофильные вещества
Важное значение имеет рН мочи
10.05.2024
63
64.
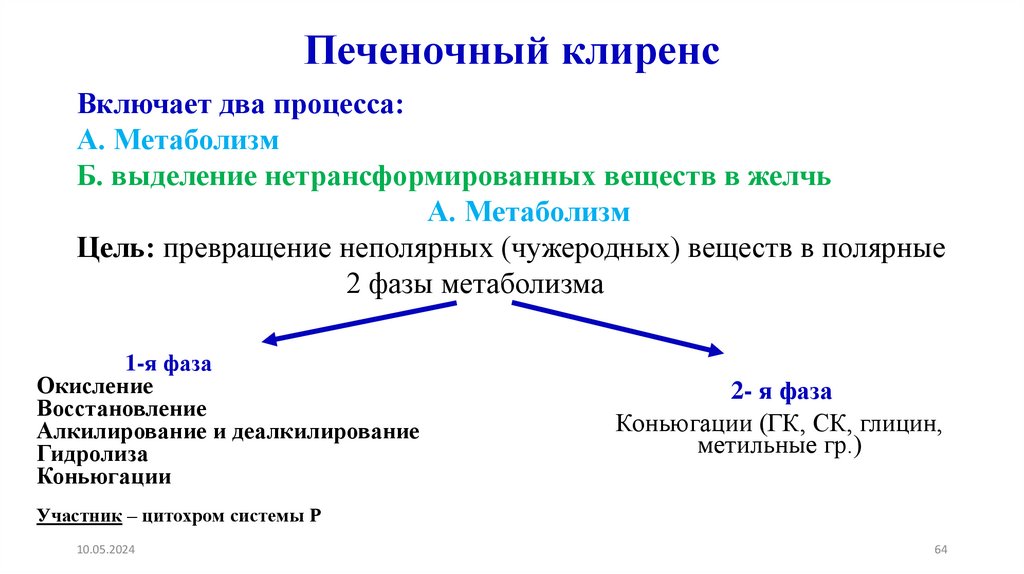
Печеночный клиренсВключает два процесса:
А. Метаболизм
Б. выделение нетрансформированных веществ в желчь
А. Метаболизм
Цель: превращение неполярных (чужеродных) веществ в полярные
2 фазы метаболизма
1-я фаза
Окисление
Восстановление
Алкилирование и деалкилирование
Гидролиза
Коньюгации
2- я фаза
Коньюгации (ГК, СК, глицин,
метильные гр.)
Участник – цитохром системы Р
10.05.2024
64
65.
Печеночный клиренс (продолжение)Б. Секреция ЛС в желчь
механизмы транспорта
- Простая диффузия
- Активный транспорт ( в меньшей степени)
Факторы, влияющие на экскрецию ЛС в желчь:
-высокая мм (> 250000)
-состояние печени и ЖВП
-связь с биополимерами печеночной клетки
-скорость печеночного кровотока
Секретируются: кислоты, основания, неионогенные вещества
Энтерогепатическая циркуляция
10.05.2024
65
66.
Ситуации, изменяющие клиренс ЛС в организме:• Взаимодействие ЛС
Конкуренция за секреторные механизмы
Конкуренция за метаболические процессы
Неспецифическая индукция метаболических процессов
Ингибирование систем метаболизма ЛС
Конкуренция за связь с белками
• Болезни:
Печени
Почек
ЖКТ
Эндокринных органов (приводят к снижению Vd и CL
• Индивидуальные особенности организма (генетические,
природные)
10.05.2024
66
67.
Основные сценарии элиминации ЛС (итог):1. Гидрофильные соединения выводятся почками в
неизмененном виде
2. Липофильные полярные соединения – выводятся с
желчью в кишечник. Могут подвергаться
энтерогепатической циркуляции.
3. Липофильные неполярные соединения –
реабсорбируются в почках, поступают в кровоток и
подвергаются печеночному метаболизму, приобретая
гидрофильные свойства, чтобы выделиться
почками .
10.05.2024
67
68.
Принципы дозирования ЛСПеременные:
1. Разовая доза- количество вещества, вводимое в организм за
один прием
2. Способ введения – адекватен целям
3. Интервал введения
4. Время достижения стационарной концентрации
5. Время полной элимимнации после прекращения введения
Основные методы введения ЛС:
• Постоянный в/в с контролем скорости введения
• Прерывистый (оральный, подкожный, в/м, в/в)
Цели введения:
достижение стационарнной концентрации вещества в
организме и поддержание ее необходимый период.
10.05.2024
68
69.
Различают 2 вида доз:Вводная ( нагрузочная) – доза, которая одномоментно обеспечивает
С ss
LD (вводная доза)= C ss *V / F
! Нагрузочная доза нужна для достижения объема распределения в
действующей концентрации
Поддерживающая доза, необходимая для поддержания
действующей концентрации в интервалы времени между
введениями
ПД (поддерживающая) =Css*Cl*T/F
! Она компенсирует потери клиренса за интервал между
введениями.
10.05.2024
69
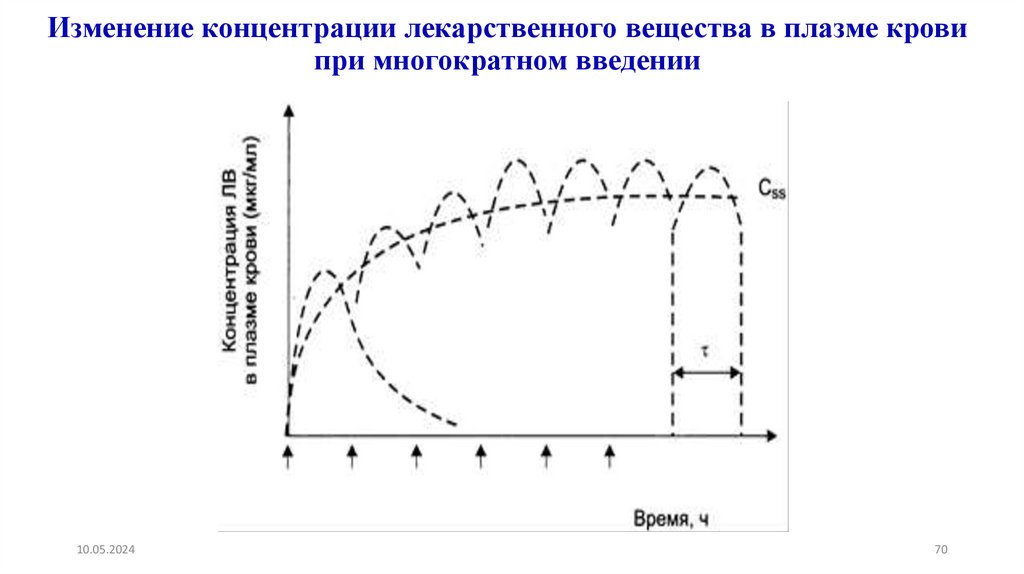
70.
Изменение концентрации лекарственного вещества в плазме кровипри многократном введении
10.05.2024
70
71.
Выводы:1. Точка стационарности достигается на 4-5 t ½
2. Время достижения Css и время элиминации равны
3. Время достижения Css не зависит от дозы
Клиническое значение выводов:
прогнозируемость времени наступления эффекта
пропуск одной дозы приводит к снижению концентрации на 50
%, а для ее достижения понадобится 3-4 t ½
прогнозируемость сроков выведения препарата из организма
Возможность увеличения безопасности
10.05.2024
71
72.
Биодоступность и биоэквивалентность• Биодоступность (F) это часть введенной дозы
лекарственного вещества (при внесистемных
способах введения), которая в неизмененном виде
достигла системного кровотока.
Выражается в процентах (при в/в 100%)
• Биоэквивалентность. Два лекарственных препарата
(в одинаковой лекарстенной форме ) являются
биоэквивалентными , если обеспечивают одинаковую
биодоступность и одинаковую скорость достижения
максимальной концентрации лекарственного
вещества в крови
10.05.2024
72
73.
Определение биодоступности лекарственного веществапри введении внутрь.
AUCвнутрь
F
100%
AUCв / в
где F - биодоступность (Fraction);
AUC – площадь под кривой концентрация-время
(Area Under the Curve).
10.05.2024
73
74.
ФАРМАКОДИНАМИКА (ФД)Это
раздел
фармакологии,
изучающий
действие
лекарственных средств на организм.
ФД изучает:
1) механизмы действия (то есть сущность процессов
взаимодействия
с
тканевыми,
клеточными
или
субклеточными рецепторами.
2) фармакологические эффекты (то есть содержание и
изменения влияния препарата в зависимости от возраста, пола
больного, характера и течения заболевания, сопутствующей
патологии),
3)
локализацию
действия
лекарств
–
места
преимущественного действия в организме.
10.05.2024
74
75.
Основные «мишени» для лекарственных веществ:• рецепторы;
• ионные каналы;
• ферменты;
• транспортные системы.
10.05.2024
75
76.
РецепторыСвойства и виды рецепторов. Взаимодействие рецепторов с
ферментами и ионными каналами
Известны 4 вида рецепторов, первые три из которых являются
мембранными рецепторами:
1)Рецепторы, непосредственно сопряженные с ферментами.
2)Рецепторы, непосредственно сопряженные с ионными
каналами
3) Рецепторы, взаимодействующие с G-белками.
4)Рецепторы,
регулирующие
транскрипцию
ДНК
10.05.2024
76
77.
Связывание вещества с рецептором.Понятие об аффинитете
• Рецепторы в фармакологическом плане представляют
собой
функциональные
биохимические
макромолекулярные
мембранные
структуры,
избирательно чувствительные к действию определенных
химических соединений (ЛС).
• Сродство
или
аффинитет
означает
способность
лекарственного вещества к связи с рецептором
• Взаимодействие лекарственных веществ с рецептором
приводит к возникновению ряда биохимических и
физиологических изменений в организме, которые
выражаются в том или ином эффекте
10.05.2024
77
78.
Внутренняя активность лекарственного средства• Способность ЛС вызывать фармакологический эффект после
взаимодействия с рецептором, обозначается как внутренняя
активность лекарственного средства или его эффективность.
• Агонисты (от греч. agonistes - соперник, agon — борьба) или
миметики — вещества, обладающие аффинитетом и внутренней
активностью.
• Полные агонисты, взаимодействуя с рецепторами, вызывают
максимально возможный эффект.
• Частичные агонисты при взаимодействии с рецепторами
вызывают эффект, меньший максимального.
10.05.2024
78
79.
• Антагонисты (от греч. antagonisma - соперничество, anti - против,agon — борьба) - вещества, обладающие аффинитетом, но
лишенные внутренней активности
• Они связываются с рецепторами и препятствуют действию на
рецепторы эндогенных агонистов (нейромедиаторов, гормонов).
Поэтому их также называют блокаторами рецепторов.
• Если антагонисты занимают те же рецепторы, что и агонисты,
антагонизм называют конкурентным, а антагонисты называются
конкурентными антагонистами.
• Если антагонисты занимают другие участки макромолекулы, не
относящиеся к специфическому рецептору, но взаимосвязанные с
ним, то их называют неконкурентными антагонистами.
• Некоторые лекарственные вещества сочетают способность
стимулировать один подтип рецепторов и блокировать другой.
Такие вещества обозначают как агонисты –антагонисты
(пентазоцин).
10.05.2024
79
80.
Другие «мишени» для лекарственных веществ• Одной из основных «мишеней» для лекарственных веществ
являются потенциалзависимые ионные каналы, которые
избирательно проводят Na+, Ca2+, К+ и другие ионы через
клеточную мембрану.
• Многие лекарственные вещества являются ингибиторами
ферментов.
• ЛС могут действовать на транспортные белки, которые
переносят молекулы некоторых веществ или ионы через
мембраны клеток.
• Перспективной «мишенью» для лекарственных средств
являются гены.
10.05.2024
80
81.
ВИДЫ ДЕЙСТВИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ• Местное и резорбтивное,
• Рефлекторное,
• Прямое и косвенное,
• Основное и побочное,
• Центральное и периферическое
• Избирательное,
• Обратимое и необратимое
10.05.2024
81
82.
ВЛИЯНИЕ РАЗЛИЧНЫХ ФАКТОРОВ НА ФАРМАКОДИНАМИКУИ ФАРМАКОКИНЕТИКУ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
СВОЙСТВА ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
СВОЙСТВА ОРГАНИЗМА
РЕЖИМ НАЗНАЧЕНИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
А. Повторное применение лекарственных веществ
Б. Комбинированное применение и взаимодействие
лекарственных веществ
ХРОНОФАРМАКОЛОГИЯ
10.05.2024
82
83.
СВОЙСТВА ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ• химическая структура,
• физико-химические свойства,
• дозы
• концентрации лекарственных веществ.
• Д о з а (от греч. dosis - порция) — количество лекарственного
вещества на один при-ем.
• Дозы приводят в весовых или объемных единицах.
• Дозы можно выражать в виде количества вещества на 1 кг
массы тела или на 1 м2 поверхности тела (например, 1 мг/кг, 1
мг/м2).
10.05.2024
83
84.
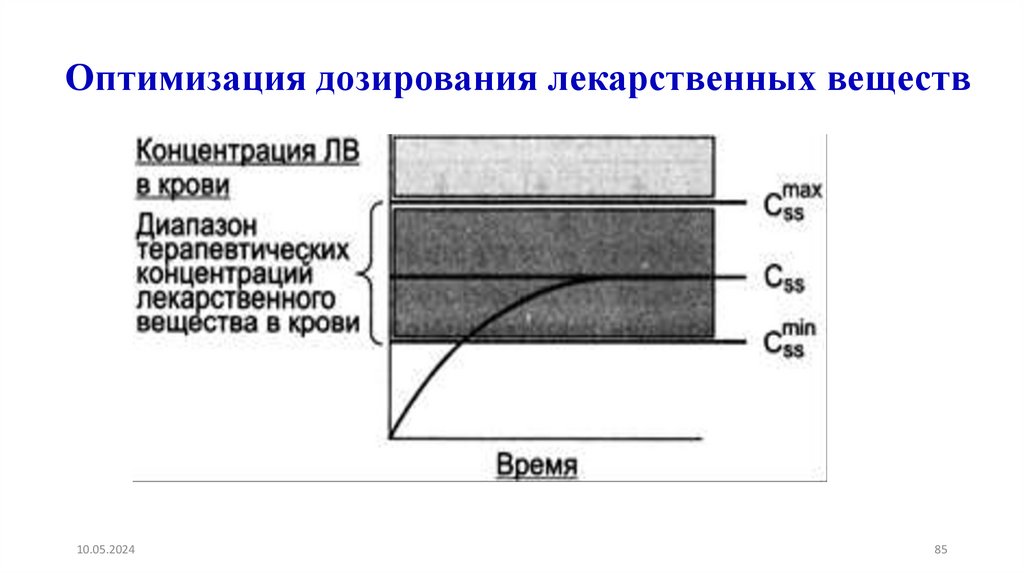
Различают дозы:Терапевтические:
-минимальные действующие (пороговые) ,
-средние терапевтические: разовая доза (pro dosi), суточная
доза (pro die).
- высшие терапевтические дозы.
Токсические - оказывающие токсическое действие на
организм,
Летальные дозы -вызывающие смертельный исход,
называются летальными (от лат. letum — смерть)…
10.05.2024
84
85.
Оптимизация дозирования лекарственных веществ10.05.2024
85
86.
Повторное применение лекарственных веществКумуляция (от лат. cumulatio — увеличение, скопление) — накопление в
организме фармакологически активного вещества или вызываемых им
эффектов.
Сенсибилизация- образование комплексов ЛС с белками плазмы крови,
которые при определенных условиях приобретают антигенные свойства.
Это сопровождается образованием антител и сенсибилизацией.
Привыкание (толерантность, от лат. tolerantia - терпение) — уменьшение
фармакологического эффекта при повторных введениях лекарственного
вещества в одной и той же дозе.
Тахифилаксия (от греч. tachys — быстрый, phylaxis — защита) - быстрое
развитие привыкания при повторных введениях препарата через короткие
промежутки времени (10—15 мин).
Лекарственная зависимость — настоятельная потребность (непреодолимое стремление) в постоянном или периодически возобновляемом
приеме определенного лекарственного вещества или группы веществ
10.05.2024
86
87.
Комбинированное применениеи взаимодействие ЛВ
• Синергизм (от греч. syn — вместе, erg — работа) —
однонаправленное действие двух или нескольких ЛВ, при котором
наблюдается более выраженный фармакологический эффект, чем у
каждого вещества в отдельности.
• Суммирование, или аддитивное действие - если эффект от
одновременного применения одинаково действующих ЛВ равен
сумме эффектов отдельных веществ, входящих в комбинацию.
• Антагонизм (от греч. ariti- против, agon — борьба) — уменьшение
или полное устранение фармакологического эффекта одного
лекарственного вещества другим при их совместном применении.
10.05.2024
87
88.
Виды взаимодействияфармацевтическое взаимодействие;
фармакологическое взаимодействие.
а) Фармакокинетический вид взаимодействия
б)Фармакодинамический вид взаимодействия
Зная эти механизмы врач может рекомендовать:
принимать лекарственные препараты не одновременно, а с интервалами в
30-40-60 мин;
заменить один из лекарственных препаратов на другой;
изменить режим дозирования препаратов (изменить дозу и интервалы между
введениями);
отменить один из препаратов (если первые три действия не устраняют
негативных последствий взаимодействия одновременно назначенной
комбинации препаратов).
10.05.2024
88
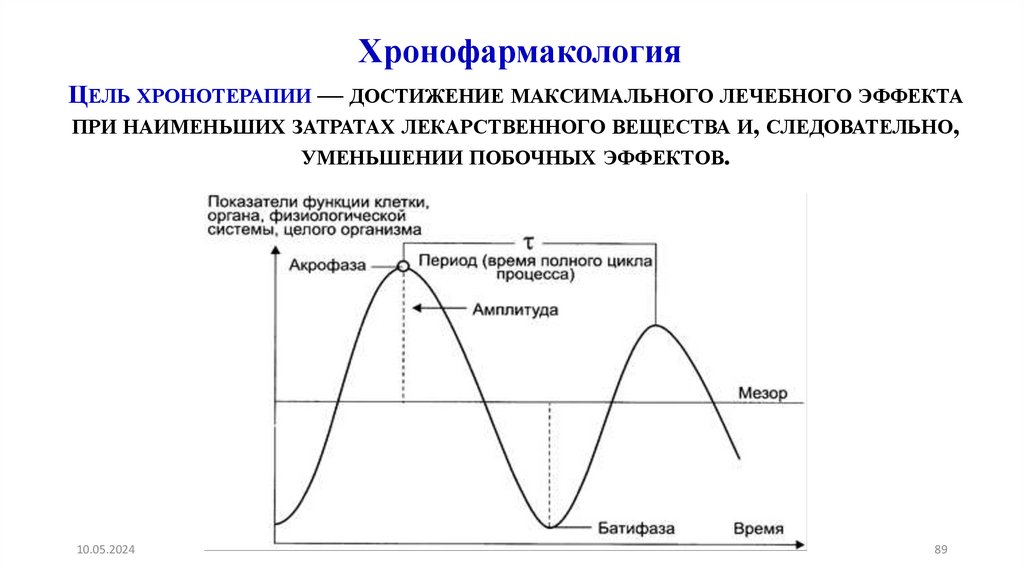
89.
ХронофармакологияЦЕЛЬ ХРОНОТЕРАПИИ — ДОСТИЖЕНИЕ МАКСИМАЛЬНОГО ЛЕЧЕБНОГО ЭФФЕКТА
ПРИ НАИМЕНЬШИХ ЗАТРАТАХ ЛЕКАРСТВЕННОГО ВЕЩЕСТВА И, СЛЕДОВАТЕЛЬНО,
УМЕНЬШЕНИИ ПОБОЧНЫХ ЭФФЕКТОВ.
10.05.2024
89
90.
10.05.202490
91.
Контрольные вопросы• Какие разделы фармакологии вам известны?
• Что означают показатели: Co, Vd, t ½
• Клиническое значение знаний фармакокинетики и
фармакодинамики.
10.05.2024
91













































































 Медицина
Медицина








