Похожие презентации:
Возможности терапии хронического лимфолейкоза. Взгляд на таргетную терапию
1.
ВОЗМОЖНОСТИТЕРАПИИ ХЛЛ. ВЗГЛЯД НА
ТАРГЕТНУЮ ТЕРАПИЮ
ОНЛАЙН ЛЕКЦИЯ:
ВОЗМОЖНОСТИ ТЕРАПИИ ХЛЛ. ВЗГЛЯД
НА ТАРГЕТНУЮ ТЕРАПИЮ
Григорьев Кирилл
Александрович
Врач гематолог
ГБУЗ НСО Областная
клиническая больница г.Новосибирск
,
Представлена только информация в рамках зарегистрированных в РФ показаний.
Лекция при поддержке компании АстраЗенека. Мнение лектора не всегда может совпадать с точкой зрения компании АстраЗенека.
Презентация подготовлена с использованием материалов конгресса Поймай волну в терапии ХЛЛ и МКЛ, Иркутск, 14-15 июня 2024 г.
CAL-RU-536-11-24 Дата одобрения: 30.10.2024 Дата истечения: 30.10.2026
Новосибирск
06.11.2024
2.
ХРОНИЧЕСКИЙ ЛИМФОЦИТАРНЫЙ ЛЕЙКОЗ (ХЛЛ) – ЭТО В-КЛЕТОЧНАЯОПУХОЛЬ ИЗ МАЛЫХ В-ЛИМФОЦИТОВ. ХЛЛ ТРЕБУЕТ ДЛИТЕЛЬНОГО
ЛЕЧЕНИЯ, ПОЭТОМУ ПЕРЕНОСИМОСТЬ – ОДИН ИЗ ВАЖНЕЙШИХ
ФАКТОРОВ ПРИ ВЫБОРЕ ЛЕКАРСТВЕННОЙ ТЕРАПИИ6
Медиана возраста на момент
установления диагноза1
62 года
≈90% пациентов
при выявлении ХЛЛ
старше 55 лет1,2
89
%
пациентов на момент
установления
диагноза имели
≥1 сопутствующих
заболеваний3
ХЛЛ в настоящее время
остается неизлечимым
заболеванием5
При назначении терапии
длительное динамическое
наблюдение рекомендовано
для всех пациентов1,4
* Исходная сопутствующая патология оценивалась путем анализа базы данных ХЛЛ клиники Мейо, включавшей данные 1195 пациентов с диагнозом ХЛЛ и лимфомой из малых лимфоцитов (ЛМЛ), которые были
зарегистрированы в период между январем 1995 г. и декабрем 2006 г.; среди этих пациентов 373 (31%) были местными/не направленными из других учреждений пациентами, включенными для анализа.3
1. Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний, под редакцией проф. Поддубной И.В., проф. Савченко В.Г., Москва, 2018. Сайт «Lymphoma Coalition».
https://www.lymphomacoalition.org/images/subtype-reports/CLL_Global_2017_Report.pdf. Дата обращения: 21.03.2024. 3. Thurmes P et al. Leuk Lymphoma. 2008;49(1):49-56. 4. World Health Organization.
https://www.who.int/selection_- medicines/committees/expert/20/applications/CLL.pdf. Дата обращения: 21.03.2024. 5. Бахтина В.И., Демко И.В., Кравченко С.К., Протопопова Е.Б. ХРОНИЧЕСКИЙ ЛИМФОЛЕЙКОЗ // Современные
проблемы науки и образования. – 2016. – № 3. 6. Электронный ресурс: https://www.astrazeneca.com/media-centre/press-releases/2019/calquence-significantly-prolonged-the-time-patients-lived-without-disease-progression-or-death-inpreviously-untreated-chronic- lymphocytic-leukaemia.html Дата обращения: 21.03.2024
3.
КОГДА НУЖНОНАЗНАЧАТЬ
ТЕРАПИЮ ХЛЛ?
4.
ТЕРАПИЯ ХЛЛ/ЛМЛ ДОЛЖНА НАЧИНАТЬСЯ ПРИНАЛИЧИИ КАК МИНИМУМ 1 ИЗ СЛЕДУЮЩИХ
ПОКАЗАНИЙ ПО КРИТЕРИЯМ IWCLL
1. Стадия С по J.L. Binet
2. Один или более симптомов интоксикации:
• потеря >10 % массы тела за 6 месяцев (если пациент не принимал меры для похудания)
• слабость (общее состояние по ECOG ≥2, нетрудоспособность)
• субфебрильная лихорадка в течение ≥2 недель без признаков инфекции
• ночные поты, сохраняющиеся более 1 месяца без признаков инфекции
3. Нарастающая анемия и/или тромбоцитопения, обусловленная инфильтрацией костного мозга
4. Аутоиммунная анемия и/или тромбоцитопения, резистентная к преднизолону
5. Большие размеры селезенки (>6 см ниже реберной дуги), явное увеличение органа
6. Массивная (≥10 см в максимальном диаметре) и/или нарастающая лимфаденопатия
7. Время удвоения числа лимфоцитов менее 6 мес
8. Экстранодальное поражение, симптомное или влияющее на функцию пораженного органа
J.L. Binet-стадирование заболевания ХЛЛ, ECOG-оценка общего состояния пациента по шкале, разработанной Восточной объединенной онкологической группой (Eastern Cooperative Oncology Group) , IWCLL- Международная рабочая
группа по изучению хронического лимфоцитарного лейкоза
Hallek M. et al. iwCLL guidelines for diagnosis, indications for treatment, response assessment, and supportive management of CLL // Blood. American Society of Hematology, 2018. Vol. 131, № 25. P. 2745–2760
5.
НАЛИЧИЕ СОПУТСТВУЮЩИХ ЗАБОЛЕВАНИЙ ВАЖНОУЧИТЫВАТЬ ДЛЯ ПОДБОРА ОПТИМАЛЬНОЙ ТЕРАПИИ ХЛЛ1-3
46 %
45%
Гипертензия
Ревматологические
патологии / болезнь
суставов
16
13%
%
Заболевания коронарных
и периферических
сосудов
Заболевания сердца
(кардиомиопатия, порок
клапана сердца,
мерцательная аритмия)
1. Thurmes PL, Call T, Slager S. Comorbid conditions and survival in unselected, newly diagnosed patients with chronic lymphocytic leukemia. Leuk Lymphoma 2008;49(1):49-56. 2. Strati P, Parikh SA, Chaffee KG, et al. Relationship between
co-morbidities at diagnosis, survival and ultimate cause of death in patients with chronic lymphocytic leukaemia (CLL): a prospective cohort study. Br J Haematol. 2017;178(3):394-402. 3. Клинические рекомендации Хроническая болезнь
почек (ХБП) 2021 https://cr.minzdrav.gov.ru/recomend/469_2 Дата обращения: 20.03.2024.
6.
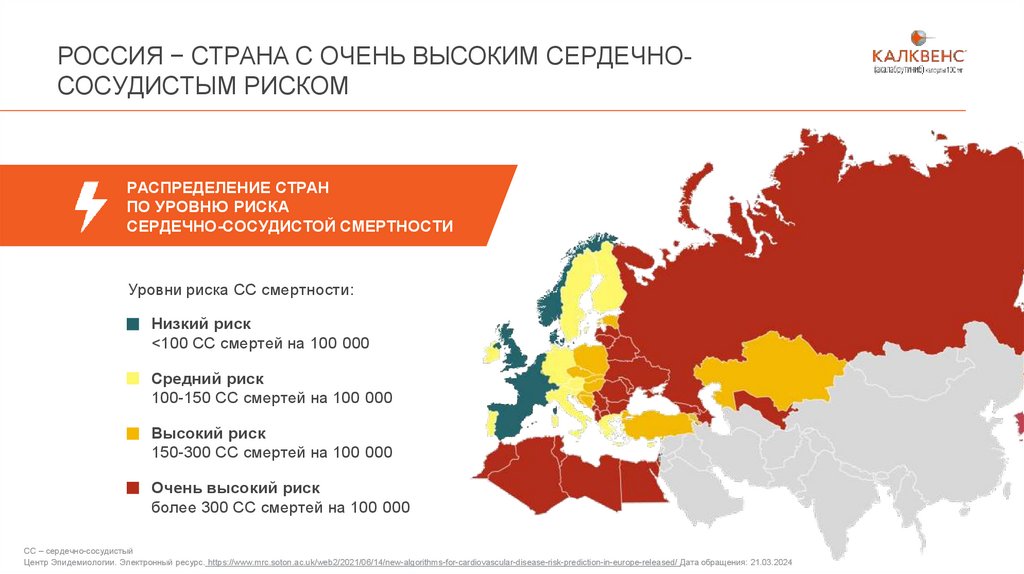
РОССИЯ − СТРАНА С ОЧЕНЬ ВЫСОКИМ СЕРДЕЧНОСОСУДИСТЫМ РИСКОМРАСПРЕДЕЛЕНИЕ СТРАН
ПО УРОВНЮ РИСКА
СЕРДЕЧНО-СОСУДИСТОЙ СМЕРТНОСТИ
Уровни риска СС смертности:
Низкий риск
<100 СС смертей на 100 000
Средний риск
100-150 СС смертей на 100 000
Высокий риск
150-300 СС смертей на 100 000
Очень высокий риск
более 300 СС смертей на 100 000
СС – сердечно-сосудистый
Центр Эпидемиологии. Электронный ресурс. https://www.mrc.soton.ac.uk/web2/2021/06/14/new-algorithms-for-cardiovascular-disease-risk-prediction-in-europe-released/ Дата обращения: 21.03.2024
7.
МЕЖДУНАРОДНЫЙ КОНСЕНСУС ПО УПРАВЛЕНИЮСЕРДЕЧНО-СОСУДИСТЫМ РИСКОМ ПРИ ПРИМЕНЕНИИ ИБТК
ПРИ ХЛЛ (2022)
ВЫБОР ТЕРАПИИ
Пациенты без факторов СС риска
Пациенты с СС риском
(например, контролируемая гипертония
или фибрилляция предсердий)
Любой таргетный препарат
(иБТК или иBCL2)
Рассмотреть выбор более селективного
иБТК 2 поколения (акалабрутиниб или др)
Если есть любые опасения по безопасности
терапии, то выбор в пользу более селективного
иБТК 2 поколения (акалабрутиниб или др)
СС – сердечно-сосудистый, иБТК – ингибитор тирозинкиназы Брутона, BCL2-белок В-клеточный лимфомы
Awan FT, Addison D, Alfraih F, Baratta SJ, Campos RN, Cugliari MS, Goh YT, Ionin VA, Mundnich S, Sverdlov AL, Tam C, Ysebaert L. International consensus statement on the management of cardiovascular risk of Bruton's tyrosine kinase
inhibitors in CLL. Blood Adv. 2022 Sep 27;6(18):5516-5525. doi: 10.1182/bloodadvances.2022007938. PMID: 35790105; PMCID: PMC9631706.
8.
РЕКОМЕНДАЦИИ NCCN (ВЕРСИЯ 1.2024)РЕКОМЕНДОВАННЫЕ РЕЖИМЫ ТЕРАПИИ ХЛЛ
без делеции 17p/ мутации TP53
ПЕРВАЯ ЛИНИЯ ТЕРАПИИ
ПРЕДПОЧТИТЕЛЬНЫЕ РЕЖИМЫ
• Акалабрутиниб ± обинутузумаб
(категория 1)
• Венетоклакс + обинутузумаб
(категория 1)
ДРУГИЕ РЕКОМЕНДОВАННЫЕ РЕЖИМЫ
• Ибрутиниб (категория 1)
• Ибрутиниб + обинутузумаб (категория 2В)
• Ибрутиниб + ритуксимаб (категория 2В)
• Ибрутиниб + венетоклакс (категория 2В)
• Занубрутиниб*
(категория 1)
Все комбинации с ИХТ были перемещены из категории
«другие рекомендованные режимы» в категорию
«в отдельных случаях»
В ОТДЕЛЬНЫХ СЛУЧАЯХ
(можно рассмотреть для
IGHV- мутированных пациентов,
<65 лет без значительной коморбидности)
• FCR
• Бендамустин + анти-CD-20 терапия
• Обинутузумаб ± хлорамбуцил
• Высокодозный метилпреднизолон +
анти-CD-20 терапия
Ибрутиниб был перемещен из списка предпочтительных схем в список
других рекомендуемых схем.
Добавлена соответствующая сноска: Консенсус группы по включению
ибрутиниба в категорию «другие рекомендованные режимы» основан на
профиле токсичности.
Перед началом лечения ибрутинибом следует провести исходную
оценку сердечной функции.
IGHV- вариабельные участки тяжелых цепей иммуноглобулинов, FCR-флударабин+циклофосфамид+ритуксимаб
* Планируется к регистрации в РФ.
NCCN Guidelines version 1.2024. Доступно онлайн: https://www.nccn.org/professionals/physician_gls/pdf/cll.pdf Дата: 1.12.2023
9.
РЕКОМЕНДАЦИИ NCCN (ВЕРСИЯ 1.2024)РЕКОМЕНДОВАННЫЕ РЕЖИМЫ ТЕРАПИИ ХЛЛ
с делецией 17p/ мутацией TP53
ПЕРВАЯ ЛИНИЯ ТЕРАПИИ
ПРЕДПОЧТИТЕЛЬНЫЕ РЕЖИМЫ
• Акалабрутиниб ± обинутузумаб
(категория 1)
ДРУГИЕ РЕКОМЕНДОВАННЫЕ РЕЖИМЫ
• Ибрутиниб (категория 1)
• Ибрутиниб + венетоклакс (категория 2В)
• Венетоклакс + обинутузумаб
(категория 1)
• Занубрутиниб*
(категория 1)
иТКБ-ингибитор тирозинкиназы Брутона
* Планируется к регистрации в РФ
NCCN Guidelines version 1.2024. Доступно онлайн: https://www.nccn.org/professionals/physician_gls/pdf/cll.pdf Дата: 1.12.2023
Все комбинации с ИХТ были перемещены из категории
«другие рекомендованные режимы» в категорию
«в отдельных случаях»
В ОТДЕЛЬНЫХ СЛУЧАЯХ
(можно рассмотреть, когда иТКБ м венетоклакс
недоступны или противопоказаны или
необходимо достичь быстрого уменьшения
объема заболевания)
• Высокодозный метилпреднизолон +
анти-CD-20 терапия
• Обинутузумаб
10.
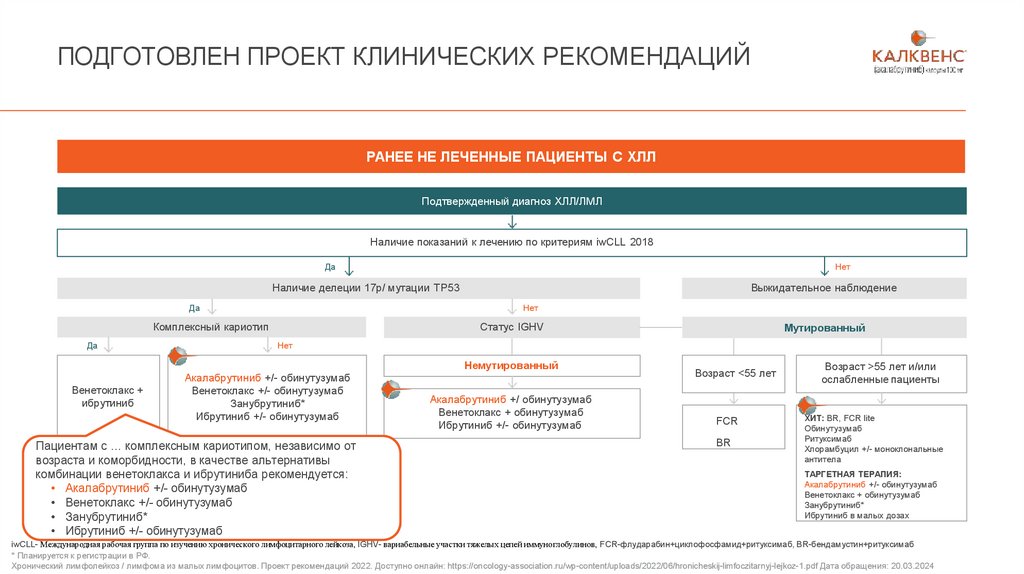
ПОДГОТОВЛЕН ПРОЕКТ КЛИНИЧЕСКИХ РЕКОМЕНДАЦИЙРАНЕЕ НЕ ЛЕЧЕННЫЕ ПАЦИЕНТЫ С ХЛЛ
Подтвержденный диагноз ХЛЛ/ЛМЛ
Наличие показаний к лечению по критериям iwCLL 2018
Да
Нет
Наличие делеции 17p/ мутации TP53
Да
Нет
Комплексный кариотип
Да
Выжидательное наблюдение
Статус IGHV
Нет
Немутированный
Венетоклакс +
ибрутиниб
Мутированный
Акалабрутиниб +/- обинутузумаб
Венетоклакс +/- обинутузумаб
Занубрутиниб*
Ибрутиниб +/- обинутузумаб
Пациентам с … комплексным кариотипом, независимо от
возраста и коморбидности, в качестве альтернативы
комбинации венетоклакса и ибрутиниба рекомендуется:
• Акалабрутиниб +/- обинутузумаб
• Венетоклакс +/- обинутузумаб
• Занубрутиниб*
• Ибрутиниб +/- обинутузумаб
Акалабрутиниб +/ обинутузумаб
Венетоклакс + обинутузумаб
Ибрутиниб +/- обинутузумаб
Возраст <55 лет
FCR
BR
Возраст >55 лет и/или
ослабленные пациенты
ХИТ: BR, FCR lite
Обинутузумаб
Ритуксимаб
Хлорамбуцил +/- моноклональные
антитела
ТАРГЕТНАЯ ТЕРАПИЯ:
Акалабрутиниб +/- обинутузумаб
Венетоклакс + обинутузумаб
Занубрутиниб*
Ибрутиниб в малых дозах
iwCLL- Международная рабочая группа по изучению хронического лимфоцитарного лейкоза, IGHV- вариабельные участки тяжелых цепей иммуноглобулинов, FCR-флударабин+циклофосфамид+ритуксимаб, BR-бендамустин+ритуксимаб
* Планируется к регистрации в РФ.
Хронический лимфолейкоз / лимфома из малых лимфоцитов. Проект рекомендаций 2022. Доступно онлайн: https://oncology-association.ru/wp-content/uploads/2022/06/hronicheskij-limfoczitarnyj-lejkoz-1.pdf Дата обращения: 20.03.2024
11.
ИНГИБИТОРЫ ТИРОЗИНКИНАЗЫ БРУТОНА ПОКАЗЫВАЮТВЫСОКИЕ РЕЗУЛЬТАТЫ В ТЕРАПИИ ХЛЛ
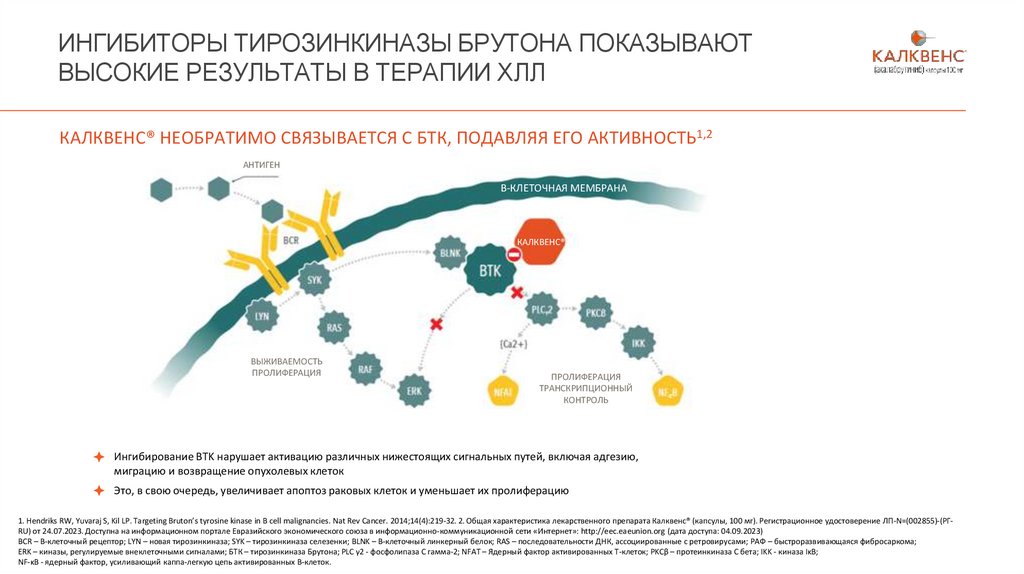
КАЛКВЕНС® НЕОБРАТИМО СВЯЗЫВАЕТСЯ С БТК, ПОДАВЛЯЯ ЕГО АКТИВНОСТЬ1,2
АНТИГЕН
В-КЛЕТОЧНАЯ МЕМБРАНА
КАЛКВЕНС®
ВЫЖИВАЕМОСТЬ
ПРОЛИФЕРАЦИЯ
ПРОЛИФЕРАЦИЯ
ТРАНСКРИПЦИОННЫЙ
КОНТРОЛЬ
Ингибирование BTK нарушает активацию различных нижестоящих сигнальных путей, включая адгезию,
миграцию и возвращение опухолевых клеток
Это, в свою очередь, увеличивает апоптоз раковых клеток и уменьшает их пролиферацию
1. Hendriks RW, Yuvaraj S, Kil LP. Targeting Bruton’s tyrosine kinase in B cell malignancies. Nat Rev Cancer. 2014;14(4):219-32. 2. Общая характеристика лекарственного препарата Калквенс® (капсулы, 100 мг). Регистрационное удостоверение ЛП-N=(002855)-(РГRU) от 24.07.2023. Доступна на информационном портале Евразийского экономического союза в информационно-коммуникационной сети «Интернет»: http://eec.eaeunion.org (дата доступа: 04.09.2023)
BCR – В-клеточный рецептор; LYN – новая тирозинкиназа; SYK – тирозинкиназа селезенки; BLNK – В-клеточный линкерный белок; RAS – последовательности ДНК, ассоциированные с ретровирусами; РАФ – быстроразвивающаяся фибросаркома;
ERK – киназы, регулируемые внеклеточными сигналами; БТК – тирозинкиназа Брутона; PLC γ2 - фосфолипаза С гамма-2; NFAT – Ядерный фактор активированных Т-клеток; PKCβ – протеинкиназа С бета; IKK - киназа IκB;
NF-κB - ядерный фактор, усиливающий каппа-легкую цепь активированных В-клеток.
12.
ЧЕМ ОТЛИЧАЕТСЯАКАЛАБРУТИНИБ
ОТ ИБРУТИНИБА?
13.
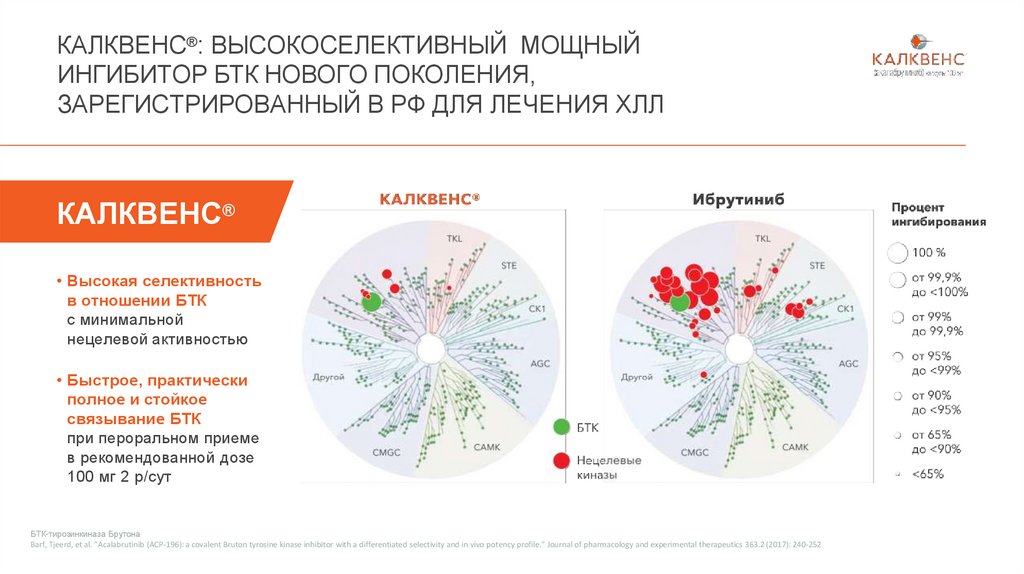
КАЛКВЕНС®: ВЫСОКОСЕЛЕКТИВНЫЙ МОЩНЫЙИНГИБИТОР БТК НОВОГО ПОКОЛЕНИЯ,
ЗАРЕГИСТРИРОВАННЫЙ В РФ ДЛЯ ЛЕЧЕНИЯ ХЛЛ
КАЛКВЕНС®
• Высокая селективность
в отношении БТК
с минимальной
нецелевой активностью
• Быстрое, практически
полное и стойкое
связывание БТК
при пероральном приеме
в рекомендованной дозе
100 мг 2 р/сут
БТК-тирозинкиназа Брутона
Barf, Tjeerd, et al. "Acalabrutinib (ACP-196): a covalent Bruton tyrosine kinase inhibitor with a differentiated selectivity and in vivo potency profile." Journal of pharmacology and experimental therapeutics 363.2 (2017): 240-252
14.
КАЛКВЕНС®: ВЫСОКОСЕЛЕКТИВНЫЙ МОЩНЫЙИНГИБИТОР БТК НОВОГО ПОКОЛЕНИЯ,
ЗАРЕГИСТРИРОВАННЫЙ В РФ ДЛЯ ЛЕЧЕНИЯ ХЛЛ1
К чему может приводить
нецелевая активность?
Уровень ингибирования ТЕС может
регулировать риск кровотечений2-3
Сигнальный путь ингибиторов EGFR
связан с возникновением кожной
сыпи и диареи4-5
Потеря функции HER2 связана
с увеличением кардиотоксичности4
1. Barf, Tjeerd, et al. "Acalabrutinib (ACP-196): a covalent Bruton tyrosine kinase inhibitor with a differentiated selectivity and in vivo potency profile." Journal of pharmacology and experimental therapeutics 363.2 (2017): 240-252. 2. Atkinson BT, Ellmeier W, and
Watson SP (2003) Tec regulates platelet activation by GPVI in the absence of BTK. Blood 102: 3592–3599. 3. Hamazaki Y, Kojima H, Mano H, Nagata Y, Todokoro K, Abe T, and Nagasawa T (1998) Tec is involved in G protein-coupled receptor- and integrinmediated signalings in human blood platelets. Oncogene 16:2773–2779. 4. Dy GK and Adjei AA (2013) Understanding, recognizing, and managing toxicities of targeted anticancer therapies. CA Cancer J Clin 63:249– 279. 5. Lynch TJ, Jr, Kim ES, Eaby B, Garey J,
West DP, and Lacouture ME (2007) Epidermal growth factor receptor inhibitor-associated cutaneous toxicities: an evolving paradigm in clinical management. Oncologist 12:610–621.
15.
КАКИЕ РЕЗУЛЬТАТЫПОКАЗЫВАЕТ иТКБ
II ПОКОЛЕНИЯ?
16.
ИССЛЕДОВАНИЕ ELEVATE-TNС 6-ЛЕТНИМ ПЕРИОДОМ НАБЛЮДЕНИЯ
Сравнение применения АКАЛАБРУТИНИБА в комбинации
с обинутузумабом или без него и комбинации обинутузумаба
и хлорамбуцила у пациентов с ХЛЛ, ранее не получавших лечения:
ИССЛЕДОВАНИЕ ELEVATE-TN
С 6-ЛЕТНИМ ПЕРИОДОМ НАБЛЮДЕНИЯ
Данные были представлены на конгрессе ASH в декабре 2023
Sharman, Jeff P., et al. "Acalabrutinib±Obinutuzumab Vs Obinutuzumab+ Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN." Blood 142 (2023): 636.
17.
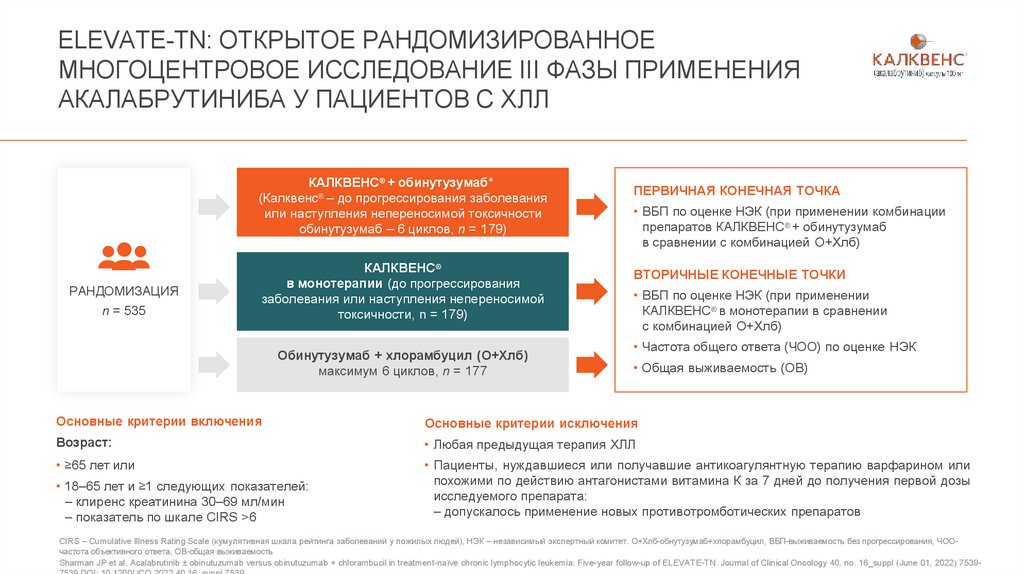
ELEVATE-TN: ОТКРЫТОЕ РАНДОМИЗИРОВАННОЕМНОГОЦЕНТРОВОЕ ИССЛЕДОВАНИЕ III ФАЗЫ ПРИМЕНЕНИЯ
АКАЛАБРУТИНИБА У ПАЦИЕНТОВ С ХЛЛ
КАЛКВЕНС® + обинутузумаб*
(Калквенс® – до прогрессирования заболевания
или наступления непереносимой токсичности
обинутузумаб – 6 циклов, n = 179)
РАНДОМИЗАЦИЯ
n = 535
КАЛКВЕНС®
в монотерапии (до прогрессирования
заболевания или наступления непереносимой
токсичности, n = 179)
Обинутузумаб + хлорамбуцил (О+Хлб)
максимум 6 циклов, n = 177
ПЕРВИЧНАЯ КОНЕЧНАЯ ТОЧКА
• ВБП по оценке НЭК (при применении комбинации
препаратов КАЛКВЕНС® + обинутузумаб
в сравнении с комбинацией О+Хлб)
ВТОРИЧНЫЕ КОНЕЧНЫЕ ТОЧКИ
• ВБП по оценке НЭК (при применении
КАЛКВЕНС® в монотерапии в сравнении
с комбинацией О+Хлб)
• Частота общего ответа (ЧОО) по оценке НЭК
• Общая выживаемость (ОВ)
Основные критерии включения
Основные критерии исключения
Возраст:
• Любая предыдущая терапия ХЛЛ
• ≥65 лет или
• Пациенты, нуждавшиеся или получавшие антикоагулянтную терапию варфарином или
похожими по действию антагонистами витамина К за 7 дней до получения первой дозы
исследуемого препарата:
– допускалось применение новых противотромботических препаратов
• 18–65 лет и ≥1 следующих показателей:
– клиренс креатинина 30–69 мл/мин
– показатель по шкале CIRS >6
CIRS – Cumulative Illness Rating Scale (кумулятивная шкала рейтинга заболеваний у пожилых людей), НЭК – независимый экспертный комитет. О+Хлб-обнутузумаб+хлорамбуцил, ВБП-выживаемость без прогрессирования, ЧООчастота объективного ответа, ОВ-общая выживаемость
Sharman JP et al. Acalabrutinib ± obinutuzumab versus obinutuzumab + chlorambucil in treatment-naïve chronic lymphocytic leukemia: Five-year follow-up of ELEVATE-TN. Journal of Clinical Oncology 40, no. 16_suppl (June 01, 2022) 75397539.DOI: 10.1200/JCO.2022.40.16_suppl.7539
18.
КАЛКВЕНС®: ЧЕРЕЗ 5 ЛЕТ ПОКАЗАТЕЛИ ВБП УКАЗЫВАЛИНА ПРЕИМУЩЕСТВО ПРИМЕНЕНИЯ АКАЛАБРУТИНИБА
5-ЛЕТНЯЯ ВБП СОСТАВИЛА 84% ПРИ ПРИМЕНЕНИИ КОМБИНАЦИИ A + O
И 72% ПРИ ПРИМЕНЕНИИ АКАЛАБРУТИНИБА В МОНОРЕЖИМЕ
А. ВБП по оценке исследования
Выживаемость
без прогрессирования
(%)
100
84% Медиана ВБП = Н/Д
А + О по сравнению с О + Clb
ОРa (95 % ДИ): 0,11 (0,07, 0,16)
р < 0,0001b
72%
A по сравнению с O + Clb
ОРa (95 % ДИ): 0,21 (0,15–0,30)
р < 0,0001b
80
60
Медиана ВБП = Н/Д
40
A + O по сравнению с A
ОРa (95 % ДИ): 0,51 (0,32, 0,81)
р = 0,0259b
20
21%
Медиана ВБП = 27,8 месяца
0
0
3
6
9
12
15
18
21
24
27
30
Число пациентов
в группе риска
А + О 179
А 179
О + Clb 177
33
36
39
42
45
48
51
54
57
60
63
66
69
72
A +O
Месяцы
175
167
163
170
163
156
168
158
153
164
156
139
163
155
125
160
153
110
157
150
100
156
149
86
156
146
82
153
142
67
152
141
66
151
137
56
146
135
49
144
133
44
141
130
40
140
129
38
138
124
31
133
120
30
99
93
20
65
63
13
39
39
8
27
22
7
7
6
2
1
1
0
A
O + Clb
a Отношение рисков оценивалось при помощи модели пропорциональных рисков Кокса, стратифицированной по статусу делеции 17p (наличие или отсутствие, на основе данных, полученных в интерактивной системе голосовой
связи/веб-связи).b P-значения оценивались при помощи логарифмического рангового критерия, стратифицированного по статусу делеции 17p (наличие или отсутствие, на основе данных, полученных в интерактивной системе
голосовой связи/веб-связи).
А – акалабрутиниб; ДИ – доверительный интервал; Clb – хлорамбуцил; Н/Д – не достигнуто; О – обинутузумаб; ВБП – выживаемость без прогрессирования.
Sharman JP et al. Acalabrutinib ± obinutuzumab versus obinutuzumab + chlorambucil in treatment-naïve chronic lymphocytic leukemia: Five-year follow-up of ELEVATE-TN. Journal of Clinical Oncology 40, no. 16_suppl (June
01, 2022) 7539-7539.DOI: 10.1200/JCO.2022.40.16_suppl.7539
19.
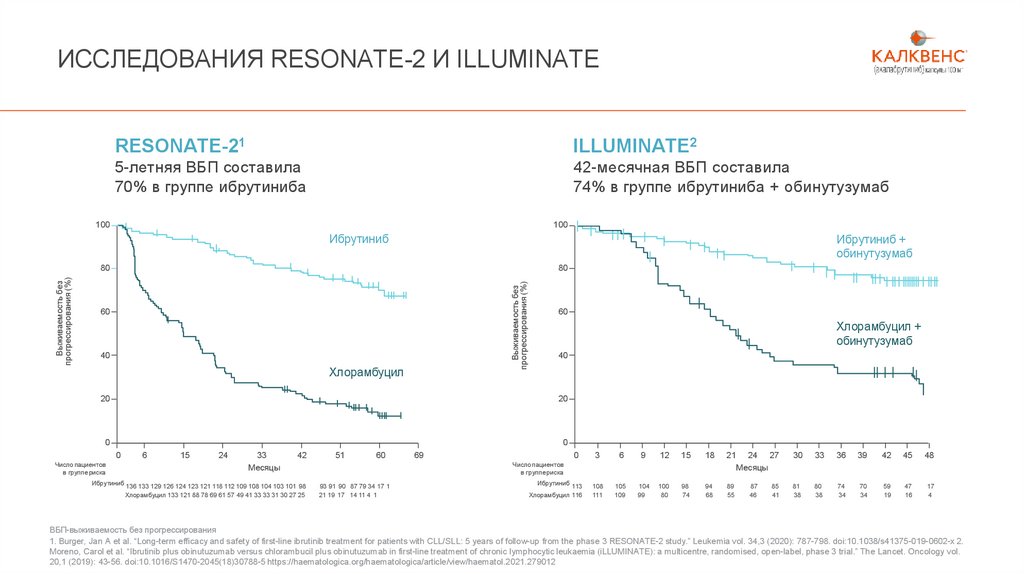
ИССЛЕДОВАНИЯ RESONATE-2 И ILLUMINATERESONATE-21
ILLUMINATE2
5-летняя ВБП составила
70% в группе ибрутиниба
42-месячная ВБП составила
74% в группе ибрутиниба + обинутузумаб
100
100
Ибрутиниб
Ибрутиниб +
обинутузумаб
80
Выживаемость без
прогрессирования (%)
Выживаемость без
прогрессирования (%)
80
60
40
Хлорамбуцил
20
Хлорамбуцил +
обинутузумаб
40
20
0
0
0
Число пациентов
в группе риска
60
6
15
24
33
Месяцы
42
Ибрутиниб 136 133 129 126 124 123 121 118 112 109 108 104 103 101 98
Хлорамбуцил 133 121 88 78 69 61 57 49 41 33 33 31 30 27 25
51
60
69
0
3
6
9
12
15
18
21
24 27
Месяцы
30
33
36
39
42
45
48
Ибрутиниб 113
Хлорамбуцил 116
108
111
105
109
104
99
100
80
98
74
94
68
89
55
87
46
81
38
80
38
74
34
70
34
59
19
47
16
17
4
Число пациентов
в группе риска
93 91 90 87 79 34 17 1
21 19 17 14 11 4 1
85
41
ВБП-выживаемость без прогрессирования
1. Burger, Jan A et al. “Long-term efficacy and safety of first-line ibrutinib treatment for patients with CLL/SLL: 5 years of follow-up from the phase 3 RESONATE-2 study.” Leukemia vol. 34,3 (2020): 787-798. doi:10.1038/s41375-019-0602-x 2.
Moreno, Carol et al. “Ibrutinib plus obinutuzumab versus chlorambucil plus obinutuzumab in first-line treatment of chronic lymphocytic leukaemia (iLLUMINATE): a multicentre, randomised, open-label, phase 3 trial.” The Lancet. Oncology vol.
20,1 (2019): 43-56. doi:10.1016/S1470-2045(18)30788-5 https://haematologica.org/haematologica/article/view/haematol.2021.279012
20.
КАЛКВЕНС®: ЧЕРЕЗ 6 ЛЕТ ПОКАЗАТЕЛИ ВБП УКАЗЫВАЛИНА ПРЕИМУЩЕСТВО ПРИМЕНЕНИЯ АКАЛАБРУТИНИБА
6-ЛЕТНЯЯ ВБП СОСТАВИЛА 78% ПРИ ПРИМЕНЕНИИ КОМБИНАЦИИ A + O
И 62% ПРИ ПРИМЕНЕНИИ АКАЛАБРУТИНИБА В МОНОРЕЖИМЕ
Выживаемость
без прогрессирования (%)
78% Медиана ВБП = Н/Д
Число пациентов
в группе риска
А + О по сравнению с О + Clb
ОРa (95 % ДИ): 0,14 (0,10-0,20)
р < 0,0001b
62%
Медиана ВБП = Н/Д
17% Медиана ВБП =
27,8 месяца
A по сравнению с O + Clb
ОРa (95 % ДИ): 0,24 (0,17–0,32)
р < 0,0001b
A + O по сравнению с A
ОРa (95 % ДИ): 0,58 (0,39-0,86)
р = 0,0259b
Месяцы
a Отношение рисков оценивалось при помощи модели пропорциональных рисков Кокса, стратифицированной по статусу делеции 17p (наличие или отсутствие, на основе данных, полученных в интерактивной системе голосовой связи/вебсвязи).b P-значения оценивались при помощи логарифмического рангового критерия, стратифицированного по статусу делеции 17p (наличие или отсутствие, на основе данных, полученных в интерактивной системе голосовой связи/вебсвязи).
А – акалабрутиниб; ДИ – доверительный интервал; Clb – хлорамбуцил; Н/Д – не достигнуто; О – обинутузумаб; ВБП – выживаемость без прогрессирования.
Sharman, Jeff P., et al. "Acalabrutinib±Obinutuzumab Vs Obinutuzumab+ Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN." Blood 142 (2023): 636.
21.
КАЛКВЕНС®: ВЫСОКИЕ ПОКАЗАТЕЛИ ВБП В РАЗНЫХПОДГРУППАХ ПАЦИЕНТОВ
ПРИ ИСПОЛЬЗОВАНИИ СХЕМЫ «КАЛКВЕНС® ± O» В СРАВНЕНИИ С OClb
ПРИ МЕДИАНЕ НАБЛЮДЕНИЯ 72 МЕС.
ВНЕ ЗАВИСИМОСТИ ОТ ТАКИХ ФАКТОРОВ, КАК:
ВОЗРАСТ:
СТАРШЕ ИЛИ
МЛАДШЕ 65 ЛЕТ
СТАДИЯ
ПО RAI
ПОЛ
ОБЩЕЕ
СОСТОЯНИЕ
ПО ECOG
СТЕПЕНЬ
ПОРАЖЕНИЯ
ЛИМФОУЗЛОВ
ЦИТОГЕНЕТИЧЕСКИЙ
РИСК
Мутация делеции17, p13, TP53,
делеции11, IGHV, комплексный
кариотип
OClb – обинутузумаб + хлорамбуцил, О-обунутузумаб, ECOG- оценка общего состояния пациента по шкале, разработанной Восточной объединенной онкологической группой (Eastern Cooperative Oncology Group) , IGHV- вариабельные участки
тяжелых цепей иммуноглобулинов
Sharman, Jeff P., et al. "Acalabrutinib±Obinutuzumab Vs Obinutuzumab+ Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN." Blood 142 (2023): 636.
22.
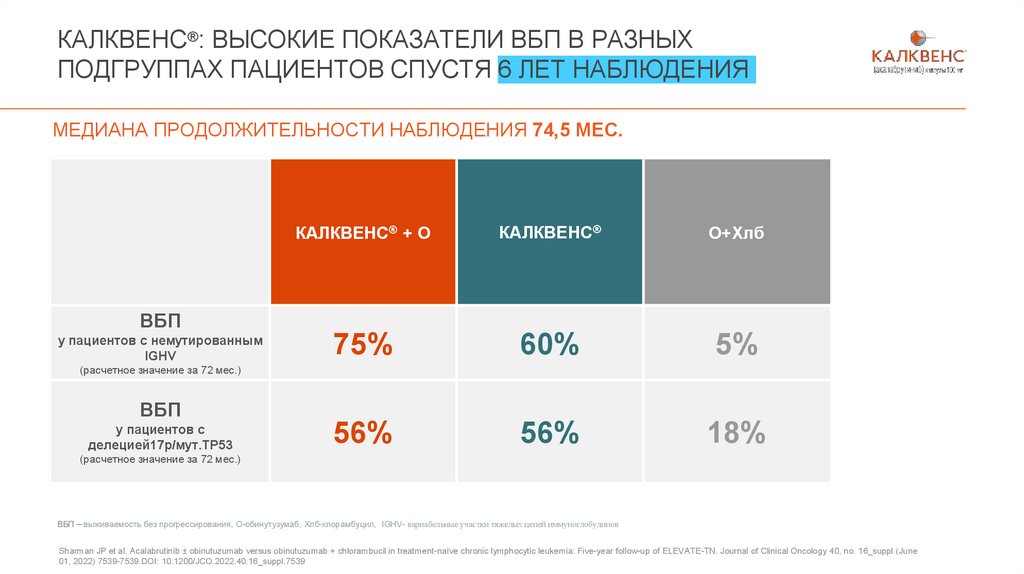
КАЛКВЕНС®: ВЫСОКИЕ ПОКАЗАТЕЛИ ВБП В РАЗНЫХПОДГРУППАХ ПАЦИЕНТОВ СПУСТЯ 6 ЛЕТ НАБЛЮДЕНИЯ
МЕДИАНА ПРОДОЛЖИТЕЛЬНОСТИ НАБЛЮДЕНИЯ 74,5 МЕС.
КАЛКВЕНС® + O
КАЛКВЕНС®
O+Хлб
75%
60%
5%
56%
56%
18%
ВБП
у пациентов с немутированным
IGHV
(расчетное значение за 72 мес.)
ВБП
у пациентов с
делецией17p/мут.ТР53
(расчетное значение за 72 мес.)
ВБП – выживаемость без прогрессирования, О-обинутузумаб, Хлб-хлорамбуцил, IGHV- вариабельные участки тяжелых цепей иммуноглобулинов
Sharman JP et al. Acalabrutinib ± obinutuzumab versus obinutuzumab + chlorambucil in treatment-naïve chronic lymphocytic leukemia: Five-year follow-up of ELEVATE-TN. Journal of Clinical Oncology 40, no. 16_suppl (June
01, 2022) 7539-7539.DOI: 10.1200/JCO.2022.40.16_suppl.7539
23.
КАЛКВЕНС®: ПРЕПАРАТ ОБЛАДАЕТ БЛАГОПРИЯТНЫМПРОФИЛЕМ БЕЗОПАСНОСТИ. 6 ЛЕТ НАБЛЮДЕНИЯ
БОЛЬШИНСТВО НЯ БЫЛИ 1-ОЙ ИЛИ 2-ОЙ СТЕПЕНИ ТЯЖЕСТИ ПО ДАННЫМ 6-ЛЕТНЕГО НАБЛЮДЕНИЯ.
НАИБОЛЕЕ ЧАСТЫЕ НЯ (≥5%) ≥ 3 СТЕПЕНИ ТЯЖЕСТИ
КАЛКВЕНС® + O (n=178)
КАЛКВЕНС® (n=179)
Нейтропения
31
12
Диарея
6
1
СOVID-19
9
7
Пневмония
7
6
Обморок
5
2
Гипертензия
4
5
ЯВЛЕНИЯ, ПРЕДСТАВЛЯЮЩИЕ КЛИНИЧЕСКИЙ ИНТЕРЕС ≥ 3 СТЕПЕНИ ТЯЖЕСТИ
КАЛКВЕНС® + O (n=178)
КАЛКВЕНС® (n=179)
Фибрилляция предсердий
2
2
Гипертензия
4
5
Вторые первичные злокачественные
заболевания
10
5
Sharman, Jeff P., et al. "Acalabrutinib±Obinutuzumab Vs Obinutuzumab+ Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN." Blood 142 (2023): 636.
24.
ЕСТЬ ЛИ ПРЯМОЕСРАВНЕНИЕ иТКБ?
25.
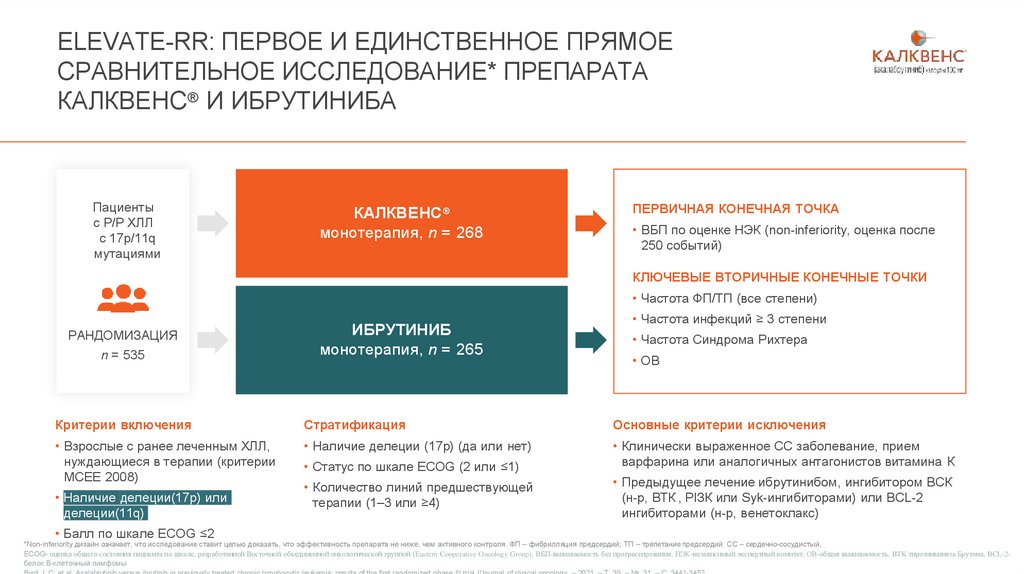
ELEVATE-RR: ПЕРВОЕ И ЕДИНСТВЕННОЕ ПРЯМОЕСРАВНИТЕЛЬНОЕ ИССЛЕДОВАНИЕ* ПРЕПАРАТА
КАЛКВЕНС® И ИБРУТИНИБА
Пациенты
с Р/Р ХЛЛ
с 17p/11q
мутациями
КАЛКВЕНС®
монотерапия, n = 268
ПЕРВИЧНАЯ КОНЕЧНАЯ ТОЧКА
• ВБП по оценке НЭК (non-inferiority, оценка после
250 событий)
КЛЮЧЕВЫЕ ВТОРИЧНЫЕ КОНЕЧНЫЕ ТОЧКИ
• Частота ФП/ТП (все степени)
РАНДОМИЗАЦИЯ
n = 535
ИБРУТИНИБ
монотерапия, n = 265
• Частота инфекций ≥ 3 степени
• Частота Синдрома Рихтера
• ОВ
Критерии включения
Стратификация
Основные критерии исключения
• Взрослые с ранее леченным ХЛЛ,
нуждающиеся в терапии (критерии
МСЕЕ 2008)
• Наличие делеции (17р) (да или нет)
• Клинически выраженное СС заболевание, прием
варфарина или аналогичных антагонистов витамина К
• Наличие делеции(17р) или
делеции(11q)
• Балл по шкале ЕСОG ≤2
• Статус по шкале ЕСОG (2 или ≤1)
• Количество линий предшествующей
терапии (1–3 или ≥4)
• Предыдущее лечение ибрутинибом, ингибитором ВСК
(н-р, ВТК ‚ РlЗК или Syk-ингибиторами) или ВСL-2
ингибиторами (н-р, венетоклакс)
*Non-inferiority дизайн означает, что исследование ставит целью доказать, что эффективность препарата не ниже, чем активного контроля. ФП – фибрилляция предсердий; ТП – трепетание предсердий. СС – сердечно-сосудистый,
ECOG- оценка общего состояния пациента по шкале, разработанной Восточной объединенной онкологической группой (Eastern Cooperative Oncology Group), ВБП-выживаемость без прогрессирования, НЭК-независимый экспертный комитет, ОВ-общая выживаемость, BTK тирозинкиназа Брутона, BCL-2белок В-клеточный лимфомы
Byrd J. C. et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial //Journal of clinical oncology. – 2021. – Т. 39. – №. 31. – С. 3441-3452.
26.
КАЛКВЕНС® ДОСТИГ ПЕРВИЧНОЙ КОНЕЧНОЙ ТОЧКИ ПО ВБП ВПРЯМОМ СРАВНЕНИИ С ИБРУТИНИБОМ У ПАЦИЕНТОВ С
РЕЦИДИВАМИ ХЛЛ ВЫСОКОГО ЦИТОГЕНЕТИЧЕСКОГО РИСКА
100
Первичная конечная точка,
ВБП по оценке независимого комитета,
оценивалась на предмет non-inferiority
ВБП (%)
80
КАЛКВЕНС® (n=268)
Ибрутиниб (n=265)
60
40
КАЛКВЕНС®
Ибрутиниб
143 (53,4)
136 (51,3)
38,4 (33,0-38,6)
38,4 (33,0-41,6)
События, n (%)
Медиана, (95% ДИ)
20
ОР (95% ДИ)
Медиана ВБП составила 38,4 мес.
в обеих группах
при медиане наблюдения 10,9 мес.
(по оценке независимого комитета)
1,00 (0,79-1,27)
0
0
3
6
9
12
15
18
21
24
Количество пациентов с риском
27
30
33
36
39
42
45
48
51
54
57
Месяцы
268
250
235
227
219
207
200
193
173
163
148
110
84
59
31
21
13
3
1
0
265
240
221
205
186
178
168
160
148
142
130
108
81
66
41
26
15
8
2
0
Сопоставимая
частота
синдрома
Рихтера
Non-inferiority дизайн означает, что исследование ставит целью доказать, что эффективность препарата не ниже, чем активного контроля, ВБП-выживаемость без прогрессирования, ОР-относительный риск
Byrd J. C. et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial //Journal of clinical oncology. – 2021. – Т. 39. – №. 31. – С. 3441-3452.
КАЛКВЕНС® (n = 10)
3,8%
ИБРУТИНИБ (n = 13)
4,9%
27.
КАЛКВЕНС®: БОЛЕЕ НИЗКАЯ КУМУЛЯТИВНАЯ ЧАСТОТАФИБРИЛЛЯЦИИ/ ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ И ГИПЕРТОНИИ
ПО СРАВНЕНИЮ С ИБРУТИНИБОМ
50
ФИБРИЛЛЯЦИЯ/ТРЕПЕТАНИЯ
ПРЕДСЕРДИЙ
ГИПЕРТОНИЯ
Накопительная частота события (%)
Накопительная частота события (%)
50
40
30
20
10
0
40
30
20
10
0
0
3
6
9 12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 57
0
3
6
9
12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 57 60
Месяцы
Месяцы
ОР (95% ДИ): 0,52 (0,32;0,86)
ОР (95% ДИ): 0,34 (0,21;0,54)
КАЛКВЕНС®
ОР-относительный риск
Byrd JC et al.,. J Clin Oncol. 2021 Jul 26:JCO2101210. doi: 10.1200/JCO.21.01210.
Ибрутиниб
28.
КАЛКВЕНС®: БОЛЕЕ НИЗКАЯ НАКОПИТЕЛЬНАЯ ЧАСТОТАКРОВОТЕЧЕНИЯ ЛЮБОЙ СТЕПЕНИ, ДИАРЕИ И АРТРАЛГИИ
ПО СРАВНЕНИЮ С ИБРУТИНИБОМ
80
80
80
60
40
20
0
60
40
20
0
0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 57
АРТРАЛГИЯ
Накопительная частота события (%)
ДИАРЕЯ
Накопительная частота события (%)
Накопительная частота события (%)
КРОВОТЕЧЕНИЕ
60
40
20
0
0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 57
0 3 6 9 12 15 18 21 24 27 30 33 36 39 42 45 48 51 54 57
Месяцы
Месяцы
Месяцы
ОР (95% ДИ): 0,63 (0,49;0,82)
ОР (95% ДИ): 0,61 (0,46;0,80)
ОР (95% ДИ): 0,61 (0,41;0,90)
КАЛКВЕНС®
ОР-относительный риск
Byrd JC et al.,. J Clin Oncol. 2021 Jul 26:JCO2101210. doi: 10.1200/JCO.21.01210.
Ибрутиниб
29.
КАЛКВЕНС®: ПОКАЗАЛ ДОСТОВЕРНО БОЛЕЕ НИЗКУЮ ЧАСТОТУФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ / ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ
ПО СРАВНЕНИЮ С ИБРУТИНИБОМ
ЧАСТОТА ФИБРИЛЛЯЦИИ ПРЕДСЕРДИЙ / ТРЕПЕТАНИЯ ПРЕДСЕРДИЙ ВСЕХ СТЕПЕНЕЙ ТЯЖЕСТИ
р = 0,02
18
Частота фибрилляции/трепетания (%)
16
14
16%
12
10
8
9,4%
6
41%
Снижение
ОР ФП/ТП
4
2
0
Ибрутиниб
n = 265
КАЛКВЕНС®
n = 268
ОР – отношение рисков, ФП – фибрилляция предсердий, ТП – трепетания предсердий
Byrd JC et al.,. J Clin Oncol. 2021 Jul 26:JCO2101210. doi: 10.1200/JCO.21.01210.
на 41% ниже риск
возникновения
ФП/ТП
при применении
препарата КАЛКВЕНС ®
по сравнению
с ибрутинибом
30.
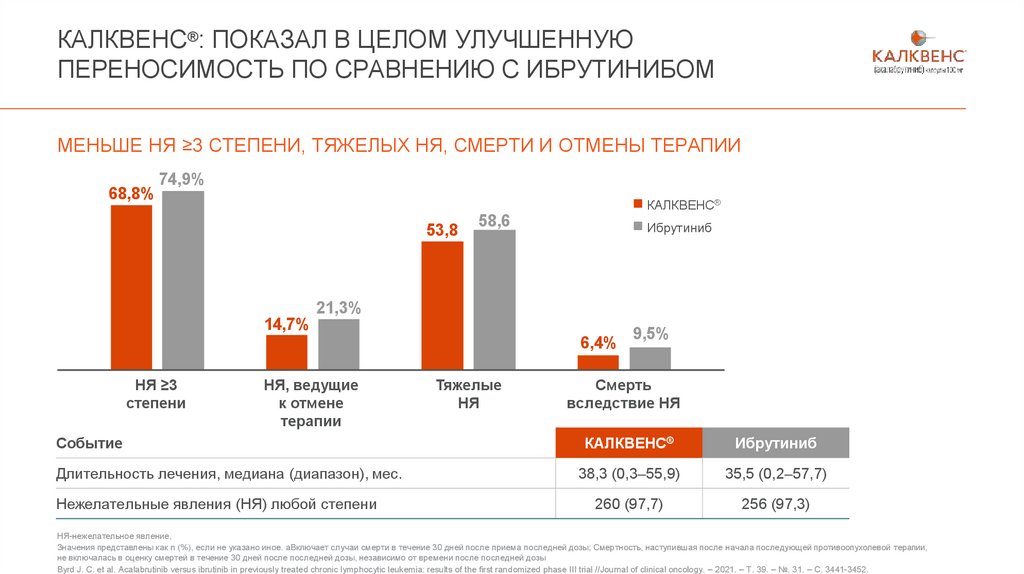
КАЛКВЕНС®: ПОКАЗАЛ В ЦЕЛОМ УЛУЧШЕННУЮПЕРЕНОСИМОСТЬ ПО СРАВНЕНИЮ С ИБРУТИНИБОМ
МЕНЬШЕ НЯ ≥3 СТЕПЕНИ, ТЯЖЕЛЫХ НЯ, СМЕРТИ И ОТМЕНЫ ТЕРАПИИ
68,8%
74,9%
КАЛКВЕНС®
53,8
%
58,6
%
Ибрутиниб
21,3%
14,7%
6,4%
НЯ ≥3
степени
НЯ, ведущие
к отмене
терапии
Тяжелые
НЯ
9,5%
Смерть
вследствие НЯ
Событие
КАЛКВЕНС®
Ибрутиниб
Длительность лечения, медиана (диапазон), мес.
38,3 (0,3–55,9)
35,5 (0,2–57,7)
260 (97,7)
256 (97,3)
Нежелательные явления (НЯ) любой степени
НЯ-нежелательное явление,
Значения представлены как n (%), если не указано иное. aВключает случаи смерти в течение 30 дней после приема последней дозы; Смертность, наступившая после начала последующей противоопухолевой терапии,
не включалась в оценку смертей в течение 30 дней после последней дозы, независимо от времени после последней дозы
Byrd J. C. et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial //Journal of clinical oncology. – 2021. – Т. 39. – №. 31. – С. 3441-3452.
31.
Пуллированный анализ: 1055 пациентов, получавших акалабрутинибВысокая эффективность вне зависимости от наличия факторов неблагоприятного прогноза у ранее
не леченных пациентов с ХЛЛ
Выживаемость без прогрессирования в зависимости от
наличия факторов неблагоприятного прогноза
Общая выживаемость в зависимости от наличия факторов
неблагоприятного прогноза
Слайд подготовлен с использованием материалов конгресса Поймай волну в терапии ХЛЛ и МКЛ, Иркутск, 14-15 июня 2024 г.
Davids, Matthew S., et al. "Acalabrutinib-based regimens in frontline or relapsed/refractory higher-risk CLL: Pooled analysis of 5 clinical trials." Blood Advances (2024): bloodadvances-2023011307.
32.
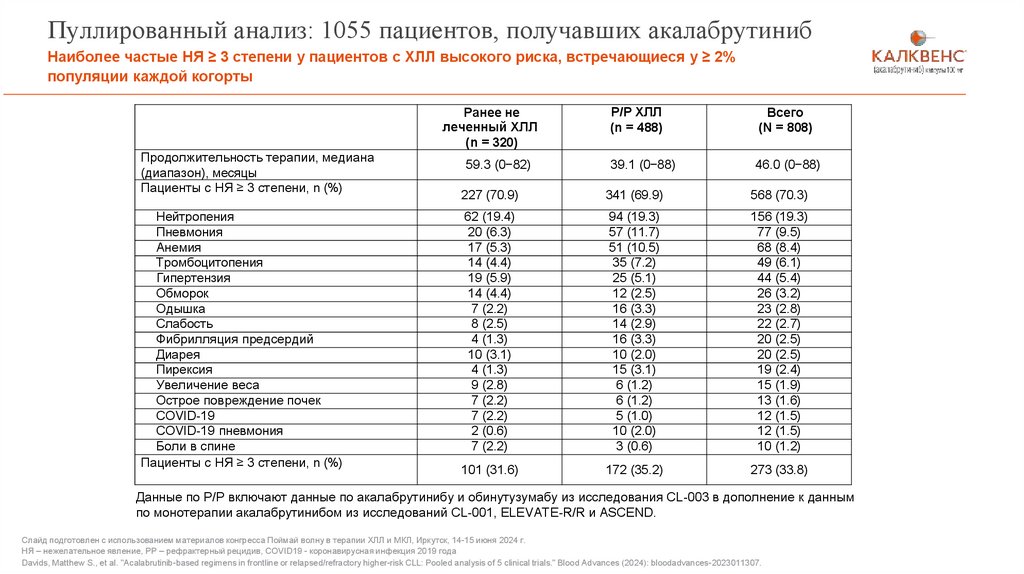
Пуллированный анализ: 1055 пациентов, получавших акалабрутинибНаиболее частые НЯ ≥ 3 степени у пациентов с ХЛЛ высокого риска, встречающиеся у ≥ 2%
популяции каждой когорты
Продолжительность терапии, медиана
(диапазон), месяцы
Пациенты с НЯ ≥ 3 степени, n (%)
Нейтропения
Пневмония
Анемия
Тромбоцитопения
Гипертензия
Обморок
Одышка
Слабость
Фибрилляция предсердий
Диарея
Пирексия
Увеличение веса
Острое повреждение почек
COVID-19
COVID-19 пневмония
Боли в спине
Пациенты с НЯ ≥ 3 степени, n (%)
Ранее не
леченный ХЛЛ
(n = 320)
Р/Р ХЛЛ
(n = 488)
Всего
(N = 808)
59.3 (0−82)
39.1 (0−88)
46.0 (0−88)
227 (70.9)
341 (69.9)
568 (70.3)
62 (19.4)
20 (6.3)
17 (5.3)
14 (4.4)
19 (5.9)
14 (4.4)
7 (2.2)
8 (2.5)
4 (1.3)
10 (3.1)
4 (1.3)
9 (2.8)
7 (2.2)
7 (2.2)
2 (0.6)
7 (2.2)
94 (19.3)
57 (11.7)
51 (10.5)
35 (7.2)
25 (5.1)
12 (2.5)
16 (3.3)
14 (2.9)
16 (3.3)
10 (2.0)
15 (3.1)
6 (1.2)
6 (1.2)
5 (1.0)
10 (2.0)
3 (0.6)
156 (19.3)
77 (9.5)
68 (8.4)
49 (6.1)
44 (5.4)
26 (3.2)
23 (2.8)
22 (2.7)
20 (2.5)
20 (2.5)
19 (2.4)
15 (1.9)
13 (1.6)
12 (1.5)
12 (1.5)
10 (1.2)
101 (31.6)
172 (35.2)
273 (33.8)
Данные по Р/Р включают данные по акалабрутинибу и обинутузумабу из исследования CL-003 в дополнение к данным
по монотерапии акалабрутинибом из исследований CL-001, ELEVATE-R/R и ASCEND.
Слайд подготовлен с использованием материалов конгресса Поймай волну в терапии ХЛЛ и МКЛ, Иркутск, 14-15 июня 2024 г.
НЯ – нежелательное явление, РР – рефрактерный рецидив, СOVID19 - коронавирусная инфекция 2019 года
Davids, Matthew S., et al. "Acalabrutinib-based regimens in frontline or relapsed/refractory higher-risk CLL: Pooled analysis of 5 clinical trials." Blood Advances (2024): bloodadvances-2023011307.
33.
Сравнение ВБП методом MAIC при применении препаратаАКАЛАБРУТИНИБ ± О в сравнении с ибрутинибом или
венетоклаксом + О у ранее не леченных пациентов с ХЛЛ пациентов
ВБП
Риск прогрессии и
смерти снижен на
ОВ
Риск смерти снижен на
АКАЛАБРУТИНИБ + О
по сравнению с
ибрутинибом (N=146)
АКАЛАБРУТИНИБ
по сравнению с
ибрутинибом (N=154)
АКАЛАБРУТИНИБ + О
по сравнению с венетоклакс
+ О (N=104)
52 %
17%
62%
59%
31%
57%
MAIC: (matching-adjusted indirect comparison) косвенное сравнение с поправкой на совпадение; ВБП – выживаемость без прогрессии; ОВ – общая выживаемость; О – обинутузумаб; ХЛЛ – хронический лимфоцитарный лейкоз;
Слайд подготовлен с использованием материалов конгресса Поймай волну в терапии ХЛЛ и МКЛ, Иркутск, 14-15 июня 2024 г.
Davids MS, Telford C, Abhyankar S, Waweru C, Ringshausen I. Matching-adjusted indirect comparisons of safety and efficacy of acalabrutinib versus other targeted therapies in patients with treatment-naïve chronic lymphocytic leukemia. Leuk Lymphoma. 2021
Oct;62(10):2342-2351..
34.
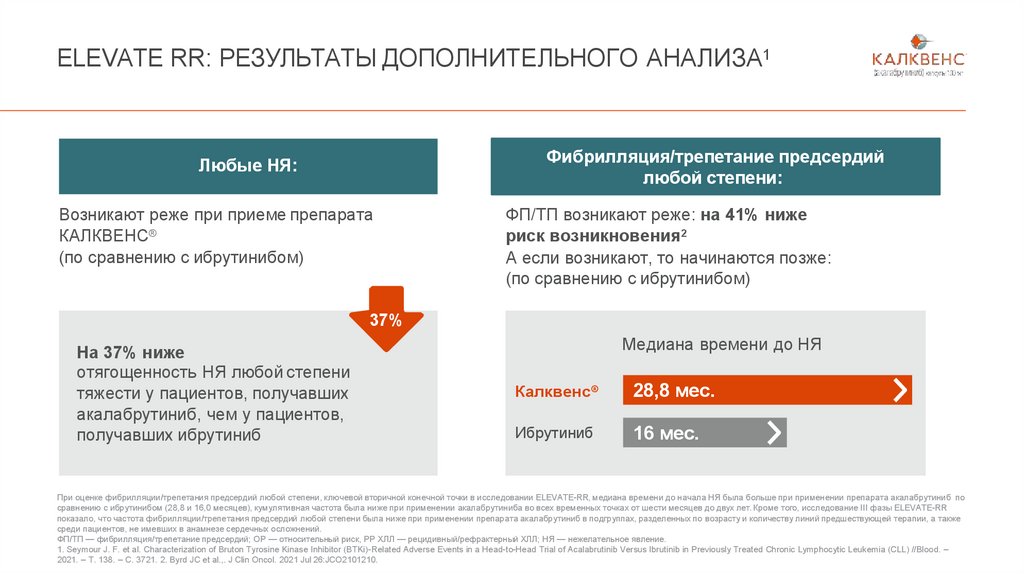
ELEVATE RR: РЕЗУЛЬТАТЫ ДОПОЛНИТЕЛЬНОГО АНАЛИЗА1Фибрилляция/трепетание предсердий
любой степени:
Любые НЯ:
Возникают реже при приеме препарата
КАЛКВЕНС®
(по сравнению с ибрутинибом)
ФП/ТП возникают реже: на 41% ниже
риск возникновения2
А если возникают, то начинаются позже:
(по сравнению с ибрутинибом)
37%
На 37% ниже
отягощенность НЯ любой степени
тяжести у пациентов, получавших
акалабрутиниб, чем у пациентов,
получавших ибрутиниб
Медиана времени до НЯ
Калквенс®
28,8 мес.
Ибрутиниб
16 мес.
При оценке фибрилляции/трепетания предсердий любой степени, ключевой вторичной конечной точки в исследовании ELEVATE-RR, медиана времени до начала НЯ была больше при применении препарата акалабрутиниб по
сравнению с ибрутинибом (28,8 и 16,0 месяцев), кумулятивная частота была ниже при применении акалабрутиниба во всех временных точках от шести месяцев до двух лет. Кроме того, исследование III фазы ELEVATE-RR
показало, что частота фибрилляции/трепетания предсердий любой степени была ниже при применении препарата акалабрутиниб в подгруппах, разделенных по возрасту и количеству линий предшествующей терапии, а также
среди пациентов, не имевших в анамнезе сердечных осложнений.
ФП/ТП — фибрилляция/трепетание предсердий; ОР — относительный риск, РР ХЛЛ — рецидивный/рефрактерный ХЛЛ; НЯ — нежелательное явление.
1. Seymour J. F. et al. Characterization of Bruton Tyrosine Kinase Inhibitor (BTKi)-Related Adverse Events in a Head-to-Head Trial of Acalabrutinib Versus Ibrutinib in Previously Treated Chronic Lymphocytic Leukemia (CLL) //Blood. –
2021. – Т. 138. – С. 3721. 2. Byrd JC et al.,. J Clin Oncol. 2021 Jul 26:JCO2101210.
35.
ДОСТУПНЫ РЕЗУЛЬТАТЫДОПОЛНИТЕЛЬНОГО
АНАЛИЗА С 5-ЛЕТНИМ
ПЕРИОДОМ НАБЛЮДЕНИЯ
36.
Данные сетевого метаанализа: сравнение эффективностилекарственных средств в 1-ой линии терапии ХЛЛ
Значительное преимущество применения комбинации акалабрутиниб + обинутузумаб по показателю
ВБП по сравнению со всеми схемами сравнения.
Анализ продемонстрировал значительное улучшение ВБП при применении акалабрутиниба в монорежиме
по сравнению с большинством схем сравнения.
Анализ В
Анализ A
Терапия
ОР (95% ДИ)
Акалабрутиниб vs
ОР (95% ДИ)
Акалабрутиниб + обинутузумаб vs
Терапия
ОР (95% ДИ)
Акалабрутиниб vs
ОР (95% ДИ)
Акалабрутиниб + обинутузумаб vs
Ибрутиниб
0,35 [0,18,0,66]
0,19 [0,09,0,38]
Ибрутиниб
0,61 [0,32,1,15]
0,46 [0,23,0,92]
Ибрутиниб + обинутузумаб
0,87 [0,46,1,63]
0,46 [0,23,0,94]
Ибрутиниб + обинутузумаб
0,63 [0,32,1,27]
0,48 [0,23,1,01]
Ибрутиниб + ритуксимаб
0,37 [0,18,0,75]
0,20 [0,09,0,44]
Ибрутиниб + ритуксимаб
0,56 [0,27,1,14]
0,43 [0,20,0,91]
Венетоклакс + обинутузумаб
0,60 [0,33,1,11]
0,32 [0,16,0,64]
Венетоклакс + обинутузумаб
0,47 [0,24,0,89]
0,36 [0,18,0,71]
Бендамустин + ритуксимаб
0,15 [0,08,0,27]
0,08 [0,04,0,16]
Бендамустин + ритуксимаб
0,19 [0,10,0,35]
0,14 [0,07,0,28]
Хлорамбуцил
0,04 [0,02,0,07]
0,02 [0,01,0,04]
Хлорамбуцил
0,03 [0,02,0,06]
0,02 [0,01,0,05]
Хлорамбуцил + обинутузумаб
0,20 [0,13,0,31]
0,11 [0,06,0,18]
Хлорамбуцил + обинутузумаб
0,16 [0,10,0,27]
0,12 [0,07,0,22]
Хлорамбуцил + офатумумаб
0,07 [0,04,0,12]
0,04 [0,02,0,07]
Хлорамбуцил + офатумумаб
0,06 [0,03,0,10]
0,04 [0,02,0,08]
Хлорамбуцил + ритуксимаб
0,08 [0,05,0,14]
0,04 [0,02,0,08]
Хлорамбуцил + ритуксимаб
0,07 [0,04,0,13]
0,06 [0,03,0,10]
0,01
0,1
В пользу акалабрутиниба или
Акалабрутиниба + обинутузумаба
0,01
1
0,1
1
В пользу препарата
сравнения
ВБП-выживаемость без прогрессирования, ОР-относительный риск, ДИ-доверительный интервал
Matthew S. Davids MMSc, Catherine Waweru PhD, Pauline Le Nouveau MSc, Amie Padhiar MSc, Gautamjeet Singh MSC, Sarang Abhyankar MSc, Veronique Leblond MD et al
https://doi.org/10.1016/j.clinthera.2020.08.017
0,01
0,1
В пользу акалабрутиниба или
Акалабрутиниба + обинутузумаба
0,01
1
В пользу препарата
сравнения
0,1
1
37.
КАЛКВЕНС®: ПЕРВЫЙ И ЕДИНСТВЕННЫЙ ИБТК,ДОКАЗАВШИЙ ЛУЧШУЮ ПЕРЕНОСИМОСТЬ ПРИ ДЛИТЕЛЬНОЙ
И ЭФФЕКТИВНОЙ ТЕРАПИИ ХЛЛ
В СРАВНИТЕЛЬНОМ ИССЛЕДОВАНИИ С ИБРУТИНИБОМ
ВЫСОКАЯ ЭФФЕКТИВНОСТЬ1
Достигнута конечная точка по сравнительной эффективности в
отношении ВПБ
ЛУЧШИЙ ПРОФИЛЬ ПЕРЕНОСИМОСТИ В КЛАССЕ1
В группе КАЛКВЕНС® реже встречалось прекращение терапии
в связи с нежелательными явлениями:
• 14,7% пациентов в группе КАЛКВЕНС®
• 21,3% пациентов в группе Ибрутиниб
ЛУЧШАЯ СЕРДЕЧНО-СОСУДИСТАЯ БЕЗОПАСНОСТЬ
В КЛАССЕ2
у пациентов с РР ХЛЛ высокого риска
• на 77% ниже риск возникновения впервые выявленной
гипертензии
• на 63% ниже риск возникновения впервые выявленной ФП/ТП
ГИПОТЕТИЧЕСКИЙ ПАЦИЕНТ
РР – рефрактерный рецидивирующий, ФП – фибрилляция предсердий, ТП – трепетания предсердий, ВБП-выживаемость без прогрессирования, иБТК-ингибитор тирозинкиназы Брутона
1. Byrd J. C. et al. Acalabrutinib versus ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase III trial //Journal of clinical oncology. – 2021. – Т. 39. – №. 31. –
С. 3441-3452. 2. Seymour, John F., et al. "Detailed safety profile of acalabrutinib vs ibrutinib in previously treated chronic lymphocytic leukemia in the ELEVATE-RR trial." Blood 142.8 (2023): 687-699.
38.
ПОЧЕМУ БЛАГОПРИЯТНЫЙПРОФИЛЬ БЕЗОПАСНОСТИ
КРИТИЧЕСКИ ВАЖЕН?
39.
ПОЧЕМУ БЛАГОПРИЯТНЫЙ ПРОФИЛЬ БЕЗОПАСНОСТИКРИТИЧЕСКИ ВАЖЕН?1-6
ПОЖИЛЫЕ
ПАЦИЕНТЫ
ДЛИТЕЛЬНАЯ
ТЕРАПИЯ
ОТСУТСТВИЕ
ДОПОЛНИТЕЛЬНОЙ
НАГРУЗКИ НА
БЮДЖЕТ
1. Российские клинические рекомендации по диагностике и лечению лимфопролиферативных заболеваний, под редакцией проф. Поддубной И.В., проф. Савченко В.Г., Москва, 2018. Сайт «Lymphoma Coalition».
https://www.lymphomacoalition.org/images/subtype-reports/CLL_Global_2017_Report.pdf. Дата обращения: 20.03.2024. 3. Thurmes P et al. Leuk Lymphoma. 2008;49(1):49-56. 4. World Health Organization.
https://www.who.int/selection_- medicines/committees/expert/20/applications/CLL.pdf. Дата обращения: 20.03.2024. 5. Бахтина В.И., Демко И.В., Кравченко С.К., Протопопова Е.Б. ХРОНИЧЕСКИЙ ЛИМФОЛЕЙКОЗ //
Современные проблемы науки и образования. – 2016. – № 3. 6. Электронный ресурс: https://www.astrazeneca.com/media-centre/press-releases/2019/calquence-significantly-prolonged-the-time-patients-lived-without-diseaseprogression-or-death-in-previously-untreated-chronic- lymphocytic-leukaemia.html Дата обращения: 20.03.2024
40.
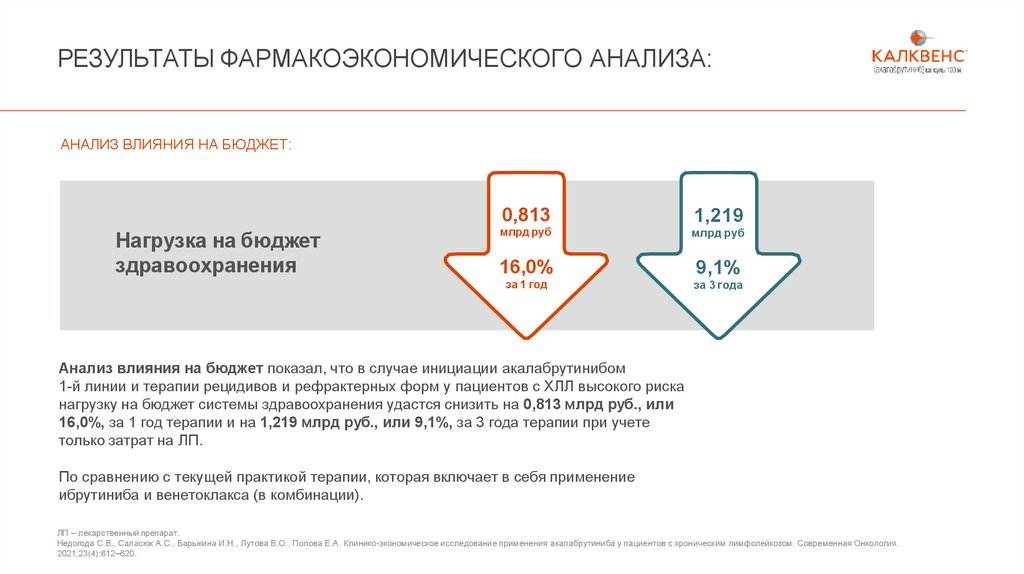
РЕЗУЛЬТАТЫ ФАРМАКОЭКОНОМИЧЕСКОГО АНАЛИЗА:АНАЛИЗ ВЛИЯНИЯ НА БЮДЖЕТ:
0,813
Нагрузка на бюджет
здравоохранения
млрд руб
16,0%
за 1 год
1,219
млрд руб
9,1%
за 3 года
Анализ влияния на бюджет показал, что в случае инициации акалабрутинибом
1-й линии и терапии рецидивов и рефрактерных форм у пациентов с ХЛЛ высокого риска
нагрузку на бюджет системы здравоохранения удастся снизить на 0,813 млрд руб., или
16,0%, за 1 год терапии и на 1,219 млрд руб., или 9,1%, за 3 года терапии при учете
только затрат на ЛП.
По сравнению с текущей практикой терапии, которая включает в себя применение
ибрутиниба и венетоклакса (в комбинации).
ЛП – лекарственный препарат.
Недогода С.В., Саласюк А.С., Барыкина И.Н., Лутова В.О., Попова Е.А. Клинико-экономическое исследование применения акалабрутиниба у пациентов с хроническим лимфолейкозом. Современная Онкология.
2021;23(4):612–620.
41.
ВЫВОДЫТаким образом, АКАЛАБРУТИНИБ
в комбинации с обинутузумабом или
в монотерапии может рассматриваться
как ВЫСОКОЭФФЕКТИВНАЯ
ОПЦИЯ 1-Й ЛИНИИ ТЕРАПИИ ХЛЛ с
приемлемым профилем безопасности
для всех групп пациентов 1
Учитывая высокую СЕЛЕКТИВНОСТЬ
ПРЕПАРАТА2, АКАЛАБРУТИНИБ
может рассматриваться как
ПРЕДПОЧТИТЕЛЬНАЯ ОПЦИЯ
для пациентов, не подходящих
для ИХТ, в том числе коморбидных
пациентов с сердечно-сосудистыми
заболеваниями или наличием
факторов риска для их развития3
1. Sharman, Jeff P., et al. "Acalabrutinib±Obinutuzumab Vs Obinutuzumab+ Chlorambucil in Treatment-Naive Chronic Lymphocytic Leukemia: 6-Year Follow-up of Elevate-TN." Blood 142 (2023): 636.
2. Barf, Tjeerd, et al. "Acalabrutinib (ACP-196): a covalent Bruton tyrosine kinase inhibitor with a differentiated selectivity and in vivo potency profile." Journal of pharmacology and experimental therapeutics 363.2 (2017): 240-252. 3. Awan,
Farrukh T., et al. "International consensus statement on the management of cardiovascular risk of Bruton’s tyrosine kinase inhibitors in CLL." Blood advances 6.18 (2022): 5516-5525.




























 Медицина
Медицина








