Похожие презентации:
Способы получения кислорода в лаборатории и промышленности (8 класс)
1.
Ильина И.В., руководитель ЦДОШ, учитель химииМБОУ «Средняя общеобразовательная школа №27
имени А.А. Дейнеки» г. Курска
E-mail мой: ilina.irina71@mail.ru
2. Способы получения кислорода в лаборатории и промышленности
L/O/G/O3.
А) В природе:1. Кислород в природе образуется в
процессе фотосинтеза.
6СО2 + 6Н2О
С6Н12О6 +6O2
2. Во время грозы: 3O2 2O3
Б) В промышленности: перегонкой
сжиженного воздуха при t = - 1830 С под
давлением.
4.
перманганаткалия
манганат
калия
оксид
кислород
марганца (IV)
Проверка собравшегося
кислорода
5.
6.
7. Способы собирания кислорода
Метод вытеснениявоздуха, т.к. немного
тяжелее воздуха,
собирается на дне сосуда
Метод вытеснения
воды, т.к. кислород
малорастворим в воде
8.
ОКСИДЫ–
это
сложные
вещества,
состоящие из двух элементов, одним из
которых является кислород
МеО неМеО
Как назвать оксиды?
1. на первом месте ставим слово ОКСИД
2. На втором месте добавляем элемент в
родительном падеже. Оксид чего?
3.В
скобках
указываем
переменную
валентность
Например: MgO оксид магния
SO3 - оксид серы (VI)
9.
В земной коре – литосфере – находится оксидAl2O3
алюминия ________
(глина), оксид кремния (IV)
SiO2 (песок), оксид железа (III) ______
Fe2O3
_____
(содержится в красном железняке). Водная
оболочка Земли – гидросфера состоит из оксид
H2O
водорода _____.
В воздухе есть оксид углерода
CO2
(IV) ______
(углекислый газ). В результате
хозяйственной деятельности человека
образуются вещества, загрязняющие
атмосферу: оксид углерода (II) _____
CO
(угарный
SO2
газ), оксид серы (IV) ______
(сернистый газ),
оксид азота (II) NO
____ и оксида азота (IV) NO
___2
10.
1. Чему равна объёмная доля кислородавоздухе?
А) 10% Б) 21% в) 5% г) 75%
д) 78%
в
2. Из чего в лаборатории получают кислород?
А) вода Б) воздух в) перманганат калия
3. Как надо держать пробирку, чтобы собрать в
неё кислород?
11.
Домашнее задание1. Параграф 13
2. Упражнение 1 и 2 (из презентации)
3. Задача 1 (из презентации)
Пишите в электронный журнал или на мою почту.
E-mail: ilina.irina71@mail.ru
Задача 1. Рассчитайте массу кислорода,
который образуется при разложении 8 г
пероксида водорода (Н2О2)
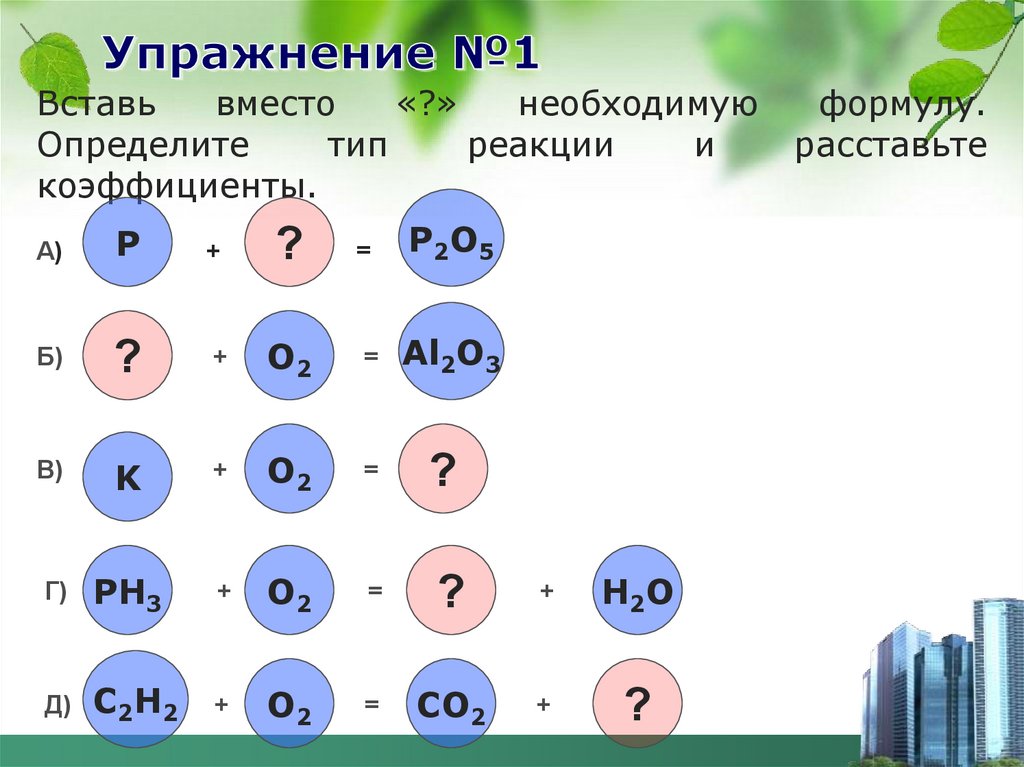
12. Упражнение №1
Вставьвместо
«?»
необходимую
Определите
тип
реакции
и
коэффициенты.
А)
P
+
?
=
P2O5
Б)
?
+
O2
=
Al2O3
В)
K
+
O2
=
?
Г)
PH3
+
O2
=
?
+
H2O
Д)
C2H2
+
O2
=
CO2
+
?
формулу.
расставьте
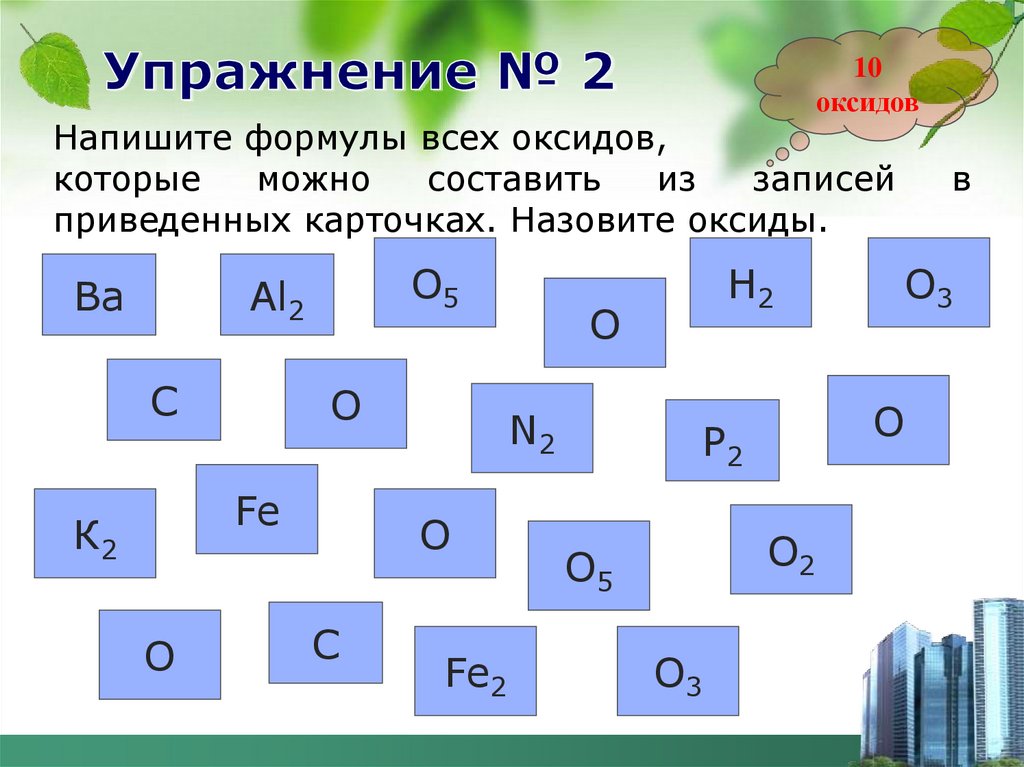
13. Упражнение № 2
10оксидов
Напишите формулы всех оксидов,
которые
можно
составить
из
записей
приведенных карточках. Назовите оксиды.
Ва
О5
Al2
С
О
Fe
К2
О
С
О
N2
О
Fe2
Н2
О2
О5
О3
О3
О
Р2
в











 Химия
Химия