Похожие презентации:
Полимеры. Молекулярная масса. Методы синтеза
1.
Современные функциональные и конструкционныематериалы
Лекция 1.
Полимеры. Молекулярная масса. Методы синтеза
03.02.2025-12.05.2025
Преподаватель: к.х.н. Морозова Софья Михайловна
E-mail: sofiionova@yandex.ru
+79859108502
1
2.
Литература1.«Высокомолекулярные соединения» под редакцией А.Б. Зезина, М: Юрайт,
2016
2.Ю.Д. Семчиков. «Высокомолекулярные соединения» М: Академия, 2003.
3. В.В. Киреев. «Высокомолекулярные соединения» М: Юрайт, 2013.
4. А.А. Тагер. «Физико-химия полимеров», М: Научный мир, 2007
5. В.Н. Кулезнев, В.А. Шершнев, «Химия и физика полимеров», М: КолосС, 2007
•Учебные материалы по химии высокомолекулярных соединений + Программа + Список
литературы// - http://www.chem.msu.ru/rus/teaching/vms.html
•Методические пособия к практикуму по высокомолекулярным соединениям //
http://www.vmsmsu.ru/what.html
•Макрогалерея // http://www. pslc.ws/russian/index.htm
2
3.
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ: вещество, характеризующееся
высокими
молекулярными
массами,
как
правило,
превышающими 1000 углеродных единиц
МАКРОМОЛЕКУЛА: совокупность
атомов или атомных групп, разных
или одинаковых по химической
природе,
соединённых
ковалентными
связями
в
длинную,
гибкую,
цепную
конструкцию
ПОЛИМЕРЫ: особый
класс
химических
соединений,
состоящих из макромолекул,
специфика свойств которых
обусловлена большой длиной,
цепным строением и гибкостью
их макромолекул.
3
4.
Определение полимера-(СН2-СН2)-
H2
C
H2
C
C
H2
H2
C
C
H2
n
полиэтилен
звено цепи
C
H2
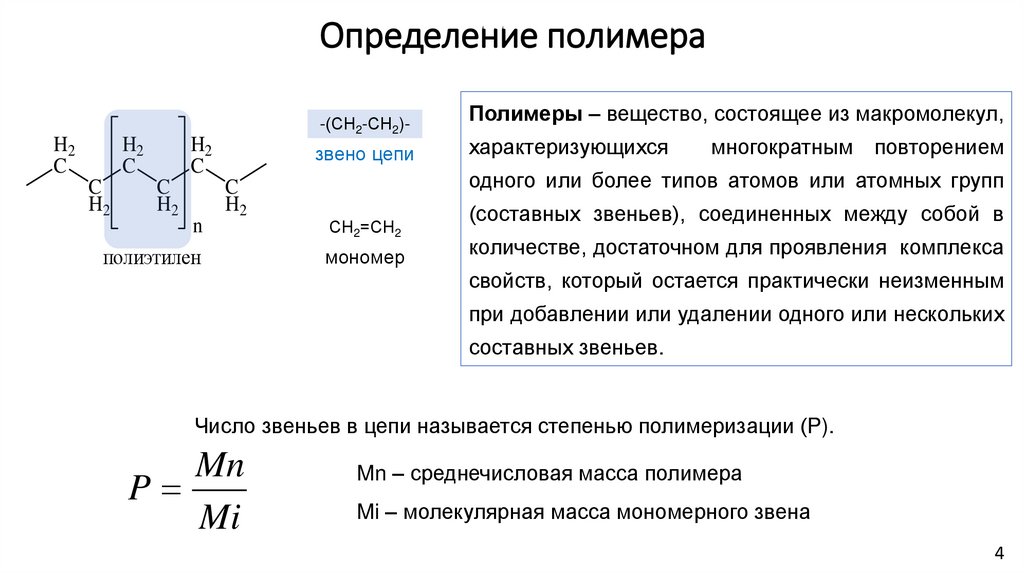
Полимеры – вещество, состоящее из макромолекул,
характеризующихся
многократным повторением
одного или более типов атомов или атомных групп
СН2=СН2
мономер
(составных звеньев), соединенных между собой в
количестве, достаточном для проявления комплекса
свойств, который остается практически неизменным
при добавлении или удалении одного или нескольких
составных звеньев.
Число звеньев в цепи называется степенью полимеризации (P).
Mn
P
Mi
Mn – среднечисловая масса полимера
Mi – молекулярная масса мономерного звена
4
5.
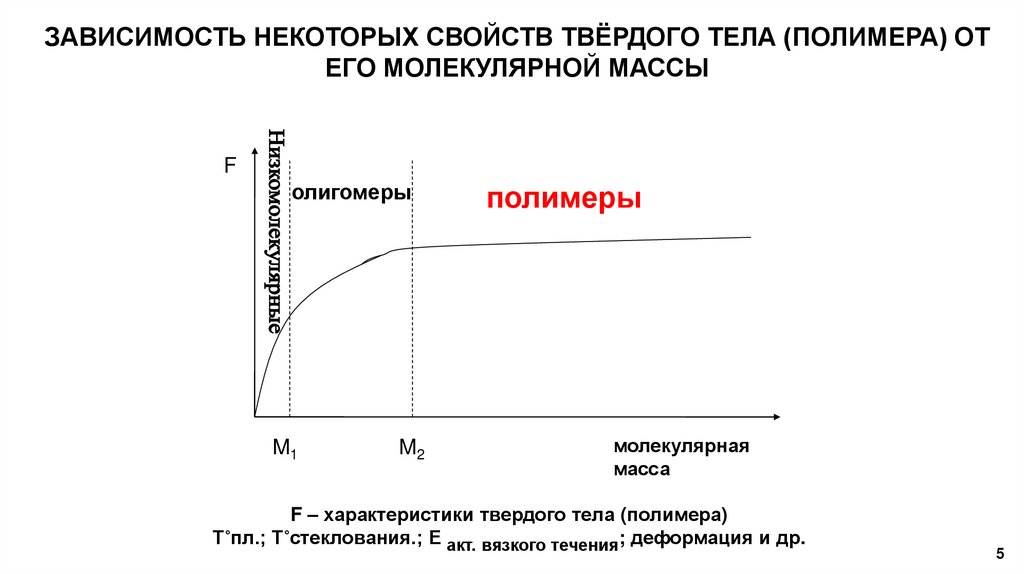
ЗАВИСИМОСТЬ НЕКОТОРЫХ СВОЙСТВ ТВЁРДОГО ТЕЛА (ПОЛИМЕРА) ОТЕГО МОЛЕКУЛЯРНОЙ МАССЫ
F
олигомеры
M1
M2
полимеры
молекулярная
масса
F – характеристики твердого тела (полимера)
T˚пл.; T˚стеклования.; Е акт. вязкого течения; деформация и др.
5
6.
Историческая справка6
7.
Историческая справка• 1835 г. — В результате опытов с хлористым винилом химик Реньо
впервые синтезировал поливинилхлорид, о чем сам Реньо не
догадывался.
• 1839 г. — Работая со стиролом, химик Симон обнаружил в колбах и
ретортах какой-то нерастворимый осадок. Однако не придал этому
значения.
• 1843 г. — Из природного каучука (белого цвета сока дерева гевеи)
получена первая в мире твердая пластическая масса — эбонит,
содержащая около 30% серы ( больше 30% и невозможно).
• 1856 г. — Англичанин Паркес получил новое
вещество паркезин (целлулоид).
7
8.
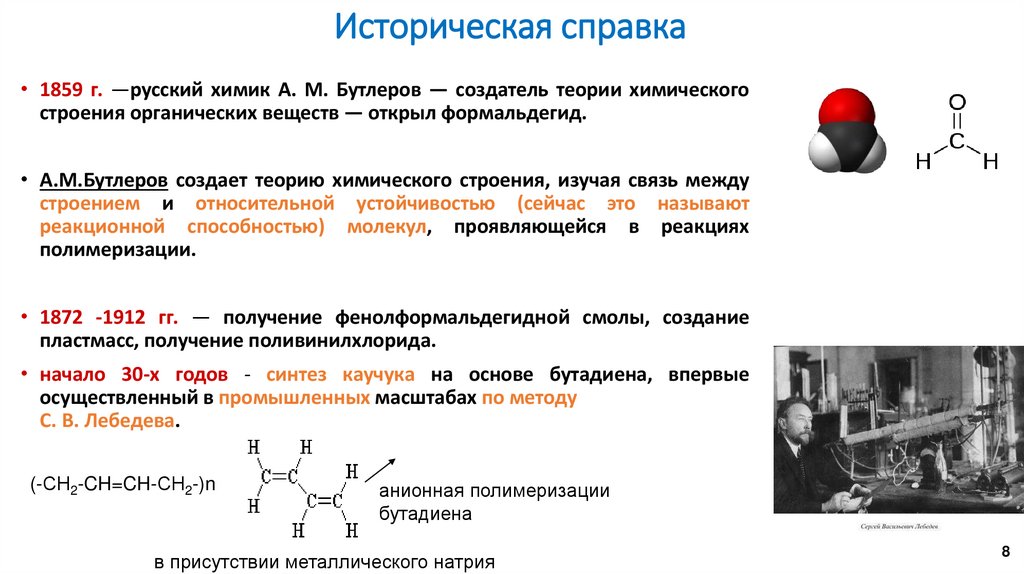
Историческая справка• 1859 г. —русский химик А. М. Бутлеров — создатель теории химического
строения органических веществ — открыл формальдегид.
• А.М.Бутлеров создает теорию химического строения, изучая связь между
строением и относительной устойчивостью (сейчас это называют
реакционной способностью) молекул, проявляющейся в реакциях
полимеризации.
• 1872 -1912 гг. — получение фенолформальдегидной смолы, создание
пластмасс, получение поливинилхлорида.
• начало 30-х годов - синтез каучука на основе бутадиена, впервые
осуществленный в промышленных масштабах по методу
С. В. Лебедева.
(-СH2-CH=CH-СH2-)n
анионная полимеризации
бутадиена
в присутствии металлического натрия
8
9.
Историческая справка• 1936 г.-получение полиэтилена полимеризацией этилена (компания “Империал кемикал
индастриз”)
Условия: очень высокие температура
(200°С) и давление (сотни атмосфер),
nCH2=CH2 → [-CH2-CH2-]n
свойства пластика не оправдали ожиданий, т.к. в жестких условиях реакции образовывались
макромолекулы разветвлённого строения
ноябрь 1953 г. - новая реакции получения полиэтилена
1953 г. (Циглер) –новый комплексный катализатор на
основе триэтилалюминия и галогенидов титана для
полимеризации этилена
способствует полимеризации
при значительно более низких
температуре и давлении
материал с гораздо лучшими
свойствами-более плотный,
твердый и устойчивый к
высоким температурам
•1957 г. ( Натта)- на промышленной установке получен изотактический
полипропилен( макромолекулы линейные и регулярного строения [-CH2-CH-]n
революция в производстве пластических материалов!
CH3
9
10.
Сбор латексагевеизагустевшего млечного
сока, вытекшего из
порезов на коре дерева
гевеи.
10
11.
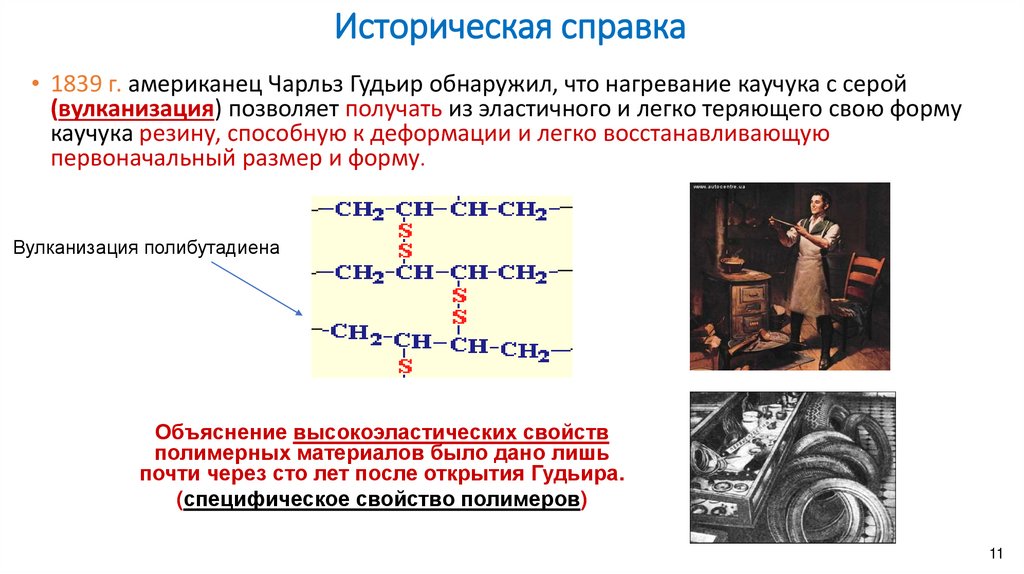
Историческая справка• 1839 г. американец Чарльз Гудьир обнаружил, что нагревание каучука с серой
(вулканизация) позволяет получать из эластичного и легко теряющего свою форму
каучука резину, способную к деформации и легко восстанавливающую
первоначальный размер и форму.
Вулканизация полибутадиена
Объяснение высокоэластических свойств
полимерных материалов было дано лишь
почти через сто лет после открытия Гудьира.
(специфическое свойство полимеров)
11
12.
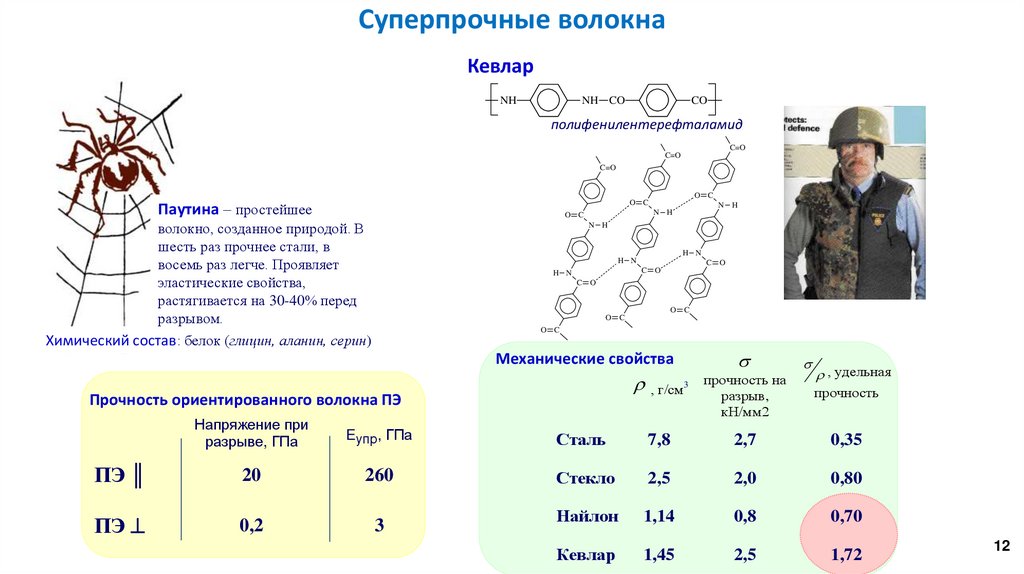
Суперпрочные волокнаКевлар
NH
NH CO
CO
полифенилентерефталамид
C=O
C=O
C=O
O C
O C
Паутина – простейшее
волокно, созданное природой. В
шесть раз прочнее стали, в
восемь раз легче. Проявляет
эластические свойства,
растягивается на 30-40% перед
разрывом.
Химический состав: белок (глицин, аланин, серин)
N H
N H
O C
N H
H N
H N
C O
C O
H N
C O
O C
O C
O C
Механические свойства
Прочность ориентированного волокна ПЭ
, г/см3
прочность на
разрыв,
кН/мм2
, удельная
прочность
Напряжение при
разрыве, ГПа
Eупр, ГПа
Сталь
7,8
2,7
0,35
ПЭ ║
20
260
Стекло
2,5
2,0
0,80
ПЭ
0,2
3
Найлон
1,14
0,8
0,70
Кевлар
1,45
2,5
1,72
12
13.
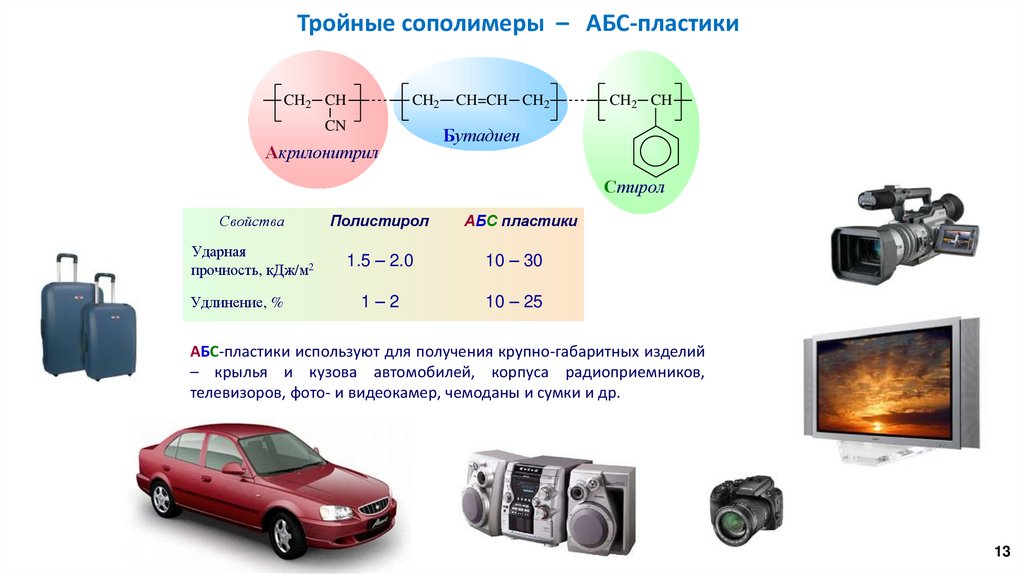
Тройные сополимеры – АБС-пластикиCH2 CH
CH2
CN
Акрилонитрил
CH=CH CH2
CH2 CH
Бутадиен
Стирол
Свойства
Полистирол
АБС пластики
Ударная
прочность, кДж/м2
1.5 – 2.0
10 – 30
1–2
10 – 25
Удлинение, %
АБС-пластики используют для получения крупно-габаритных изделий
– крылья и кузова автомобилей, корпуса радиоприемников,
телевизоров, фото- и видеокамер, чемоданы и сумки и др.
13
14.
ОСНОВНЫЕ ВИДЫ ВЫСОКОМОЛЕКУЛЯРНЫХ СОЕДИНЕНИЙМашиностроение;
Авиационная промышленность; автомобилестроение;
Космическая промышленность;
Электротехника; электроника (DVD и CD диски)
Бытовая техника (телевизоры, видеосистемы, компьютеры);
Строительство; телекоммуникация
ПЛАСТИКИ
ВОЛОКНА
Текстильная и легкая промышленность;
Природные (шерсть, хлопок) и искусственные (нейлон,
полиэфиры) волокна
ЭЛАСТОМЕРЫ
(КАУЧУКИ)
Упаковочные материалы;
Аудио-, видео- пленки;
Сельское хозяйство (парники)
ПЛЕНКИ
ПОКРЫТИЯ
КЛЕИ
БУМАГА
Авто- и авиационные, эластичные материалы
Лакокрасочная промышленность;
Мебельная промышленность
Разнообразные виды промышленности
14
Целлюлозно-бумажная промышленность
14
15.
1516.
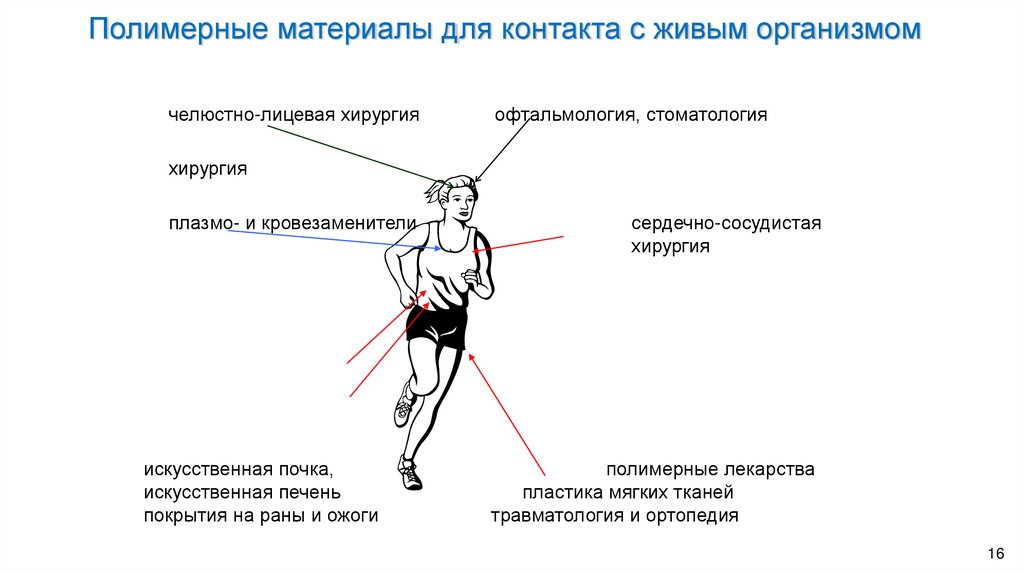
Полимерные материалы для контакта с живым организмомчелюстно-лицевая хирургия
офтальмология, стоматология
хирургия
плазмо- и кровезаменители
искусственная почка,
искусственная печень
покрытия на раны и ожоги
сердечно-сосудистая
хирургия
полимерные лекарства
пластика мягких тканей
травматология и ортопедия
16
17.
Роль макромолекул в структурной иерархии биологических системОрганеллы клетки (ядро, митохондрии,
хлоропласты, вакуоли, аппарат Гольджи и т.д.)
Супрамолекулряные комплексы (рибосомы,
цитоскелет, многоферментные комплексы)
106 109 а.е.м.
Биополимеры (белки, нуклеиновые кислоты,
полисахариды, липиды), 103 109 а.е.м.
17
18.
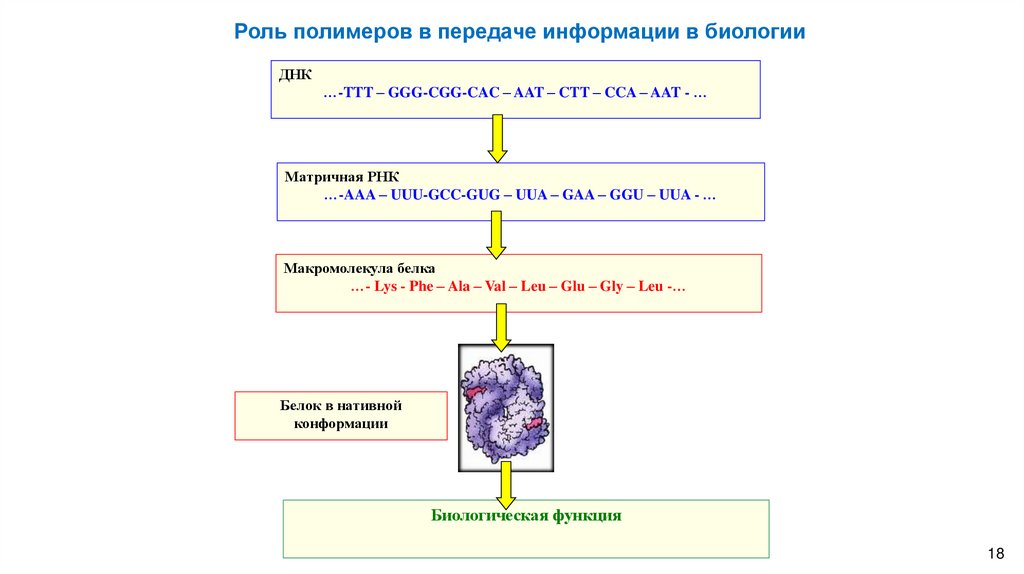
Роль полимеров в передаче информации в биологииДНК
…-TTT – GGG-CGG-CAC – AAT – CTT – CCA – AAT - …
Матричная РНК
…-AAA – UUU-GCC-GUG – UUA – GAA – GGU – UUA - …
Макромолекула белка
…- Lys - Phe – Ala – Val – Leu – Glu – Gly – Leu -…
Белок в нативной
конформации
Биологическая функция
18
19.
Основоположник российской полимерной науки• Растворы полимеров, - термодинамически
обратимые
системы,
подчиняющиеся
правилу фаз (Ф + С = К +1) (конец 1930-х г.)
• Исследования
механических
свойств
полимеров - выводы о природе физических и
фазовых состояний полимеров.
• Идея
о
связи
надмолекулярной
(супрамолекулярной) структуры с физикомеханическими свойствами полимера.
• Синтез
и
химическая
модификации
макромолекул
как
средство
целенаправленного создания полимерных
материалов
с
требуемыми
эксплуатационными свойствами.
1907-1969
академик Валентин Алексеевич Каргин –
основатель российской полимерной
школы, в 1955 г. организовал и
возглавил кафедру
высокомолекулярных соединений в МГУ
имени М.В.Ломоносова
19
20.
Особенности полимеров иклассификация
20
21.
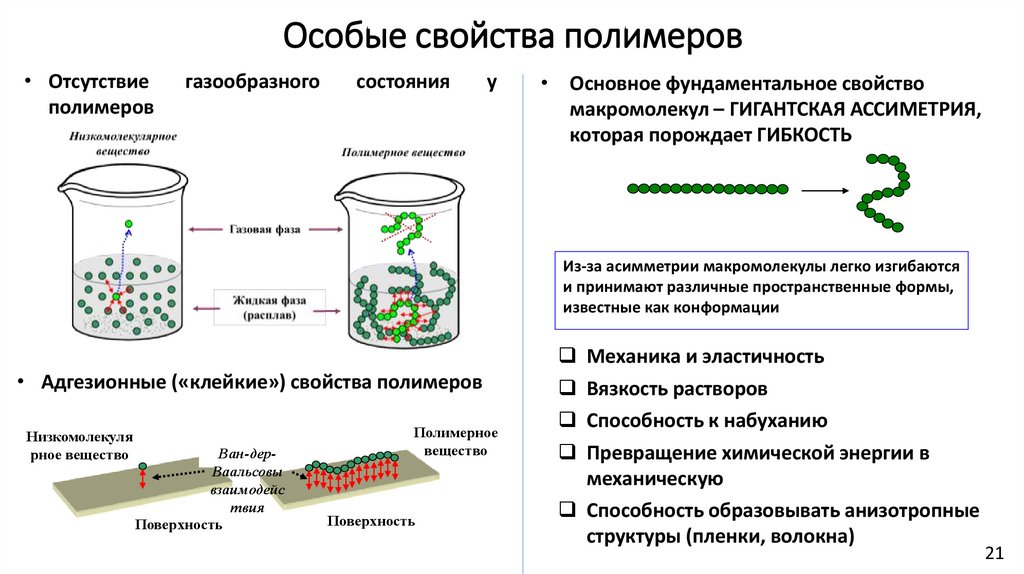
Особые свойства полимеров• Отсутствие
полимеров
газообразного
состояния
у
• Основное фундаментальное свойство
макромолекул – ГИГАНТСКАЯ АССИМЕТРИЯ,
которая порождает ГИБКОСТЬ
Из-за асимметрии макромолекулы легко изгибаются
и принимают различные пространственные формы,
известные как конформации
• Адгезионные («клейкие») свойства полимеров
Низкомолекуля
рное вещество
Ван-дерВаальсовы
взаимодейс
твия
Поверхность
Полимерное
вещество
Поверхность
Механика и эластичность
Вязкость растворов
Способность к набуханию
Превращение химической энергии в
механическую
Способность образовывать анизотропные
структуры (пленки, волокна)
21
22.
КЛАССИФИКАЦИЯ ПОЛИМЕРОВA. По происхождению
1. природные
2. искусственные
3. синтетические
Б. По геометрии основной цепи
1. линейные
2. разветвленные
3. гребнеобразные
4. лестничные
5. дендритные и др.
Г. По типу мономерных звеньев
1. гомополимеры
2. сополимеры
а) статистические
б) чередующиеся
в) блочные
г) привитые
В. По типу атомов в молекуле
Органические (карбоцепные и гетероцепные)
элементоорганические
неорганические
Д. По функциональным группам в
макромолекуле
углеводороды
спирты
кислоты
амиды
амины
простые и сложные эфиры
ацетали и др.
2222
22
23.
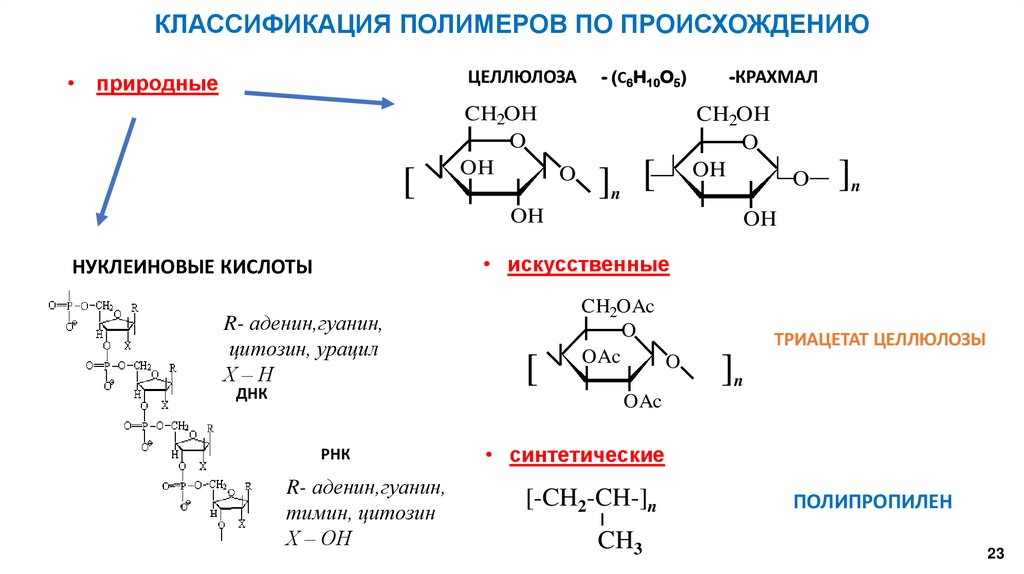
КЛАССИФИКАЦИЯ ПОЛИМЕРОВ ПО ПРОИСХОЖДЕНИЮЦЕЛЛЮЛОЗА
• природные
[
CH2OH
O
OH
O
- (С6H10O5)
]n [
OH
-КРАХМАЛ
CH2OH
O
OH
O
]n
OH
• искусственные
НУКЛЕИНОВЫЕ КИСЛОТЫ
R- аденин,гуанин,
цитозин, урацил
Х–Н
ДНК
[
CH2OAc
O
OAc
O
ТРИАЦЕТАТ ЦЕЛЛЮЛОЗЫ
]n
OAc
РНК
R- аденин,гуанин,
тимин, цитозин
Х – ОН
• синтетические
[-CH2-CH-]n
CH3
ПОЛИПРОПИЛЕН
23
24.
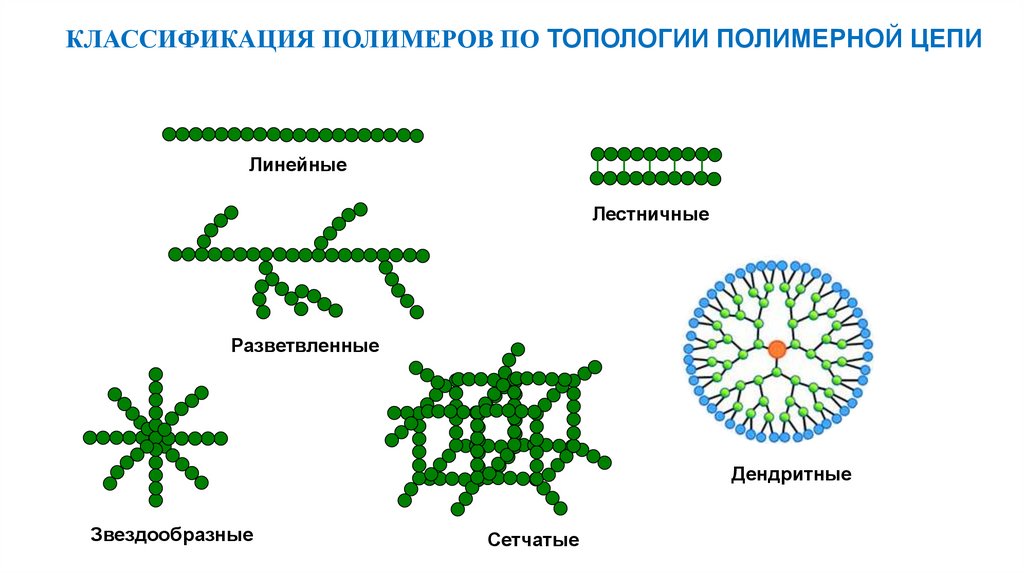
КЛАССИФИКАЦИЯ ПОЛИМЕРОВ ПО ТОПОЛОГИИ ПОЛИМЕРНОЙ ЦЕПИЛинейные
Лестничные
Разветвленные
Дендритные
Звездообразные
Сетчатые
25.
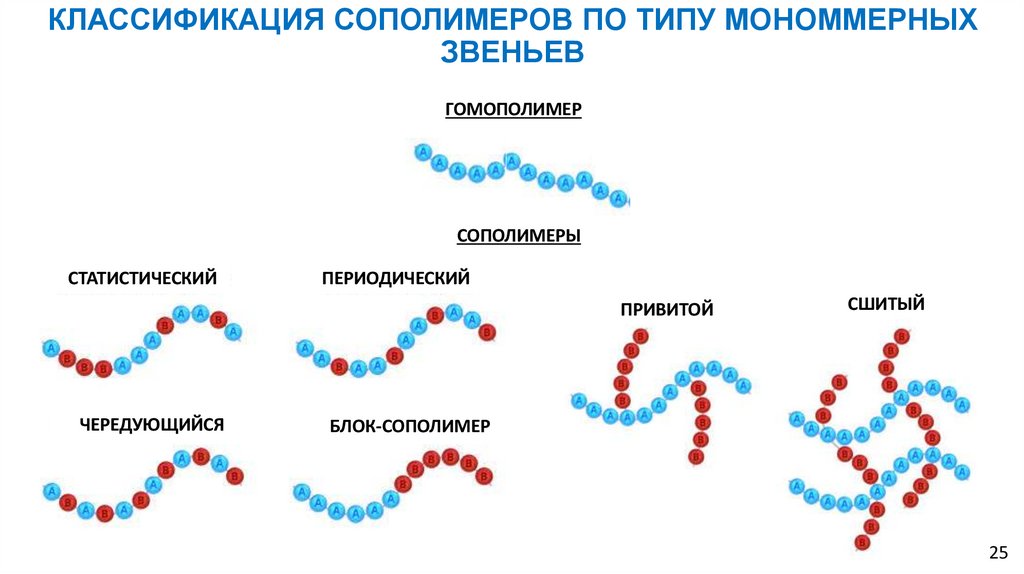
КЛАССИФИКАЦИЯ СОПОЛИМЕРОВ ПО ТИПУ МОНОММЕРНЫХЗВЕНЬЕВ
ГОМОПОЛИМЕР
СОПОЛИМЕРЫ
СТАТИСТИЧЕСКИЙ
ПЕРИОДИЧЕСКИЙ
ПРИВИТОЙ
ЧЕРЕДУЮЩИЙСЯ
СШИТЫЙ
БЛОК-СОПОЛИМЕР
25
26.
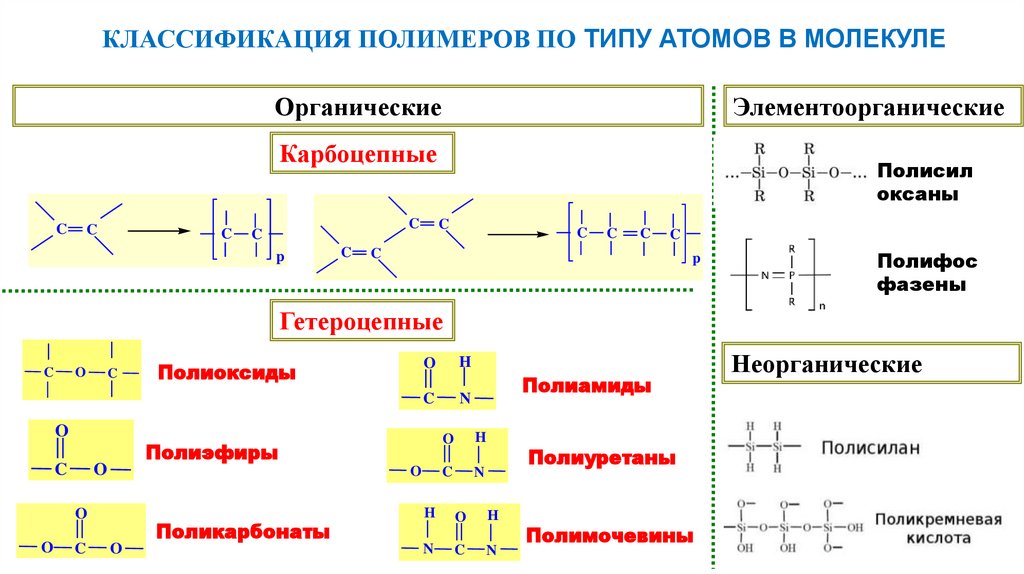
КЛАССИФИКАЦИЯ ПОЛИМЕРОВ ПО ТИПУ АТОМОВ В МОЛЕКУЛЕОрганические
Элементоорганические
Карбоцепные
C
C
C
C
C
p
C
Полисил
оксаны
C
C
C
C
C
C
p
Полифос
фазены
Гетероцепные
C
O
C
O
C
O
C
O
H
C
N
Полиэфиры
O
O
O
Полиоксиды
Поликарбонаты
O
Полиамиды
O
H
C
N
Полиуретаны
H
O
H
N
C
N
Полимочевины
Неорганические
27.
КЛАССИФИКАЦИЯ ПОЛИМЕРОВ ПО ФУНКЦИОНАЛЬНЫМГРУППАМ В МАКРОМОЛЕКУЛЕ
27
28.
Конформация и конфигурацияполимеров
28
29.
ОСНОВНЫЕ ТЕРМИНЫ И ПОНЯТИЯКОНФОРМАЦИЯ
макромолекулы
–
взаимное
расположение атомов или атомных
групп в макромолекуле, которое
может изменяться без разрыва
ковалентных связей основной цепи
за счет внутреннего вращения вокруг
химических связей основной цепи, а
также упругости химических связей и
валентных углов.
КОНФИГУРАЦИЯ
макромолекулы
–
взаимное
расположение атомов или атомных
групп в макромолекуле, которое
формируется
при
синтезе
полимера и не может изменяться
без разрыва ковалентных связей
основной
полимерной
цепи
(алгоритм,
согласно
которому
мономерные звенья соединены
друг с другом в макромолекуле).
29
30.
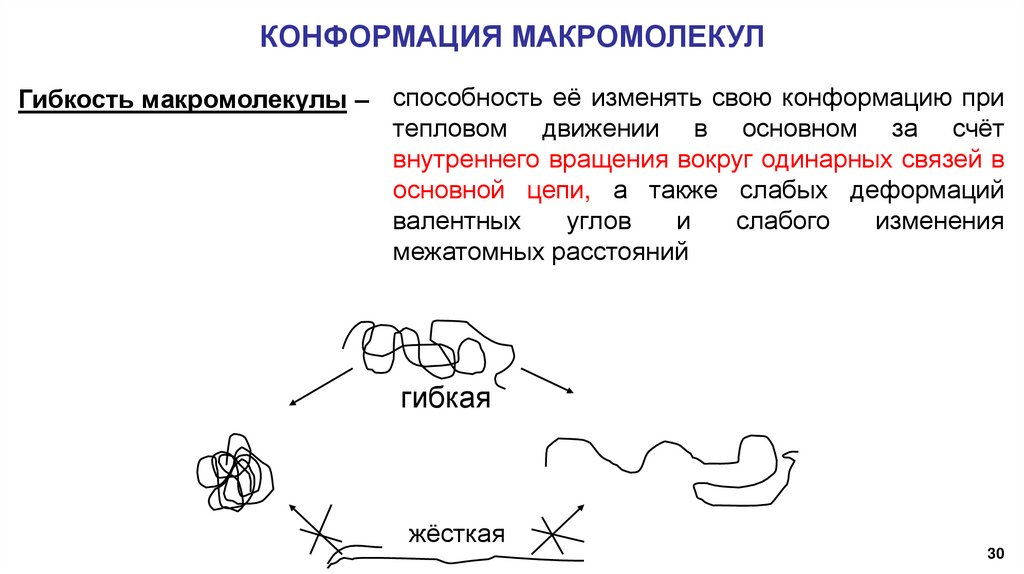
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛГибкость макромолекулы – способность её изменять свою конформацию при
тепловом движении в основном за счёт
внутреннего вращения вокруг одинарных связей в
основной цепи, а также слабых деформаций
валентных
углов
и
слабого
изменения
межатомных расстояний
гибкая
жёсткая
30
31.
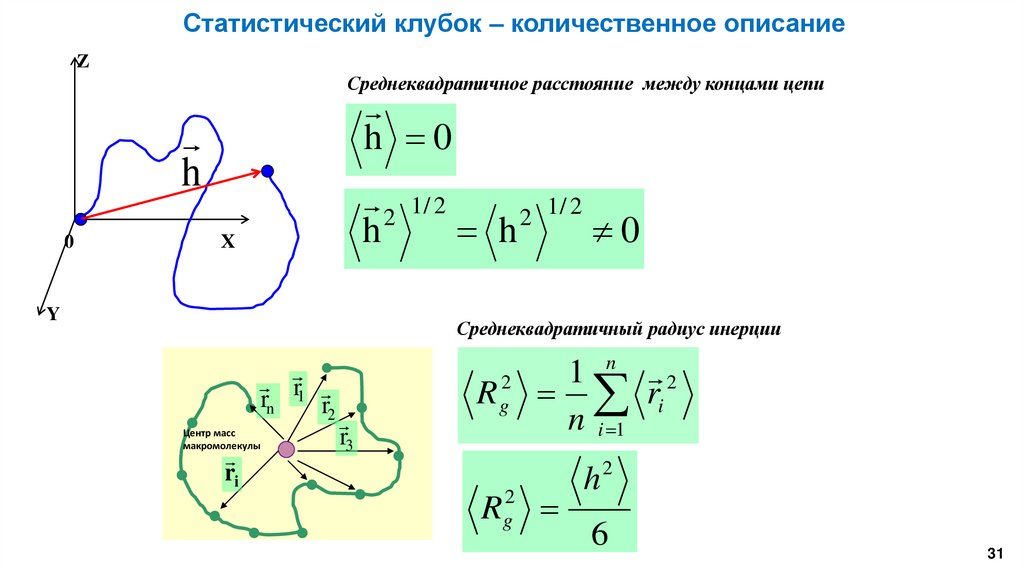
Статистический клубок – количественное описаниеZ
Среднеквадратичное расстояние между концами цепи
h 0
h
0
2 1/ 2
2 1/ 2
h
h
0
Х
Y
Среднеквадратичный радиус инерции
r1
rn
r2
Центр масс
макромолекулы
ri
r3
R g2
R
2
g
1 n 2
ri
n i 1
h2
6
31
32.
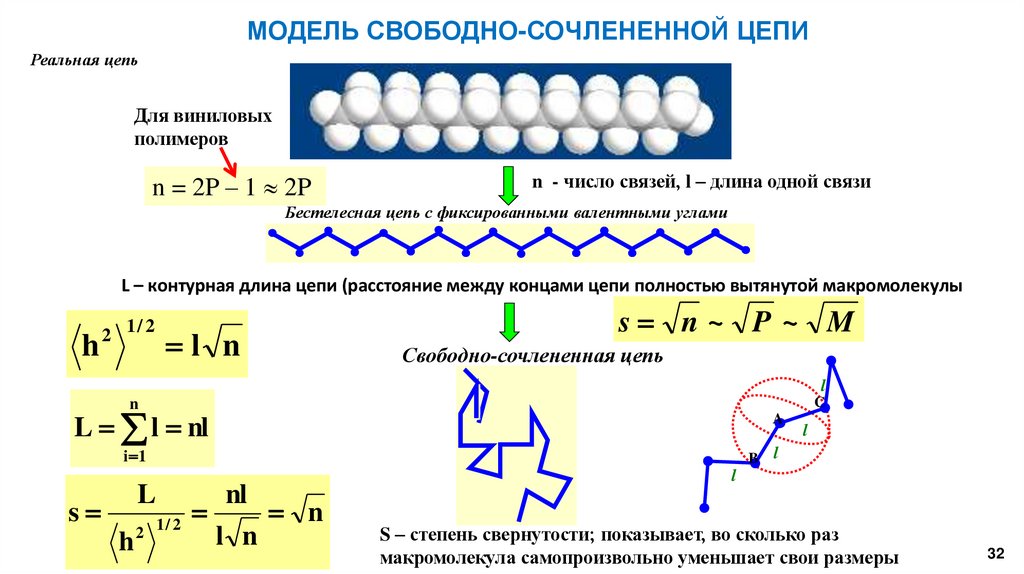
МОДЕЛЬ СВОБОДНО-СОЧЛЕНЕННОЙ ЦЕПИРеальная цепь
Для виниловых
полимеров
n = 2P – 1 2P
n - число связей, l – длина одной связи
Бестелесная цепь с фиксированными валентными углами
L – контурная длина цепи (расстояние между концами цепи полностью вытянутой макромолекулы
h
2 1/ 2
l n
s n~ P ~ M
Свободно-сочлененная цепь
l
C
n
L l nl
A
i 1
L
nl
s
n
1
/
2
l n
h2
l
B l
l
S – степень свернутости; показывает, во сколько раз
макромолекула самопроизвольно уменьшает свои размеры
32
33.
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛСТАТИСТИЧЕСКИЙ СЕГМЕНТ (СЕГМЕНТ КУНА)
– модельный условный отрезок-вектор, соединяющий первое и i
мономерные звенья реальной макромолекулы. На i–м звене теряется корреляция
взаимного влияния звеньев при вращении вокруг связей основной цепи (сочленение
между сегментами Куна свободное(!) - угол меняется от 0 до 360º).
сегмент
сегменты
h ZA
2
2
A –длина сегмента, Z – число сегментов в цепи
33
34.
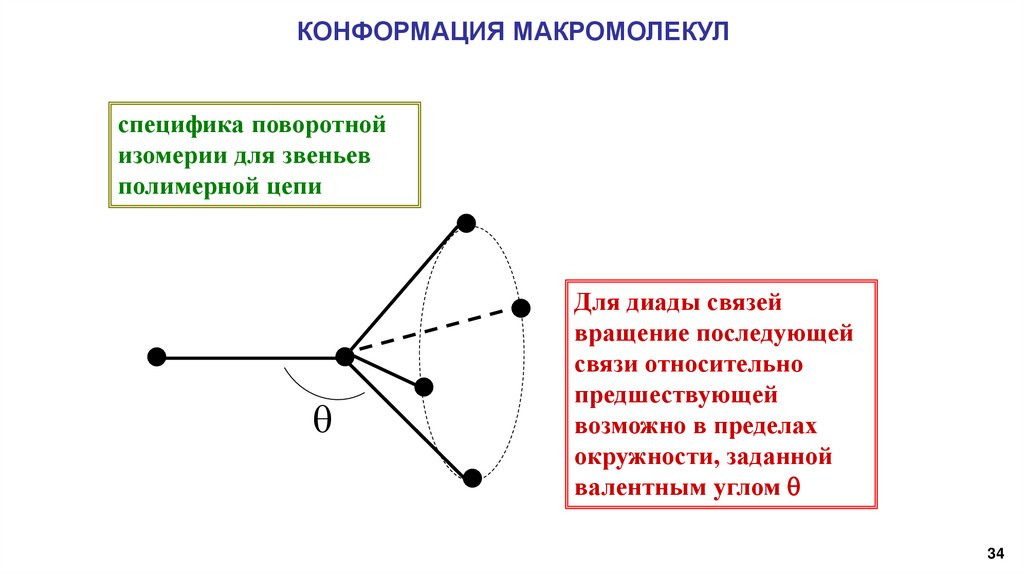
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛспецифика поворотной
изомерии для звеньев
полимерной цепи
Для диады связей
вращение последующей
связи относительно
предшествующей
возможно в пределах
окружности, заданной
валентным углом
34
35.
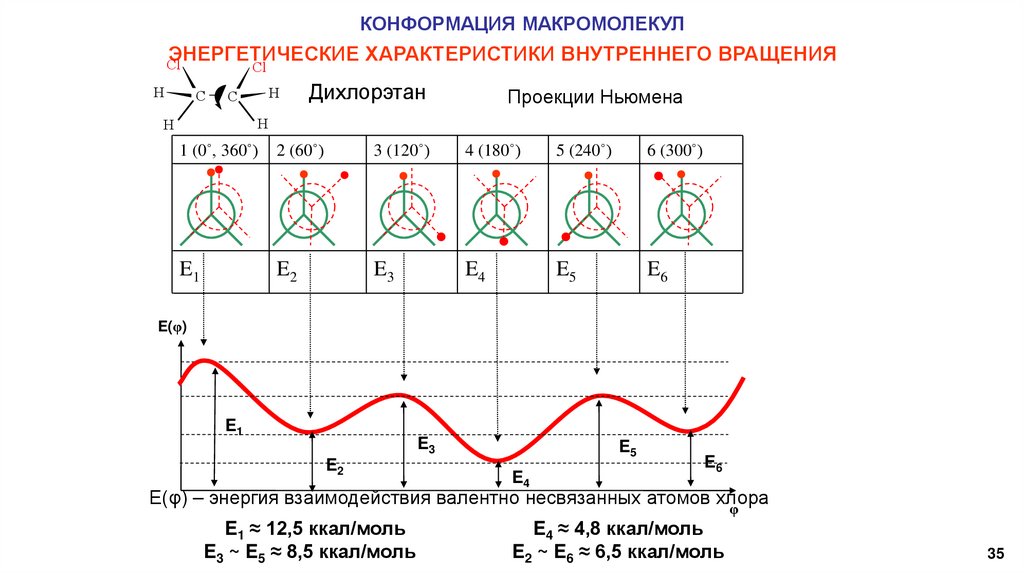
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛЭНЕРГЕТИЧЕСКИЕ ХАРАКТЕРИСТИКИ ВНУТРЕННЕГО ВРАЩЕНИЯ
Cl
H
Cl
C
H
C
Дихлорэтан
Проекции Ньюмена
H
H
1 (0˚, 360˚)
2 (60˚)
3 (120˚)
4 (180˚)
5 (240˚)
6 (300˚)
E1
E2
E3
E4
E5
E6
E(φ)
E1
E3
E2
E5
E4
E6
E(φ) – энергия взаимодействия валентно несвязанных атомов хлора
φ
E1 ≈ 12,5 ккал/моль
E3 ~ E5 ≈ 8,5 ккал/моль
E4 ≈ 4,8 ккал/моль
E2 ~ E6 ≈ 6,5 ккал/моль
35
36.
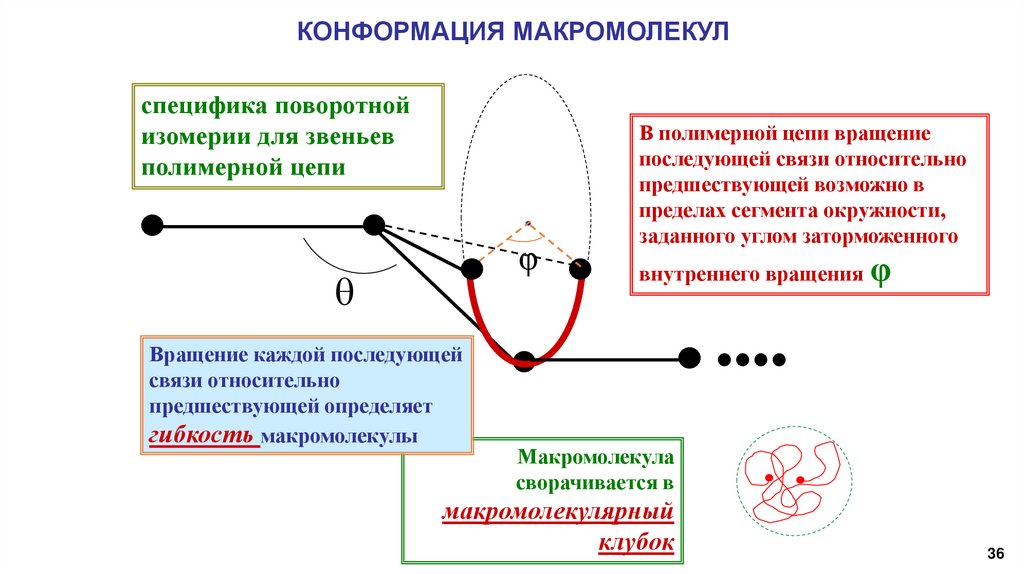
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛспецифика поворотной
изомерии для звеньев
полимерной цепи
φ
Вращение каждой последующей
связи относительно
предшествующей определяет
гибкость макромолекулы
В полимерной цепи вращение
последующей связи относительно
предшествующей возможно в
пределах сегмента окружности,
заданного углом заторможенного
внутреннего вращения φ
Макромолекула
сворачивается в
макромолекулярный
клубок
36
37.
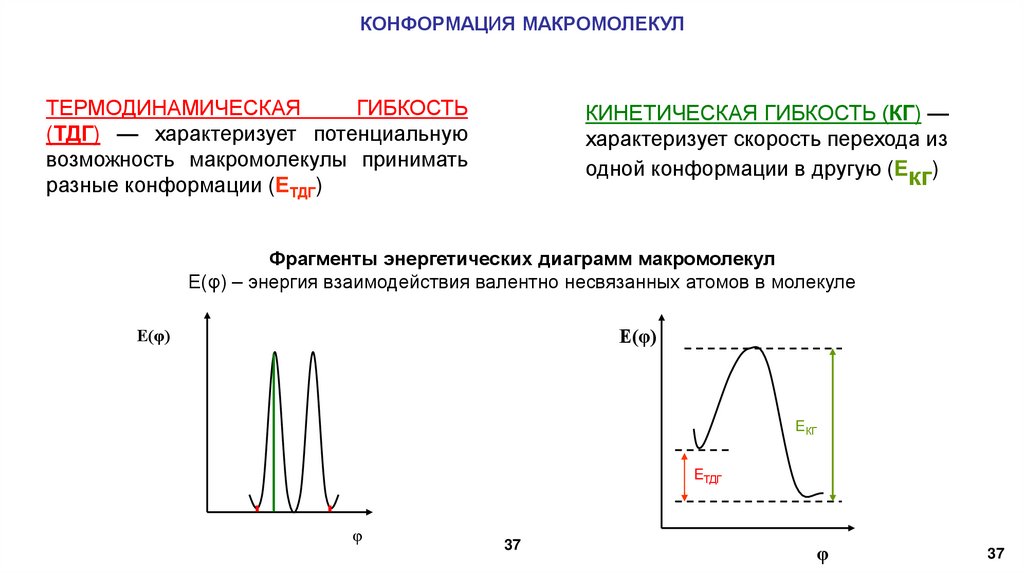
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛТЕРМОДИНАМИЧЕСКАЯ
ГИБКОСТЬ
(ТДГ) — характеризует потенциальную
возможность макромолекулы принимать
разные конформации (ЕТДГ)
КИНЕТИЧЕСКАЯ ГИБКОСТЬ (КГ) —
характеризует скорость перехода из
одной конформации в другую (Eкг)
Фрагменты энергетических диаграмм макромолекул
E(φ) – энергия взаимодействия валентно несвязанных атомов в молекуле
E(φ)
E(φ)
EКГ
EТДГ
φ
37
φ
37
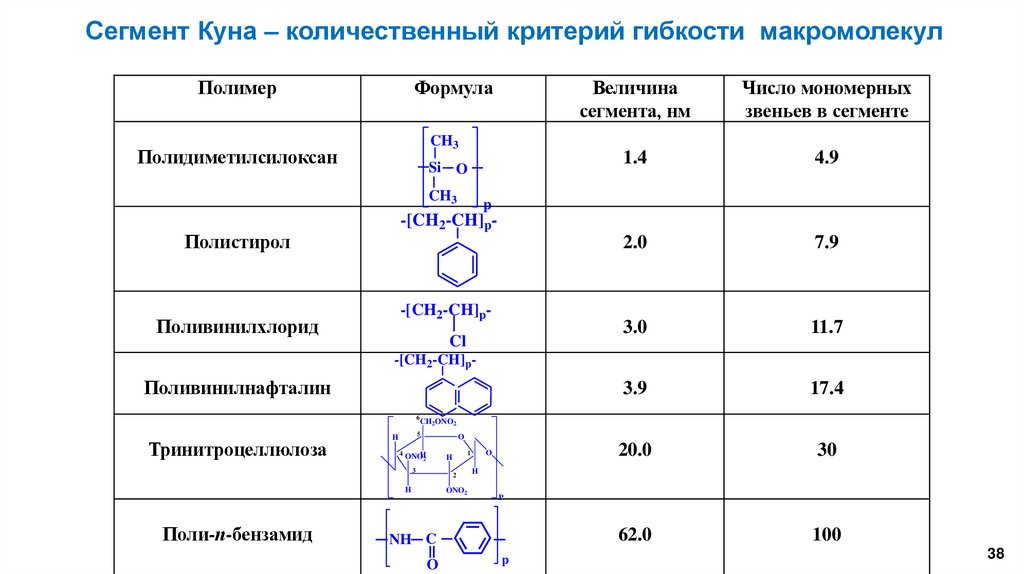
38.
Сегмент Куна – количественный критерий гибкости макромолекулПолимер
Формула
CH3
Полидиметилсилоксан
Si O
CH3
Величина
сегмента, нм
Число мономерных
звеньев в сегменте
1.4
4.9
2.0
7.9
3.0
11.7
3.9
17.4
20.0
30
62.0
100
p
-[CH2-CH]p-
Полистирол
-[CH2-CH]p-
Поливинилхлорид
Cl
-[CH2-CH]p-
Поливинилнафталин
6
Тринитроцеллюлоза
CH2ONO2
5
H
O
4 ONOH
3
2
H
Поли-п-бензамид
O
1
H
2
ONO2
H
P
NH C
O
p
38
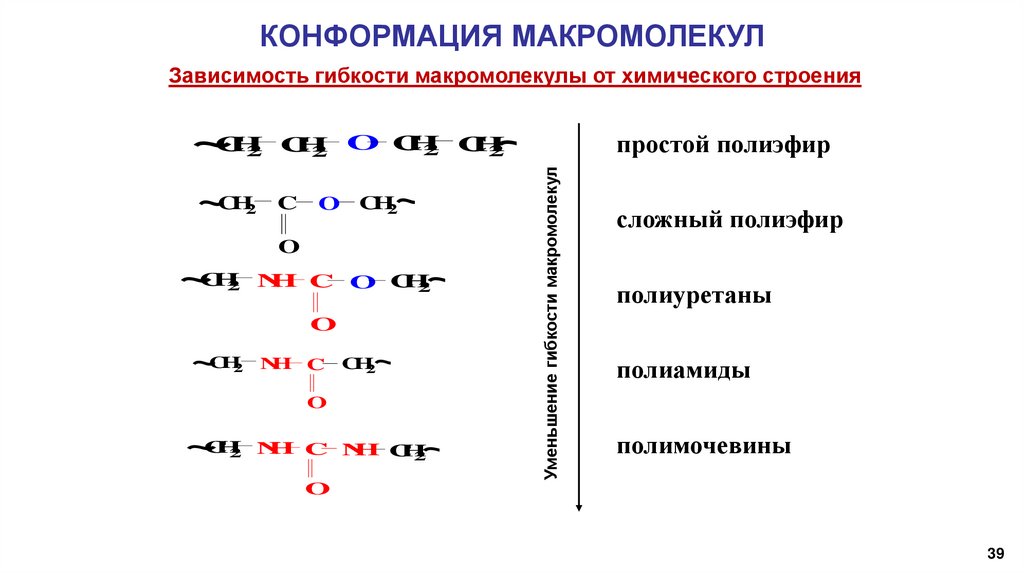
39.
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛЗависимость гибкости макромолекулы от химического строения
~CH CH O CH CH~
2
2
~CH C O CH~
2
2
O
~CH NH C O CH~
2
2
O
~CH NH C CH~
2
2
O
~CH NH C NH CH~
2
2
простой полиэфир
2
Уменьшение гибкости макромолекул
2
сложный полиэфир
полиуретаны
полиамиды
полимочевины
O
39
40.
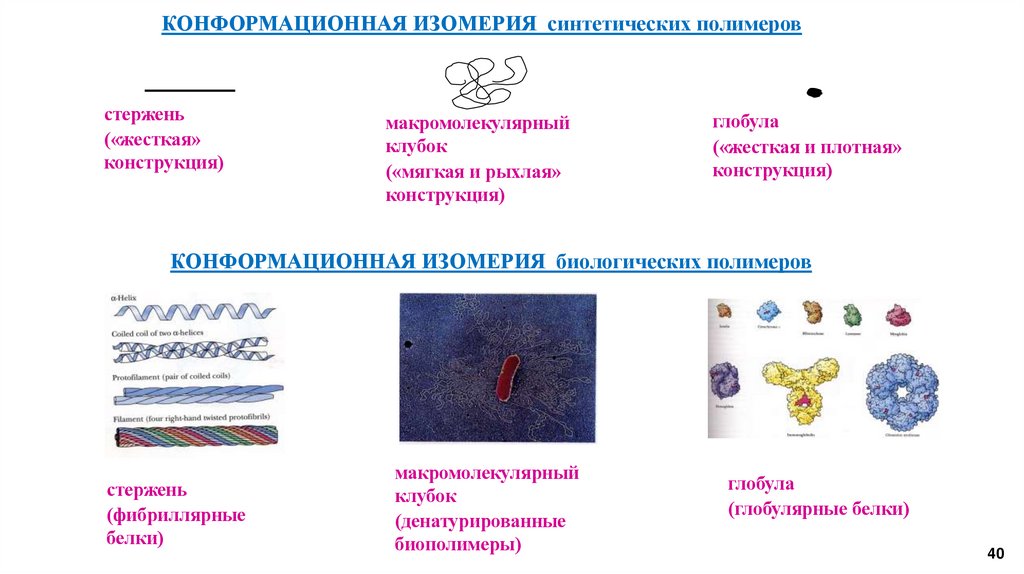
КОНФОРМАЦИОННАЯ ИЗОМЕРИЯ синтетических полимеровстержень
(«жесткая»
конструкция)
макромолекулярный
клубок
(«мягкая и рыхлая»
конструкция)
глобула
(«жесткая и плотная»
конструкция)
КОНФОРМАЦИОННАЯ ИЗОМЕРИЯ биологических полимеров
стержень
(фибриллярные
белки)
макромолекулярный
клубок
(денатурированные
биополимеры)
глобула
(глобулярные белки)
40
41.
КОНФОРМАЦИЯ МАКРОМОЛЕКУЛФакторы, уменьшающие гибкость (КГ и ТДГ) макромолекулы
A. Наличие в основной цепи:
1. кратных связей (-С=С-, -С=N-)
2. жёстких фрагментов (ароматические
кольца, ангидридные циклы)
3. объёмистых заместителей
4. внутримолекулярных взаимодействий
(водородные связи, кулоновские
взаимодействия)
Б. Несимметричность строения основной цепи
В. Нерегулярность строения цепи
41
42.
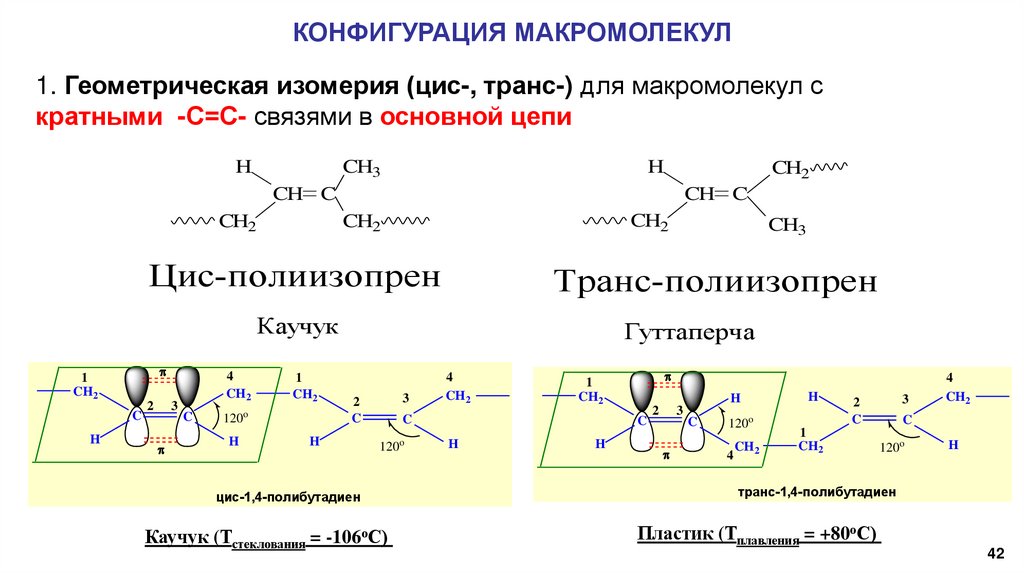
КОНФИГУРАЦИЯ МАКРОМОЛЕКУЛ1. Геометрическая изомерия (цис-, транс-) для макромолекул с
кратными -С=С- связями в основной цепи
H
CH3
H
CH2
CH C
CH2
CH C
CH2
CH2
Цис-полиизопрен
Транс-полиизопрен
Каучук
1
CH2
C
H
2
3
4
CH2
C
120
H
1
CH2
o
CH3
Гуттаперча
3
2
C
H
4
CH2
C
120o
цис-1,4-полибутадиен
Каучук (Тстеклования = -106оС)
1
CH2
H
C
H
H
2
3
C
120o
4
CH2
H
3
2
C
1
CH2
4
CH2
C
120o
H
транс-1,4-полибутадиен
Пластик (Тплавления = +80оС)
42
43.
КОНФИГУРАЦИЯ МАКРОМОЛЕКУЛ2. ”Локальная” изомерия (на примере макромолекул винилового ряда
для двух соседних мономерных звеньев)
г
о
л
о
в
а
H
C
H
2 C
х
в
о
с
т
а)
б)
CH2
CH2
CH
CH
X
X
CH
CH2
X
в)
CH
X
CH2
X
CH2
голова-голова (Г-Г)
CH
голова-хвост (Г-Х)
ю
X
CH2
CH
X
хвост-хвост (Х-Х)
43
44.
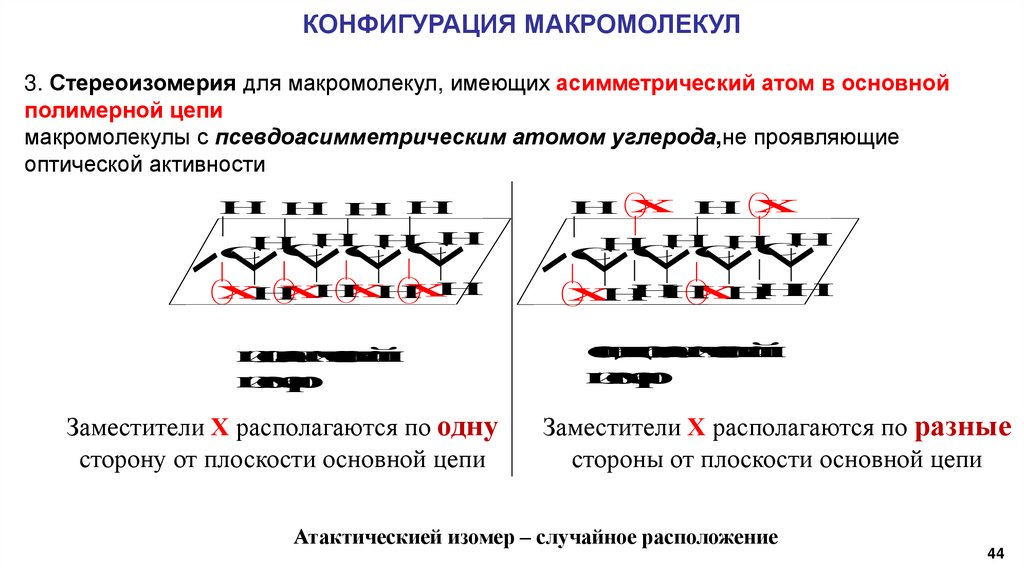
КОНФИГУРАЦИЯ МАКРОМОЛЕКУЛ3. Стереоизомерия для макромолекул, имеющих асимметрический атом в основной
полимерной цепи
макромолекулы с псевдоасимметрическим атомом углерода,не проявляющие
оптической активности
H H H H
H X H X
H H H H
С С С С
H
H H
H
С
С
С
С
H
X
X
H
X
H
X
H
H
H
H
H
X
H
X
H
и
з
о
т
а
к
т
и
ч
е
с
к
и
й
и
з
о
м
е
р
Заместители Х располагаются по одну
сторону от плоскости основной цепи
с
и
н
д
и
о
т
а
к
т
и
ч
е
с
к
и
й
и
з
о
м
е
р
Заместители Х располагаются по разные
стороны от плоскости основной цепи
Атактическией изомер – случайное расположение
44
45.
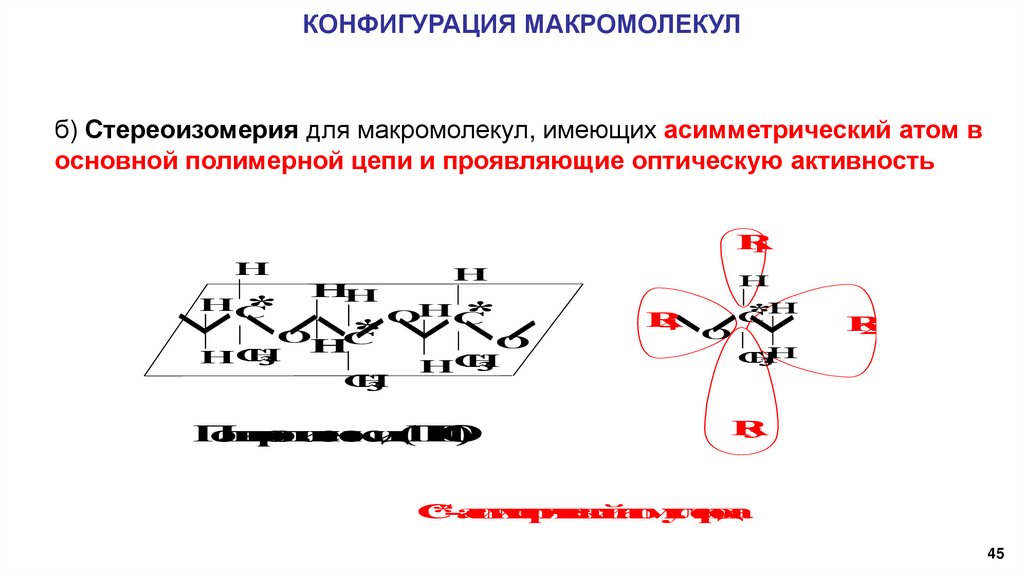
КОНФИГУРАЦИЯ МАКРОМОЛЕКУЛб) Стереоизомерия для макромолекул, имеющих асимметрический атом в
основной полимерной цепи и проявляющие оптическую активность
R
1
H
HH
H
HС
*
*
OHС
*
O
С
O
H
C
H
H 3
H
3
HC
C
H
3
П
о
л
и
п
р
о
п
и
л
е
н
о
к
с
и
д
(
П
П
О
)
H
R
4
O
*H
С
R
2
H
C
H
3
R
3
C
*
-а
с
и
м
м
е
т
р
и
ч
е
с
к
и
й
а
т
о
м
у
г
л
е
р
о
д
а
45
46.
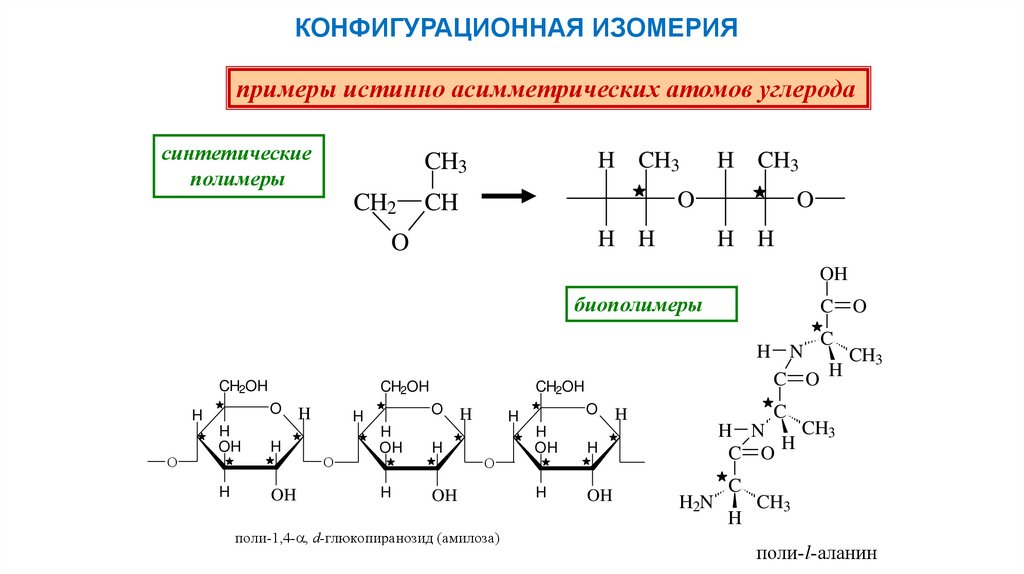
КОНФИГУРАЦИОННАЯ ИЗОМЕРИЯпримеры истинно асимметрических атомов углерода
синтетические
полимеры
CH2
CH3
H CH3
H CH3
CH
O
O
H H
O
H H
OH
биополимеры
CH2OH
O
H
O
CH2OH
H
OH
H
H
OH
H
O
C
H N
CH3
C O H
CH2OH
O
H
C O
H
OH
H
H
OH
H
O
H
O
поли-1,4- , d-глюкопиранозид (амилоза)
H
OH
H
H
OH
C
H
CH3
H N
H
C O
H2N
C
H
CH3
поли-l-аланин
47.
Молекулярная масса полимеров47
48.
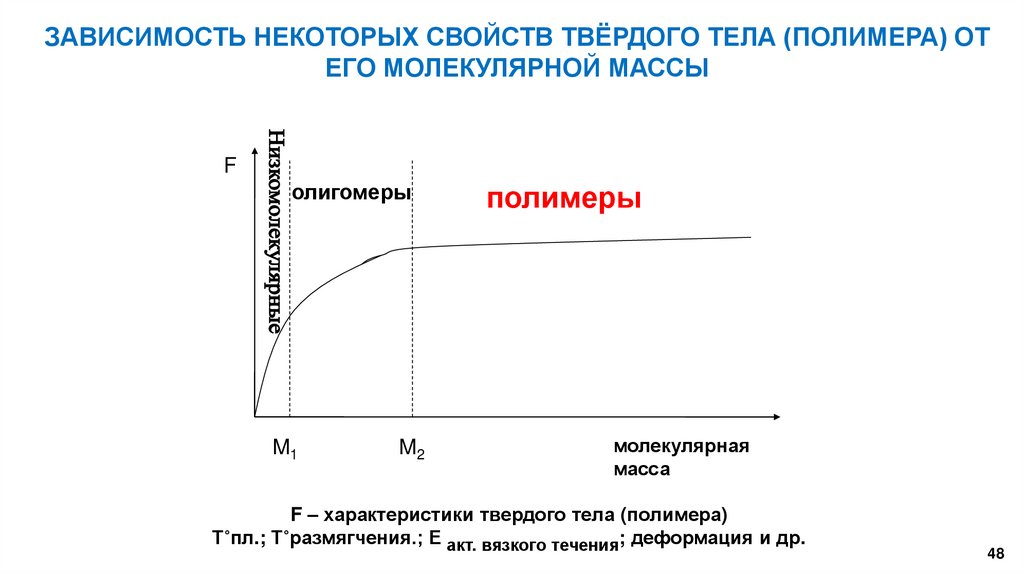
ЗАВИСИМОСТЬ НЕКОТОРЫХ СВОЙСТВ ТВЁРДОГО ТЕЛА (ПОЛИМЕРА) ОТЕГО МОЛЕКУЛЯРНОЙ МАССЫ
F
олигомеры
M1
M2
полимеры
молекулярная
масса
F – характеристики твердого тела (полимера)
T˚пл.; T˚размягчения.; Е акт. вязкого течения; деформация и др.
48
49.
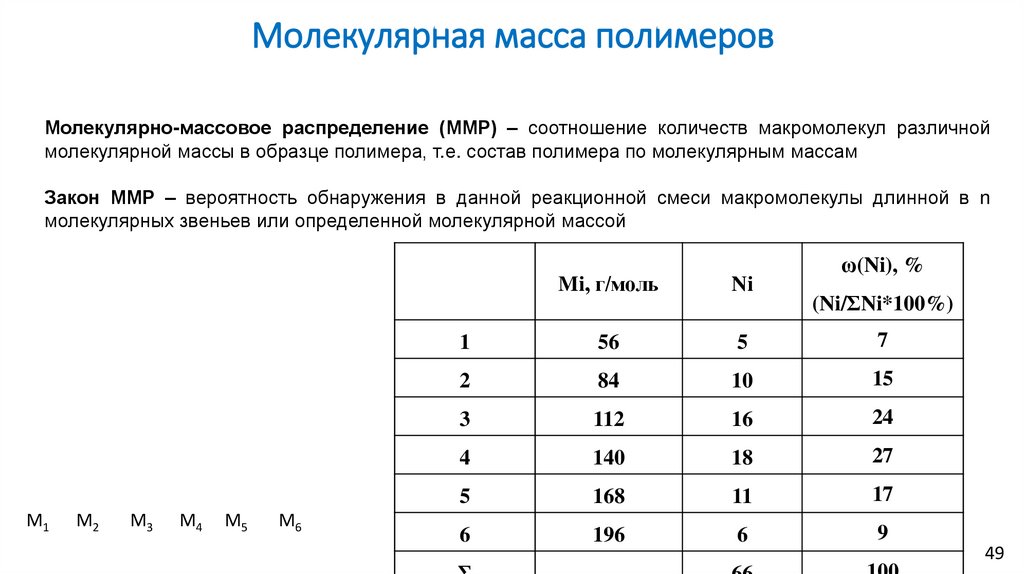
Молекулярная масса полимеровМолекулярно-массовое распределение (ММР) – соотношение количеств макромолекул различной
молекулярной массы в образце полимера, т.е. состав полимера по молекулярным массам
Закон ММР – вероятность обнаружения в данной реакционной смеси макромолекулы длинной в n
молекулярных звеньев или определенной молекулярной массой
M1
M2
M3
M4
M5
M6
ω(Ni), %
Mi, г/моль
Ni
1
56
5
7
2
84
10
15
3
112
16
24
4
140
18
27
5
168
11
17
6
196
6
9
(Ni/ΣNi*100%)
49
50.
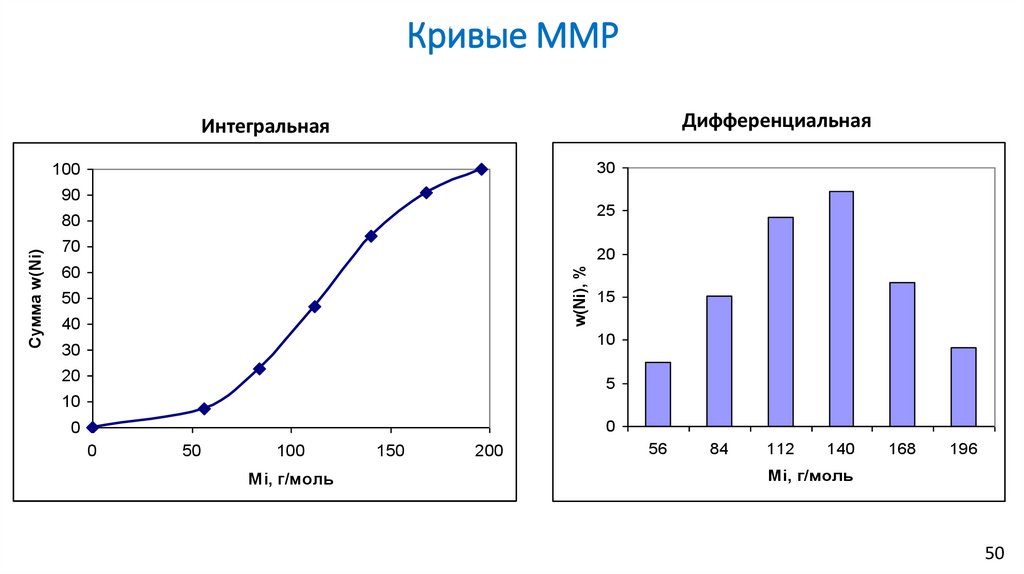
Кривые ММРДифференциальная
Интегральная
30
100
90
25
70
20
60
w(Ni), %
Сумма w(Ni)
80
50
40
15
10
30
20
5
10
0
0
0
50
100
Mi, г/моль
150
200
56
84
112
140
168
196
Mi, г/моль
50
51.
Молекулярная масса полимеровСреднечисловая молекулярная масса
(Mn) – является среднеарифметической
величиной
и
равна
отношению
молекулярной массы образца (Mi) к
общему числу макромолекул (Ni):
M N
M
N
i
n
i
i
Средневесовая молекулярная масса
(Mw) – является отношением доли
каждой молекулярной массы фракции
макромолекул
(xi)
к
общей
молекулярной массе смеси:
N M
M M x
N M
i
i
2
i
i
i
i
fn (M)MdM Mn
0
51
52.
Молекулярная масса полимеровMi, г/моль
Ni
Mi*Ni
1
56
5
280
2
84
10
840
3
112
16
1792
4
140
18
2520
5
168
11
1848
6
196
6
1176
66
8456
Σ
Среднечисловая молекулярная масса (Mn)
M N
M
N
i
n
M N
8456
M
128,12 г / моль
66
N
i
i
i
i
n
i
52
53.
Молекулярная масса полимеровMi, г/моль
Ni
Mi*Ni
Ni*Mi2
1
56
5
280
15680
2
84
10
840
70560
3
112
16
1792
200704
4
140
18
2520
352800
5
168
11
1848
310464
6
196
6
1176
230496
66
8456
1180704
Σ
Ni M i
Средневесовая молекулярная масса (Mw)
N M
M M x
N M
i
i
2
i
i
i
i
2
1180704
M M i xi
139,63г / моль
8456
Ni M i
53
54.
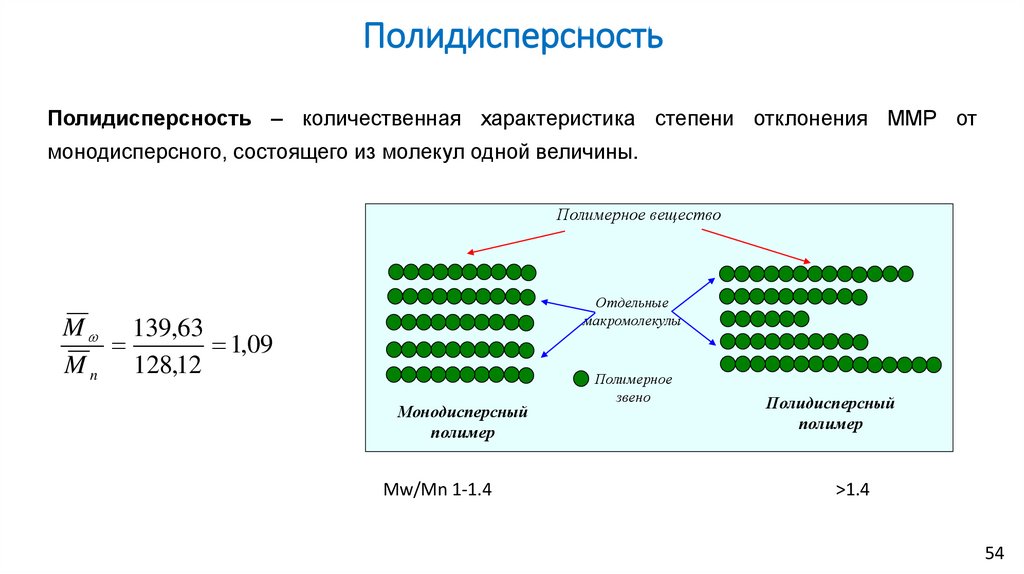
ПолидисперсностьПолидисперсность – количественная характеристика степени отклонения ММР от
монодисперсного, состоящего из молекул одной величины.
Полимерное вещество
Отдельные
макромолекулы
M 139,63
1,09
M n 128,12
Монодисперсный
полимер
Mw/Mn 1-1.4
Полимерное
звено
Полидисперсный
полимер
>1.4
54
55.
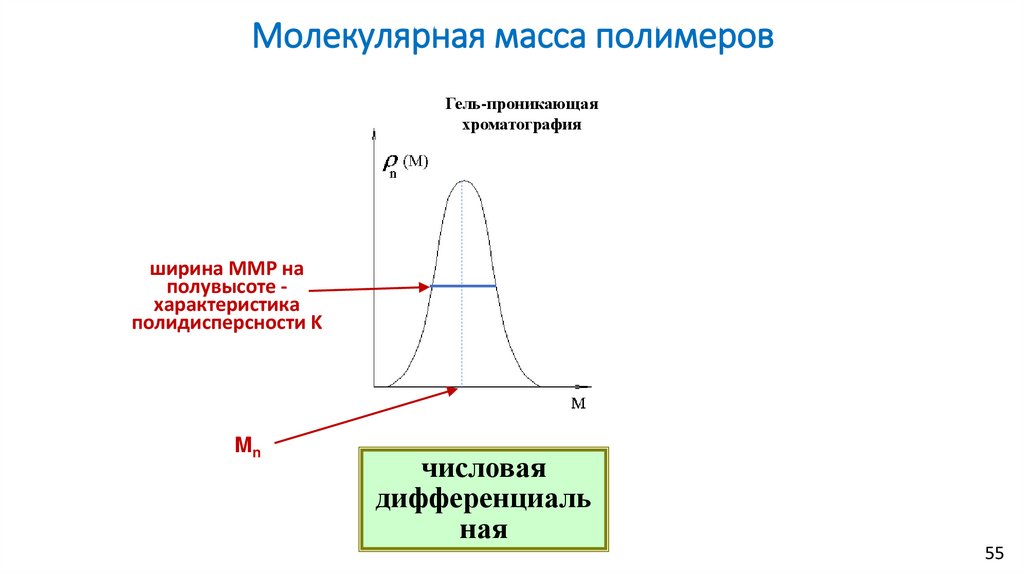
Молекулярная масса полимеровГель-проникающая
хроматография
ширина ММР на
полувысоте характеристика
полидисперсности K
Mn
числовая
дифференциаль
ная
55
56.
Молекулярная масса полимеровZ-средневесовая
молекулярная
масса
(Mz,
седиментационное
равновесие) – физического смысла не
имеет, в настоящее время практически
не используется
MZ
NiM
3
i
i
NiM
i
2
i
Средневязкостная молекулярная масса (Mη)
Уравнение Марка-Хунвика-Флори
KM
уд
c lim 0
c
- 0
уд
0
56
57.
Методы синтеза полимеров57
58.
Методы синтеза полимеров• Свободнорадикальная полимеризация
• Живая полимеризация (катионная, анионная)
• Псевдоживая полимеризация
• Поликонденсация
58
59.
ПОЛИМЕРИЗАЦИЯ (цепной процесс)Радикальная
Анионная
Катионная
(актив. центр R●)
(актив. центр R▬)
(актив. центр R+)
1. Инициирование (присоединение радикалов инициатора к кратной связи мономеров против правила
Марковникова)
Инициирующий радикал становится сначала одной концевой группой в макрорадикале
I
I
I + СН2=СН
ICН2-СН
I
2I
I
Х
X
Появление радикалов при окислительно-восстановительных реакциях
а) H2O2 + Fe2+ HO- +HO +Fe3+ реактив Фентона
Появление радикалов при гомолитическом разрыве связей, например, O-O
C6H5-C-O-O-C-C6H5
O
O
.
2C H -C-O
6
5
O
.
2C6H5 + 2CO2
59
60.
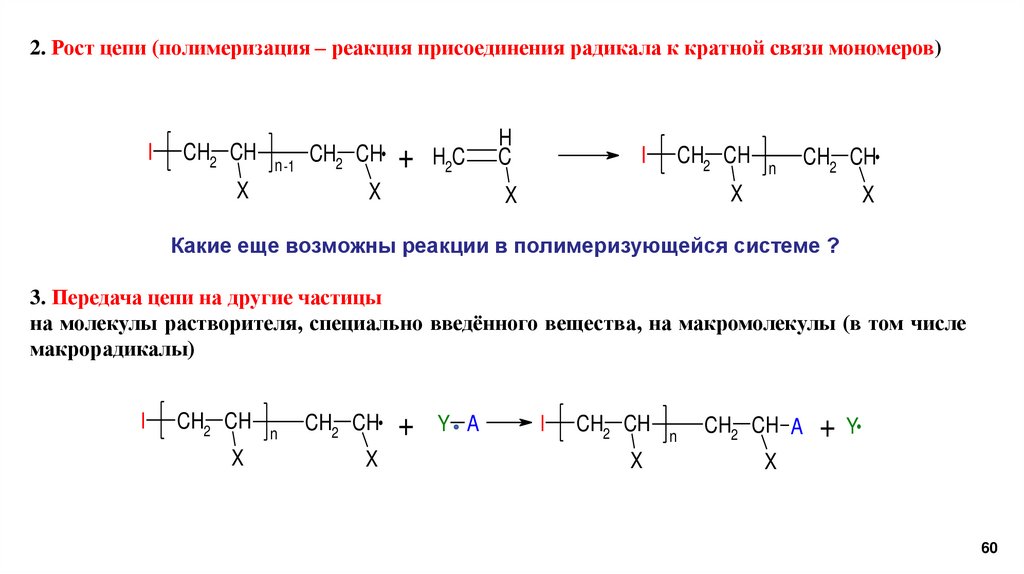
2. Рост цепи (полимеризация – реакция присоединения радикала к кратной связи мономеров)I
CH2 CH
n -1
X
CH2 CH + H2C
X
H
C
I
CH2 CH
n
CH2 CH
X
X
X
Какие еще возможны реакции в полимеризующейся системе ?
3. Передача цепи на другие частицы
на молекулы растворителя, специально введённого вещества, на макромолекулы (в том числе
макрорадикалы)
I
CH2 CH
X
n
CH2 CH
X
+ Y A
I
CH2 CH
X
n
CH2 CH A
+Y
X
60
61.
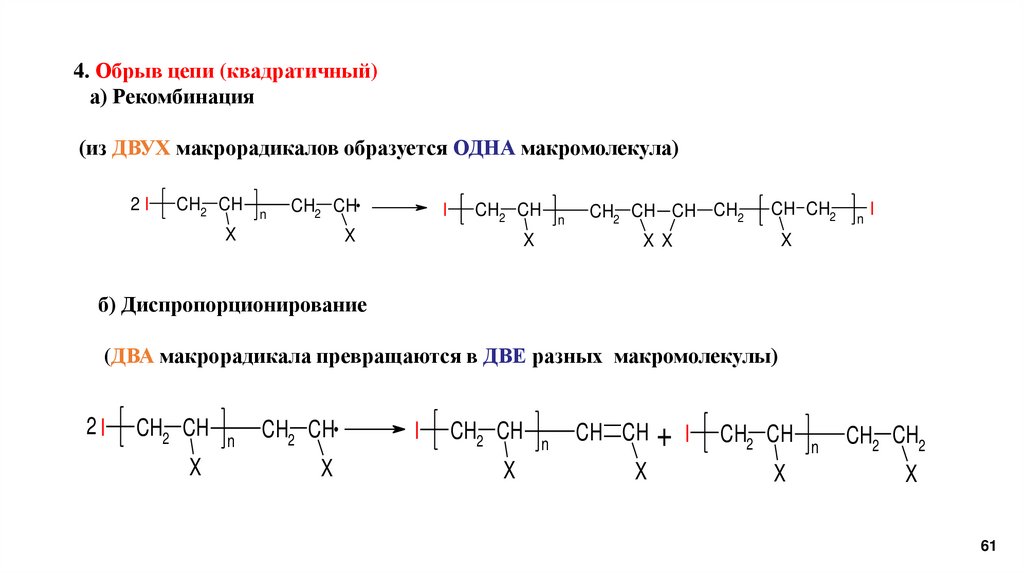
4. Обрыв цепи (квадратичный)а) Рекомбинация
(из ДВУХ макрорадикалов образуется ОДНА макромолекула)
2I
CH2 CH
n
CH2 CH
X
I
CH2 CH
X
X
n
CH2 CH CH CH2
CH CH2
n
I
X
X X
б) Диспропорционирование
(ДВА макрорадикала превращаются в ДВЕ разных макромолекулы)
2I
CH2 CH
X
n
CH2 CH
X
I
CH2 CH
X
n
CH CH + I
X
CH2 CH
X
n
CH2 CH2
X
61
62.
АНИОННАЯ ПОЛИМЕРИЗАЦИЯМономеры
ВИНИЛОВЫЕ мономеры с электроноакцепторными заместителями
CH2
CH
Роль X – стабилизация аниона
X – нитрил, сложноэфирная группа, арил, винил.
X
CH3
CH2
CH
CN
CH2
CH2
CH
C
CH2
COOCH3
акрилонитрил метилметакрилат
стирол
CH
CH
CH2
1,3-бутадиен
Образование обобщенной единой ароматической системы ПИ-связей (бензольного
ядра) приводит к значительному энергетическому повышению устойчивости системы
примерно на 40 ккал\моль по сравнению с системой с тремя изолированными кратными
связями. Это является одной из причин того, что в зависимости от конкретных условий
реакции, ароматическое кольцо проявляет либо электроно-акцепторные, либо электронодонорные свойства
62
63.
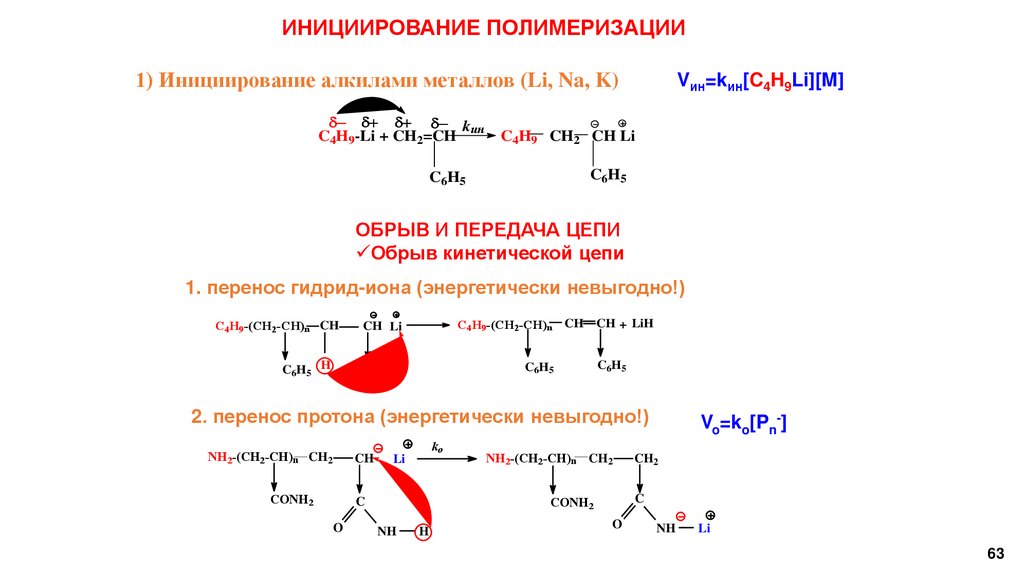
ИНИЦИИРОВАНИЕ ПОЛИМЕРИЗАЦИИ1) Инициирование алкилами металлов (Li, Na, K)
kин
C4H9-Li + CH2=CH
Vин=kин[C4H9Li][M]
C4H9 CH2 CH Li
C6H5
C6H5
ОБРЫВ И ПЕРЕДАЧА ЦЕПИ
Обрыв кинетической цепи
1. перенос гидрид-иона (энергетически невыгодно!)
C4H9-(CH2-CH)n CH
C6H5 H
C4H9-(CH2-CH)n CH
CH Li
C6H5
C6H5
CH + LiH
C6H5
2. перенос протона (энергетически невыгодно!)
NH2-(CH2-CH)n CH2
CH
CONH2
ko
Li
NH
H
CH2
C
CONH2
C
O
NH2-(CH2-CH)n CH2
Vo=ko[Pn-]
O
NH
Li
63
64.
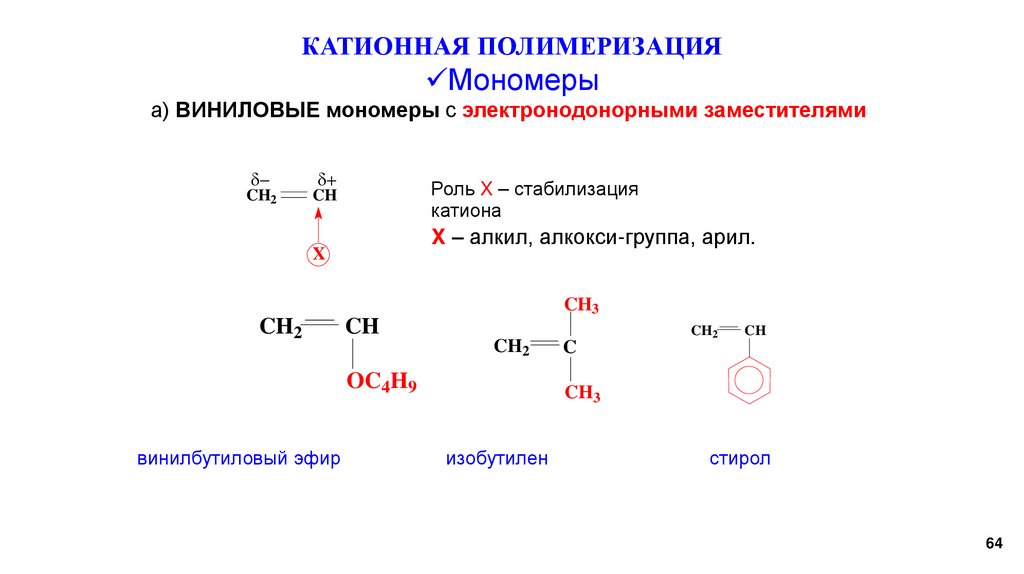
КАТИОННАЯ ПОЛИМЕРИЗАЦИЯМономеры
а) ВИНИЛОВЫЕ мономеры с электронодонорными заместителями
CH2
CH
Роль X – стабилизация
катиона
X – алкил, алкокси-группа, арил.
X
CH3
CH2
CH
CH2
OC4H9
винилбутиловый эфир
C
CH2
CH
CH3
изобутилен
стирол
64
65.
ИНИЦИИРОВАНИЕ ПОЛИМЕРИЗАЦИИа) В случае протонных кислот
k ин
HX +
M
HM+X
CH2
CH
+
H
[ClO4]
kин
HCH2
OC4H9
CH
[ClO4]
OC4H9
Vин=kин[HX][M]
б) В случае кислот Льюиса
образование активного комплекса
BF3 +H+OH- H+[BF3OH] Активность комплекса зависит от его способности отдавать протон.
образование активного центра (карбкатиона)
CH2
CH
+
OC4H9
H [BF3OH]
kин
HCH2
CH [BF3OH]
OC4H9
Более медленная стадия – образование карбкатиона!
Vин=kин[H+(BF3OH)-][M]
65
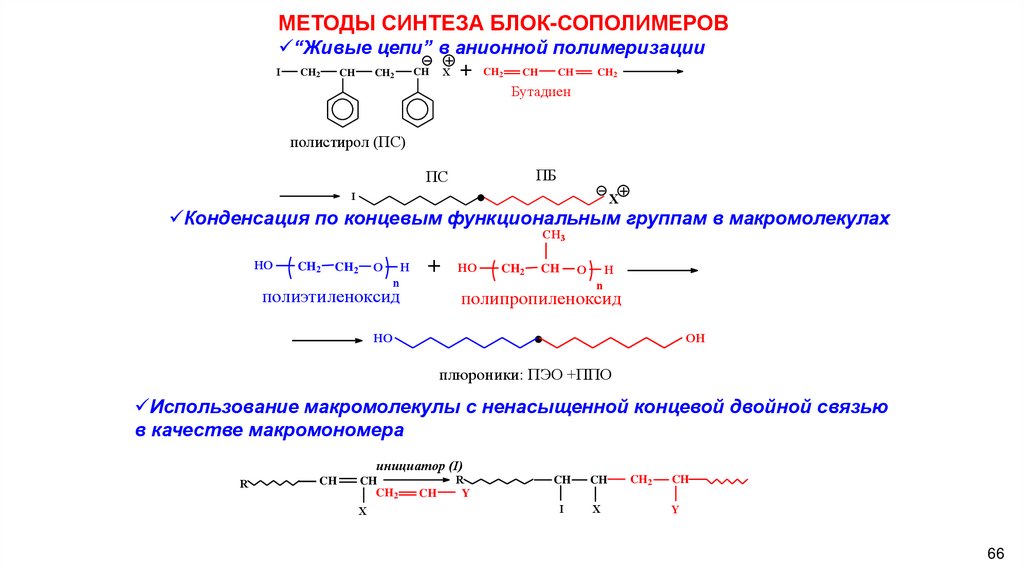
66.
МЕТОДЫ СИНТЕЗА БЛОК-СОПОЛИМЕРОВ“Живые цепи” в анионной полимеризации
CH X + CH2
I
CH2
CH
CH
CH2
CH
CH2
Бутадиен
полистирол (ПС)
ПБ
ПС
I
X
Конденсация по концевым функциональным группам в макромолекулах
CH3
HO
CH2
O
CH2
H
n
+
полиэтиленоксид
HO
CH2
CH
O
H
n
полипропиленоксид
HO
OH
плюроники: ПЭО +ППО
Использование макромолекулы с ненасыщенной концевой двойной связью
в качестве макромономера
инициатор (I)
R
CH
CH
CH2
X
CH
R
Y
CH
CH
I
X
CH2
CH
Y
66
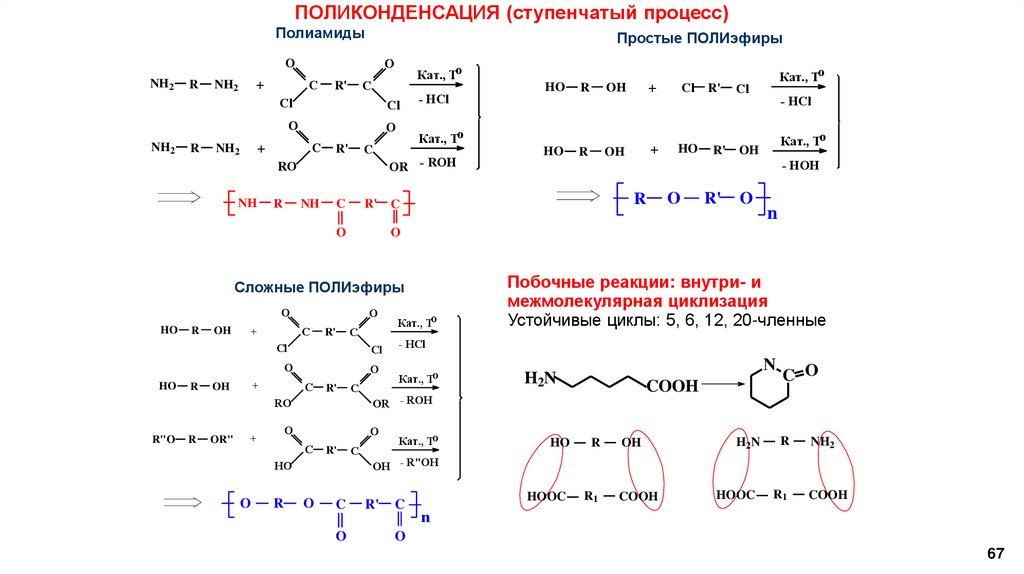
67.
ПОЛИКОНДЕНСАЦИЯ (ступенчатый процесс)Полиамиды
Простые ПОЛИэфиры
O
NH2
NH2
R
R
C
+
NH2
O
C
R'
Cl
Cl
O
O
C
+
NH2
C
R'
RO
NH
Кат., To
R
NH
C
R'
O
- HCl
HO
R
OH
OR - ROH
Cl
Cl
- HCl
O
O
+
OH
C
C
R'
R'
C
RO
R"O
R
OR"
O
+
R'
HO
O
R
O
C
O
OH
R'
Cl
+
HO
R'
OH
Кат., To
- HCl
Кат., To
- HOH
O
R'
O
n
C
Кат., To
Побочные реакции: внутри- и
межмолекулярная циклизация
Устойчивые циклы: 5, 6, 12, 20-членные
N
H2N
COOH
OR - ROH
O
C
R
+
Cl
R
Кат., To
C
HO
C
O
+
OH
O
O
R
R
Кат., To
Сложные ПОЛИэфиры
HO
HO
Кат., To
HO
R
OH
HOOC
R1
COOH
C O
H2N
R
NH2
HOOC
R1
COOH
OH - R"OH
R'
C
n
O
67
68.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА СТЕПЕНЬ ПОЛИМЕРИЗАЦИИ1. Концентрация низкомолекулярного вещества ( )
PN
Для синтеза
высокомолекулярно
го
полимера
необходимо удалять
низкомолекулярное
вещество
Pn
K равн
q
10
0
[v] = 10-3
моль/л
[v] = 0,3
моль/л
[v] = 5 моль/л
10
2. Образование циклов
Устойчивые циклы: 5, 6, 12, 20-членные
внутримолекулярная циклизация
Vцикл.~k[M]
Vp~k[M]2
10
0
H2N
Кравн.
N
COOH
C O
разбавление реакционной системы
увеличивает вероятность циклизации
межмолекулярная циклизация
HO
R
OH
HOOC
R1
COOH
H2N
R
NH2
HOOC
R1
COOH
Реакции циклизации препятствуют образованию высокомолекулярного
продукта
68
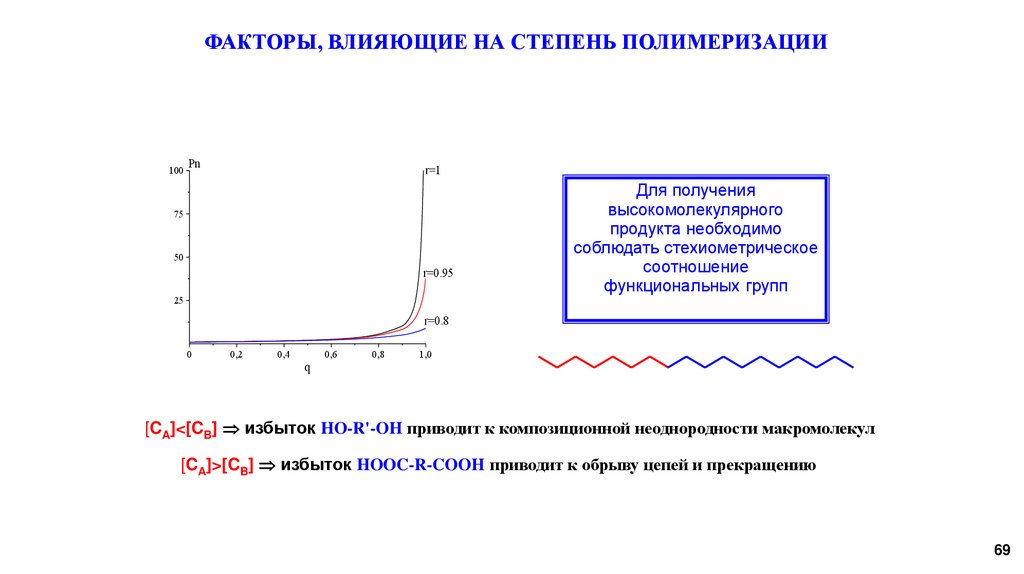
69.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА СТЕПЕНЬ ПОЛИМЕРИЗАЦИИ100
Pn
r=1
75
50
r=0.95
25
Для получения
высокомолекулярного
продукта необходимо
соблюдать стехиометрическое
соотношение
функциональных групп
r=0.8
0
0,2
0,4
0,6
0,8
1,0
q
[CA]<[CB] избыток HO-R'-OH приводит к композиционной неоднородности макромолекул
[CA]>[CB] избыток HOOC-R-COOH приводит к обрыву цепей и прекращению
69
70.
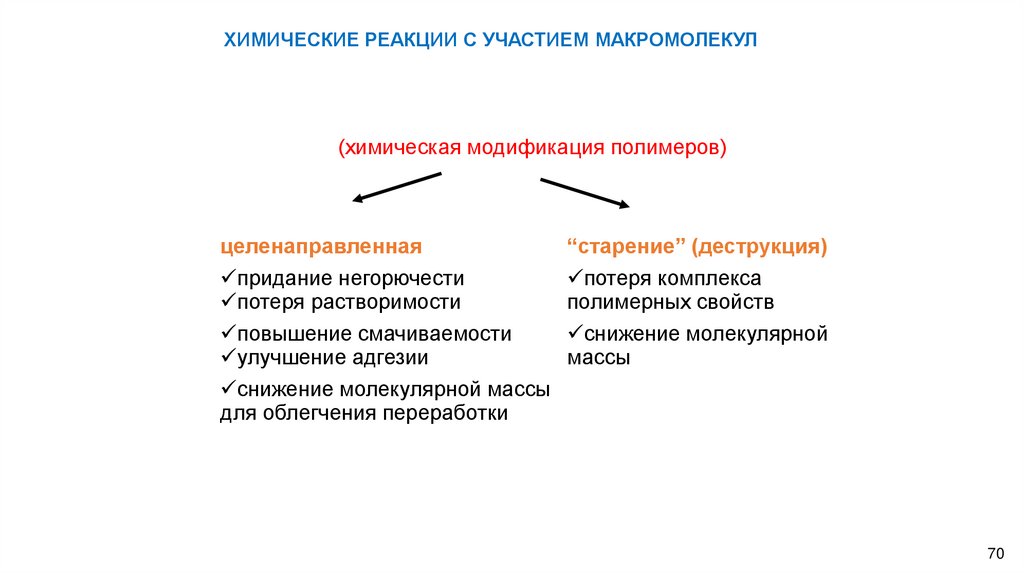
ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ МАКРОМОЛЕКУЛ(химическая модификация полимеров)
целенаправленная
придание негорючести
потеря растворимости
повышение смачиваемости
улучшение адгезии
снижение молекулярной массы
для облегчения переработки
“старение” (деструкция)
потеря комплекса
полимерных свойств
снижение молекулярной
массы
70
71.
Изменение свойств ПЭ при хлорировании (Cl2, УФ)CH2
Cl2,УФ
CH2
n
-HCl
CH2
CH
CH2
CH2
Cl
CH
Cl
появление хлора в макромолекулах:
- повышает адгезию пленок к различным поверхностям;
- изменяет смачиваемость
H2O
H2O
ПЭ
ПЭ-Cl
- нарушает регулярность строения исходных макромолекул полиэтилена
нерегулярные молекулы не кристаллизуются!!!
T,˚C
размягчения
0
~ 90
8
~ 70
28
~ 20
40
~ 10
Прочность,
кг/см2
% Cl
100
50
10 20 30
% Cl
71
72.
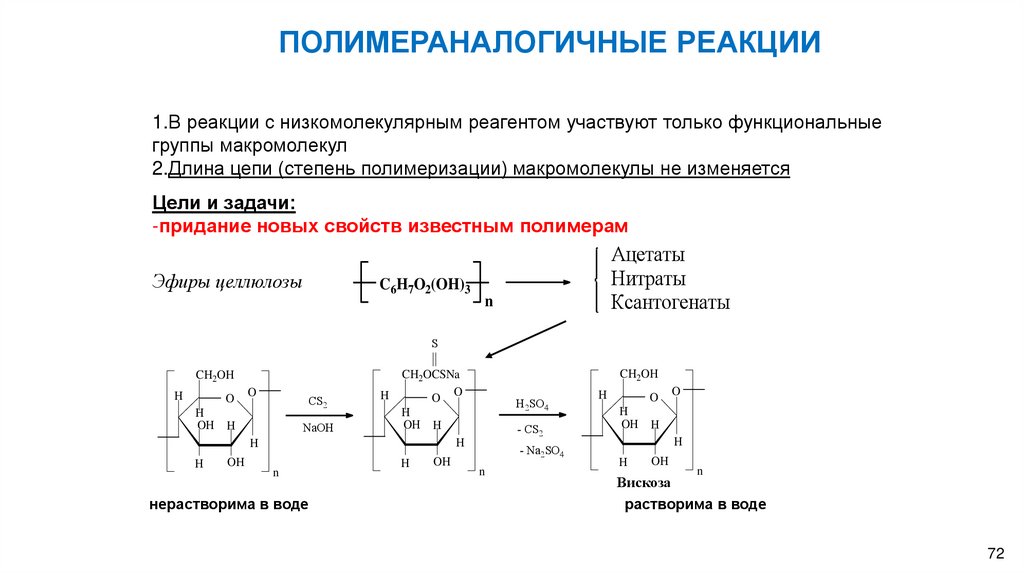
ПОЛИМЕРАНАЛОГИЧНЫЕ РЕАКЦИИ1.В реакции с низкомолекулярным реагентом участвуют только функциональные
группы макромолекул
2.Длина цепи (степень полимеризации) макромолекулы не изменяется
Цели и задачи:
-придание новых свойств известным полимерам
Эфиры целлюлозы
C6H7O2(OH)3
Ацетаты
Нитраты
Ксантогенаты
n
S
CH2OH
H
O
O
CS2
H
OH H
NaOH
H
OH
H2SO4
H
OH H
- CS2
H
H
H
CH2OH
CH2OCSNa
O O
n
нерастворима в воде
H
OH
- Na2SO4
n
H
O
O
H
OH H
H
H
OH
n
Вискоза
растворима в воде
72
73.
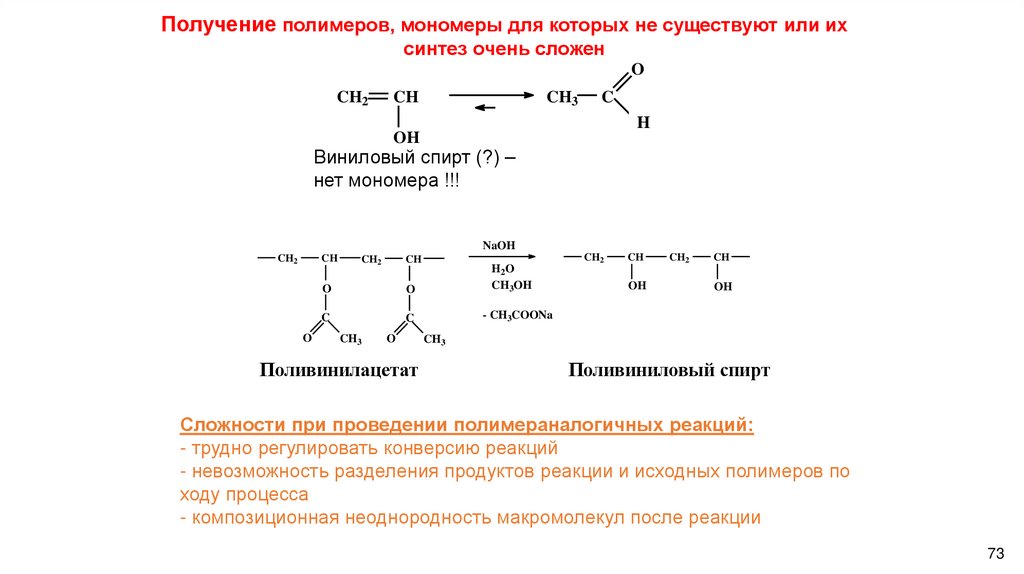
Получение полимеров, мономеры для которых не существуют или ихсинтез очень сложен
O
CH2
CH
CH3
C
OH
H
OH
Виниловый спирт (?) –
нет мономера !!!
NaOH
CH2
CH
O
CH2
CH2
CH
O
O
H2O
CH3OH
C
C
- CH3COONa
CH3
O
Поливинилацетат
CH
OH
CH2
CH
OH
CH3
Поливиниловый спирт
Сложности при проведении полимераналогичных реакций:
- трудно регулировать конверсию реакций
- невозможность разделения продуктов реакции и исходных полимеров по
ходу процесса
- композиционная неоднородность макромолекул после реакции
73
74.
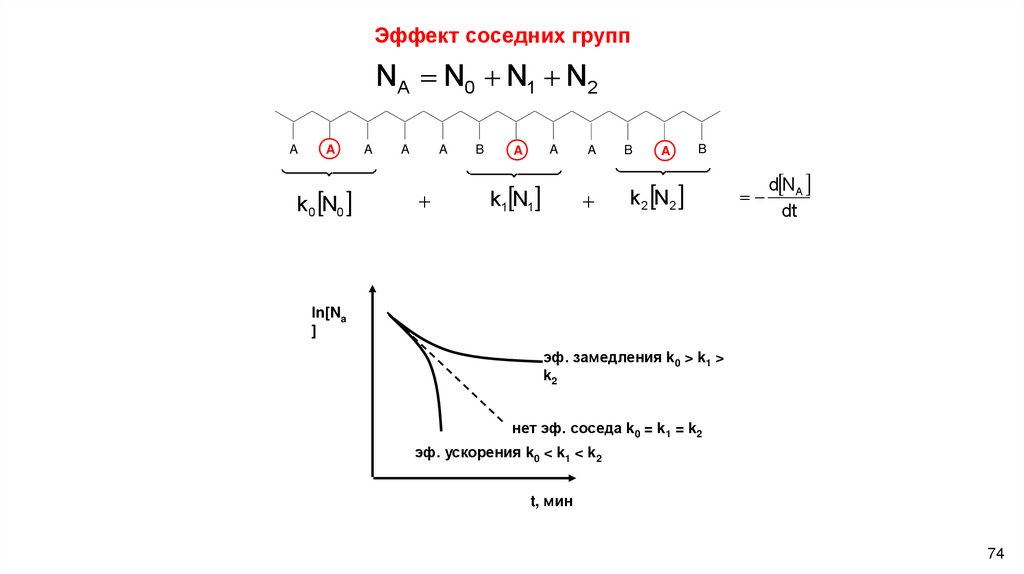
Эффект соседних группNA N0 N1 N2
A
A
k 0 N0
A
A
A
B
A
A
k1 N1
A
B
k 2 N2
A
B
d NA
dt
ln[Na
]
эф. замедления k0 > k1 >
k2
нет эф. соседа k0 = k1 = k2
эф. ускорения k0 < k1 < k2
t, мин
74
75.
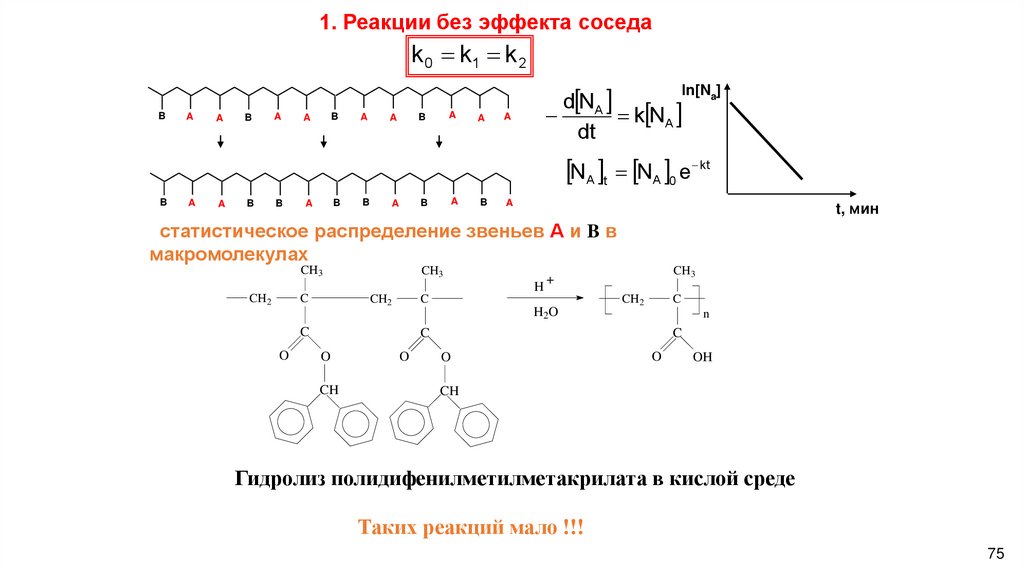
1. Реакции без эффекта соседаk 0 k1 k 2
d NA
k NA
dt
ln[Na]
B
A
A
B
A
B
A
A
A
B
A
A
A
NA t NA 0 e kt
B
A
A
B
B
B
A
B
A
B
A
B
A
t, мин
статистическое распределение звеньев А и B в
макромолекулах
CH3
CH2
CH3
H
C
CH2
C
H2O
C
O
CH3
+
CH2
C
n
C
O
CH
O
C
O
O
OH
CH
Гидролиз полидифенилметилметакрилата в кислой среде
Таких реакций мало !!!
75
76.
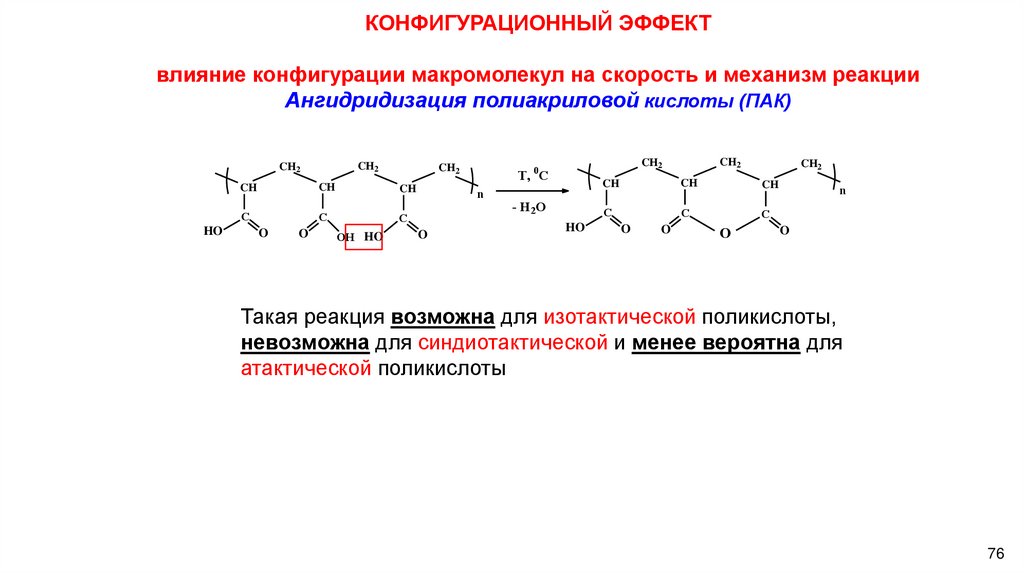
КОНФИГУРАЦИОННЫЙ ЭФФЕКТвлияние конфигурации макромолекул на скорость и механизм реакции
Ангидридизация полиакриловой кислоты (ПАК)
CH2
CH2
HO
CH2
CH
CH
CH
C
C
C
O
O
OH HO
n
O
CH2
CH2
T, 0C
CH
- H2O
C
HO
O
O
CH2
CH
CH
C
C
O
n
O
Такая реакция возможна для изотактической поликислоты,
невозможна для синдиотактической и менее вероятна для
атактической поликислоты
76
77.
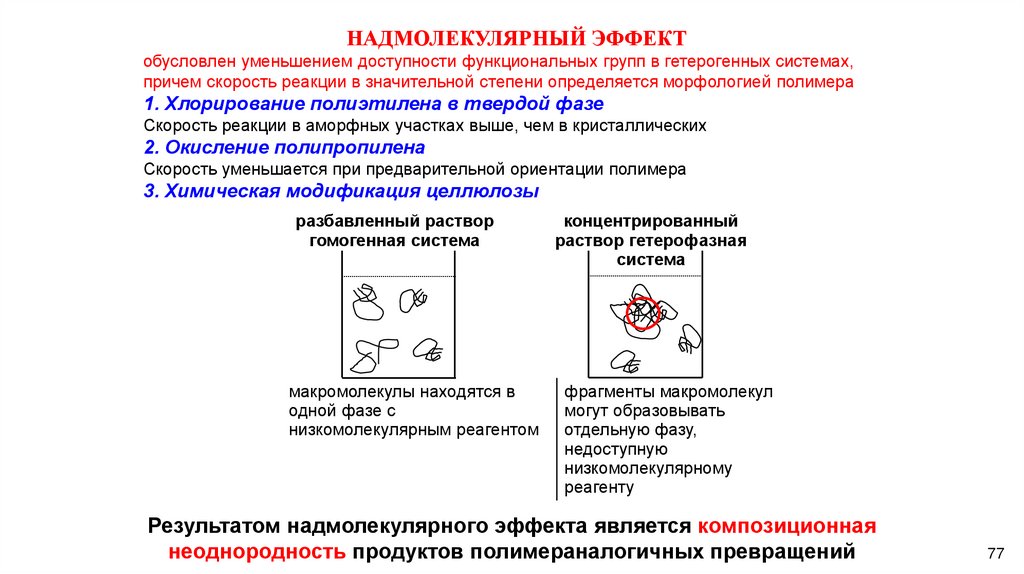
НАДМОЛЕКУЛЯРНЫЙ ЭФФЕКТобусловлен уменьшением доступности функциональных групп в гетерогенных системах,
причем скорость реакции в значительной степени определяется морфологией полимера
1. Хлорирование полиэтилена в твердой фазе
Скорость реакции в аморфных участках выше, чем в кристаллических
2. Окисление полипропилена
Скорость уменьшается при предварительной ориентации полимера
3. Химическая модификация целлюлозы
разбавленный раствор
гомогенная система
концентрированный
раствор гетерофазная
система
макромолекулы находятся в
одной фазе с
низкомолекулярным реагентом
фрагменты макромолекул
могут образовывать
отдельную фазу,
недоступную
низкомолекулярному
реагенту
Результатом надмолекулярного эффекта является композиционная
неоднородность продуктов полимераналогичных превращений
77
78.
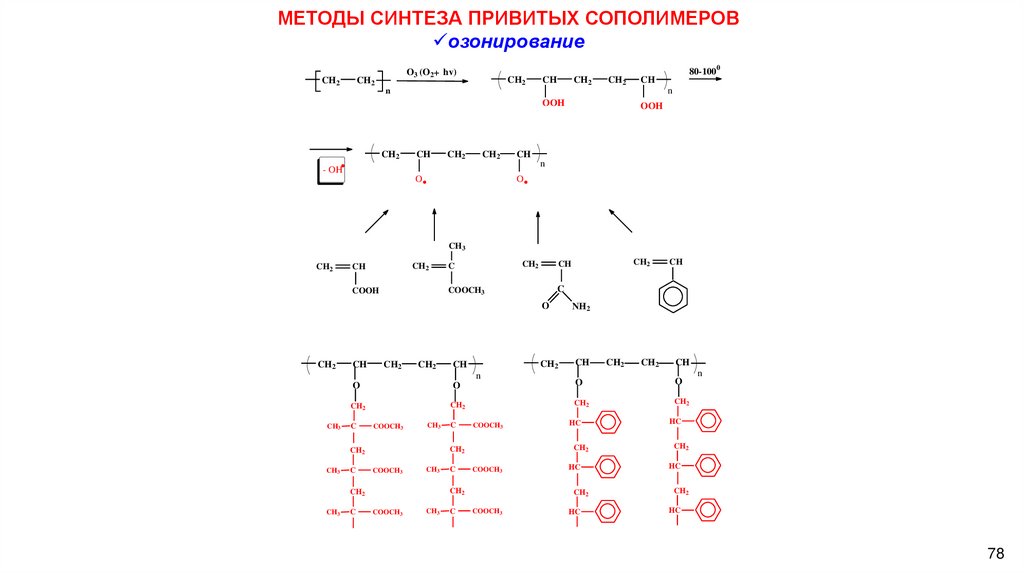
МЕТОДЫ СИНТЕЗА ПРИВИТЫХ СОПОЛИМЕРОВозонирование
CH2
O3 (O2+ hv)
CH2
CH2
CH
CH2
CH2
n
n
OOH
.
CH2
CH
CH2
CH2
.
- OH
80-1000
CH
CH
.
O
OOH
n
O
CH3
CH2
CH2
CH
CH
CH2
CH2
CH
n
CH3
C
O
NH2
CH2
CH
CH2
CH2
CH
O
O
O
CH2
CH2
CH2
CH2
HC
HC
CH2
CH2
HC
HC
CH2
CH2
HC
HC
C
COOCH3
CH3
C
C
C
COOCH3
CH2
COOCH3
CH3
C
COOCH3
CH2
CH2
CH3
CH
O
CH2
CH3
CH2
CH
COOCH3
COOH
CH2
CH2
C
COOCH3
CH3
C
COOCH3
n
78
79.
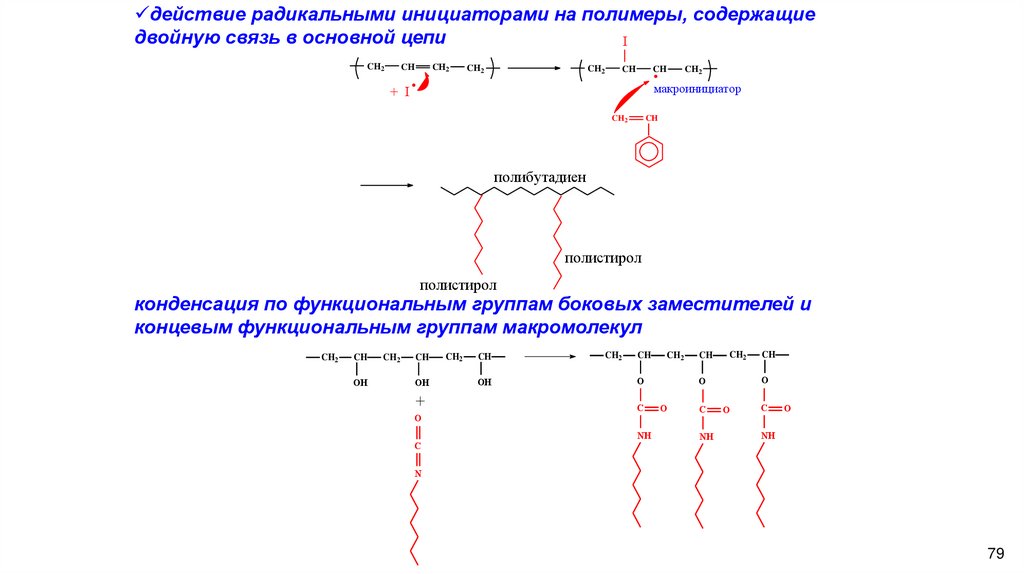
действие радикальными инициаторами на полимеры, содержащиедвойную связь в основной цепи
I
CH2
CH
CH2
CH2
CH2
CH
CH
CH2
макроинициатор
+ I
CH2
CH
полибутадиен
полистирол
полистирол
конденсация по функциональным группам боковых заместителей и
концевым функциональным группам макромолекул
CH2
CH
OH
CH2
CH
OH
+
O
C
CH2
CH
OH
CH2
CH
CH2
O
C
NH
CH
CH2
O
O
O
C
NH
CH
O
C
O
NH
N
79
80.
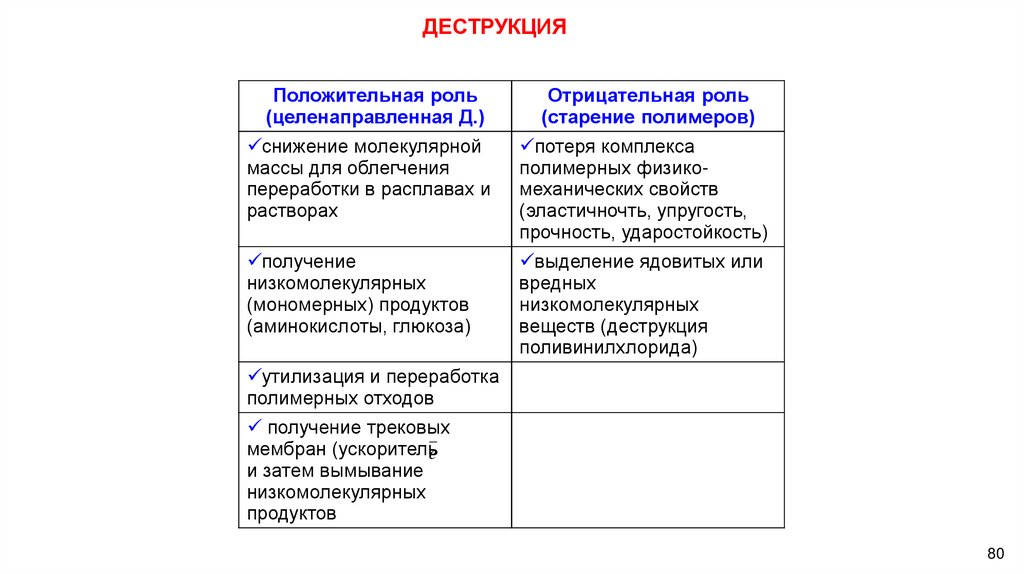
ДЕСТРУКЦИЯПоложительная роль
(целенаправленная Д.)
Отрицательная роль
(старение полимеров)
снижение молекулярной
массы для облегчения
переработки в расплавах и
растворах
потеря комплекса
полимерных физикомеханических свойств
(эластичночть, упругость,
прочность, ударостойкость)
получение
низкомолекулярных
(мономерных) продуктов
(аминокислоты, глюкоза)
выделение ядовитых или
вредных
низкомолекулярных
веществ (деструкция
поливинилхлорида)
утилизация и переработка
полимерных отходов
получение трековых
мембран (ускорительe
и затем вымывание
низкомолекулярных
продуктов
80
81.
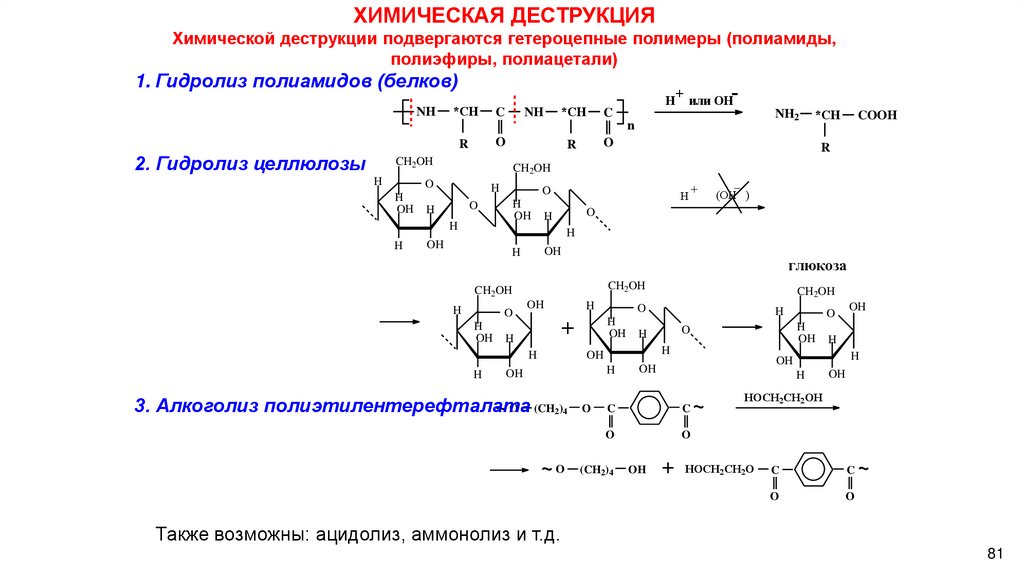
ХИМИЧЕСКАЯ ДЕСТРУКЦИЯХимической деструкции подвергаются гетероцепные полимеры (полиамиды,
полиэфиры, полиацетали)
1. Гидролиз полиамидов (белков)
NH
2. Гидролиз целлюлозы
*CH
C
R
O
NH
CH2OH
H
H
O
H
H
H
*CH
C
R
O
NH2
n
O
H
OH
*CH
COOH
R
CH2OH
O
H
OH
H+ или ОН-
H
+
_
(OH )
O
H
H
OH
OH
H
глюкоза
CH2OH
CH2OH
H
O
H
OH
OH
H
+
H
H
H
O
H
OH
~O
O
O
O
OH
H
H
C
~
OH
H
OH
OH
C
(CH2)4
O
H
OH
O
H
H
3. Алкоголиз полиэтилентерефталата
~ O (CH2)4
H
H
OH
OH
CH2OH
OH
HOCH2CH2OH
+ HOCH2CH2O
C
C
O
O
~
Также возможны: ацидолиз, аммонолиз и т.д.
81
82.
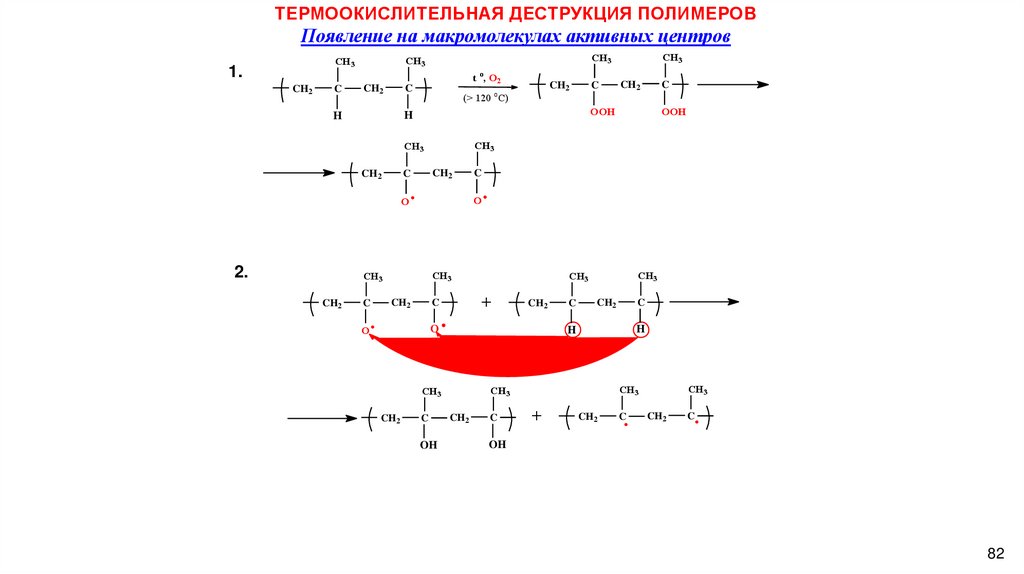
ТЕРМООКИСЛИТЕЛЬНАЯ ДЕСТРУКЦИЯ ПОЛИМЕРОВПоявление на макромолекулах активных центров
1.
CH2
C
CH2
t o, O2
C
CH2
CH2
C
OOH
C
CH3
CH2
CH2
O
OH
C
CH2
C
H
H
CH2
C
CH3
CH3
CH3
CH3
C
CH3
CH3
+
C
O
CH2
C
O
CH3
C
CH2
CH3
O
CH2
C
OOH
CH3
2.
CH2
(> 120 oC)
H
H
CH3
CH3
CH3
CH3
+
CH2
C
CH2
C
OH
82
83.
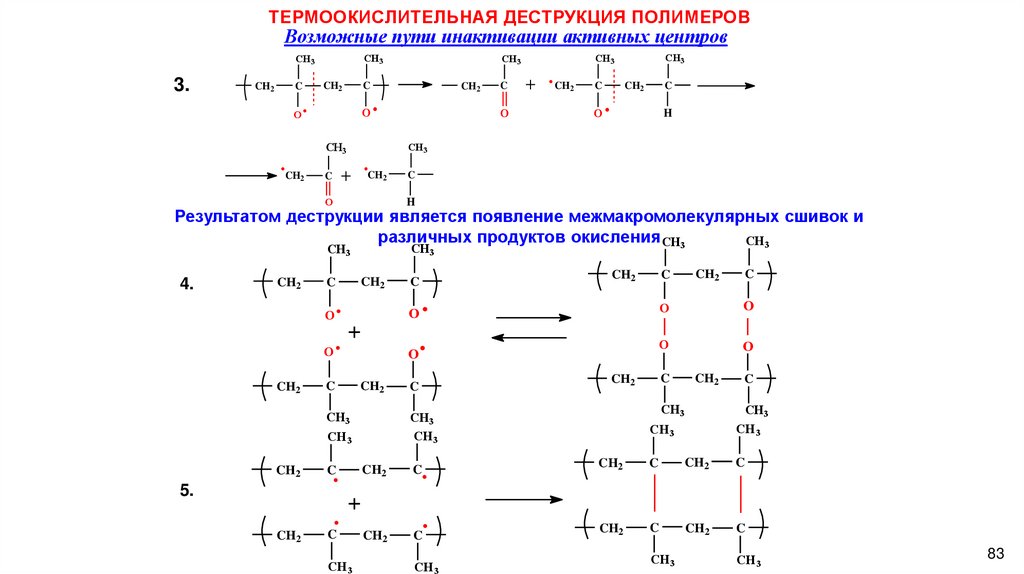
ТЕРМООКИСЛИТЕЛЬНАЯ ДЕСТРУКЦИЯ ПОЛИМЕРОВВозможные пути инактивации активных центров
CH3
CH3
3.
CH2
C
CH2
C
O
O
C
C
O
+
CH2
CH2
C
C
O
H
CH3
CH3
CH2
CH2
CH3
CH3
CH3
+
CH2
C
O
H
CH3
CH3
Результатом деструкции является появление межмакромолекулярных сшивок и
различных продуктов окисления CH3
CH3
4.
CH2
CH2
C
O
+
C
CH2
5.
C
O
O
O
O
C
CH2
CH2
CH3
CH3
CH3
CH3
C
C
CH2
C
O
CH3
CH2
CH2
O
O
CH2
C
C
CH3
CH3
CH3
CH2
C
CH2
C
CH2
C
CH2
C
CH2
C
CH2
C
+
CH2
C
CH3
CH3
CH3
CH3
83
84.
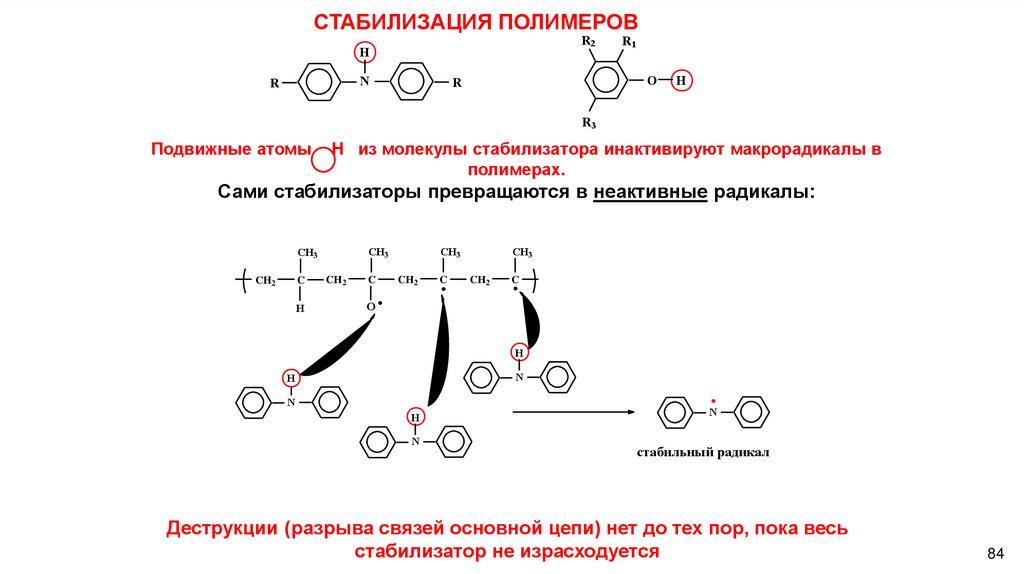
СТАБИЛИЗАЦИЯ ПОЛИМЕРОВR2
H
N
R
R1
O
R
H
R3
Подвижные атомы
H из молекулы стабилизатора инактивируют макрорадикалы в
полимерах.
Сами стабилизаторы превращаются в неактивные радикалы:
CH3
CH3
CH2
C
H
CH2
C
CH3
CH2
C
CH3
CH2
C
O
H
N
H
N
H
N
N
стабильный радикал
Деструкции (разрыва связей основной цепи) нет до тех пор, пока весь
стабилизатор не израсходуется
84
85.
СТАБИЛИЗАЦИЯ ПОЛИМЕРОВP[O2],
мм.рт.ст
давление
100
τ
C1
50
1
2
C3
C2
3
4
5
6
t, часы
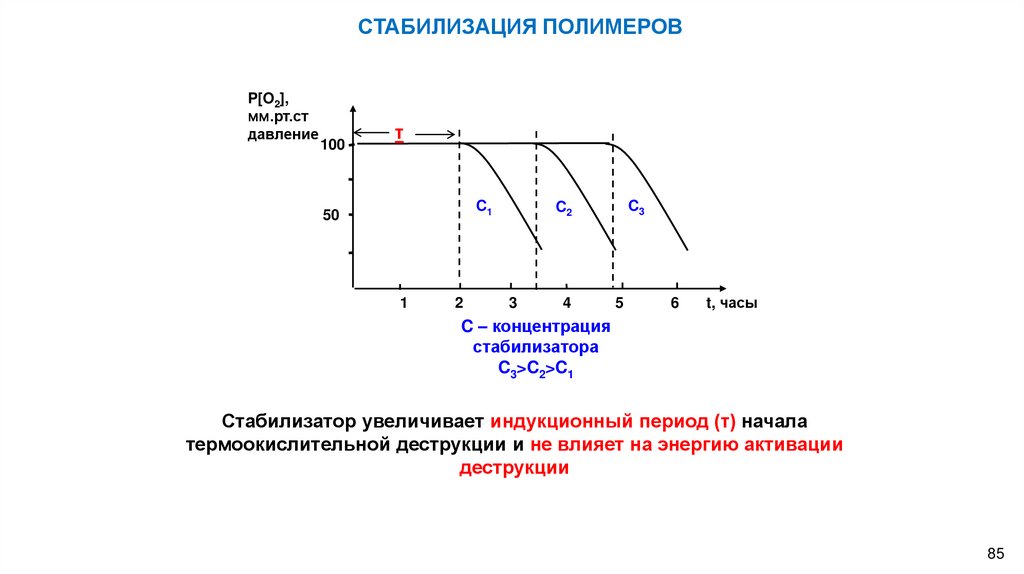
C – концентрация
стабилизатора
C3>C2>C1
Стабилизатор увеличивает индукционный период (τ) начала
термоокислительной деструкции и не влияет на энергию активации
деструкции
85
86.
Основные выводы• Полимеры обладают уникальными свойствами по сравнению с
низкомолекулярными соединениями – гибкость, отсутствие газовой фазы,
адгезия, формирование волокон и пленок
• Для макромолекулы существуют понятия «конформация» (без разрыва
связей) и «конфигурация» (разрыв связей)
• Молекулярная масса полимера – статистическое понятие. Полимеры
полидисперсны
• Метод синтеза полимера влияет на его ММР, значит и на его свойства
86
87.
ЗадачиЗадача 1. Опишите как классифицируется полиамид 6,6 и крахмал.
Задача 2. Вычислите среднечисловую и средневесовую молекулярные массы, а также
коэффициент полидисперсности полимера, представляющего собой смесь двух
равных по молям фракций макромолекул с молекулярными массами 100 и 1000.
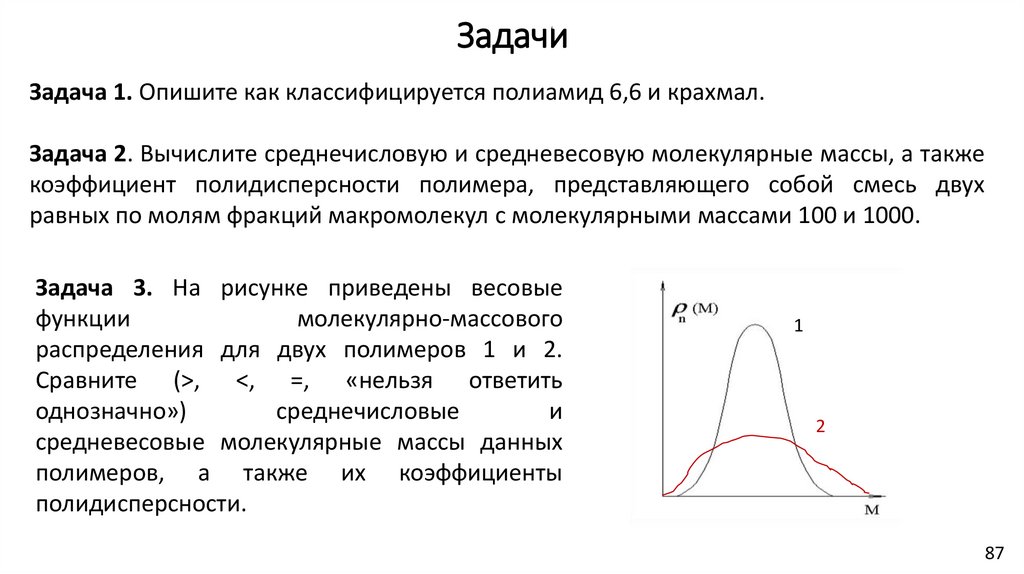
Задача 3. На рисунке приведены весовые
функции
молекулярно-массового
распределения для двух полимеров 1 и 2.
Сравните (>, <, =, «нельзя ответить
однозначно»)
среднечисловые
и
средневесовые молекулярные массы данных
полимеров, а также их коэффициенты
полидисперсности.
1
2
87
88.
Литература1.«Высокомолекулярные соединения» под редакцией А.Б. Зезина, М: Юрайт,
2016
2.Ю.Д. Семчиков. «Высокомолекулярные соединения» М: Академия, 2003.
3. В.В. Киреев. «Высокомолекулярные соединения» М: Юрайт, 2013.
4. А.А. Тагер. «Физико-химия полимеров», М: Научный мир, 2007
5. В.Н. Кулезнев, В.А. Шершнев, «Химия и физика полимеров», М: КолосС, 2007
•Учебные материалы по химии высокомолекулярных соединений + Программа + Список
литературы// - http://www.chem.msu.ru/rus/teaching/vms.html
•Методические пособия к практикуму по высокомолекулярным соединениям //
http://www.vmsmsu.ru/what.html
•Макрогалерея // http://www. pslc.ws/russian/index.htm
88

































 Химия
Химия