Похожие презентации:
Сложные эфиры
1.
Презентация на тему: Сложные эфиры.СЛОЖНЫЕ ЭФИРЫ –
класс соединений на основе
минеральных (неорганических) или органических
карбоновых кислот, у которых атом водорода в НОгруппе замещен органической группой R.
Прилагательное «сложные» в названии эфиров
помогает отличить их от соединений, именуемых
простыми эфирами.
2.
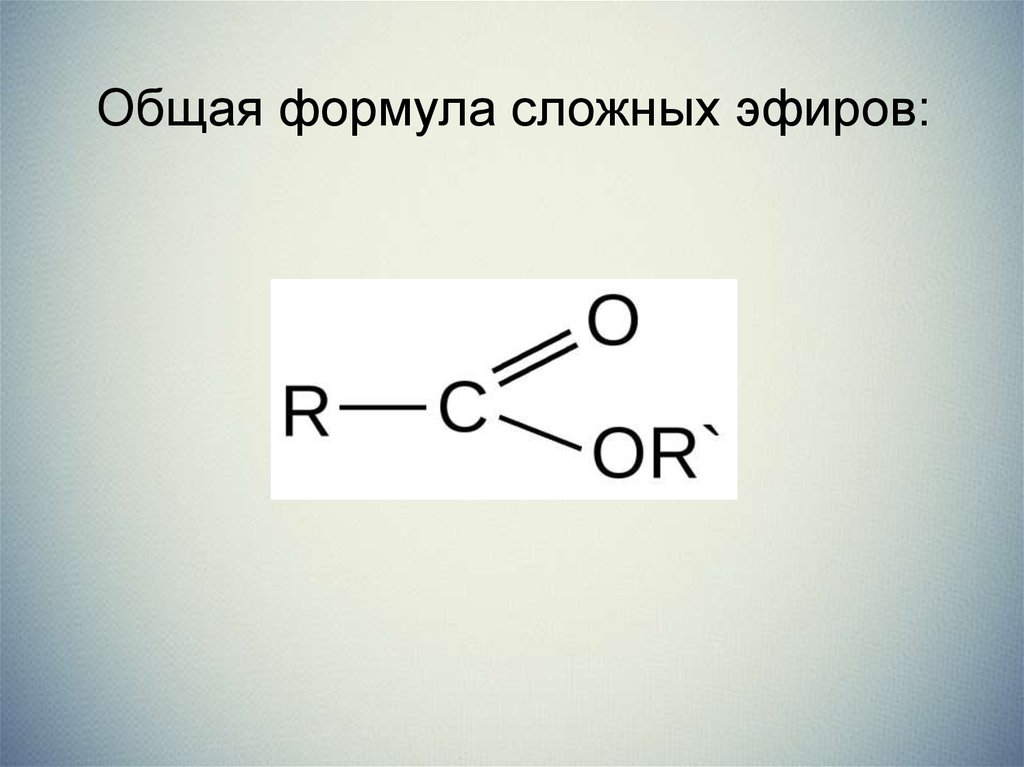
Общая формула сложных эфиров:3.
Физические свойства.Сложные эфиры - бесцветные жидкости,
малорастворимые или совсем не растворимые
в воде, обладают специфическим запахом.
Сложные эфиры высших спиртов и высших
кислот - твердые вещества.
4.
Химические свойства.Наиболее характерная реакция для сложных
эфиров – гидролиз.При гидролизе сложного
эфира в присутствии кислот образуется
карбоновая кислота и спирт:
5.
Применение сложных эфиров.Этилформиат НСООС2Н5 и этилацетат Н3СООС2Н5 используются как растворители
целлюлозных лаков используются в пищевой промышленности при создании
фруктовых эссенций, а сложные эфиры на основе ароматических спиртов – в
парфюмерной промышленности.
Жиры вместе с углеводами и белками составляют набор необходимых для
питания пищевых продуктов, они входят в состав всех растительных и животных
клеток, кроме того, накапливаясь в организме, играют роль энергетического
запаса. Из-за низкой теплопроводности жировой слой хорошо предохраняет
животных от переохлаждения.
Животные и растительные жиры представляют собой сырье для получения
высших карбоновых кислот, моющих средств и глицерина, используемого в
косметической промышленности.
Нитроглицерин – известный лекарственный препарат и взрывчатое вещество,
основа динамита.
На основе растительных масел изготавливают олифы ,составляющие основу
масляных красок.
Эфиры серной кислоты используют в органическом синтезе как алкилирующие
реагенты, а эфиры фосфорной кислоты– как инсектициды.
6.
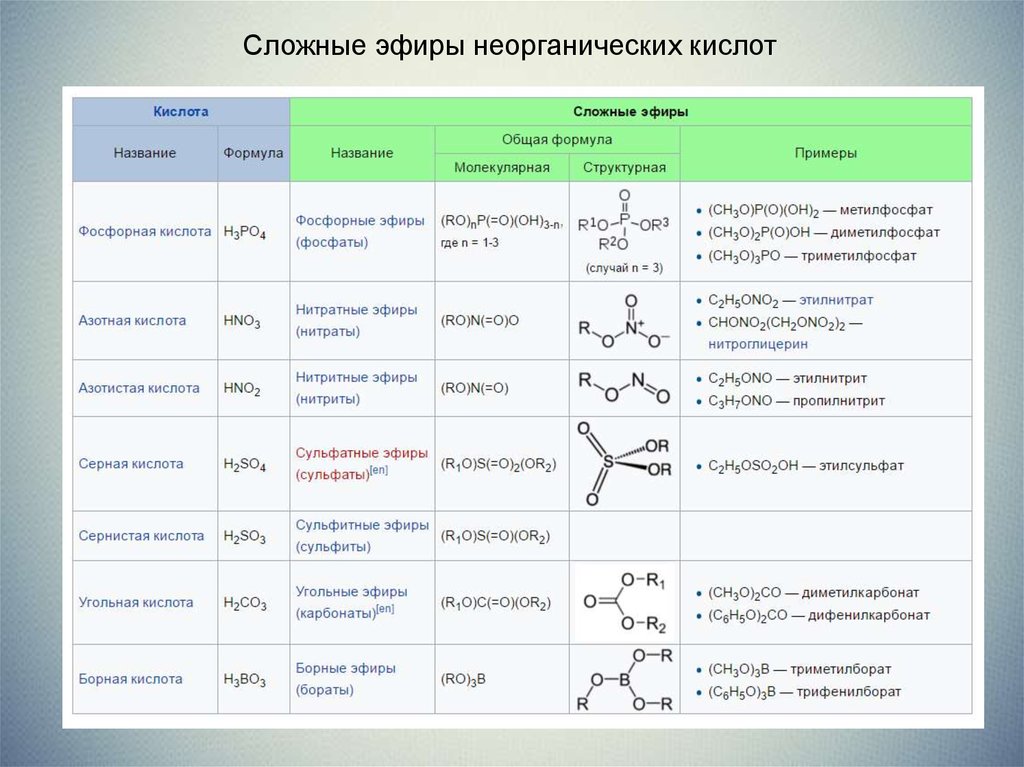
Сложные эфиры неорганических кислотКислота
Сложные эфиры
Общая формула
Название
Формула
Название
Молекул
ярная
Структур
ная
Примеры
•(CH3O)P(
O)(OH)2
—
метилфо
сфат
•(CH3O)2P
(O)OH —
диметил
фосфат
•(CH3O)3P
O—
триметил
фосфат
H3PO4
Фосфорн
ые
эфиры
(фосфаты
)
HNO3
Нитратн
ые
эфиры
(нитраты
)
Азотиста
я кислота
HNO2
Нитритн
ые
эфиры
(нитриты
)
Серная
кислота
H2SO4
Сульфатн
ые
(R1O)S(=
эфиры
O)2(OR2)
(сульфат
ы)[en]
Серниста
я кислота
H2SO3
Сульфитн
ые
(R1O)S(=
эфиры
O)(OR2)
(сульфит
ы)
H2CO3
Угольные
эфиры
(R1O)C(=
(карбона O)(OR2)
ты)[en]
•(CH3O)2C
O—
диметил
карбонат
•(C6H5O)2
CO —
дифенил
карбонат
H3BO3
Борные
эфиры
(бораты)
•(CH3O)3B
—
триметил
борат
•(C6H5O)3
B—
трифени
лборат
Фосфорн
ая
кислота
Азотная
кислота
Угольная
кислота
Борная
кислота
(RO)nP(=
O)(OH)3-n,
где n = 13
(случай n
= 3)
(RО)N(=O
)O
•C2H5ON
O2 —
этилнитр
ат
•CHONO2
(CH2ONO
2)2 —
нитрогл
ицерин
(RO)N(=O
)
•C2H5ON
O—
этилнитр
ит
•C3H7ON
O—
пропилн
итрит
(RO)3B
•C2H5OSO
2OH —
этилсуль
фат
7.
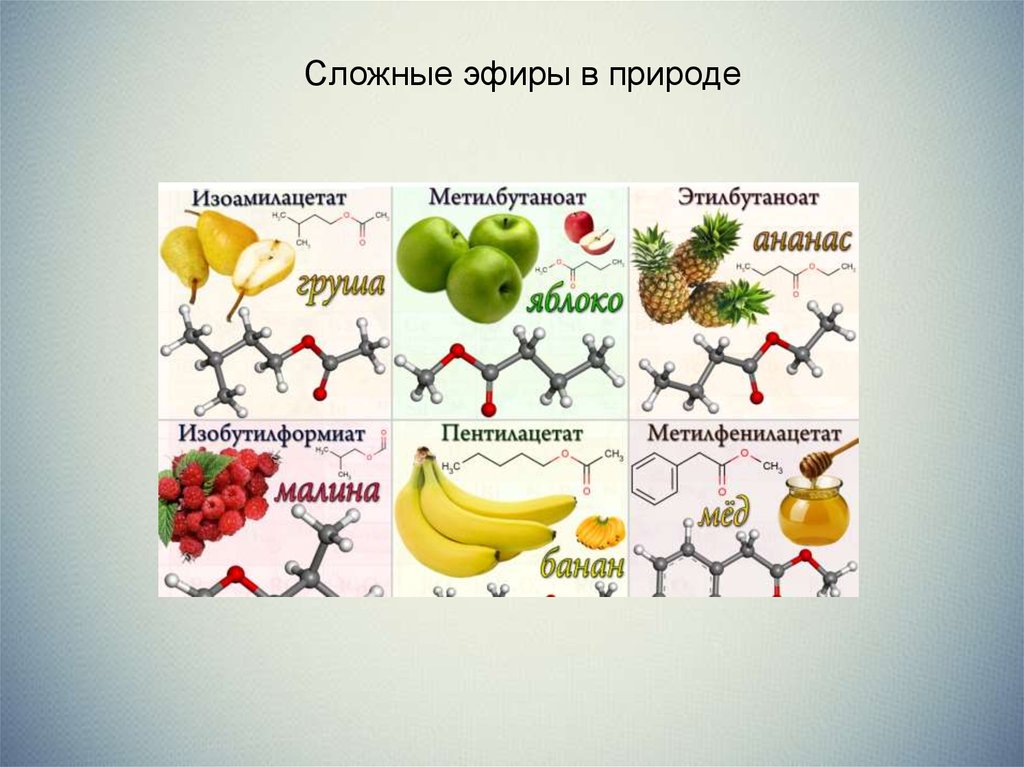
Сложные эфиры в природе8.
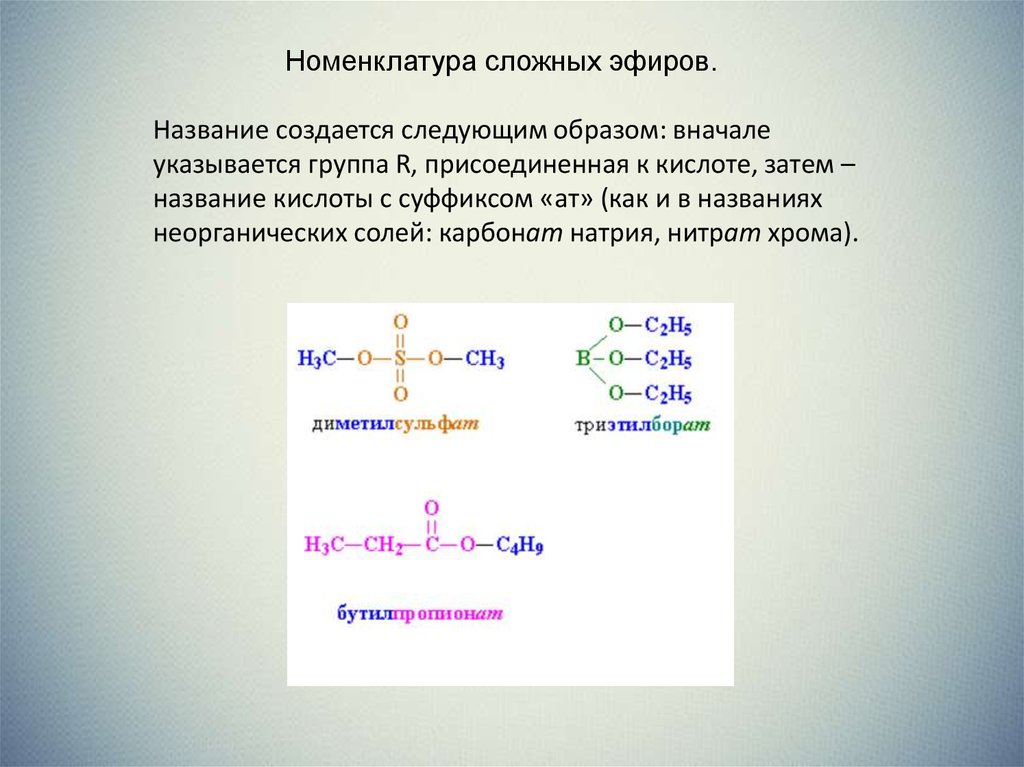
Номенклатура сложных эфиров.Название создается следующим образом: вначале
указывается группа R, присоединенная к кислоте, затем –
название кислоты с суффиксом «ат» (как и в названиях
неорганических солей: карбонат натрия, нитрат хрома).
9.
Образование сложных эфировСпирты вступают в реакции с минеральными и органическими кислотами,
образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз
сложных эфиров).





 Химия
Химия