Похожие презентации:
Уравнение Аррениуса. Уравнение Михаэлиса - Ментена
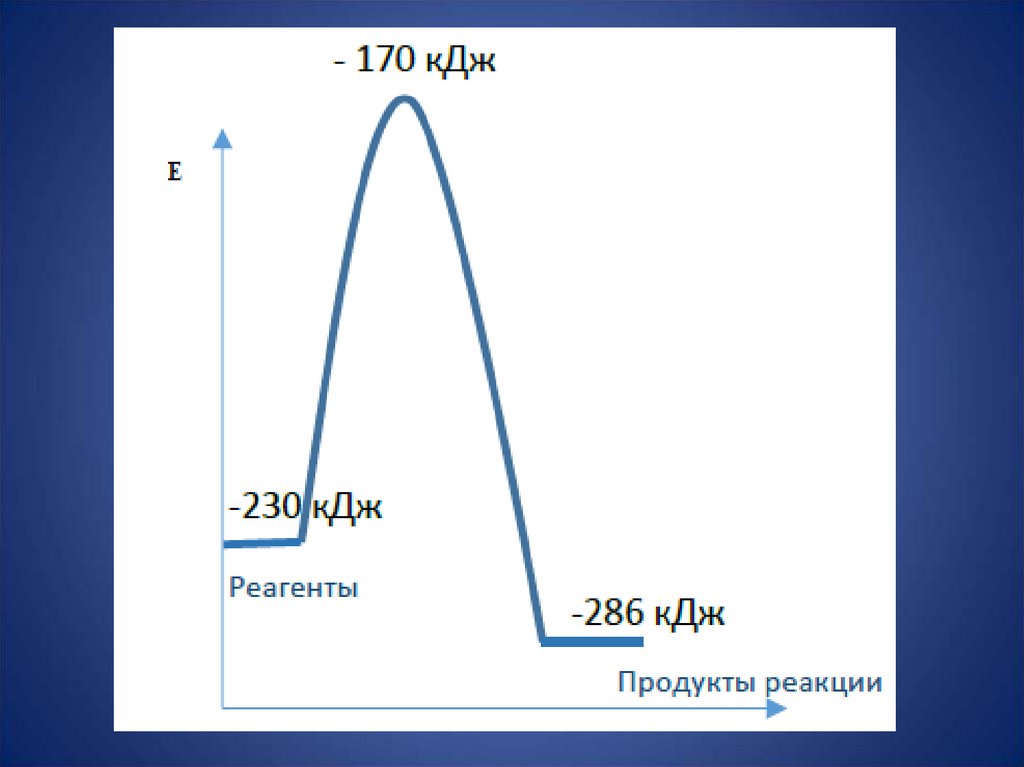
1. 5.4. Уравнение Аррениуса
2.
3.
4.
5.
6.
7.
8.
9.
10. 5.5. Уравнение Михаэлиса-Ментена
11.
12.
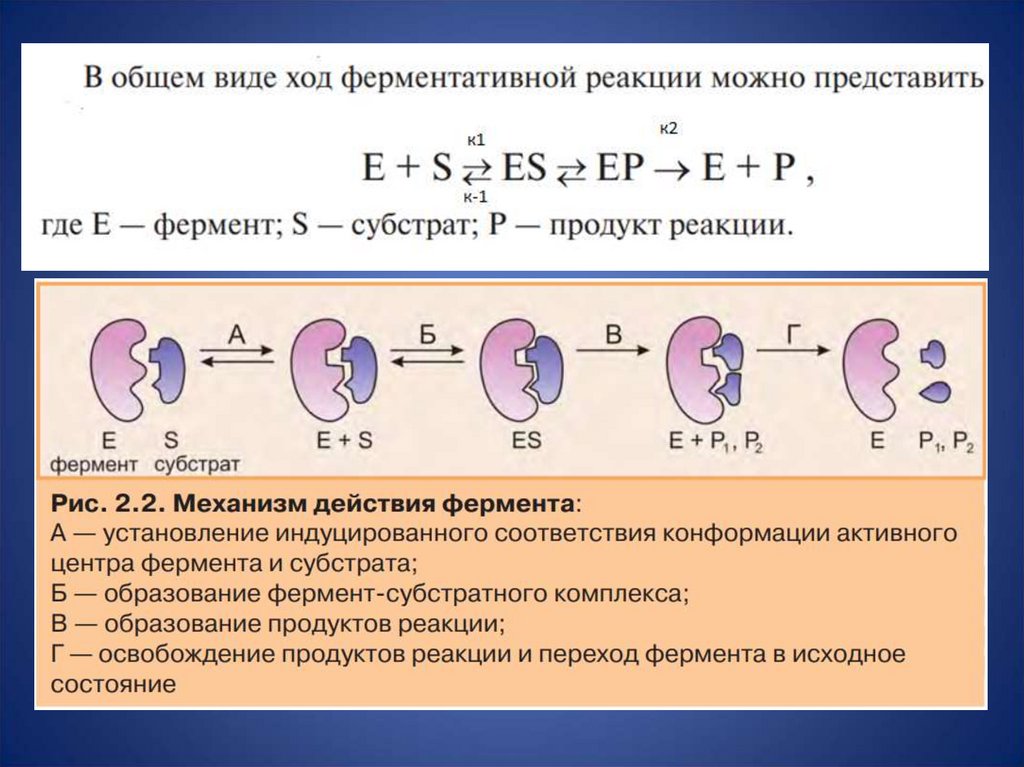
13. Фермент Е (от английского энзим) реагирует с субстратом S с образованием комплекса ES. Этот комплекс очень реакционно
способный,в нём субстрат быстро превращается в
продукт Р, после чего комплекс ЕР
необратимо распадается на снова готовый к
реакции фермент Е и продукт Р. к1 –
константа скорости образования ферментсубстратного комплекса ES, это константа
процесса «вхождения ключа в замок». к-1 –
константа распада комплекса ES. к2 –
константа скорости итогового образования
продукта. Это и есть к kat
14. Концентрация фермента в организме имеет какое-то предельное значение, обусловленное особенностями данного организма. Например,
тем, что написано в наших генах.Эту концентрацию можно
обозначить как [E]0.
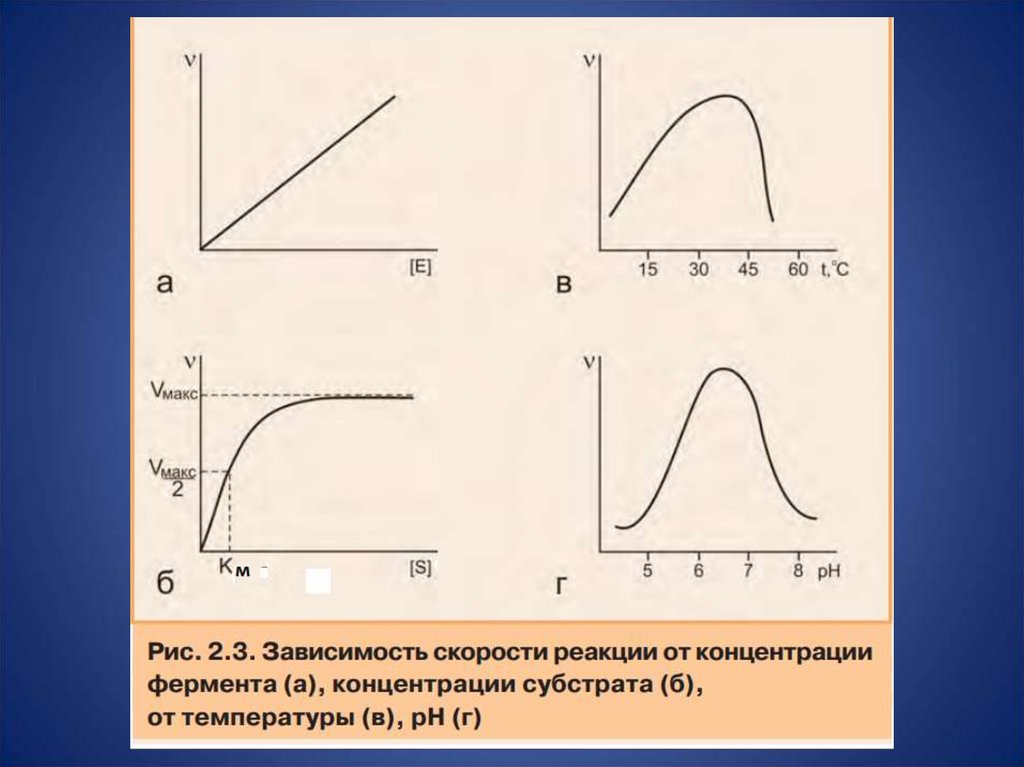
15. Максимальная скорость ферментативной реакции v max наступит в тот момент, когда все имеющиеся молекулы фермента связаны с
субстратом, т.е. когдався концентрация [E]0 участвует в
реакции, и все активные центры
фермента заняты.
v max = к2*[E]0
16. Константы, отвечающие за распад комплекса ES – это к-1 и к2, а константа его образования – это к1. Во время ферментативной
реакции столькоже молекул комплекса ES распадается,
сколько и образуется. Можно сказать, что
наступает полное химическое равновесие.
Константа этого равновесия К (то есть
константа распада комплекса ES) Кравн с
одной стороны равна:
К равн = [E][S]/[ES]
С другой стороны К равн = (к-1 + к2)/к1.
17.
18. Общая максимальная концентрация фермента равна [E]0. [E]0 = [ES] + [E]: сумма фермента, находящегося в виде комплекса ES и
свободного фермента Е.[ES] = [E]0 - [E] = [E]0 – [ES]Км/[S],
[ES](1 + Км/[S]) = [E]0
[ES] = [E]0[S]/( Км + [S]).
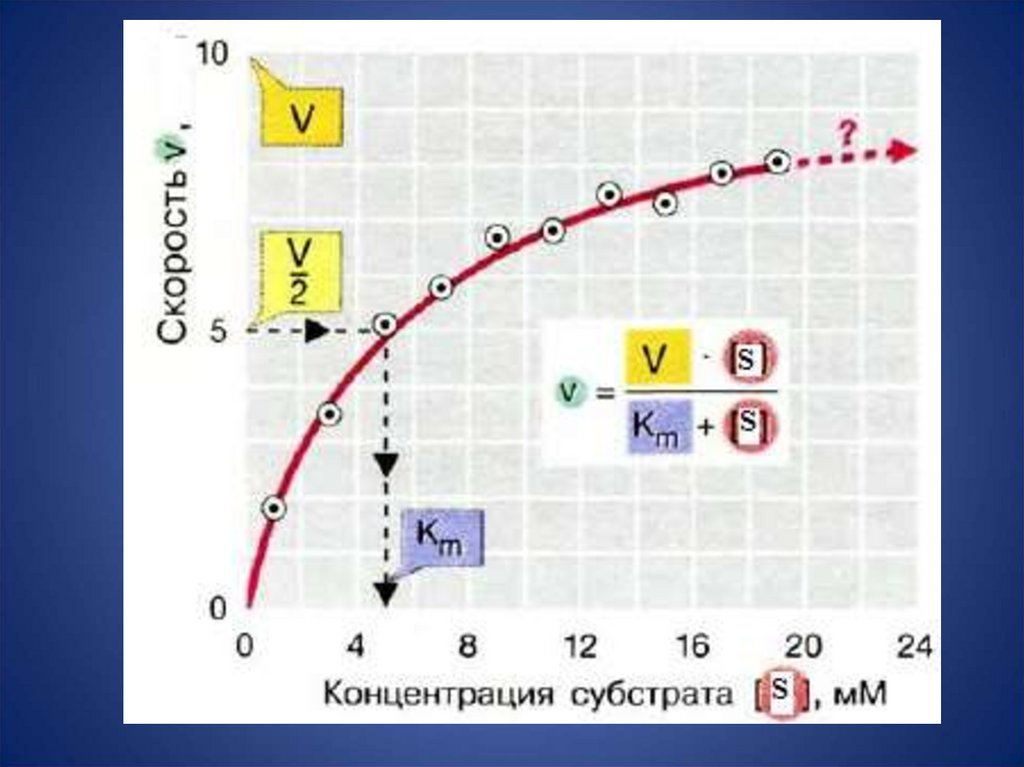
Т.к. v = k2[ES], то чаще всего уравнение
Михаэлиса-Ментена записывают через
скорость ферментативной реакции:















![Общая максимальная концентрация фермента равна [E]0. [E]0 = [ES] + [E]: сумма фермента, находящегося в виде комплекса ES и Общая максимальная концентрация фермента равна [E]0. [E]0 = [ES] + [E]: сумма фермента, находящегося в виде комплекса ES и](https://cf5.ppt-online.org/files5/slide/0/04y5nw8FMBqsOuRcVoZ2kHGpLeKEQ9a1jdhrbS/slide-17.jpg)

![Км – это концентрация субстрата [S] при v реакции = 0,5* v max. Чем выше Км, тем меньше сродство фермента и субстрата. Км – это концентрация субстрата [S] при v реакции = 0,5* v max. Чем выше Км, тем меньше сродство фермента и субстрата.](https://cf5.ppt-online.org/files5/slide/0/04y5nw8FMBqsOuRcVoZ2kHGpLeKEQ9a1jdhrbS/slide-19.jpg)


 Биология
Биология








